واکسن آدنوویروس حاوی قطع شده SARS-CoV-2 زیر واحد پروتئین Spike S1 منجر به پاسخ ایمنی خاص در موش میشود
Dec 12, 2023
ابستراسی تی٪3aتوسعه یک واکسن کارآمد و ایمن برای بیماری کروناویروس 2019 (COVID-19) رویکردی حیاتی برای مدیریت همهگیری بیماری حاد تنفسی ویروس کرونا 2 (SARS-CoV-2) با توجه به شرایط فعلی است. در این مطالعه، ما یک بخش کوتاهشده از ژن بهینهشده SARS-CoV-2 (2043 جفت باز که S1 نامیده میشود) تولید کردیم که قادر به رمزگذاری یک پروتئین کوتاهشده S1 بود. این پروتئین برای تعیین اینکه آیا میتواند ایمنسازی کارآمد را در موشها علیه SARS-CoV ایجاد کند، آزمایش شد. حضور پروتئین S1 با ایمونوفلورسانس و وسترن بلات تایید شد. یک واکسن آدنوویروس حاوی قطعه ژن S1 (Ad-S1) به صورت داخل عضلانی به موش ها چهار بار در طول 4 هفته تزریق شد. SARS-CoV{18} ایمنی هومورال پروتئین S1 در تمام موشهای واکسینه شده نشان داده شد. سرم موش های واکسینه شده فعالیت ضد عفونت عالی را در شرایط آزمایشگاهی نشان داد. یک پاسخ ایمنی هومورال قوی علیه SARS-CoV{22}} در موشها پس از واکسیناسیون با Ad-S1 مشاهده شد، که نشان میدهد واکسن آدنوویروس ممکن است به ساخت واکسنهایی علیه SARS-CoV-2 و سایر عوامل ژنتیکی متمایز کمک کند. ویروس ها

cistanche tubulosa - سیستم ایمنی را بهبود می بخشد
کلمات کلیدی: SARS-CoV-2; واکسن ها؛ ناقل آدنوویروسی؛ ژن S1؛ مصونیت
1. معرفی
بیماری کروناویروس 2019 (COVID-19) اغلب با نارسایی ارگان های متعدد و میزان مرگ و میر بالا [1] همراه است و یک تهدید بزرگ برای امنیت عمومی در سراسر جهان است. از 15 ژوئیه 2022، همهگیری کووید{5}} در سراسر جهان با 557,917,904 مورد تایید شده از جمله 6,358,899 مورد مرگ، به سازمان بهداشت جهانی (WHO) گزارش شده است. علاوه بر این، در مجموع 12130881147 دوز واکسن تا 11 ژوئیه 2022 تجویز شده است. بنابراین، طراحی و توسعه واکسنهای جدید کرونا (nCoV) از اهمیت زیادی برخوردار است و یکی از اولویتهای بهداشت جهانی است. پروتئین S یک عامل کلیدی در ورود SARS-CoV{19}} بیماری حاد تنفسی حاد ویروس کرونا 2 (SARS-CoV-2) به سلولهای میزبان است [2،3]. پروتئین به گیرنده میزبان متصل می شود و به ویروس اجازه می دهد تا به راحتی وارد سلول میزبان شود [4]. گلیکان های متصل به N از سطح تریمر بیرون زده و پروتئین S را به طور گسترده ای تزئین می کنند و بر تاخوردگی پروتئین S، ایمنی هومورال و پردازش پروتئاز سلول میزبان تأثیر می گذارند [5]. پروتئین SARS-CoV{29}} S دارای چگالی گلیکان مرتبط با N کمتری نسبت به سایر پروتئینهای بیماریزای انسانی ناشی از ویروس کرونا است [6]. بنابراین، پروتئین S ممکن است بسیار ایمنی زا باشد و هدف اصلی آنتی بادی های خنثی کننده باشد. پروتئین S دارای سه حوزه ساختاری است که در میان آنها دامنه S1 مهمترین آنتی ژن سطحی پروتئین S است [4]. به دلیل دشواری تولید پروتئین های نوترکیب بزرگ (دامنه خارج سلولی پروتئین S حدود 1300 اسید آمینه است) و خطر افزایش وابسته به آنتی بادی (ADE) عفونت، S1 (حدود 700 اسید آمینه) و دامنه اتصال گیرنده آن (RBD، حدود 200 اسید آمینه) به طور گسترده به عنوان جذاب ترین اهداف بالقوه برای واکسن کرونا در نظر گرفته می شود [7،8]. سروتیپ آدنوویروس انسانی 5 (HAdV-C5) به طور گسترده در ویروس شناسی پایه به عنوان یک ژن درمانی و ناقل تحویل واکسن استفاده می شود [9]. HAdV-C5 دارای تنوع طبیعی است و میتواند بیشتر میزبانها را انگلی کند، که اساس توسعه آزمایشهای حیوانی را تشکیل میدهد. ناقلهای آدنوویروس نوترکیب با نقصهای همانندسازی و همانندسازی ساخته شده از HAdV-C5 به طور گسترده در تحویل واکسن و ژن درمانی استفاده شدهاند [9،10]. در حال حاضر، آدنوویروسها به عنوان واکسنهایی در برابر عفونتهای حاد تنفسی تأیید شدهاند و آزمایشهای زیادی در مورد این واکسنها مانند مالاریا و HIV انجام شده است [9]. در این مقاله، ما یک واکسن ناقل آدنوویروس دارای کمبود تکثیر انسانی SARS-CoV و تهیه و کاربرد آن را شرح میدهیم. در این مطالعه، واکسن آدنوویروس به شرح زیر ساخته شد: ناقل آدنوویروس HAdV-C5 با نقص همانندسازی انسانی با حذف E1 و E3، پلاسمید اسکلت آدنوویروس نوترکیب با pBHGlox∆E1,3Cre، رده سلولی بستهبندی سلول HEK293 بود. و ژن هدف، ژن پروتئین S1 کوتاه SARS-CoV{68}} بود. بیان پروتئین S1 در واکسن با روش وسترن بلات و ایمونوفلورسانس شناسایی شد. برای تعیین کیفیت پاسخ های ایمنی ناشی از نامزدهای واکسن مبتنی بر سنبله، پاسخ آنتی بادی پس از واکسیناسیون با جزئیات مورد بررسی قرار گرفت. فواید ایمنی واکسن با آزمایش آنتی بادی اتصال (آزمون ایمونوسوربنت متصل به آنزیم [ELISA]) و تست آنتی بادی خنثیسازی ارزیابی شد. یافتههای ما مبنایی برای توسعه و ارزیابی واکسنها و درمانهای کووید-19 بر اساس پروتئین S1 فراهم میکند.
2. مواد و روش
2.1. سلول ها و حیوانات
در این مطالعه از رده های سلولی کلیه میمون های HEK293 و Vero E6 استفاده شد. هر دو رده سلولی در محیط Eagle اصلاح شده Dulbecco (DMEM) همراه با 2٪ سرم جنین گاو (FBS) و 1٪ پنی سیلین و استرپتومایسین در دمای 37 درجه سانتیگراد با 5٪ CO2 و رطوبت اشباع رشد کردند. بیست موش ماده C57BL/6 (6 تا 8 هفته) از مرکز آزمایشی حیوانات ژجیانگ، استان ژجیانگ خریداری شدند. موش ها به طور تصادفی به دو گروه با 1{20}} موش در هر گروه تقسیم شدند. یک گروه (تزریق داخل صفاقی 100 میکرولیتر) با وکتور Ad5 بیان کننده پروتئین SARS-CoV{15}} (Ad{16}}S) و گروه دیگر با PBS (تزریق داخل صفاقی 100 میکرولیتر) به عنوان شاهد واکسینه شدند. مقدار کل ویروس 5 × 109 VP بود. همه موش ها با تزریق عضلانی D0/D14 ایمن شدند [11،12]. در D14، خون محیطی 100 میکرولیتر گرفته شد، سرم جدا شد و تزریق دوم دو ساعت پس از خونگیری انجام شد. در D28، خون با سوراخ رترو-اوربیتال جمع آوری شد و سرم جدا شد. آنتی بادی های اتصال 3 روز پس از هر خون گیری، آنتی بادی های خنثی کننده 7 روز پس از هر خون گیری و سیتوکین ها 7 روز پس از خون گیری دوم شناسایی شدند. همه موش ها معدوم شدند. همه آزمایشها بر اساس «دستورالعملهای مراقبت و استفاده از حیوانات آزمایشی جمهوری خلق چین» انجام شد و توسط شورای اخلاق دانشگاه ژجیانگ شورن تأیید شد.
2.2. واکسن ها
همه سویههای SARS-CoV-2 مورد استفاده در این مطالعه از بیماران کووید-19 با رضایت جمعآوری شدند. آزمایشگاه کلیدی دولتی برای تشخیص و درمان بیماریهای عفونی یک واکسن آدنوویروس (سلول Vero، سویه WuHan، شماره GISAID: EPI_ISL_415711) علیه SARS-CoV-2 و سپس واکسن در یک محیط سازگار با سطح ایمنی زیستی (BSL) ساخته شد. مشخصات واکسن 0.5 میلیلیتر در دوز است و حاوی Tris، NaCl، قند نیشکر، MgCl2.6H2O، C6H9N3O2، اتانول مطلق و پروتئین SARS-CoV-2 S1 است.
2.3. ساخت آدنوویروس نوترکیب
توالی پروتئین SARS-CoV{1}} S1 (شماره QRU91950.1) از PubMed به دست آمد. با توجه به انحطاط ژنی، توالی نوکلئوتیدی کدون بهینه شده مناسب برای بیان سلول پستانداران بر اساس این فرض طراحی شد که توالی اسید آمینه پروتئین محصول کدگذاری شده توسط پروتئین SARS-CoV-2 S1 بدون تغییر باقی ماند. طول کل 2043 جفت باز بود. توالی 50 پیش ساز با فعال کننده پلاسمینوژن بافتی (tPA) سنتز شد و توالی رمزکننده SARS-CoV{11}} S1 آمینو اسید 2-688 و توالی پیش ساز tPA پیوند داده شد. یک توالی Kozak و یک سایت محدودیت SpeI در جلوی کدون شروع و سایت محدودیت XbaI بعد از کدون پایان اضافه شد. توالی های نوکلئوتیدی ژن های فوق توسط Sangon Biotech سنتز و در pUC18 کلون شدند تا پلاسمید کلون شده ژن مصنوعی بدست آید. توالی ژن S1 سنتز شده و ناقل pDC316 با اندونوکلئازهای محدود SpeI و XbaI هضم شدند. قطعه و وکتور هدف از ژل استخراج و به هم متصل شدند تا یک پلاسمید شاتل تشکیل دهند. پلاسمید شاتل SARS-CoV{19}} با پلاسمید اسکلت سیستم آدنوویروس AdMax pBHGloxd∆E1 و 3Cre با ترانسفکشن مشترک سلولهای HEK293 بستهبندی شد. محلول ویروس اولیه پس از انجماد-ذوب مکرر و سانتریفیوژ به دست آمد و ویروس تکثیر و پس از خالص سازی پلاک کشت شد.

فواید سیستانچ برای مردان - تقویت سیستم ایمنی بدن
برای مشاهده محصولات Cistanche Enhance Immunity اینجا را کلیک کنید
【بیشتر بخواهید】 ایمیل:cindy.xue@wecistanche.com / Whats App: 0086 18599088692 / Wechat: 18599088692
2.4. تعیین تیتر آدنوویروس
سلولهای HEK293 که از سلامت خوبی برخوردار بودند، انتخاب و مجدداً معلق شدند تا یک سوسپانسیون سلولی 5.0 × 105 سلولی در میلیلیتر تهیه شود، که در یک صفحه 24- چاهی (1 میلیلیتر در چاهک) کاشته شد. ) و در دمای 37 ◦C در محیط 5% CO2 کشت داده شد. نمونه به صورت متوالی ده برابر رقیق شد و یک نمونه رقیق شده (0.1 میلی لیتر) از 10-5 تا 10-8 سلول در یک صفحه چاهک تلقیح شد. . سپس پلیت ها در دمای 37 درجه سانتیگراد با 5% CO2 به مدت 48 ساعت در معرض آلودگی قرار گرفتند. پس از آن، محیط کشت برداشته شد، متانول از قبل خنک شده (0.5 میلی لیتر) اضافه شد و نمونه ها در دمای 20- درجه سانتیگراد به مدت 20 دقیقه ثابت شدند. پس از تثبیت، نمونه ها با سالین بافر فسفات (PBS) شسته و با آلبومین سرم گاوی 1% (BSA، 0.2 میلی لیتر) در دمای 37 درجه سانتیگراد به مدت 1 ساعت مسدود شدند. سپس آنتیبادیهای اولیه (هگزون ضد آدنوویروس موش، AbD Serotec 04000079، 1:2000) و ثانویه (Goat pAb به MS IgG2a (HRP)، Abcam ab97245، 1:1000) اضافه شدند و به مدت 1 ساعت انکوبه شدند. برای شستشو استفاده می شد پس از انکوباسیون، محلول کاری تازه تهیه شده (0.2 میلی لیتر) اضافه شد و به مدت 5 تا 10 دقیقه در دمای اتاق انکوبه شد. سپس محلول کار دور ریخته شد، نمونه ها با PBS شسته شدند و PBS (1 میلی لیتر) دوباره اضافه شد. میانگین تعداد سلولهای مثبت در میدان میکروسکوپی (cat. CKX53، میکروسکوپ سیستم معکوس تحقیقاتی OLYMPUS) محاسبه شد، که در آن یک گرادیان با 5-50 سلول مثبت در میدان دید انتخاب شد و حداقل پنج ناحیه بهطور تصادفی برای شمارش انتخاب شدند. . تعداد میدانهای بصری در هر چاه 24- صفحه چاه محاسبه شد. سپس تیتر ویروس طبق فرمول (1) زیر محاسبه شد:

2.5. Real-Time PCR
برای تشخیص بیان mRNA سلول HEK293 به دنبال عفونت ویروسی، ما RNA میانی را مطابق دستورالعمل های عملیاتی TRIZol (Invitrogen، Waltham، MA، USA) استخراج کردیم. RNA کل با استفاده از TRIzol استخراج شد و با RQ1 RNase-free DNase I (Promega، Madison، WI، USA) برای از بین بردن DNA باقیمانده پردازش شد. DNA مکمل (cDNA) با رونویسی معکوس RNA استخراج شده با استفاده از کیت معرف PrimerScript™ RT با کیت پاک کن gDNA (Takara، Kusatsu، ژاپن) به دست آمد. قطعات DNA با پرایمرهای خاص P1 (50 -GGTGATTCTTCTTCAGGTTGGA-30) و P2 (50 - GTTTCTGAGAGAGAGGGTCAAGTG-30) ژن هدف (S1) تولید شد. ژن با آغازگرهای P3 (50 -GTCTTCACCACCATGGAGAA-30) و P4 (50 -TAAGCAGTTGGTGTGTGCAG-30) به عنوان کنترل داخلی (GAPHD) تکثیر شد.
2.6. وسترن بلات
لیزات سلولی و مایع رویی با الکتروفورز ژل سدیم دودسیل سولفات-پلی آکریل آمید (SDS-PAGE) جدا شدند و سپس به غشاهای پلی وینیلیدین فلوراید (PVDF) منتقل شدند. لکه ها با تجهیزات تصویربرداری وسترن بلات (Bio-Rad، Hercules، CA، USA) تجسم شدند. به طور خلاصه، غشاها به TBST (5{7}} میلیلیتر Tris-HCl، pH 7.5، 8 گرم NaCl [0.5 میلیلیتر]، 0.2 گرم KCl، 0.5 میلیلیتر توئین» منتقل شدند. -20) با پودر شیر خشک بدون چربی 5% و به مدت 1 ساعت روی شیکر رنگبری در دمای اتاق تکان دهید. غشاهای گروه آزمایش و کنترل از محلول آب بندی خارج شدند و با آنتی بادی اولیه انکوبه شدند: [SARS-CoV{18}} ({19}}nCoV) Spike Antibody (1:5000، cat. #40591- T62, Sino Biological, Beijing, China)] در دمای اتاق. آنتیبادیهای اولیه تکان داده شدند و یک شبه روی یک شیکر رنگزدایی در دمای 4 درجه سانتیگراد انکوبه شدند. بلات با محلول TBST شسته شد و به مدت 2 ساعت با آنتی بادی ثانویه [ایمونوگلوبولین G ضد خرگوش بز (IgG) H&L (HRP) (1:10000، گربه #ab6721، Abcam، کمبریج، انگلستان)] انکوبه شد. پس از شستشو، لکه ها به مدت 1 دقیقه با کیت محلول LumiBest ECL Substrate (cat. #4AW{33}}، 4A Biotech) انکوبه شدند و سپس در یک تصویرگر مشاهده شدند.
2.7. سنجش ایمونوفلورسانس
سلول های HEK293 (3 × 106/چاه) در صفحات {3} چاه کاشته شدند. پس از 48 ساعت، سلول ها با آدنوویروس حاوی ژن S1 (Ad-S1) آلوده شدند. پس از 48 ساعت، محیط آسپیره شد و سلول ها یک بار با PBS حاوی 2% BSA شسته شدند و به مدت 15 دقیقه با متانول که به مدت 15 دقیقه در دمای ◦-20 از قبل سرد شده بود، تثبیت شدند. پس از سه بار شستشو با 2% BSA در PBS، سلول ها با 0.5% Triton X{17}} به مدت 10 دقیقه نفوذپذیر شدند. سپس سلول ها به مدت 1 ساعت با 2 میلی لیتر BSA 2% مسدود شدند، محلول مسدود کننده دور ریخته شد و سلول ها سه بار با PBS شسته شدند. متعاقبا، 2 میلی لیتر آنتی بادی اولیه [SARS-CoV-2 ({25}}nCoV) Spike Antibody (1:2000، گربه #40591-T62، Sino Biological)] به هر چاه اضافه شد و در دمای اتاق به مدت 1 ساعت یا 4 درجه سانتیگراد در طول شب انکوبه می شود. سپس نمونه سه بار با 2% BSA به مدت 5 دقیقه در هر شستشو شستشو داده شد. سپس، 2 میلی لیتر آنتی بادی ثانویه [IgG H&L ضد خرگوش بز (Alexa Fluor 488) (1:1000، cat. #550037، ZenBio)] به هر چاهک اضافه شد و به مدت 1 ساعت در دمای اتاق انکوبه شد. پس از آن، نمونه ها سه بار با BSA 2% به مدت 5 دقیقه در هر شستشو شستشو داده شدند. محلول 40،6-دیامیدینو{45}}فنیلیندول (DAPI) (2 میلیلیتر، 1 میلیگرم بر میلیلیتر) (1:400، cat. #S0001، Bioss، Woburn، MA، USA) به هر چاهک اضافه شد. و به مدت 10 دقیقه در تاریکی واکنش نشان داد. تجزیه و تحلیل با یک سیستم تصویربرداری EVOS™ M7000 (گروه #AMF7000، Invitrogen) مشاهده شد.
2.8. الایزا
پروتئین SARS-CoV-2 (1 میکروگرم در میلی لیتر) یک شبه در 96-صفحات چاهک (100 میکرولیتر/چاه) با 0 پوشانده شد. 0بافر بی کربنات 5 M. پس از شستشو با PBST (0.2 گرم KH2PO4، 2.9 گرم Na2HPO4·12H2O، 8.0 گرم NaCl، 0.2 گرم KCl، 0.5 میلی لیتر Tween-20، به 1000 میلی لیتر آب اضافه کنید) پنج بارها محلول مسدودکننده اضافه شد و در دمای 37 درجه سانتیگراد به مدت 1 ساعت انکوبه شد. نمونه سرم رقیق شد و به هر چاهک (100 میکرولیتر در چاهک) اضافه شد. پس از 1 ساعت انکوباسیون در دمای 37 درجه سانتیگراد، نمونه ها پنج بار با PBST شسته شدند. آنتی بادی اولیه [SARS-CoV{31}} ({32}}nCoV) Spike Antibody (1:2000, cat. #40591-T62, Sino Biological)] اضافه شد و به مدت 1 ساعت انکوبه شد، سپس نمونه ها پنج بار با PBST شسته شدند و سپس 1 ساعت انکوباسیون در دمای 37 درجه سانتیگراد با آنتی بادی ثانویه کونژوگه با پراکسیداز ترب کوهی [IgG H&L ضد خرگوش بز (HRP) (1:10000، گربه #ab6721، abcam)] و پنج شستشو با PBST پس از افزودن 3، 30، 5 و 50-تترا متیل بی فنیل انیدرید به مدت 5 دقیقه، واکنش با اسید سولفوریک 2 مولار متوقف شد. چگالی نوری در nm 450 و nm 630 توسط یک ابزار آنزیمی نشاندار (Molecular Devices, SpectraMax 190) اندازهگیری شد و سپس بر روی یک منحنی استاندارد قرار گرفت.

فواید سیستانچ توبولوزا-تقویت سیستم ایمنی بدن
2.9. تعیین سیتوکین
پلیت (گروه #T-k15048D-1، MSD) سه بار با بافر شستشوی 150 میکرولیتر در چاه شسته شد و یک نمونه 50 میکرولیتری آماده شده به هر چاهک اضافه شد. سپس، صفحه با مهر و موم صفحه چسبنده مهر و موم شد و در دمای اتاق با تکان دادن به مدت 2 ساعت انکوبه شد. سپس پلیت سه بار با بافر شستشوی 150 میکرولیتر در چاه شسته شد و به هر چاهک 25 میکرولیتر محلول آنتی بادی تشخیص اضافه شد. صفحه دوباره مهر و موم شد و در دمای اتاق با تکان دادن به مدت 2 ساعت انکوبه شد. سپس، صفحه سه بار با حداقل 150 میکرولیتر در چاه بافر شستشو شسته شد. 150 میکرولیتر 2× Read Buffer T (MSD) به هر چاهک اضافه شد و پلیت روی دستگاه MSD آنالیز شد.
2.10. آنتی بادی خنثی کننده
2.10.1. سنجش خنثی سازی شبه ویروس
فعالیت خنثی سازی سرم موش با استفاده از سیستم شبه ویروسی ویروس استوماتیت تاولی (VSV) مورد آزمایش قرار گرفت. سرم در یک حمام آب به مدت {{0}}.5 ساعت در دمای 56 درجه سانتیگراد غیرفعال شد و سپس به صورت سریال تا محدوده مورد نیاز رقیق شد. سلول های HEK293 در یک 96- صفحه چاه قرار گرفتند. سرم رقیق شده با 200 CCID50 (دوز ویروسی که می تواند 50 درصد کشت سلولی را آلوده کند) / 100 میکرولیتر سوسپانسیون ویروس به نسبت 1:1 مخلوط شد و در انکوباتور CO2 (1 ± 37 درجه سانتیگراد) قرار داده شد. 2 ساعت سپس، 100 میکرولیتر محلول نگهدارنده ویروس حاوی 0.5 درصد آنتیبادی دوگانه پنیسیلین-استرپتومایسین به هر چاهک اضافه شد و مخلوط خنثیشده در یک صفحه چاه حاوی سلولها با حجم 100 میکرولیتر در هر چاه، با دو چاهک تکراری تلقیح شد. هر رقت در همان زمان، یک کنترل سلولی نرمال تنظیم شد و سلول ها در انکوباتور CO2 (37 ± 1◦C) به مدت 96 ساعت انکوبه شدند. سپس 200 CCID50/100 میکرولیتر از محلول ویروس به 10-1~{29}} رقیق شد. محیط کشت سلولی در صفحه چاه دور ریخته شد، 150 میکرولیتر از محلول نگهداری ویروس به هر چاهک اضافه شد و رقت محلول ویروس با غلظت 10-1~{33} تلقیح شد. } را در چاههای صفحه چاه 96- (50 میکرولیتر در هر چاهک). هر رقت در 8 چاه تکرار شد. یک کنترل سلولی طبیعی در همان زمان تنظیم شد و پس از آن کشت به مدت 96 ساعت انجام شد. تغییرات در CPE سلول در زیر میکروسکوپ معکوس مشاهده شد. کنترل سلول طبیعی نباید تغییرات سیتوپاتیک داشته باشد و کنترل مثبت باید تغییرات CPE داشته باشد. نقاط پایانی خنثی سازی (رقت های سرم تبدیل به لگاریتم) با مشاهده CPE محاسبه شد. معیار سرم منفی/مثبت 1:12 به عنوان معیار مثبت/منفی بود.<1:12 was negative, and ≥1:12 was positive.
2.10.2. آزمایش خنثی سازی زنده
فعالیت خنثی سازی سرم موش با آزمایش خنثی سازی زنده مورد ارزیابی قرار گرفت. سرم رقیق شده با SARS-CoV{1}} مخلوط شد و در دمای 37 درجه سانتیگراد به مدت 1 ساعت انکوبه شد. مخلوط به یک صفحه چاهی 96- اضافه شد تا سلول های Vero E6 را آلوده کند. پس از 72- ساعت انکوباسیون در دمای 37 درجه سانتیگراد، اثر سیتوپاتیک ویروس (CPE) تحت بزرگنمایی 40 × مشاهده شد و تیتر خنثی سازی (رقت متقابل 50 درصد سرم مورد نیاز برای خنثی کردن عفونت ویروسی) محاسبه شد. مراحل فوق همه در محیط ایمنی زیستی سطح 3 انجام شد.
2.11. تحلیل آماری
تجزیه و تحلیل آماری با استفاده از آزمون t دو نمونه ای با استفاده از نرم افزار SPSS 26 انجام شد. مقادیر p کمتر یا مساوی 05/0 0 معنی دار در نظر گرفته شد. گرایش مرکزی با تیتر میانگین هندسی (GMT) اندازه گیری شد.
3. نتایج
3.1. ساخت آدنوویروس نوترکیب
پلاسمید شاتل آدنوویروس نوترکیب pAdeno-CMV-S1 با درج صحیح به دست آمد. نمودار ساختار آن در شکل 1 نشان داده شده است. آدنوویروس نوترکیب حاوی ژنوم HAdV-C5 فاقد ناحیه E1/E3 است. یک نمودار شماتیک از وکتور آدنوویروس نوترکیب بدست آمده توسط پلاسمید شاتل و پلاسمید اسکلت سلولی در سلول های HEK293 در شکل 1 نشان داده شده است.
3.2. خصوصیات آدنوویروس نوترکیب
پلاسمید نوترکیب حاوی ژن هدف توسط PCR شناسایی شد (شکل 2A را برای نتایج الکتروفورز ژل ببینید). این یک آزمایش تکراری بود. توالیهای آغازگر MCMV-F ggtataagaggcgcgaccag و S{2}}R acaataagtagggactgggtc بودند، و توالییابی تأیید کرد که توالی با طرح مطابقت دارد. بیان SARS-CoV{4}} S1 در سلول ها با وسترن بلات (شکل 2B) و ایمونوفلورسانس غیرمستقیم (شکل 2C) شناسایی شد. رنگبندی باند (~75 کیلو دالتون) توسط وسترن بلات تشخیص داده شد و با موقعیت باند مورد انتظار مطابقت داشت. در سطح رونویسی، بیان در شرایط آزمایشگاهی S1 توسط PT-PCR شناسایی شد. نتایج نشان داد که بیان mRNA ژن S1 در سلولهای HEK{12}} بهطور معنیداری بیشتر از گروه کنترل بود.

شکل 1. ساخت واکسن آدنوویروس نوترکیب و استراتژی تجربی. (الف) pAdeno-CMV-S1 یک پلاسمید شاتل آدنوویروس نوترکیب حاوی ژن هدف S1 است. pBHGlox∆E1,3Cre پلاسمید اسکلت آدنوویروس است. pBHGlox∆E1،3Cre و pAdeno-CMV-S1 با کیت استخراج پلاسمید QIAGEN (شرکت بازرگانی Beijing North Yitao، LTD، پکن، چین) استخراج شدند. یک روز قبل از ترانسفکشن، سلولهای HEK293 در فلاسک کشت سلولی 25 سانتیمتر مربعی پاساژ شدند. محیط کشت DMEM حاوی 5% FBS بدون آنتی بیوتیک بود. در روز دوم، 60 تا 80 درصد سلولها انتخاب شدند و محلول ترانسفکشن به سلولها اضافه شد. پس از گذشت 7 روز از ترانسفکشن، سلول ها خراشیده شدند، سانتریفیوژ شدند، مایع رویی دور ریخته شد و سلول ها با PBS احیا شدند. سلول ها به طور مکرر در دمای -80 درجه سانتیگراد و 37 درجه سانتیگراد منجمد-ذوب شدند. پس از سانتریفیوژ، مایع رویی حاوی محلول ویروس اولیه بود. سویه آدنوویروس نوترکیب خالص، تکثیر و پس از پردازش بیشتر بدست آمد و Ad-S1 نامگذاری شد. این واکسن برای مطالعات بعدی به صورت عضلانی به موش ها تزریق شد. (ب) مقیاس زمانی نشان داده شده ایمن سازی و خروج خون.
3.3. تیتر آدنوویروس
در این آزمایش به طور متوسط 6 سلول مثبت در پنج میدان میکروسکوپی محاسبه شد و ویروس موجود در چاه 108 بار رقیق شد. بر اساس فرمول شرح داده شده در بخش مواد و روش، تیتر آدنوویروس 4.74 × 1011 واحد تشکیل پلاک (pfu)/mL بود (شکل 2D).
3.4. ایمنی سلولی پس از واکسیناسیون
در طول دوره آزمایش، تغییرات آماری معنیداری در سیتوکینهای سرم وجود داشت (p کمتر یا مساوی 0.05)، که عمدتاً نشان داد که غلظت مواد شیمیایی جذب کننده کراتینوسیت/آنکوژن تنظیمشده با رشد انسانی (KC/GRO) بود. کاهش یافت، و غلظت IFN-، IL-10، IL-12p70، IL-1، IL-2، IL-4، IL{10} } و TNF- افزایش یافتند، در حالی که غلظت IL{12}} تغییر معنی داری نداشت (شکل 3).

شکل 2. شناسایی پروتئین نوترکیب HAdV-C5-SARS-CoV{4}} S1 و تعیین تیتر آدنوویروس. (الف) تشخیص PCR پلاسمید نوترکیب با ژن هدف S1. (ب) تشخیص وسترن بلات SARS-CoV{8}}. سلولهای HEK293 با رشد نمایی به مدت 48 ساعت با SARS-CoV{12}} آلوده شدند، سپس پروتئین سلولی استخراج و توسط SDS-PAGE جدا شد. بیان SARS-CoV{16} توسط وسترن بلات با IgG ضد خرگوش بز تأیید شد. (C) میکروسکوپ ایمونوفلورسانس سلولهای HEK{18}} آلوده به Ad-S1 (سبز). سلول ها با 40، 6-دیامیدینو- 2- فنیلندول (DAPI) رنگ آمیزی شدند تا هسته ها رنگ آمیزی شوند. نوار مقیاس 1000 میکرومتر. (د) برای اندازه گیری از روش سنجش پلاک استفاده شد. میکروگرافهایی که رقتسازی 10-5، 10-6، 10-7 و 10-8 را نشان میدهند (از چپ به راست).
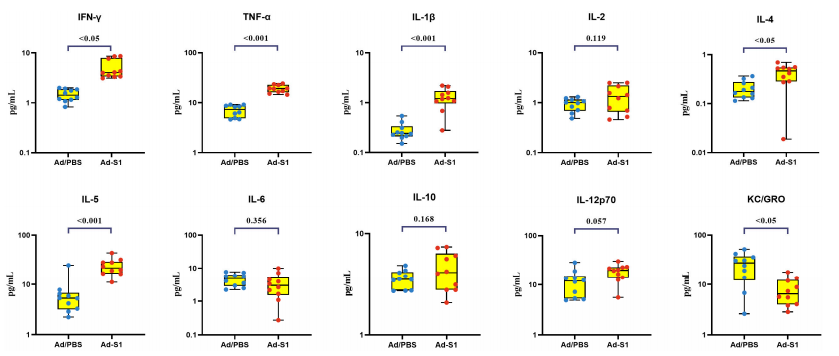
شکل 3. Ad-S1 باعث تغییر سطوح پلاسمایی سیتوکین های نوع 1/2، اینترفرون های نوع 1 و سایر سیتوکین ها شد. نتایج با خون گیری از موش ها 7 روز پس از اولین ایمن سازی مشخص شد. داده ها به صورت نمودار پراکندگی جعبه و سبیل ارائه می شوند. هر دایره نشان دهنده یک فرد واحد است. مقادیر p با استفاده از آزمون t دو نمونه ای محاسبه شد.
3.5. تشخیص آنتی بادی های ضد SARS-CoV{4}} S1 پس از ایمن سازی
ELISA نشان داد که آنتیبادیهای اختصاصی SARS-CoV در موشهایی که Ad-S1 اول و دوم تزریق شدهاند، وجود دارد، اما در موشهایی که با کپسید آدنوویروس کنترلی یا محلول PBS (Ad/PBS) تزریق شدهاند، وجود ندارد (شکل 4A). تیترهای IgG 1:210 و 1:212 به ترتیب در موشهای{10}}واکسینه شده با Ad-S دو هفته پس از واکسیناسیون اول و دوم شناسایی شد. تیتر رقت در 28 روز پس از واکسیناسیون (D28، GMT 2297.4) 6.{17}}برابر بیشتر از D14 (GMT 378.9) بود.
شکل 4. Ad-S1 تیترهای بالایی از آنتی بادی ها (A) و فعالیت خنثی سازی (B, C) را در موش القا کرد. (الف) الایزای SARS-CoV{4}}IgG اختصاصی سرم از موشهای ایمنسازی شده با Ad-S{{6}. (ب) تجزیه و تحلیل فعالیتهای شبه ویروس سرم از موشهای ایمنسازی شده Ad-S{8}. (C) تجزیه و تحلیل فعالیتهای خنثیکننده سرم موشهای{10}}ایمنشده Ad-S
3.6. سنجش آنتی بادی خنثی کننده
چالش SARS-CoV-2 سلولهای Vero E6، تشخیص فعالیت خنثیکننده را در سرم موش واکسینهشده فعال کرد (شکل 4B، C). تیترهای خنثیسازی D14 و D28 سلولهای Ad-S1-ایمنسازی شده Vero E6 در برابر چالش ویروس زنده SARS-CoV{{10}} در شرایط آزمایشگاهی به ترتیب 1:24.3 و 1:26.3 بود. سنجش شبه ویروس نتایج مشابهی با نتایج آزمایش ویروس زنده به همراه داشت، با عیار خنثی سازی تا 1:28.1 و 1:29.6 در D14 و D28، به ترتیب. تیتر خنثی کننده شبه ویروس D28 (GMT 769.0) 2.{29}} برابر بیشتر از D14 (GMT 283.7) بود.
4. بحث
We have been working to develop vaccines to stop the COVID-19 pandemic and its rapid spread. The hunt for an effective vaccination against SARS-CoV-2 continues and existing vaccine development strategies include whole virus particle vaccines, live attenuated virus vaccines, purified virus subunit vaccines, and genetic vaccines [13–17]. The epitopes on spike proteins detected in infected serum are highly antigenic, with the ability to induce a strong humoral immune response and neutralize antibodies in individuals infected with SARS-CoV-2 and recovered from COVID-19 [18,19]. The S protein appears to be an ideal target for vaccination against SARS-CoV-2 infection [20]. The S protein S1 subunit induced effective immunity against SARS-CoV-2 and protected against SARS-CoV-2 in animal models [21,22]. The SARS-CoV-2 truncated N protein has a better expression effect than the N protein [23]. Based on this, we selected the truncated S1 protein in this experiment. In other studies, more than 90% of the neutralization activity of the Moderna mRNA vaccine was caused by the RBD antibody, and the neutralization titer directly decreased from >1000 تا<25 after the RBD antibody had been eliminated [24]. Higher levels of RBD-specific IgG were associated with increased serum neutralization [25]. Evidently, the S protein demonstrates a greater immune response to the RBD region, and the S1 protein containing RBD can induce neutralizing antibodies with a higher titer than the S protein [26]. Antigens delivered by adenovirus vectors induce strong cellular and humoral immunity after a single immunization, making them useful as an emergency prevention tool in a pandemic [27]. Adenovirus-based vaccine strategies are therefore an important part of the fight against SARS-CoV-2 infection.
در این مطالعه، یک واکسن نوترکیب آدنوویروس SARS-CoV-2 حاوی زیرواحد SARS-CoV-2 S1 ساختیم و آن را Ad-S1 تعیین کردیم. مانند CanSinoBIO که برای بازاریابی تایید شده است [28]، ما از HAdV-C5 در این واکسن استفاده کردیم. آدنوویروس به طور گسترده در ژن درمانی نوترکیب و به عنوان یک ناقل واکسن استفاده می شود. با این حال، میزان مثبت HAdV-C5 در جمعیت عادی به 75 تا 80 درصد می رسد [29]. این بدان معناست که ایمنی پیش از ذخیره سازی در برابر ناقل های HAdV-C5 به طور قابل توجهی ایمنی ناشی از واکسن را کاهش می دهد. ChAdOx1 nCoV{20}} که در دانشگاه آکسفورد در انگلستان توسعه یافته است، از یک ناقل آدنوویروس شامپانزه استفاده میکند که در مقابل، نرخ سرمی مثبت کمتری در انسان دارد و وقتی مثبت است، معمولاً تیتر آنتیبادی سرم پایینتری را نشان میدهد [30] . بنابراین، ناقلهای آدنوویروسی که میتوانند از ایمنی از قبل موجود فرار کنند، میتوانند برای افزایش کارایی محافظتی واکسن آدنوویروس مورد بررسی قرار گیرند. در مطالعه حاضر، وضعیت سرمی موشها قبل و بعد از ایمنسازی با استفاده از آزمون الایزا و خنثیسازی تعیین شد و شواهدی مبنی بر ایمنی هومورال برای کاندیدای واکسن به دست آمد. سرم تولید شده پس از تزریق عضلانی واکسن در موش به طور موثری از سلول های Vero E6 در برابر عفونت SARS-CoV{25}} در شرایط آزمایشگاهی محافظت کرد (شکل 4). ما همچنین پاسخ ایمنی قویتر و محافظت بهتر را در موشها پس از ایمنسازی دوم شناسایی کردیم (شکل 4). نتایج تجربی ما مشابه نتایج تجربی اصلی است.
همانطور که تحقیقات SARS-CoV-2 ادامه دارد، چندین مطالعه نشان دادهاند که طوفان سیتوکین ثانویه به عفونت SARS-CoV{3}} ممکن است بر تولید سلول T تأثیر بگذارد و حفظ ایمنی طولانیمدت را برای بیماران دشوار کند. SARS-CoV{7}} [31]. بنابراین، تعیین اینکه آیا Ad-S1 می تواند مصونیت با واسطه سلول T را در موش ایجاد کند ضروری است. نتایج ما نشان داد که غلظت IFN و IL{14}} افزایش یافته و غلظت IL-4 در گروه Ad-S1 کاهش یافته است، که نشان میدهد که بقا و رشد سلول Th1 توسط واکسن در موشها ایجاد شده است. ترشح IL{20}}، IL-10 و TNF- توسط سلولهای Th1 در گروه آزمایش کمی افزایش یافت. این نتایج نشان داد که Ad-S1 به طور موثر پاسخ سلول T باطرف Th{26}} را در موش القا میکند [32]. افزایش IL{29}} نشان داد که سلول های Th2 نیز در پاسخ ایمنی شرکت می کنند و اثرات خاصی ایجاد می کنند. غلظت KC/GRO در گروه آزمایش به طور قابل توجهی در مقایسه با گروه کنترل PBS کاهش یافت، که ممکن است به دلیل کاهش کموتاکسی نوتروفیل باشد که پاسخ التهابی را سرکوب کرده و اجازه می دهد تا عوارض جانبی واکسن کمی کنترل شود. این امر برای افراد دارای نقص ایمنی، مانند افراد مسن یا بیمارانی که تحت شیمی درمانی قرار می گیرند، مفیدتر است. لی ام.، و همکاران. [29] یک واکسن آدنوویروس را با استفاده از Ad68 به عنوان یک ناقل توسعه داد. نتایج نشان داد که فعالیت خنثیکننده SARS-CoV{34}} را میتوان در عرض دو هفته پس از ایمنسازی عضلانی موشهای BALB/c شناسایی کرد و سپس به افزایش ادامه داد و تیتر آنتیبادی خنثیکننده (PRNT ID50) در 8 به 957.3 رسید. هفته ها در همین حال، در مطالعه Liu J.، و همکاران. [33]، واکسن هایی با استفاده از AdC6 و AdC68 به عنوان ناقل ساخته شدند. هر دو پاسخ آنتی بادی اتصال و خنثی کننده پس از ایمن سازی، 14 روز پس از دوز، با تیتر IgG 7108 (میانگین هندسی تیتر، GMT؛ AdC6) و 5489 (GMT، AdC68) ایجاد شد. تیتر خنثی سازی 50 (NT50) در روش خنثی سازی شبه ویروس 125 (GMT، AdC6) و 67 (GMT، AdC68) بود.

cistanche tubulosa - سیستم ایمنی را بهبود می بخشد
در مطالعه حاضر، موشهای واکسینهشده با Ad-S1 دارای تیتر IgG 1:1010 و 1:122 بودند که بهترتیب دو هفته پس از اولین و دومین واکسیناسیون توسط ELISA شناسایی شدند. تیتر رقت ad-s1 378.9 (GMT) در 14 روز پس از تلقیح و 2297.4 (GMT) در 28 روز پس از تلقیح بود. در آزمایش آنتی بادی خنثیسازی، سلولهای Vero E6 ایمنسازی شده با Ad-S1 به ترتیب خنثیسازی 1:24.3 و 1:26.3 را در D14 و D28 در برابر چالش ویروس زنده SARS-CoV{26}} در شرایط آزمایشگاهی نشان دادند. تیتر خنثی سازی شبه ویروس در D14 و D28 به ترتیب 283.7 (GMT) و 769.0 (GMT) بود. بنابراین، واکسن در این مطالعه از نظر پاسخ ایمنی در مدل موش موثرتر بود.
به دلیل محدودیت شرایط تجربی، ما آنالیز نقطه ایمونوسوربنت متصل به آنزیم (ELISpot) سلول های ایمنی طحال موش های آزمایشگاهی را انجام ندادیم. علاوه بر این، آزمایشهای محافظت از حمله SARS-CoV-2 روی موشها به دلیل محدودیتهای آزمایشگاه حفاظت فیزیکی انجام نشد. با این حال، ما تشخیص دادیم که واکسن کارایی بالایی در مدلهای موش دارد و میتواند به عنوان یک سویه واکسن ذخیره ایدهآل استفاده شود. علاوه بر این، ایمنی زایی، ایمنی و اثربخشی واکسن SARS-CoV{4}} باید در مدلهای حیوانی دیگر (مانند خرگوش، پستانداران، راکون، سگ) بررسی شود، زیرا ممکن است مدلهای موش به طور کامل ایمنیشناسی انسان را تکرار نکنند. امکانات.

گیاه سیستانچ سیستم ایمنی را افزایش می دهد
5. نتیجه گیری ها
داده های به دست آمده از مطالعات پیش بالینی ما در مورد واکسن آدنوویروس نشان داد که واکسن دارای ایمنی و اثربخشی کافی است. بنابراین، ممکن است یک واکسن پیشگیرانه امیدوارکننده و عملی علیه عفونت SARS-CoV-2 باشد.
منابع
1. Trougakos، IP; استاماتلوپولوس، ک. ترپوس، ای. Tsitsilonis، OE; آیوالیوتی، ای. پاراسکویس، دی. کاستریتیس، ای. پاولاکیس، GN; Dimopoulos، MA Insights to SARS-CoV-2 چرخه زندگی، پاتوفیزیولوژی، و درمان های منطقی که عوارض بالینی COVID-19 را هدف قرار می دهند. جی. بیومد. علمی 2021، 28، 9. [CrossRef]
2. Pillay، ژن ماه TS: پروتئین جدید اسپایک کروناویروس 2019-nCoV/SARS-CoV-2. جی. کلین. پاتول. 2020، 73، 366-369. [CrossRef]
3. شینین، م. جونگ، بی. Paydi, RK; Pahan, K. رگرسیون سرطان ریه در موش توسط تزریق داخل بینی SARS-CoV-2 Spike S1. Cancers 2022, 14, 5648. [CrossRef]
4. کدام، س.ب. صخرمانی، جی اس; بیشنوی، پ. پابل، AA; باروکار، VT SARS-CoV-2، همهگیری کرونا ویروس: بینشهای مولکولی و ساختاری. J. میکروبیول پایه. 2021، 61، 180-202. [CrossRef]
5. استرنبرگ، ا. Naujokat، C. ویژگیهای ساختاری پروتئین اسپایک کرونا ویروس SARS-CoV{{2}: اهداف برای واکسیناسیون. زندگی علمی. 2020, 257, 118056. [CrossRef] [PubMed]
6. دیوارها، AC; Tortorici، MA; فرنز، بی. اسنایدر، جی. لی، دبلیو. ری، FA; دی مایو، اف. بوش، بیجی؛ محافظ Veesler، D. Glycan و پوشاندن اپی توپ پروتئین اسپایک کروناویروس که با میکروسکوپ کرایو الکترونی مشاهده شد. نات ساختار. مول. Biol. 2016، 23، 899-905. [CrossRef] [PubMed]
7. وانگ، ی. وانگ، ال. کائو، اچ. Liu, C. SARS-CoV-2 S1 نسبت به RBD به عنوان آنتی ژن زیر واحد واکسن کووید{4}} برتری دارد. جی. مد. ویرول. 2021، 93، 892-898. [CrossRef]
8. Theoharides، TC; Conti، P. از پروتئین SARS-CoV-2 آگاه باشید: بیش از آنچه که به نظر می رسد وجود دارد. جی بیول. منظم. Homeost. عوامل 2021، 35، 833-838. [CrossRef] [PubMed]
9. Guo، X. دنگ، ی. چن، اچ. لان، جی. وانگ، دبلیو. زو، ایکس. هونگ، تی. لو، ز. Tan، W. ایمنی سیستمیک و مخاطی در موشها با یک ایمنسازی با آدنوویروس انسانی نوع 5 یا واکسنهای مبتنی بر ناقل 41 که حامل پروتئین اسپایک کروناویروس سندرم تنفسی خاورمیانه هستند، ایجاد شد. ایمونولوژی 2015، 145، 476-484. [CrossRef] [PubMed]
10. گائو، ج. مسه، ک. Bunz، O. Ehrhardt، A. بردار شناسی آدنوویروس انسانی پیشرفته برای رویکردهای درمانی. FEBS Lett. 2019، 593، 3609–3622. [CrossRef]
11. زینگ، ک. Tu، XY; لیو، ام. لیانگ، ZW; چن، JN; لی، جی جی. جیانگ، ال جی؛ زینگ، FQ; جیانگ، ی. اثربخشی و ایمنی واکسنهای کووید-19: بررسی سیستماتیک. Zhongguo Dang Dai Er Ke Za Zhi 2021, 23, 221–228. [CrossRef]
12. وویسی، م. کلمنس، SAC; مدی، SA; Weckx، LY; فوله گاتی، نخست وزیر Aley، PK; آنگوس، بی. بیلی، وی.ال. بارناباس، اس ال. بورات، QE; و همکاران ایمنی و اثربخشی واکسن ChAdOx1 nCoV-19 (AZD1222) در برابر SARS-CoV-2: تجزیه و تحلیل موقت از چهار کارآزمایی تصادفیسازی و کنترلشده در برزیل، آفریقای جنوبی و بریتانیا. Lancet 2021، 397، 99-111. [CrossRef] [PubMed]
13. لی، سی. گوا، ی. نیش، ز. ژانگ، اچ. ژانگ، ی. Chen, K. تجزیه و تحلیل اثر حفاظتی واکسنهای تأیید شده کووید-19 در برابر جهشیافتههای مختلف. جلو. ایمونول. 2022, 13, 804945. [CrossRef] [PubMed]
14. Tanriover، MD; Do ˘ganay، HL; آکوا، م. گونر، منابع انسانی؛ آزاپ، ا. آخان، س. Köse، ¸S. اردینچ، اف. Akalın، EH; تاباک، Ö.F. و همکاران اثربخشی و ایمنی واکسن SARS-CoV{3}} غیرفعال کامل ویریون (CoronaVac): نتایج موقت یک کارآزمایی دوسوکور، تصادفی، کنترلشده با دارونما، فاز 3 در ترکیه. Lancet 2021, 398, 213-222. [CrossRef]
15. شیا، اس. ژانگ، ی. وانگ، ی. وانگ، اچ. یانگ، ی. گائو، جی اف. تان، دبلیو. وو، جی. خو، ام. Lou, Z. ایمنی و ایمنی زایی واکسن غیرفعال SARS-CoV-2، BBIBP-CorV: یک کارآزمایی تصادفی، دوسوکور، کنترل شده با دارونما، فاز 1/2. عفونت لانست دیس 2021، 21، 39-51. [CrossRef] [PubMed]
16. یانگ، اس. لی، ی. دای، ال. وانگ، جی. او، پ. لی، سی. نیش، ایکس. وانگ، سی. ژائو، ایکس. هوانگ، ای. و همکاران ایمنی و ایمنی زایی واکسن زیرواحد پروتئینی مبتنی بر RBD دایمری با تکرار پشت سر هم نوترکیب (ZF2001) در برابر COVID{4}} در بزرگسالان: دو کارآزمایی تصادفی، دوسوکور، کنترل شده با دارونما، فاز 1 و 2. عفونت لانست دیس 2021، 21، 1107-1119. [CrossRef]
17. مالاپاتی، واکسن کووید DNA در جنوب هند اولین بار در جهان است، واکسن های بیشتری در راهند. طبیعت 2021، 597، 161-162. [CrossRef]
18. گریفونی، ع. ویسکوف، دی. رامیرز، SI; متئوس، جی. دان، جی.ام. Moderbacher، CR; Rawlings، SA; ساترلند، آ. پریمکومار، ال. Jadi، RS; و همکاران اهداف پاسخهای سلول T به ویروس SARS-CoV-2 در انسانهای مبتلا به بیماری کووید-19 و افراد در معرض تماس. Cell 2020, 181, 1489–1501.e1415. [CrossRef]
19. کائو، ی. زیر.؛ گوا، ایکس. سان، دبلیو. دنگ، ی. بائو، ال. زو، س. ژانگ، ایکس. ژنگ، ی. گنگ، سی. و همکاران آنتیبادیهای خنثیکننده قوی علیه SARS-CoV-2 شناسایی شده توسط توالییابی تک سلولی با توان بالای سلولهای B بیماران در حال نقاهت. Cell 2020, 182, 73-84.e16. [CrossRef]
20. امانت، ف. Krammer, F. SARS-CoV{2}} واکسن: گزارش وضعیت. مصونیت 2020، 52، 583-589. [CrossRef]
21. لی، ی. بی، ی. شیائو، اچ. یائو، ی. لیو، ایکس. هو، ز. دوان، جی. یانگ، ی. لی، ز. لی، ی. و همکاران یک فرمول جدید واکسن ترکیبی از DNA و پروتئین کووید-19 محافظت کاملی در برابر SARS-CoV-2 در ماکاکهای رزوس ارائه میکند. ظهور. میکروب ها عفونی می کنند. 2021، 10، 342-355. [CrossRef]
22. دو، ال. سلام.؛ ژو، ی. لیو، اس. ژنگ، بی جی؛ جیانگ، اس. پروتئین اسپایک SARS-CoV - هدفی برای توسعه واکسن و درمان. نات Rev. Microbiol. 2009، 7، 226-236. [CrossRef] [PubMed]
23. یو، ال. کائو، اچ. زی، تی. لانگ، آر. لی، اچ. یانگ، تی. یان، م. Xie, Z. پروتئین نوکلئوکپسید ناقص N پایانه SARS-CoV{3}} به عنوان یک نشانگر سرولوژیکی بهتر از پروتئین نوکلئوکپسید کامل در ارزیابی ایمنیزایی SARS-CoV غیرفعال شده-2. جی. مد. ویرول. 2021، 93، 1732-1738. [CrossRef] [PubMed]
24. گرینی، ای جی; لوس، AN; جنتلز، LE; کرافورد، KHD; ستاره، TN; مالون، KD; چو، HY; بلوم، JD واکسن SARS-CoV-2 mRNA-1273 باعث خنثیسازی بیشتر متمرکز بر RBD میشود، اما با اتصال آنتیبادی گستردهتر در RBD. bioRxiv 2021. [CrossRef]
25. مانتوس، جی. Nyhoff، LE; Kauffman، RC; Edara، VV; لای، ال. فلوید، ک. شی، پی. Menachery، VD; ادوپوگانتی، اس. شرر، EM; و همکاران ارزیابی پاسخهای سلولی و سرولوژیکی به عفونت حاد SARS-CoV-2 اهمیت عملکردی دامنه اتصال گیرنده را نشان میدهد. J. Immunol. 2021، 206، 2605-2613. [CrossRef]
26. او، ی. ژو، ی. لیو، اس. کو، ز. لی، دبلیو. فرزان، م. جیانگ، S. دامنه اتصال گیرنده پروتئین SARS-CoV، آنتی بادی های خنثی کننده بسیار قوی را القا می کند: مفهوم برای ایجاد واکسن زیر واحد. بیوشیمی. بیوفیز. Res. اشتراک. 2004، 324، 773-781. [CrossRef]
27. دنگ، س. لیانگ، اچ. چن، پی. لی، ی. لی، ز. فن، اس. وو، ک. لی، ایکس. چن، دبلیو. Qin، Y. و همکاران توسعه و کاربرد واکسن ناقل ویروسی در طول همه گیری کووید-19. Microorganisms 2022, 10, 1450. [CrossRef]
28. زو، اف سی; Guan، XH; لی، YH; هوانگ، جی. جیانگ، تی. Hou، LH; Li، JX; یانگ، BF; وانگ، ال. وانگ، WJ; و همکاران ایمنی زایی و ایمنی واکسن نوع آدنوویروس نوترکیب-5-ناقل کووید-19 در بزرگسالان سالم ۱۸ سال یا بالاتر: یک کارآزمایی تصادفی، دوسوکور، کنترل شده با دارونما، فاز ۲. Lancet 2020، 396، 479-488. [CrossRef]
29. لی، م. گوا، جی. لو، اس. ژو، آر. شی، اچ. شی، ایکس. چنگ، ال. لیانگ، کیو. لیو، اچ. وانگ، پی. و همکاران ایمن سازی تک دوز با واکسن مبتنی بر آدنوویروس شامپانزه باعث ایجاد ایمنی پایدار و محافظتی در برابر عفونت SARS-CoV-2 می شود. جلو. ایمونول. 2021, 12, 697074. [CrossRef]
30. گوا، ج. موندال، م. ژو، دی. توسعه واکسنهای جدید: ناقلهای آدنوویروسی شامپانزه. هوم واکسن Immunother. 2018، 14، 1679–1685. [CrossRef]
31. کانکو، ن. کو، اچ. بوکائو، جی. کشاورز، JR; آلارد-چمارد، اچ. ماهاجان، VS; Piechocka-Trocha، A. لفتری، ک. آزبورن، ام. بالز، جی. و همکاران از دست دادن Bcl-6-بیان سلول های کمکی فولیکولی T و مراکز ژرمینال در COVID-19. Cell 2020, 183, 143-157.e113. [CrossRef] [PubMed]
32. Lexberg، MH; تاوبنر، ا. آلبرشت، آی. Lepenies, I.; ریشتر، آ. کامرادت، تی. رادبروخ، ا. Chang، HD IFN- و IL-12 برای تبدیل Th17 تولید شده در داخل بدن به سلول های Th1/Th17 هم افزایی می کنند. یورو J. Immunol. 2010، 40، 3017–3027. [CrossRef] [PubMed]
33. لیو، جی. خو، ک. زینگ، ام. ژو، ی. گوا، جی. دو، م. وانگ، کیو. An، Y. لی، جی. گائو، پی. و همکاران ایمنسازیهای هترولوگ تقویتکننده اولیه با ناقلهای آدنوویروسی شامپانزه، ایمنی قوی و محافظتی در برابر عفونت SARS-CoV-2 ایجاد میکند. Cell Discov. 2021، 7، 123. [CrossRef] [PubMed]
