یک مدل پیشبینی اولیه برای بیماری مزمن کلیوی
Jul 17, 2023
خلاصه
بر اساس شیوع بالای بیماری مزمن کلیوی (CKD) در سالهای اخیر، یک مدل پیشبینی زودهنگام بهتر برای شناسایی افراد پرخطر قبل از وقوع نارسایی کلیه در مرحله نهایی (ESRD) مورد نیاز است. ما یک مطالعه مورد-شاهدی تودرتو را در 348 نفر (116 مورد و 232 فرد کنترل) از "کوهورت بیماریهای مزمن دانشگاه پزشکی تیانجین" انجام دادیم. همه آزمودنی ها در ابتدا CKD نداشتند و به مدت 5 سال تا 2 آگوست 18 0 پیگیری شدند. با استفاده از تحلیل رگرسیون چند متغیره کاکس، ما پنج عامل خطر غیر ژنتیکی مرتبط با خطرات CKD را پیدا کردیم. رگرسیون لجستیک برای انتخاب پلیمورفیسمهای تک نوکلئوتیدی (SNPs) که از تجزیه و تحلیل GWAS بانک زیستی بریتانیا و سایر پایگاههای داده بهدستآمدیم، انجام شد. ما از یک مدل رگرسیون لجستیک و وزندهی ارزش لگاریتم طبیعی برای ایجاد مدلهای پیشبینی خطر ژنتیکی/غیر ژنتیکی CKD استفاده کردیم. علاوه بر این، مدل پیشبینی جامع نهایی، مجموع حسابی دو مدل بهینه است. AUC مدل پیشبینی به 0.894 رسید، در حالی که حساسیت 0.827، و ویژگی 0.801 بود. ما دریافتیم که سن، دیابت و مقادیر بالای نرمال نیتروژن اوره، TGF- و ADMA عوامل خطر مستقل برای CKD هستند. یک مدل پیشبینی جامع نیز ایجاد شد، که ممکن است به شناسایی افرادی که احتمال ابتلا به CKD در مراحل اولیه را دارند کمک کند.

اینجا را کلیک کنید تا بدانید سیستانچ چه مزایایی دارد
معرفی
بیماری مزمن کلیه (CKD) به ویژه عوارض ناشی از آن، سلامت عمومی را در سراسر جهان تهدید جدی کرده است. نرخ جهانی مرگ و میر در تمام سنین ناشی از بیماری مزمن کلیه بین سالهای 1990 تا 20171 به میزان 41.5 درصد افزایش یافت. یک مطالعه مقطعی نشان داد که شیوع بیماری مزمن کلیوی در چین تقریباً 10.8 درصد بوده است. چین.
تا به امروز، برخی از عوامل خطر به شدت با بیماری مزمن کلیوی مرتبط هستند، از جمله سن 3، جنس زن 4، چاقی 5، و دیابت. اخیراً چندین بیومارکر مرتبط با CKD پیدا شده است. چند مطالعه قبلی نشان داده اند که افزایش سطوح ADMA (دی متیل آرژینین نامتقارن) می تواند باعث آسیب کلیوی شود. مطالعات متعدد نشان داده اند که ADMA یک نشانگر زیستی قدرتمند برای پیش بینی مرگ و میر ناشی از بیماری مزمن کلیه است. همچنین نشان داده شده است که سطوح بیان NFAL (لیپوکالین مرتبط با ژلاتیناز نوتروفیل) به نظر می رسد با درجه اختلال عملکرد کلیوی مرتبط است، که ممکن است به شناسایی بیماران در معرض خطر بالا برای کاهش سریعتر عملکرد کلیوی کمک کند. علاوه بر این، کاهش CysC سرم (سیستاتین C) با کاهش غلظت eGFR12 مرتبط است. حدس زده شده است که CysC می تواند همراه با کراتینین سرم به عنوان یک بیومارکر جدید یا به عنوان جایگزینی برای کراتینین سرم برای شناسایی بهتر بروز بیماری کلیوی در جمعیت عمومی استفاده شود. TGF- (تبدیل کننده رشد فاکتور) تنظیم کننده اصلی فیبروز بینابینی لوله ای است 15 و سیگنال دهی TGF می تواند بر چند پاسخ آسیب کلیوی مهم در سایر مسیرهای سیگنال دهی فاکتور رشد تأثیر بگذارد 16،17 و در نهایت بر شروع CKD18 تأثیر بگذارد. مطالعات قبلی گزارش داده اند که بیش از 50 پلی مورفیسم تک نوکلئوتیدی (SNPs) با شاخص های عملکرد کلیوی یا CKD در سراسر جهان مرتبط است.
The treatment of chronic kidney disease and renal failure is costly and rarely effective. However, less than 5% of patients with early CKD report awareness of their disease20. Once CKD can be diagnosed, glomerular damage has reached over 50% and is usually irreversible. Effective prediction of chronic kidney disease can be immensely useful in this aspect. Therefore, several CKD prediction models for different populations were21–24 introduced. Recently, a study developed equations for predicting CKD based on 34 multinational cohorts25. Nevertheless, few models have considered both genetic and nongenetic risk factors. Although many prediction models reached high prediction power in a relatively large population, early prediction [at least when eGFR>60 ml/(min·1.73 m2)] برای درمان و پیشگیری CKD ضروری است. در این مطالعه، ما مدلهای ژنتیکی، غیر ژنتیکی (از جمله نشانگرهای زیستی) و پیشبینی امتیاز خطر جامع برای CKD را در یک مطالعه مورد-شاهدی تودرتو ایجاد کردیم.

سیستانچه توبولوزا
بحث
پیشبینی اولیه CKD چالش برانگیز است. دهه ها تحقیق نشان داده است که نفروپاتی دیابتی، گلومرولونفریت اولیه، فشار خون بالا، نفریت بینابینی و کلیه پلی کیستیک همگی می توانند باعث ایجاد CKD شوند. آگاهی از بیماری مزمن کلیه بسیار کم است. پس از ایجاد CKD، درمان معمولاً تا زمانی که آخرین درمان دیالیز و پیوند کلیه برای ESRD مورد نیاز نباشد، محدود میشود. eGFR یک شاخص حساس عملکرد کلیه است. با این حال، این یک پیش بینی کننده اولیه CKD نیست. اگرچه بسیاری از نشانگرهای زیستی برای CKD آزمایش شده اند، ارزیابی مجدد در مطالعات کوهورت آینده نگر با حجم نمونه بزرگ مورد نیاز است. به دنبال یک مدل پیشبینی زودهنگام، حساس، آسان و مقرونبهصرفه.
ما یک مطالعه مورد-شاهدی تودرتو برای پیشبینی CKD از "همگروه بیماری مزمن دانشگاه پزشکی تیانجین" 26،27 انجام دادیم، با مناسبت قوی، پیشبینی آسان 5-سال احتمال شروع بیماری مزمن کلیوی در این ناحیه. . میانگین سنی افراد مورد مطالعه 63 سال بود. بنابراین، این افراد بیشتر از افراد جوانتر به CKD مبتلا می شوند.
ما شاخصهای آزمایشگاهی سنتی، نشانگرهای زیستی متعدد مرتبط با عملکرد کلیه و جایگاههای SNP را برای توسعه مدلهای پیشبینی CKD ترکیب کردیم. در مدل NGRS، ما نه تنها برخی از شاخصها را که در مطالعات دیگر مورد استفاده قرار گرفتند، مانند دیابت و سن 25، 28، 29، وارد کردیم، بلکه چندین نشانگر زیستی، بهویژه TGF- و ADMA نیز بهعنوان پیشبینیکنندههای اولیه CKD در مدل مورد استفاده قرار گرفتند.
اگرچه صدها ارتباط بین CKD و ژنهای حساسیت پیدا شد، GWAS با اندازه نمونه بزرگ نیز نتایج بسیار مهمی به همراه داشت و عوامل ژنتیکی فقط کمی بهبود مدل پیشبینی را ارائه کردند. با توجه به SNP خاص، خطر نسبی ژنتیکی (GRR) می تواند بالا باشد. با این حال، سهم آن در خطرات CKD در جمعیت عمومی محدود بود. همه 17 SNP به کار گرفته شده در مطالعه ما از GWAS های خارج از Biobank انگلستان و سایر گروه های بزرگ بودند. با این حال، AUC مدل خطر ژنتیکی (GRS) تنها 0.643 بود و فقط یک بهبود حاشیه ای در AUC در مدل جامع ایجاد کرده بود (از 0}.889 تا 0 .894). مطالعهای در ژاپن نشان داد که پیشبینیکنندههای ژنتیکی کمک قابلتوجهی به بهبود کارایی پیشبینی مدل پیشبینی جامع ندارند. اگرچه SNP های خاصی با CKD در GWAS های با اندازه نمونه بزرگ (یعنی خطر نسبی ژنتیکی بالا، GRR) ارتباط بسیار مهمی با CKD داشتند، سهم آنها در واریانس فنوتیپ ممکن است محدود باشد.
چندین نشانگر زیستی مورد آزمایش قرار گرفتند و در مدل پیشبینی ما گنجانده شدند. سطح TGF پلاسما، به تنهایی با ADMA، ارزش پیشبینی بهتری نسبت به نشانگر فیلتراسیون گلومرولی مستقیمتر سیستاتین C ارائه میدهد. در مطالعه قبلی ما، دریافتیم که ژنهای مسیر TGF در کلیههای نفروپاتی دیابتی در مراحل اولیه بسیار بیان میشوند. بیوپسی کلیه، مدتها قبل از فیبروز کلیه و کاهش فیلتراسیون رخ داده است. در واقع، غربالگری نشانگرهای زیستی اولیه قبل از کاهش eGFR ممکن است چندین سال زودتر پیشبینی CKD را ارائه دهد، اگرچه درمان زودهنگام میتواند مانع دیگری برای غلبه بر آن باشد.
این مطالعه دارای چند محدودیت است. ابتدا، تحقیق روی نشانگرهای زیستی مرتبط با بیماری مزمن کلیه در یک مطالعه مورد-شاهدی تودرتو انجام شد که از گروهی از بیماریهای مزمن انتخاب شد و حجم نمونه نسبتاً کوچک بود. بنابراین، نتایج حاصل از مطالعه ممکن است دارای انحرافات خاصی باشد. دوم، مدل پیشبینی خطر ما فقط بر شروع بیماری مزمن کلیوی متمرکز بود، اما پیشرفت بیماری مزمن کلیوی به نارسایی کلیوی یا سایر عوارض را ارزیابی نکرد. سوم، شرکتکنندگانی که «کوهورت بیماریهای مزمن دانشگاه پزشکی تیانجین» را تشکیل میدادند، بیشتر معلمان و کارمندان دولت بودند که در مناطق شهری کار میکردند. این دسته از افراد دارای نظم و انضباط بیشتری بودند و به سلامت توجه بیشتری داشتند. اینکه آیا مدل پیشبینی ما میتواند برای گروههای دیگر از مردم اعمال شود، نیاز به اعتبار خارجی بیشتری دارد. مطالعات آتی ما نشانگرهای زیستی مرتبط با عملکرد کلیوی بیشتری را در گروههای بزرگتر شناسایی خواهد کرد تا مدل پیشبینی CKD را تأیید و بهبود بخشد.
اخیراً مدلهای پیشبینیکننده متعددی ایجاد شده و در کلینیک برای تصمیمگیری مورد استفاده قرار گرفتهاند. در میان آنها، چندین مدل وجود دارد که خطر ابتلا به CKD22،28-31 را برآورد می کند. با این حال، به دلیل تفاوت در نژاد، سبک زندگی، و محیط جغرافیایی، هنوز هم لازم است یک مدل پیشبینیکننده موثر برای بیماری مزمن کلیوی در گروههای قومی مختلف ایجاد شود، که میتواند به شناسایی زودهنگام افراد مبتلا به بیماری مزمن کلیه کمک کند، در نتیجه مراقبتهای بهداشتی را بهبود میبخشد. تخصیص منابع به افرادی که بیشتر از آن سود می برند و در عین حال از سوء استفاده بالقوه از منابع مراقبت های بهداشتی توسط افرادی که در معرض خطر هستند جلوگیری می کند.

عصاره سیستانچ
مواد و روش ها
1. طرح مطالعه و جمعیت.
این تحقیق بهعنوان یک مطالعه مورد-شاهدی تودرتو با 348 شرکتکننده از «کوهورت بیماریهای مزمن دانشگاه پزشکی تیانجین» طراحی شد. این کوهورت در سال 2006 با تعداد اولیه 2068 نفر برای معاینه فیزیکی سالانه تاسیس شد. تا پایان سال 2018، در مجموع 21750 نفر به این گروه جذب شدند که طولانی ترین دوره پیگیری 13 سال بود. ما نشانگرهای جمعیت شناختی، نشانگرهای آزمایشگاهی، و نتایج ژنوتیپ را برای 110 جایگاه (شامل 380 مورد با داده های ژنوتیپ ژنومی) جمع آوری کردیم. ما بیمارانی را که معیارهای زیر را داشتند غربال کردیم: (من) با یک دوره پیگیری حداقل 5 ساله. (ii) عدم وجود CKD در اولین معاینه فیزیکی. (iii) نمونه خون و سایر اطلاعات مهم که در میان آنها 1804 واجد شرایط بودند. 116 نفر به عنوان گروه مورد انتخاب شدند. و 232 نفر به عنوان گروه کنترل با تطابق جنس و سن 3± سال انتخاب شدند. بنابراین، در مجموع 348 نفر وارد شدند. همه افراد سابقه خانوادگی بیماری های ارثی و مصرف داروهای نفروتوکسیک را انکار کردند.
این مطالعه توسط کمیته اخلاق دانشگاه پزشکی تیانجین مورد بررسی و تایید قرار گرفت و همه شرکت کنندگان فرم های رضایت آگاهانه را امضا کردند.
2. معیارهای تشخیصی.
معیارهای تشخیصی CKD eGFR بود<60 mL/(min·1.73 m2 ) or positive proteinuria (≥1+). The glomerular filtration rate is estimated using the simplified Chinese MDRD equation 32. The determination of diabetes mellitus (DM) is based on the diagnostic criteria of diabetes published by the World Health Organization (WHO) in 1999: fasting plasma glucose≥7.0 mmol/L and/or 2 h postprandial glucose≥11 mmol/L. Obesity was defined as a body mass index (BMI)≥28 kg/m2 according to the recommendation of the "Guidelines for the Prevention and Control of Overweight and Obesity among Chinese Adults"33 by the Ministry of Health. Hypertension was defined as systolic blood pressure (SBP)≥140 mmHg and/or diastolic blood pressure (DBP)≥90 mmHg or a self-reported history of physician-diagnosed hypertension. The diagnostic criteria for hyperuricemia (HUA)34 were blood uric acid levels≥420 μmol/L in men and≥360 μmol/L in women.
3. اندازه گیری نشانگرهای زیستی.
پس از دوازده ساعت ناشتایی، نمونههای خون وریدی شرکتکنندگان در ساعت 7:30 تا 9:30 صبح در لولههای خونگیری غیرضد انعقاد جمعآوری شد، به مدت نیم ساعت در دمای اتاق انکوبه شد و سپس با سرعت 3000 دور در دقیقه در 4 درجه سانتریفیوژ شد. به مدت 10 دقیقه تا سرم جدا شود. سرم قبل از تجزیه و تحلیل در دمای 80- درجه نگهداری شد. سطوح گلوکز پلاسما ناشتا، کراتینین سرم، نیتروژن اوره، اسید اوریک سرم، کلسترول تام، تری گلیسیرید، آلانین آمینوترانسفراز، پروتئین کل، آلبومین، گلوبولین، بیلی روبین تام و بیلی روبین مستقیم با استفاده از آنالایزر بیوشیمیایی خودکار هیتاچی تعیین شد. سیستاتین C (CysC)، فاکتور رشد تبدیل بتا (TGF-)، دی متیل آرژینین نامتقارن (ADMA) و لیپوکالین مرتبط با ژلاتیناز نوتروفیل (NGAL) توسط کیت های ELISA (شرکت بیوتکنولوژی شانگهای هویو، LTD) اندازه گیری شد.

پودر سیستانچ
4. انتخاب عوامل خطر غیر ژنتیکی/ژنتیکی مرتبط با CKD.
ما 21 عامل خطر بالقوه، از جمله چندین نشانگر زیستی، را در مدل خطر متناسب کاکس تک متغیره وارد کردیم، و سپس عوامل مهم به عنوان متغیرهای توضیحی در نظر گرفته شد و در مدل رگرسیون خطر متناسب کاکس چند متغیره گنجانده شد. در نهایت، پنج عامل خطر غیر ژنتیکی را به دست آوردیم. پس از به دست آوردن بخشی از دسترسی به داده ها به پایگاه داده UK-Biobank، ما از PLINK برای انجام تجزیه و تحلیل ارتباط ژنومی (GWAS) برای شاخص های مرتبط با عملکرد کلیه، از جمله eGFR، SCr، و CysC استفاده کردیم. نتایج GWAS در نمودار منهتن نشان داده شده است (شکل S1 تکمیلی). همراه با نتایج مطالعات قبلی، در مجموع 10 جایگاه SNP روی 10 ژن غربالگری شد (جدول تکمیلی S1). در همین حال، پس از ادغام اطلاعات از پایگاههای داده GWAS، پایگاه دادههای بیوانفورماتیک ژنومیک UCSC و نتایج GWAS برای فنوتیپهای مرتبط با عملکرد کلیه در آسیا یا چین 35-37، جایگاههای SNP با خطر نسبی ژنوتیپ بالا (GRR) و امتیاز پلی ژنتیکی گسترده ژنوم (GPS) ) برای CKD انتخاب شدند. در نهایت، ما در مجموع 27 جایگاه SNP از 24 ژن را برای ساخت یک مدل خطر ژنتیکی برای CKD انتخاب کردیم (جدول S2 تکمیلی). 27 SNP انتخاب شده در این مطالعه در 348 فرد مورد-شاهد تو در تو با استفاده از پلت فرم طیف سنجی جرمی زمان پرواز یونیزاسیون دفعی لیزر (MALDI-TOF-MS) به کمک ماتریس ژنوتیپ شدند. تعادل هاردی واینبرگ (HWE) برای همه 27 SNP بررسی شد و ما 2 SNP را که HWE ناموفق بودند حذف کردیم. بنابراین، داده های ژنوتیپ برای 25 SNP ثبت شد.
5. توسعه مدل های پیش بینی.
در این مطالعه، مدلهای امتیاز ریسک ژنتیکی (GRS) و مدلهای امتیاز ریسک غیر ژنتیکی (NGRS) از وزن لگاریتمهای طبیعی ( ) مقادیر OR عوامل خطر مختلف ساخته شدند. اثرات ترکیبی هر یک از عوامل غیر ژنتیکی یا ژنتیکی به روش وزنی محاسبه شد و روش ترکیبی بهینه برای توسعه مدل پیشبینی CKD انتخاب شد. معادله GRS بر اساس مشارکت های مختلف هر مکان نامزد SNP در پاتوژنز CKD ایجاد شد. هر سایت SNP یک عامل خطر بالقوه برای CKD در نظر گرفته شد. وزن های مختلف برای مشارکت در شروع CKD با مقادیر مختلف OR (یا) از تجزیه و تحلیل رگرسیون لجستیک برای ایجاد چندین ترکیب و غربالگری برای ترکیب بهینه تعیین شد. با استفاده از یک امتیاز خطر ژنتیکی وزنی (ωGRS)، ωGRS{{0}} I 1 iGi (i وزن I امین SNP است، Gi تعداد آلل ها در SNP من است و مقدار 0 را اختصاص می دهد، 1، 2). وزن لگاریتم طبیعی نسبت شانس (OR) SNP ها است و می تواند یک اثر تخمینی (ضریب) باشد. برای هر فرد، ωGRS مجموع تعداد آلل های خطر وزن شده با مقدار OR () هر سایت SNP در رگرسیون لجستیک است. برای جزئیات بیشتر به فرمول (1) مراجعه کنید.

در فرمول فوق، برای تثبیت وزن از قبل، از مقدار آللهای تک ریسکی تبدیلشده با لگاریتم در مطالعات با حجم نمونه بزرگ و قابلیت اطمینان بالا (مثلاً متاآنالیز) به عنوان وزن در ساخت مدل واقعی استفاده کردیم. اصل ساختمان مدل امتیاز ریسک غیر ژنتیکی همان GRS است. یعنی، با توجه به سهم متفاوت عوامل خطر غیر ژنتیکی مرتبط با CKD شناسایی شده (به عنوان مثال، مقدار طبیعی بالای TGF-، افراد مسن) در بروز CKD، مقادیر مختلف OR (یا) تجزیه و تحلیل رگرسیون لجستیک استفاده می شود. تعیین وزن های مختلف برای شروع CKD، ایجاد ترکیبات مختلف و انتخاب ترکیب بهینه. امتیاز خطر غیر ژنتیکی وزنی (ωNGRS) استفاده شد، ωNGRS= I 1 iSi (i وزن یکمین عامل خطر غیر ژنتیکی مربوطه در خطر ابتلا به CKD است، و Si یکمین عامل خطر غیر ژنتیکی مربوطه است). و وزن، لگاریتم طبیعی مقدار OR را می گیرد که با تجزیه و تحلیل رگرسیون لجستیک عوامل خطر مختلف به دست آمده است. برای هر فرد، ωNGRS مجموع عوامل خطر وزن شده با ارزش OR () عوامل خطر غیر ژنتیکی مختلف در رگرسیون لجستیک است. برای جزئیات بیشتر به فرمول (2) مراجعه کنید.
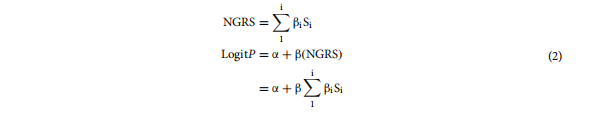
در فرمول بالا، S نشان دهنده مجموعه بردار گروهی از عوامل خطر غیر ژنتیکی است (Si نشان دهنده وضعیت یکمین عامل خطر غیر ژنتیکی است؛ اگر فرد عامل خطر را داشته باشد، مقدار 1 است، اگر نه، مقدار {{ 1}}). ارزش مورد استفاده در این مطالعه، ارزش هر یک از عوامل خطر غیر ژنتیکی در تحلیل رگرسیون لجستیک بود.
ساخت مدل جامع امتیازدهی ریسک، مدل بهینه GRS و مدل NGRS را که مجموع این دو مدل است، ادغام می کند. برای جزئیات بیشتر به فرمول (3) مراجعه کنید.

6. ارزیابی مدل پیش بینی.
ارزیابی مدل GRS ساخته شده، مدل NGRS، و مدل پیشبینی جامع، ناحیه منحنی مشخصه عملکرد گیرنده (ROC) را تحت روش منحنی (AUC) اتخاذ کرد. از نرم افزار MedCalc برای تعیین نقطه برش بهینه منحنی ROC و حساسیت و ویژگی در نقطه برش بهینه استفاده شد. در نهایت، ارزیابی اثربخشی پیشبینی مدل پیشبینی CKD ساخته شده محقق میشود. مدل GRS ساختهشده، مدل NGRS و مدل پیشبینی جامع بهصورت داخلی در یک مطالعه موردی-شاهدی تودرتو با استفاده از اعتبارسنجی متقاطع پنج برابری بوت استرپ تأیید شدند. تجزیه و تحلیل تمامی داده ها با استفاده از نرم افزار SPSS 21.{6}} انجام شد. اهمیت آماری با مقدار آستانه P تعیین شد<0.05.
تمامی روش ها بر اساس دستورالعمل ها و مقررات مربوطه انجام شد.

کپسول سیستانچ
نتیجه
سن، دیابت، مقادیر بالای کراتینین طبیعی، TGF- و ADMA شاخص های مستقلی برای بروز CKD هستند. یک مدل پیشبینی جامع ایجاد شد، اگرچه عوامل ژنتیکی که در مطالعه ما تجزیه و تحلیل شد، مقادیر پیشبینی محدودی را برای بروز CKD به همراه داشت. برای جلوگیری از بدتر شدن و حتی غیرقابل برگشت شدن، می توان مداخله زودهنگام و مناسب را انجام داد.
منابع
1. Bikbov، B. et al. بار جهانی، منطقه ای و ملی بیماری مزمن کلیوی، 1990-2017: تجزیه و تحلیل سیستماتیک برای مطالعه بار جهانی بیماری 2017. Lancet 395، 709 (2020).
2. Zhang، L. و همکاران. شیوع بیماری مزمن کلیه در چین: یک بررسی مقطعی Lancet 379, 815 (2012).
3. O'Sullivan، ED، Hughes، J. & Ferenbach، DA پیری کلیه: علل و پیامدها. مربا. Soc. نفرول. 28, 407 (2017).
4. Carrero, JJ, Hecking, M., Chesnaye, NC & Jager, KJ نابرابری های جنسیتی و جنسیتی در اپیدمیولوژی و پیامدهای بیماری مزمن کلیوی. نات کشیش نفرول. 14, 151 (2018).
5. یون، HR و همکاران. چاقی، ناهنجاری متابولیک و پیشرفت CKD. صبح. جی. کلیه دیس. 72, 400 (2018).
6. تسای، دبلیو و همکاران. عوامل خطر برای ایجاد و پیشرفت بیماری مزمن کلیوی. پزشکی 95, e3013 (2016).
7. فلیزر، دی و همکاران. دی متیل آرژینین نامتقارن و پیشرفت بیماری مزمن کلیه: مطالعه بیماری کلیوی خفیف تا متوسط مربا. Soc. نفرول. 16, 2456 (2005).
8. روانی، ص و همکاران. دی متیل آرژینین نامتقارن پیشرفت به دیالیز و مرگ را در بیماران مبتلا به بیماری مزمن کلیوی پیش بینی می کند: رویکرد مدل سازی ریسک های رقابتی. مربا. Soc. نفرول. 16, 2449 (2005).
9. میازاکی، اچ و همکاران. مهارکننده نیتریک اکسید سنتاز درون زا: یک نشانگر جدید آترواسکلروز. تیراژ 9، 1141 (1999).
10. تریپپی، جی و همکاران. التهاب و دی متیل آرژینین نامتقارن برای پیش بینی مرگ و حوادث قلبی عروقی در بیماران ESRD کلین مربا. Soc. نفرول. 6, 1714 (2011).
11. Viau, A. et al. لیپوکالین 2 برای پیشرفت بیماری مزمن کلیوی در موش و انسان ضروری است. جی. کلین. تحقیق کنید 120, 4065 (2010).
12. Ferguson, MA & Waikar, SS نشانگرهای ایجاد و در حال ظهور عملکرد کلیه. کلین شیمی. 58, 680 (2012).
13. فیلر، جی و همکاران. سیستاتین C به عنوان نشانگر GFR - تاریخچه، نشانه ها و تحقیقات آینده. کلین بیوشیمی. 38، 1 (2005).
14. Ferguson, TW, Komenda, P. & Tangri, N. Cystatin C به عنوان نشانگر زیستی برای تخمین میزان فیلتراسیون گلومرولی. Curr. نظر. نفرول. فشار خون بالا 24, 295 (2015).
15. Meng, X., Nikolic-Paterson, DJ & Lan, HY TGF-: تنظیم کننده اصلی فیبروز است. نات کشیش نفرول. 12, 325 (2016).
16. Tazat, K., Hector-Greene, M., Blobe, GC & Henis, YI Tibetan به طور مستقل گیرنده های TGF-beta نوع I و II را برای مهار سیگنالینگ TGF-بتا متصل می کند. مول. Biol. سلول 26, 3535 (2015).
17. Wang, S., Wilkes, MC, Leof, EB & Hirschberg, R. Noncanonical TGF- مسیرهای mTORC1 و Abl در فیبروژنز بینابینی کلیوی. صبح. جی. فیزیول. Renal 298, F142 (2010).
18. Nlandu-Khodo، S. et al. مسدود کردن تداخل اپیتلیال TGF-بتا و بتا-کاتنین باعث تشدید CKD می شود. مربا. Soc. نفرول. 28, 3490 (2017).
19. O'Seaghdha، CM & Fox، CS مطالعات ارتباط ژنوم گسترده در پیوند کلیه: مزایا و محدودیت ها. نات کشیش نفرول. 8، 89 (2011).
20. Chen, TK, Knicely, DH & Grams, ME تشخیص و مدیریت بیماری مزمن کلیه. JAMA 322, 1294 (2019).
21. Carrillo-Larco، RM و همکاران. امتیاز خطر برای اولین غربالگری بیماری مزمن کلیوی شایع تشخیص داده نشده در پرو: امتیاز خطر Te CRONICASCKD. BMC Nephrol. 18, 343 (2017).
22. تنگری، ن. و همکاران. یک مدل پیشبینی پویا برای پیشرفت CKD صبح. جی. کلیه دیس. 69, 514 (2017).
23. Ma, J., Yang, Q., Hwang, S., Fox, CS & Chu, AY امتیاز خطر ژنتیکی و خطر بیماری مزمن کلیوی مرحله 3. BMC Nephrol. 18, 32 (2017).
24. ایمای، ای و همکاران. شیوع بیماری مزمن کلیوی در جمعیت عمومی ژاپن کلین انقضا نفرول. 13, 621 (2009).
25. نلسون، آر جی و همکاران. توسعه معادلات پیشبینی خطر بیماری مزمن کلیوی JAMA 322, 2104 (2019).
26. ژائو، جی و همکاران. تری گلیسیرید یک پیشبینیکننده مستقل دیابت نوع 2 در میان بزرگسالان میانسال و مسنتر است: یک مطالعه آیندهنگر با پیگیری 8-سال در دو گروه. J. Transl. پزشکی 17, 403 (2019).
27. وی، اف و همکاران. ارتباط بین اسید اوریک سرم و بروز فشار خون: یک مطالعه کوهورت دینامیک ارشد چینی. J. Transl. پزشکی 14, 110 (2016).
28. Chien، K. و همکاران. یک مدل پیشبینی برای خطر بروز بیماری مزمن کلیوی صبح. جی. مد. 123, 836 (2010).
29. O'Seaghdha, CM et al. امتیاز خطر بیماری مزمن کلیه در جمعیت عمومی. صبح. جی. مد. 125، 270 (2012).
30. مدل های خطر Echoufo-Tcheugui، JB & Kengne، AP برای پیش بینی بیماری مزمن کلیوی و پیشرفت آن: یک بررسی سیستماتیک. PLoS Med. 9, e1001344 (2012).
31. فوجی، آر و همکاران. ارتباط امتیاز خطر ژنتیکی و بیماری مزمن کلیوی در جمعیت ژاپنی نفرولوژی 24، 670 (2019).
32. Ma، YC و همکاران. بهبود تخمین GFR با ترکیب اندازه گیری کراتینین و سیستاتین C. کلیه بین المللی 72، 1535 (2007).
33. قاسم، ع و همکاران. در مورد منشا چاقی: شناسایی محرک های بیولوژیکی، محیطی و فرهنگی خطر ژنتیکی در بین جمعیت های انسانی. چاق ها Rev. 19, 121 (2018).
34. Bardin, T. & Richette, P. تعریف هیپراوریسمی و شرایط نقرس. Curr. نظر. روماتول. 26, 186 (2014).
35. اوکادا، ی و همکاران. متاآنالیز جایگاه های متعدد مرتبط با صفات مرتبط با عملکرد کلیه را در جمعیت های شرق آسیا شناسایی می کند. نات ژنت 44, 904 (2012).
36. O'Seaghdha، CM & Fox، CS مطالعات ارتباط ژنومی بیماری مزمن کلیوی: ما چه آموخته ایم؟ نات کشیش نفرول. 8، 89 (2011).
37. Ried, JS et al. یک متاآنالیز مؤلفه اصلی بر روی صفات تنسنجی چندگانه، جایگاههای جدیدی را برای شکل بدن شناسایی میکند. نات اشتراک. 7, 13357 (2016).
Jing Zhao1,4, Yuan Zhang1,2,4, Jiali Qiu1,4, Xiaodan Zhang1,4, FengjiangWei1, Jiayi Feng1, Chen Chen3, Kai Zhang3, Shuzhi Feng3, Wei-Dong Li1
1 گروه ژنتیک، کالج علوم پزشکی پایه، دانشگاه پزشکی تیانجین، تیانجین 300070، چین.
2 دانشکده بهداشت عمومی، دانشگاه پزشکی تیانجین، تیانجین، چین.
3 بیمارستان عمومی تیانجین، دانشگاه پزشکی تیانجین، تیانجین 300052، چین.
4 این نویسندگان به طور مساوی کمک کردند: جینگ ژائو، یوان ژانگ، جیالی کیو، و شیائودان ژانگ






