تصویربرداری واضح و کمی کردن کلیه در سه بعدی
Feb 27, 2022
برای چندین دهه، اندازه گیری هایکلیهمیکروآناتومی با استفاده از بخشهای 2-بعدی، دانش دقیقی را در اختیار ما قرار داده است کلیه مورفولوژی تحت شرایط فیزیولوژیکی و پاتولوژیک. با این حال، توسعه سریع روشهای پاکسازی بافت در سالهای اخیر، در ترکیب با توسعه روشهای جدید تصویربرداری {{0}بعدی، بینش جدیدی را در موردکلیهساختار و عملکرد این مقاله مروری طیف وسیعی از بینشهای بدیع را شرح میدهدکلیهتوسعه و بیماری اخیراً با استفاده از این رویکردهای روش شناختی جدید به دست آمده است. به عنوان مثال، در حال توسعهکلیهاین رویکردها درک جدیدی از مورفوژنز انشعاب حالب، تکثیر و تعهد سلول های پیش ساز نفرون، تعاملات بین سلول های نوک حالب و سلول های پیش ساز نفرون، و ایجاد تقسیم بندی نفرون ارائه کرده اند. در کل موش بالغکلیه هاپاکسازی بافت همراه با میکروسکوپ ورقه ای نوری می تواند تعداد کل گلومرول ها را تصویربرداری و کمیت کند که یک پیشرفت بزرگ در این زمینه است. رویکردهای مشابه، بینش جدیدی را در مورد ساختار عروق کلیوی و عصب، بازسازی لولههای بینابینی، از دست دادن سلولهای بدن و هیپرتروفی، تشکیل کیست، تکامل هلالهای سلولی، و ساختار سد فیلتراسیون گلومرولی ارائه کردهاند. پیشرفت های بسیار بیشتر در درککلیهزیست شناسی و آسیب شناسی را می توان انتظار داشت زیرا تکنیک های پاکسازی و تصویربرداری اضافی توسط محققان بیشتری توسعه یافته و به کار گرفته می شوند.
کلید واژه ها:تصویربرداری سه بعدی؛ گلومرول؛ رشد کلیه؛ نفروپاتولوژی؛ پاکسازی بافت؛ لوله ها کلیه

CISTANCHE عملکرد کلیه/کلیه را بهبود می بخشد
تعداد نفرون کل در هر انسان عادیکلیهاز حدود 200،000 تا بیش از 2 میلیون، 1 به طور متوسط تقریباً 1 میلیون متغیر است. این نفرون ها و همچنین سایر اجزای تشکیل دهندهکلیهاز جمله مجاری جمع آوری، رگ های خونی، بینابینی، و رشته های عصبی با دقت میکروآناتومیکی عالی مرتب شده اند. 2 این الگوبرداری دقیق زیربنای عادی استعملکرد کلیهو سلامتی که در صورت تغییر ساختار بافت به دلیل هیپرتروفی یا انقباض گلومرولی یا لولهای، از دست دادن نفرون، ناهنجاریهای مادرزادی، نادر شدن عروق و فیبروز بینابینی میتواند به شدت مختل شود. طیف وسیعی از رویکردهای تصویربرداری به درک جامع ما از این موضوع کمک کرده استکلیهمیکروآناتومی در طول رشد و در بزرگسالان سالم و بیمارکلیه. در بیشتر موارد، این درک از تجزیه و تحلیل بخشهای 2-بعدی (2 بعدی) حاصل شده است، خواه بخشهای فیزیکی میکروسکوپی نور یا الکترونی باشند یا بخشهای نوری هم کانونی. کمی سازی این میکروآناتومی بیشتر به تجزیه و تحلیل های استریولوژیکی بخش هایی بستگی دارد که تخمین هایی از تعداد، طول ها، مساحت سطح و حجم گلومرول ها، لوله ها، عروق، بینابینی و اجزای سلولی آنها ارائه کرده است. 3،4 تا همین اواخر، تجسم سه بعدی ازکلیهریزساختار تا حد زیادی به میکروسکوپ کانفوکال محدود شده بود، که برش نوری و بازسازی سه بعدی را تا عمق 50 تا 80 متر متر ممکن میسازد. متأسفانه، خواص انکساری پروتئین و اجزای چربی در بافت، نور را پراکنده می کند و با افزایش عمق، کیفیت تصویر را به شدت کاهش می دهد. در سالهای اخیر، طیف وسیعی از روشهای پاکسازی برای حذف محتوای چربی و رنگدانه بافت و مطابقت با خواص انکساری بافت و محیطهای نصب برای شفاف کردن بافت ایجاد شده است. 5 روش های پاکسازی از نظر پیچیدگی از انکوباسیون بافت در محلول های مختلف در طی چند ساعت تا روش های طولانی شامل تجهیزات الکتروشیمیایی سفارشی متغیر است. ما خوانندگان را به بررسی های اخیر 5،6 برای مروری دقیق از روش های فعلی و مقالات ذکر شده در اینجا برای روش های خاص و موارد استفاده هدایت می کنیم.
ساختارهای درون سلولی و کل جمعیت سلول ها را می توان در اندام های کامل پاک شده یا بخش های ضخیم حل کرد. تصویربرداری دقیق از ویژگیهای بافت پاکشده، نیازمند میکروسکوپهای تخصصی و پردازش تصویر برای گرفتن و بازسازی دادههای حجمی از نمونههایی است که اندازه آنها از صدها میکرون تا سانتیمتر متغیر است. میکروسکوپ های کانفوکال دیسک اسکن نقطه ای و چرخاندن به طور موثری برای تصویربرداری از ویژگی های پاک شده استفاده شده اند.کلیهبافت اما از کاهش وضوح در محور Z و کاهش تدریجی شدت فلورسانس در عمق به دلیل یک محور روشنایی و تصویربرداری رنج میبرد. تکنیکهای میکروسکوپ ورقهای نوری بهویژه برای تصویربرداری از بافتهای پاکشده مناسب هستند، زیرا امکان دستیابی سریع حجمهای سه بعدی بزرگ را فراهم میکنند و میتوانند شامل روشنایی و تصویربرداری چند زاویهای باشند. توموگرافی پروجکشن اپتیکال روش دیگری است که شامل تصویربرداری چند زاویه ای و بازسازی دیجیتال برای تولید داده هایی است که در آن محورهای X، Y و Z هر وکسل وضوح یکسانی دارند. صرف نظر از رویکرد خاص، پاکسازی بافت و تصویربرداری کل مانت فرصت جدیدی برای کشف ریزمحیطهای سلولی ناشناخته و ساختار بافتی درجه بالاتر فراهم میکند. در این بررسی، برخی از بینش های جدید را برجسته می کنیمکلیهرشد، بزرگسالکلیهساختار، و آسیب شناسی که از پاکسازی بافت به دنبال آنالیز کمی سه بعدی حاصل شده است.
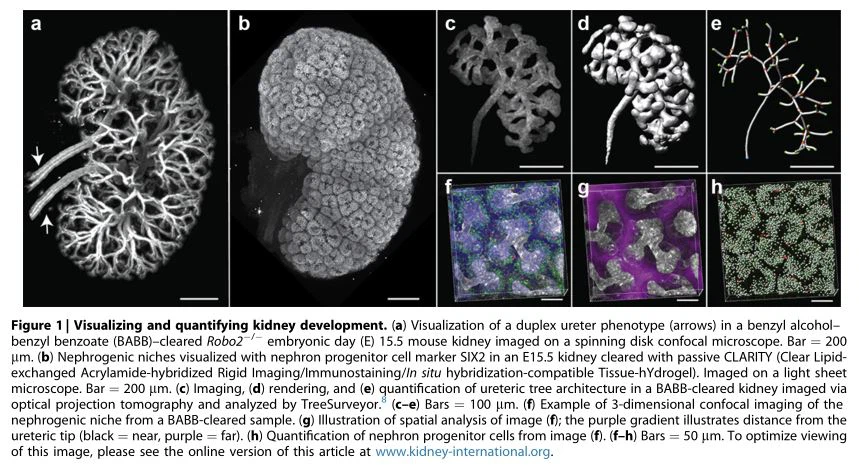
بینش جدید در مورد رشد کلیهدههها پروفایل بیان ژن و مطالعات حذفی منجر به درک دقیق انواع سلول، شبکههای تنظیمکننده ژن و مسیرهای سیگنالی که پستانداران را کنترل میکنند، شده است.کلیهتوسعه. این دانش به تشخیص بیماری مادرزادی کمک کرد و تولید آن را امکان پذیر کردکلیهانواع سلول از سلول های بنیادی پرتوان 7 با این حال، اندازه، کدورت، و پیچیدگی در حال توسعهکلیهمانع مهمی برای اندازهگیری دقیق مورفوژنز این اندام و توزیع سه بعدی سلولها و پروتئینها در آن است. کاربرد پاکسازی بافت و تصویربرداری چند مقیاسی درکلیهتجسم و تجزیه و تحلیل کمی مورفوژنز انشعاب حالب، جمعیت سلول های پیش ساز و وقف نفرون در اندام های دست نخورده را فعال کرده است (شکل 1). 8 این رویکردها ظرفیت جدیدی را برای فنوتیپ کردن دقیق و راه های باز برای تجزیه و تحلیل محرک های سلولی و مولکولی ایجاد می کند.کلیهرشد و بیماری مادرزادی
تصویربرداری و تجزیه و تحلیل مورفوژنز انشعاب در سه بعدیاستقرار درخت حالب یکی از ویژگی های تعیین کننده استکلیهتوسعه و به طور گسترده با استفاده از ژنتیک موش و مسطح مورد مطالعه قرار گرفته استکلیهکشت های ریزنمونه ای با این حال، درک اینکه چگونه ژنهای منفرد در رشد، شکل و الگوی این ساختار مجرای اپیتلیال منشعب در داخل بدن نقش دارند، نیاز به ظرفیت تصویربرداری و تجزیه و تحلیل این شبکه پیچیده در طیف وسیعی از اندازههای نمونه دارد. شورت و همکاران 8 با استفاده از ایمونوفلورسانس کل کوه، پاکسازی مبتنی بر حلال (بنزیل الکل بنزیل بنزوات) و تصویربرداری از کل اندام ها با توموگرافی پروجکشن نوری به این مسائل پرداخت. استفاده از این رویکرد برای گرفتن عکس های فوری سه بعدی از اوایل تا اواسطکلیهدر توسعه، تیم نرم افزار تجزیه و تحلیل سفارشی را برای به دست آوردن جزئیات بی سابقه در مورد درخت حالب از جمله تعداد نوک، زوایای شاخه و طول، حجم شاخه ها، و تعداد نسل های انشعاب از درختان حالب سالم ایجاد کرد (شکل 1c و d). 8 در ابتدا برای توصیف و شناسایی جنبههای جدید انشعاب کلیه استفاده شد، 9،10 تلاش مداوم به دنبال تعریف اصول و تنظیمکنندههای کلیدی است که بر الگوی شاخهای در داخل بدن حاکم است. 1
پیوند دینامیک اجداد با مورفوژنز اندام با تصویربرداری چند مقیاسیفعل و انفعالات مولکولی بین سلول های حالب و سلول های پیش ساز نفرون نقش مهمی در ایجاد مکمل نفرون ایفا می کند که تسهیل کنندهعملکرد کلیهدر زندگی بزرگسالی اجداد نفرون القا نشده عواملی را تولید می کنند که باعث افزایش می شوندکلیهرشد از طریق انشعاب حالب در حالی که نشانه های فضایی محدود در نوک حالب، هم وضعیت پیش ساز نفرون را حفظ می کند و هم زیر مجموعه ای از این پیش سازها را وادار می کند تا به نفرون اولیه تمایز پیدا کنند. این فعل و انفعالات باعث ایجاد چرخه ای از انشعاب و القای نفرون می شود که در حوالی تولد متوقف می شود، زمانی که اجداد نفرون باقی مانده تمایز پیدا می کنند. قبل از روش های پاکسازی بافت، درک ما از پویاییکلیهمورفوژنز و فراوانی نسبی جمعیت های سلولی پیش ساز در طول زمان به شدت محدود بود. این با توسعه روش های تصویربرداری چند مقیاسی با استفاده از پروتکل های ایمونوفلورسانس توسعه یافته، پاکسازی بافت و رویکردهای تصویربرداری برای تعیین کمیت تغییر کرد.کلیهتوسعه در سطح سلولی (کانفوکال) و کل اندام (توموگرافی پروجکشن نوری، صفحه نور). 9,10 آشکار شد که نرخ هایکلیهرشد به طور چشمگیری تغییر می کند و سرعت انشعاب و تکثیر اولیه در مراحلی کاهش می یابد که با کاهش تعداد سلول های پیش ساز در طاقچه نفروژنیک مرتبط است. 10 تصویربرداری کانفوکال سه بعدی از کل جنین انسان پاک شدهکلیه ها(هفته 11) یا نمونه هایی ازکلیهکورتکس (هفته های 11-23) تأیید می کند که این کاهش در اندازه طاقچه در بین گونه ها حفظ می شود. 12 تجزیه و تحلیل مقایسه ای بیشتر از طاقچه نفروژنیک انسان و موش در بافت پاک شده منجر به یک مدل جدید استخدام مبتنی بر زمان برای تشکیل نفرون شد، که در آن سلول های پیش ساز به تدریج به نفرون اولیه اضافه می شوند و هویت بخش را مطابق ترتیبی که به آن می رسند اتخاذ می کنند. . 13 در مطالعه دیگری که بر تعهد پیش ساز نفرون متمرکز بود، یک روش پاکسازی بافت مبتنی بر هیدروژل (تصویربرداری سفت و سخت هیبرید شده با اکریل آمید تعویض شده با لیپید شفاف غیرفعال / رنگ آمیزی ایمنی / هیبریداسیون درجا سازگار با بافت هیدروژل [CLARITY] برای آن استفاده شد) توانایی حفظ فلورسانس یک گزارشگر درون زا tdTomato تجزیه و تحلیل برچسبگذاری tdTomato در بافت پاکشده نشان داد که سلولهای درون نفرون در حال ارتکاب اولیه میتوانند به حالت اولیه بازگردند، جایی که نتایج قبلی نشان میداد تعهد یک طرفه بود. بنابراین، پاکسازی بافت، درک ما را از فرآیندهای رشد پویا در مقیاسها و گونهها بهبود بخشیده است.
فنوتیپ دقیق. پیشرفتها در پاکسازی بافت و تجزیه و تحلیل کمی، ظرفیت جدیدی را برای فنوتیپسازی دقیق فراهم کرده است. تغییرات آماری قوی در تعداد انشعاب و نفرون در مدلهای موش با فنوتیپهای ظریف مانند Ret þ/? و Six2 þ/? موش ها (شکل 2) که قبلاً به عنوان "عادی" طبقه بندی می شدند. 10,16 تصویربرداری کانفوکال با وضوح بالا از Wnt11 پاک شده ?/?کلیه هایک فنوتیپ سلولی جدید را شناسایی کرد که در آن اجداد نفرون به دلیل ناتوانی در ایجاد پیوست های سلولی پایدار با نوک حالب و تمایز زودهنگام، به هم ریخته به نظر می رسند. این روشها همچنین برای تعیین کمیت چگونگی تأثیر تنظیمکنندههای جدید حالت سلول پیشساز نفرون مانند DNA متیل ترانسفراز 1، میکروRNAهای Lin28 و Let7 و TSC1 مورد استفاده قرار گرفتهاند.کلیهرشد و تعداد نفرون 18-20 فنوتیپ دقیق احتمالاً ابزار مهمی در تلاش ما برای درک اثر افزایشی عوامل ژنتیکی و محیطی است که به تعداد نفرون کم و مستعد ابتلا به مزمن کمک می کند.بیماری کلیوی.
مدلسازی ریاضی ازکلیهمورفوژنز داده هایی که از توسعه پاک شده تولید می شوندکلیهموجی از مدلسازی ریاضی مبتنی بر تصویر را تحریک میکنند که تلاش میکند تشخیص دهد که چگونه شکل ماکروسکوپی و عملکرد یک بافت از برهمکنشهای مولکولی بین جمعیتهای سلولی پیشساز ناشی میشود. 11،21-23 کاربرد بیشتر تصویربرداری از کل اندام در بافت پاک شده برای درک محرک های مولکولی و سلولی الگوی بافت سه بعدی حیاتی خواهد بود و ممکن است کلید بهبود ساختار و دقت مدل های سلول های بنیادی را داشته باشد.کلیه
مورفولوژی سه بعدی و آسیب شناسی کلیه بزرگسالانمورفولوژی پیچیده بزرگسالانکلیهاستفاده از ابزارهای مورفولوژیکی دوبعدی را محدود می کند زیرا ممکن است ادراک ناقص یا گمراه کننده از ساختار سه بعدی را منتقل کنند. در اینجا، ما برخی از پیشرفتهای روششناختی مهم در سالهای اخیر را مورد بحث قرار میدهیم که اکنون امکان تجزیه و تحلیل سه بعدی قوی ساختارها را در بزرگسالان فراهم میکند.کلیه، اعم از دست نخوردهکلیه هاتمام راه تا اجزای سد فیلتراسیون گلومرولی (شکل 3). 2
CISTANCHE نارسایی کلیه/کلیه را بهبود می بخشد
تعداد نفرون و اندازهانسانکلیهسطح بالایی از تنوع درون و بین موضوعی را در تعداد نفرون و حجم نشان می دهد که در مطالعات کالبد شکافی از افراد بدون آشکار توضیح داده شده است.بیماری های کلیوی1،30،31 و با اختلالات رشدی مرتبط است. برای چندین دهه، ابزار استاندارد طلایی برای تعیین کمیت عدد نفرون در نمونههای تجربی و انسانی، روش تجزیهکننده/قطعکننده، یک روش استریولوژیکی مبتنی بر طراحی بوده است. 3،4 در حالی که این رویکرد دقیق و دقیق است، همچنین عملی، زمان بر است و به آموزش قابل توجهی نیاز دارد. به همین دلیل، رویکردهای جایگزینی برای ابداع روشهای کارآمدی پیشنهاد شدهاند که میتوانند نقاط پایانی با کیفیت بالا ارائه کنند: برای مثال، ترکیبی از روشهای پاکسازی نوری، از جمله آبگریز (که قبلاً به عنوان مبتنی بر حلال شناخته میشد)، هیدروفیل یا مبتنی بر هیدروژل، با روشهای پیشرفته. میکروسکوپ نوری (به عنوان مثال، کانفوکال، چند فوتونی یا صفحه نور).
طبق اطلاعات ما، اولین گزارشی که ترکیبی از پاکسازی نوری و میکروسکوپ صفحه نوری برای تجزیه و تحلیل تعداد نفرون و اندازه بود توسط کلینگبرگ و همکاران منتشر شد. 24 در یک مقاله برجسته که چندین پیشرفت مهم را نشان می دهد. ابتدا، این گزارش اتیل سینامات را معرفی کرد، یک حلال غیرخطرناک که میتواند جایگزین مواد شیمیایی سمی مانند بنزیل الکل-بنزیل بنزوات شود، که تا آن زمان به طور منظم در پروتکلهای پاکسازی آبگریز استفاده میشد. دوم، محققین شمارش نفرون را در موش دست نخورده انجام دادندکلیه ها in یک مدل تهاجمی و پیشرونده از سیستم ایمنیبیماری کلیوی، شناسایی از دست دادن نفرون در طول دوره بیماری. علاوه بر این، گامهای قابل توجهی به سمت اتوماسیون کامپیوتری الگوریتمهای تقسیمبندی تصویر معرفی شد که مسیری برای بهبود کارایی قابلتوجه فراهم میکند. اخیرا، Østergaard و همکاران. 25 یک روش پاکسازی آبگریز مشابه همراه با میکروسکوپ صفحه نوری و قطعهبندی خودکار تصویر ارائه کرد که هم تعداد نفرون کل و هم حجم گلومرولی منفرد را در مدل موش نفروپاتی دیابتی ارائه میکند. علاوه بر این، این مطالعه نشانگذاری عملکردی ظریف توبولهای پروگزیمال را از طریق تزریق آلبومین در داخل بدن برای تجسم اتصال لولهای گلومرولی و یک پروتکل ساده برای هیستوپاتولوژی همبستگی در همان نمونههای پاکشده نوری نشان داد. این گزارش انعطافپذیری این پروتکلها را نشان میدهد که در حال تبدیل شدن به خطوط لوله چند لایه برای پروفایل بافت جامع هستند.
عروق کلیوی و عصب.دنبال کردن مسیرهای انشعاب عروق یا رشته های عصبی در بزرگسالانکلیهدر بافت شناسی معمولی دو بعدی تقریبا غیرممکن است زیرا اندازه اندام و پیچیدگی توزیع ساختاری نیاز به برش سریال گسترده و متخصص دارد. اخیرا، هوانگ و همکاران. 33 یک رنگ فلورسنت کاتیونی نزدیک به مادون قرمز (MHI{2}}PEI) را برای برچسب زدن خاص رگ های خونی گزارش کرد که می تواند با یک پروتکل پاکسازی اصلاح شده و تسریع شده بر اساس اتیل سینامات ترکیب شود تا زمان پردازش بافت را کوتاه کند. این رویکرد راه های جدیدی را برای تحقیقات عروقی در جهان باز می کندکلیه،به خصوص زمانی که تصویربرداری با وضوح بالا در سه بعدی مورد نیاز است. به طور مشابه، هاسگاوا و همکاران. 26 دستگاه از کوکتلهای تصویربرداری بدون مانع مغز/بدن و تجزیه و تحلیل محاسباتی (CUBIC) همراه با یک سیستم میکروسکوپ نوری سفارشی برای شناسایی توزیع عصب سمپاتیک در کلیه دست نخورده موش استفاده کردند. اعصاب سمپاتیک عمدتاً در اطراف شریان ها توزیع می شوند. پس از 10 روز ایسکمی یا آسیب خونرسانی مجدد، تراکم عصب سمپاتیک به طور قابل توجهی کاهش یافت که با کاهش سطح نوراپی نفرین در ارتباط بود.بافت کلیه. این تغییرات تا حدی 28 روز پس از آسیب اولیه ادامه یافت و نشان میدهد که تغییرات سمپاتیک مداوم ممکن است در طول پیشرفت مزمن پیدا شود.بیماری کلیوی.
بازسازی لوله بینابینی.تجزیه و تحلیل سیستم لولهای کلیوی در سه بعدی دشوار است. مورفولوژی پیچیده و پیچیده چالش های متعددی را برای روش های مرسوم مبتنی بر برش سریال و میکروسکوپ نوری استاندارد ایجاد می کند. با این حال، پاکسازی نوری امکان تجزیه و تحلیل لوله های دست نخورده و ریزمحیط اطراف آنها را فراهم می کند. ساریتاس و همکاران 34 ترکیبی از پاکسازی نوری مبتنی بر هیدروژل و آبگریز را به دنبال میکروسکوپ نوری پیشرفته و تجزیه و تحلیل سه بعدی نیمه خودکار برای مشخص کردن بازسازی لوله دیستال به دلیل محرومیت از پتاسیم در رژیم غذایی انجام دادند. محققان هیپرپلازی توبولی را کمی کردند و افزایش سلولهای در حال تکثیر در توبولو اینترستیتیوم را تشخیص دادند. این مطالعه از تطبیق پذیری پاکسازی نوری و
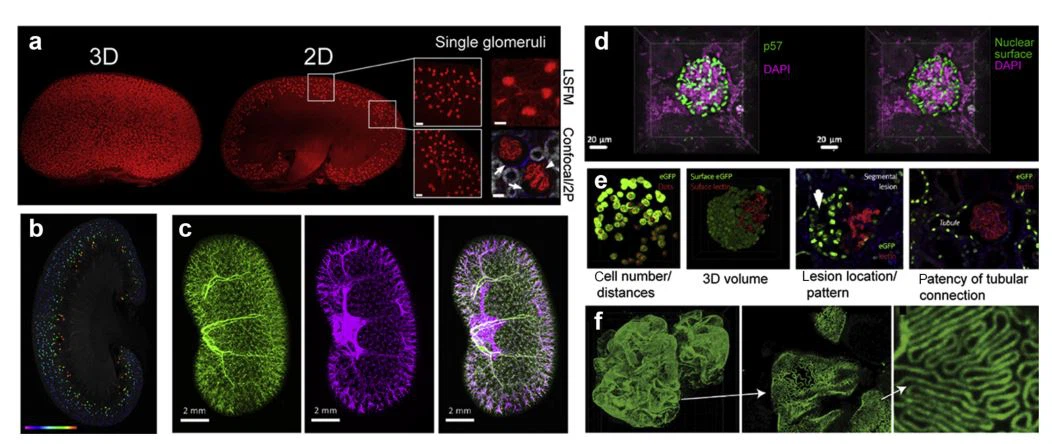
شکل 3| مورفومتری سه بعدی (سه بعدی) در کلیه بزرگسالان. (الف) شمارش نفرون ها در کل کلیه ها با استفاده از برچسب CD31 سلول های اندوتلیال. پانل یک بازسازی سه بعدی (سمت چپ)، یک بخش نوری در نمای دو بعدی (2 بعدی) (وسط) و مناطق ویژه را نشان می دهد که گلومرول های منفرد را در مقایسه بین میکروسکوپ صفحه نوری (LSFM) و کانفوکال و 2- نشان می دهد. میکروسکوپ فوتون (2P) اقتباس شده با مجوز انجمن نفرولوژی آمریکا، از مجله انجمن نفرولوژی آمریکا، ارزیابی کاملا خودکار تعداد کل گلومرولی و اندازه توفت مویرگی در کلیه های نفریتی با استفاده از میکروسکوپ نوری، کلینگبرگ A، هاسنبرگ ای، لودویگ، پورت آلوگ .، جلد 28، شماره 2، 2017; مجوز از طریق مرکز پاکسازی حق نسخهبرداری، Inc. 24 (ب) اندازهبندی گلومرولها با ثبت فضایی—کدگذاری رنگ نشاندهنده اندازه گلومرولی است، جایی که قرمز بزرگترین جسم و صورتی کوچکترین است. اقتباس شده با مجوز انجمن نفرولوژی آمریکا، از Kidney360، Automated Image Analyses of Glomerular Hypertrophy in a Mouse Model of Diabetic Nephropathy, Østergaard MV, Sembach FE, Skytte JL, et al., volume 6, number 6 ، 2020; مجوز از طریق مرکز پاکسازی حق چاپ، Inc. 25 (ج) ردیابی عروق و عصب، شامل بازسازی سه بعدی یک کلیه دست نخورده با برچسب ایمنی اعصاب سمپاتیک (سبز)، عروق (سرخابی)، و ادغام شده (سمت چپ). اقتباس از Kidney International، جلد 96، شماره 1، Hasegawa S، Susaki EA، Tanaka T، و همکاران، تجزیه و تحلیل جامع سه بعدی (CUBIC-Kidney) اعصاب سمپاتیک غیرطبیعی کلیوی را پس از آسیب ایسکمی/پرفیوژن مجدد، صفحات 129-138 تجسم می کند. حق چاپ ª 2019، با مجوز از انجمن بین المللی نفرولوژی. 26 (د) مورفومتری پودوسیت در گلومرولهای فردی با استفاده از برچسبگذاری ایمنی برای نشانگر p57 اختصاصی پودوسیت (سبز) و نشانگر DNA 4 0،6-دیامیدینو-2-فنیلیندول (DAPI). پانل ها (سمت چپ) یک بازسازی سه بعدی و (راست) سطوح رندر شده را نشان می دهند. اقتباس شده با مجوز انجمن نفرولوژی آمریکا، از مجله انجمن نفرولوژی آمریکا، اعتبارسنجی روش سه بعدی برای شمارش و اندازه پودوسیت ها در کل گلومرول، Puelles VG، van der Wolde JW، Schulze KE، و همکاران، جلد 27، شماره 10، 1395; مجوز از طریق مرکز پاکسازی حق نسخهبرداری، Inc. 27 (ه) دینامیک سلولی با استفاده از ردیابی نسب، نشان دادن پودوسیتها (سمت چپ)، سلولهای اپیتلیال جداری (PEC) که هلالهای سلولی را بهصورت سه بعدی (وسط سمت چپ) تشکیل میدهند، نمای دوبعدی از PECها در حال حمله سمت گلومرولی با آسیب عروقی (وسط-راست)، و تجسم دوبعدی خروجی لوله ای (سمت راست). اقتباس از Kidney International، جلد 96، شماره 2، Puelles VG، Fleck D، Ortz L، و همکاران، تجزیه و تحلیل سه بعدی جدید با استفاده از پاکسازی بافت نوری، تکامل گلومرولونفریت سریع پیشرونده موش، صفحات 505-516، حق چاپ ª 2019، بین المللی، انجمن نفرولوژی، تحت مجوز CC BY-NC-ND (http://creativecommons.org/licenses/by-nc-nd/4.0/). 28 (f) تجسم دیافراگم شکاف در افزایش بزرگنمایی از چپ به راست. برگرفته از Kidney International، جلد 99، شماره 4، Unnersjö-Jess D، Butt L، Höhne M، و همکاران، پروتکل پاکسازی و تورم سریع و ساده برای تصویربرداری سه بعدی در محل کلیه در مقیاس ها، صفحات 1010-1020 ، حق چاپ ª 2021، انجمن بین المللی نفرولوژی، تحت مجوز CC BY-NC-ND (http://creativecommons.org/licenses/by-nc-nd/4.0/). 29 برای مشاهده بهینه این تصویر، لطفاً نسخه آنلاین این مقاله را در آدرس زیر مشاهده کنیدwww.kidney-international.org.
میکروسکوپ نوری برای انجام آنالیز لولهای در کلیههای دست نخورده با استفاده از میکروسکوپ تعبیهشده با هیدروژل و میکروسکوپ ورقهای نور، و همچنین کمیسازی تک سلولی در برشهای کلیه با استفاده از شفافسازی آبگریز و میکروسکوپ کانفوکال، زیرا هر ترکیب برای سؤال تحقیق خاص مناسبتر بود. ترکیبی از پاکسازی نوری و میکروسکوپ نوری پیشرفته توسط طاهایی و همکاران استفاده شد. 35 که دیمورفیسم جنسی را در طول لوله پیچیده دیستال مشخص می کند، که ممکن است ظرفیت آن را برای سازگاری با استرس فیزیولوژیکی تعیین کند، و شوه و همکاران. 36 که تفاوت های محوری را در جذب لیگاند توبول پروگزیمال و عملکرد اندولیزوزوم نشان داد، و تاکید کرد که بخش S1 برای بازجذب پروتئین ها از طریق اندوسیتوز با واسطه گیرنده بسیار تخصصی است. در یک مطالعه اخیر، Blanc و همکاران. 2 مدلی از تشکیل کیست را تجزیه و تحلیل کرد و نشان داد که کیستها فقط در بخشهای نفرون خاصی ایجاد میشوند که شکل آنها را تعیین میکند و در مجاورت لولههای گشاد نشده طبیعی قرار دارند. به طور کلی، ما اکنون نمونه های متعددی از کاربرد مستقیم پاکسازی نوری برای تجزیه و تحلیل سیستماتیک محفظه توبولو بینابینی داریم.
از دست دادن پودوسیت و هیپرتروفی.گلومرول یک مثال منحصر به فرد برای تجزیه و تحلیل واحدهای عملکردی دست نخورده در یک اندام است. به طور خاص، مطالعه کاهش سلولهای بدن به طور مستقیم از این پیشرفتهای تکنولوژیک سود برده است، زیرا روشهای مبتنی بر طراحی استاندارد طلا نیازمند سرمایهگذاری قابل توجهی در زمان و منابع هستند. 37 اولین ابزار برای تجزیه و تحلیل مورفومتریک پودوسیت سه بعدی گلومرول های دست نخورده موش نشانگر ترکیبی ایمنیکلیهبرش ها با استفاده از پروتکل اصلاح شده ایمونوفلوورهای غیرمستقیم، پاکسازی نوری آبگریز، و میکروسکوپ کانفوکال، که تعیین کمیت تعداد پودوسیت کل را در کل گلومرول های فردی با حجم شناخته شده تسهیل می کند. ما معتقدیم که این رویکرد برای مطالعه فرآیندهایی که بر زیرمجموعه خاصی از ساختارها تأثیر میگذارند (به عنوان مثال، از دست دادن سلولهای بدن که منجر به گلومرولواسکلروز کانونی و سگمنتال میشود) ایدهآل است. 27 همین تکنیک بعداً برای توصیف نقش هیپرتروفی پودوسیت به عنوان یک پاسخ جبرانی به دنبال از دست دادن پودوسیت، مکانیزمی که توسط هدف پستانداران مسیر سیگنال دهی راپامایسین واسطه می شود، به کار رفت. در حالی که این 2 مطالعه بر تجزیه و تحلیل پودوسیتهای گلومرولی متمرکز بودند، این خط لوله مبتنی بر نشانگذاری ایمنی معمولی میتواند برای توصیف تغییرات مورفولوژیکی از هر نوع سلولی در وضوح فضایی بالا استفاده شود.
تکامل هلال های سلولی.ابزار مهم دیگری که باید با موفقیت در جعبه ابزار سه بعدی ادغام می شدکلیهمورفومتری ردیابی نسب ژنتیکی است. اکثر روشهای پاکسازی نوری تمایل به القای درجه خاصی از خاموش کردن فلورسانس دارند (که از خفیف تا شدید متفاوت است). ما اخیراً پروتکلی ارائه کردهایم که ردیابی اصل و نسب، پاکسازی نوری و میکروسکوپ چند فوتونی را برای تجزیه و تحلیل جامع از بین رفتن سلولهای پودوسیت و فعالسازی سلولهای اپیتلیال جداری ارائه میکند. 28 در این مطالعه، از دست دادن پودوسیت به عنوان یکی از ویژگیهای نفریت هلالی تجربی با استفاده از برچسبگذاری متابولیکی پودوسیتها با پروتئین فلورسنت سبز افزایش یافته شناسایی شد. تکامل هلالهای سلولی بر اساس تکثیر و مهاجرت سلولهای اپیتلیال جداری، که با افزایش پروتئین فلورسنت سبز نیز مشخص شدهاند و در طول یک مدل تجربی نفریت هلالی ردیابی شدهاند، مشاهده و کمیتیابی شد. تجزیه و تحلیل گلومرول های دست نخورده امکان شناسایی از دست دادن پودوسیت کانونی و تشکیل ضایعه را فراهم کرد که منجر به انسداد لوله ای توسط سلول های اپیتلیال جداری شده و منجر به تشکیل گلومرول های آتوبولی شد. این مطالعه راه را برای مطالعات آینده در مورد فعل و انفعالات پیچیده ایمنی-اپیتلیال در داخل دست نخورده هموار می کندکلیه ها.

سیستانچ دیالیز کلیه/کلیه را بهبود می بخشد
سد فیلتراسیون گلومرولییک ابزار تشخیصی مهم برای ارزیابی معمول بیماریهای گلومرولی، آنالیز فوق ساختاری بیوپسیهای کلیوی توسط میکروسکوپ الکترونی است. جایگزینی برای میکروسکوپ الکترونی را می توان در زمینه میکروسکوپ انبساطی یافت که بنا به تعریف هدف آن افزایش وضوح نوری با افزایش ابعاد بافت است. در طول سالها، Unnersjo-Jess و همکاران. 39،40 پروتکل های متعددی برای تجسم ساختارهای نانومقیاس درکلیهاخیرا، این محققان یک روش سریع و ساده را برای تجسم سه بعدی گزارش کردندکلیهمورفولوژی، ترکیب مفاهیم پاکسازی نوری و گسترش بافت برای حل ساختارهای نانومقیاس با استفاده از میکروسکوپ کانفوکال معمولی. 29 این پروتکل برای تجسم و تعیین کمیت چند ویژگی پاتولوژیک در موش و انسان به کار گرفته شدکلیهبیوپسیها شامل افاسمان فرآیند پا، تغییرات غشای پایه گلومرولی، طول شکاف دیافراگم، رسوبات IgG و ویژگیهای پاتولوژی کلاسیک (مانند گلومرولو-اسکلروز، فیبروز بینالمللی توبولی و آتروفی لولهای). به طور خلاصه، این روش با استفاده از یک روش ساده و ابزارهای قابل دسترسی تجزیه و تحلیل تصویر، امکان تجسم چند مقیاسی و کمی سازی آسیب شناسی کلیه را فراهم می کند. مقیاس پذیری و اجرای این رویکرد در عمل بالینی احتمالاً با نیاز به تجهیزات میکروسکوپ نوری پیشرفته و توسعه ابزارهای تجزیه و تحلیل تصویر خودکار تعیین می شود.
نتیجه
طیف فعلی روشهای پاکسازی بافت شامل تکنیکهای سادهای است که میتوان آنها را در اکثر آزمایشگاهها برای بهبود تصویربرداری سهبعدی روی میکروسکوپهای معمولی در دسترس پیادهسازی کرد. با آشکار شدن فرصتهای ارائه شده توسط این رویکردهای جدید، ما پیشبینی میکنیم که سیستمهای میکروسکوپی تخصصی برای تصویربرداری مؤثر از بافت پاکشده با وضوح بالا و توسعه تحقیقات و گردشهای کاری بالینی مناسب برای پاسخگویی به سؤالات خاص، جذب گستردهتر شوند. حوزه علوم اعصاب به عنوان محل آزمایشی برای روش ها و کاربردهای تصویربرداری بافت پاک شده عمل کرده است. تجزیه و تحلیل خودکار تصویر، رویکردهای جدید برای مطالعه اتصال سلولی، و پروژه های اطلس بیان ژن و پروتئین در سطح بافت در این زمینه توسعه داده شده است. این احتمال وجود دارد که رویکردهای مشابه بینش جدیدی را در مورد آناتومی سلولی و وابستگی متقابل جمعیت سلولی در بزرگسالان و در حال رشد به دست آورند.کلیه
محدودیتهای عملی برای این پیشرفتها شامل هزینه سختافزار تصویربرداری، و مشکلات در مدیریت، ذخیرهسازی و تجزیه و تحلیل مجموعههای داده بزرگ است. سایر محدودیتها ناشی از عدم تکرارپذیری رنگآمیزی با بافتهایی است که به طور متغیر تحت تأثیر شرایط تثبیت و برچسبگذاری آنتیبادی قرار دارند. در نتیجه، نیاز به تحلیلهای سه بعدی جدید برای ارزیابی انتقادی و مقایسه با روشهای موجود وجود دارد. با وجود پیشرفت های چشمگیر در ارزیابیکلیهرشد و بزرگسالیکلیهساختار و بیماری که در این بررسی برجسته شده است، ما معتقدیم که بهترین پاکسازی بافت و تصویربرداری سه بعدی هنوز در راه است و احتمالاً یک منطقه هیجان انگیز برای رشد است.کلیهتحقیق برای دهه های آینده
