رژیم غذایی به طور قابل توجهی بر آسیب شناسی ایمنی و شدت آسیب کلیه تأثیر می گذارد
Feb 22, 2022
مخاطب: emily.li@wecistanche.com
جان ای بروس و همکاران
خلاصه:
"رژیم غذایی یک عامل خطر اصلی برای عوارض و مرگ و میر در سراسر جهان است، اما به ندرت در طراحی مطالعات پیش بالینی حیوانی مورد توجه قرار می گیرد. نشان داده شده است که چندین مورد از نارسایی های تغذیه ای گزارش شده در آمریکایی ها مضر استکلیهسلامتی; با این حال، مکانیسم های مسئول نامشخص است و تا حد زیادی به توسعه دیابت یا فشار خون بالا نسبت داده شده است. در اینجا، ما تعیین کردیم که آیا رژیم غذایی بر حساسیت به آسیب کلیه در موشهای نر C57Bl/6 تأثیر میگذارد یا خیر. موشها به مدت 12 هفته قبل از القای این بیماری، با یک رژیم غذایی استاندارد، یک رژیم غذایی "غربی" تجاری (WD) یا یک رژیم غذایی آمریکایی جدید (AD) تغذیه شدند.کلیهصدمهبا استفاده از مدلهای نفروپاتی اسید فولیک (FAN) یا آسیب یکطرفه ایسکمی-پرفیوژن مجدد کلیه (uIRI). در FAN، موشهایی که با WD و AD تغذیه شدند، شواهد بافتشناختی بدتری از آسیب بافتی و بیان کلیوی بیشتر ژنهای مرتبط با سمیت کلیوی در مقایسه با موشهای تغذیهشده با غذا داشتند. موش هایی که با AD تغذیه شده بودند به دنبال FAN دچار هیپرتروفی شدید کلیوی شدند و داده های بیان ژن نشان می دهد که مکانیسم FAN در بین رژیم های غذایی متفاوت است. در همین حال، موشهایی که با WD تغذیه شدند، بیشترین غلظت اینترلوکین{1}} در گردش را داشتند. در uIRI، هیچ تفاوتی در آسیب بافت کلیوی بین رژیمهای غذایی مشاهده نشد. با این حال، موش های تغذیه شده با WD و AD شواهدی از پاسخ التهابی سرکوب شده را نشان دادند. در مجموع، دادههای ما از این فرضیه پشتیبانی میکنند که رژیم غذایی مستقیماً بر شدت و پاتوفیزیولوژی تأثیر میگذاردکلیهمرضو یک متغیر تجربی حیاتی است که باید در مطالعات پیش بالینی حیوانی مکانیکی در نظر گرفته شود.
کلمات کلیدی: رژیم غذایی غربی موش؛ حادکلیهصدمه; کیفیت رژیم غذایی؛ تغذیه

برای دریافت اطلاعات بیشتر در مورد محصولات Cistanche برای بهبود کلیه اینجا را کلیک کنید
1. مقدمه
سبک زندگی نقش مهمی در سلامت کلی دارد و به طور قابل توجهی بر پیامدهای بیماری قلبی عروقی (CVD) بدون توجه به خطر ژنتیکی تأثیر می گذارد [1]. رژیم غذایی یکی از اجزای اصلی سبک زندگی است و رژیم غذایی نامناسب و بیماری های مرتبط با رژیم بیش از هشت مورد از 30 عامل خطر اصلی مرگ و میر در سراسر جهان را تشکیل می دهند [2]. با این حال، مکانیسمهایی که چگونگی تأثیر منفی تغذیه نامناسب بر سلامت را توصیف میکنند، بهطور شگفتآوری نامشخص است.
یک مانع عمده در تحقیقات تغذیه، مشکل در مدلسازی نامناسب ماهیت پیچیده و چندوجهی عادات غذایی انسان در مطالعات پیشبالینی حیوانات مکانیکی بوده است. جیره های چاو به دلیل کیفیت غذایی بالا، پایداری ذخیره سازی و هزینه های تولید نسبتا پایین، پرمصرف ترین منبع غذایی در مطالعات پیش بالینی جوندگان هستند. از مخلوطهای مبتنی بر غلات که با روغنهای باکیفیت و مخلوطهای ویتامین/معدنی تکمیل میشوند، رژیمهای غذایی چو نشاندهنده ضعیفی از کیفیت تغذیهای نسبتا پایین گزارششده در جوامع توسعهیافته هستند. این امر منجر به ایجاد انواع رژیم های غذایی بیماری زا شده است که اکثر آنها بر مصرف کالری بالا در کشورهای توسعه یافته تمرکز دارند و باعث چاقی و اختلال متابولیک در حیوانات نوع وحشی می شوند. اگرچه چاقی و اختلال عملکرد متابولیک همچنان نگرانیهای عمده سلامتی در سراسر جهان باقی مانده است، رژیمهای غذایی پرکالری در دسترس تجاری کنونی نمایانگر دیدگاهی افراطی و بسیار محدود از نارساییهای غذایی پیچیده گزارششده در جوامع غربی است. اثرات فیزیولوژیکی یک ماده مغذی معین اغلب به وجود و فراوانی مواد مغذی دیگر بستگی دارد (مانند نسبت سدیم به پتاسیم [3،4]) و این فعل و انفعالات در رژیم های غذایی ایجاد کننده بیماری در دسترس تجاری در نظر گرفته نمی شود. بنابراین، ممکن است رویکرد تقلیلگرایی که در تحقیقات تغذیه رایج است، به طور ناخواسته مانع از ترجمه موفقیتآمیز دادههای مکانیکی از جوندگان به انسان شده باشد.
در تلاش برای پرداختن به این موضوع، ما در حال توسعه یک رژیم غذایی آمریکایی جدید (AD) هستیم که شامل چندین مورد از نارسایی های تغذیه ای گزارش شده در آمریکایی ها است [5]. AD یک رژیم غذایی دو گلوله ای است که از یک گلوله مبتنی بر دانه و یک گلوله مصنوعی "شیرین و نمکی" تشکیل شده است و با علاقه به مطالعه ترجیحات غذایی ایجاد شده است و ممکن است اثرات نامطلوب گزارش شده رژیم غذایی سنتی جوندگان با کالری بالا را جبران کند [6] ]. جالب توجه است، چندین مورد از تغییرات مواد مغذی ایجاد شده در AD برای تأثیرگذاری پیشنهاد شده استکلیهسلامتیبه صورت مستقیم یا غیر مستقیم [7-10].کلیهاختلال عملکردیکی از علل اصلی CVD و یک پیامد شایع در بیماری های ناشی از رژیم غذایی ماننددیابتوفشار خون. تجزیه و تحلیل های اخیر نشان داده است که کیفیت پایین رژیم غذایی باعث افزایش بروز این بیماری می شودکلیهصدمهومرض[11]؛ با این حال، مکانیسم های مسئول همچنان نامشخص است. بنابراین، ما تصمیم گرفتیم تعیین کنیم که آیا رژیم غذایی به طور قابل توجهی بر نتایج دو مدل آسیب کلیوی مختلف موش تأثیر می گذارد یا خیر.
2. مواد و روشها
2.1. حیوانات و رژیم های غذایی
همه آزمایشهای حیوانی طبق پروتکلهای تایید شده توسط کمیته مراقبت و استفاده از حیوانات نهادی دانشگاه لیبرتی و مطابق با راهنمای مراقبت و استفاده از حیوانات آزمایشگاهی [12] انجام شد. موشهای نر C57Bl/6 از شیر گرفته ({1}}هفتهای) از آزمایشگاه جکسون خریداری شدند و به صورت گروهی (3 تا 5 موش در قفس) با بستر ذرت، یک غذای استاندارد جوندگان (Teklad Global 18% , #). 2018)، و آب لوله کشی فیلتر شده با کربن. پس از یک دوره سازگاری 1-هفتهای، به موشها به طور آزاد به یکی از سه رژیم غذایی دسترسی داده شد: چو (Teklad Global 18% , #2018, n=14)، یک رژیم غذایی غربی تجاری موجود ("WD, " #TD.88137, n=13)، یا رمان ما "AD" (n=14).
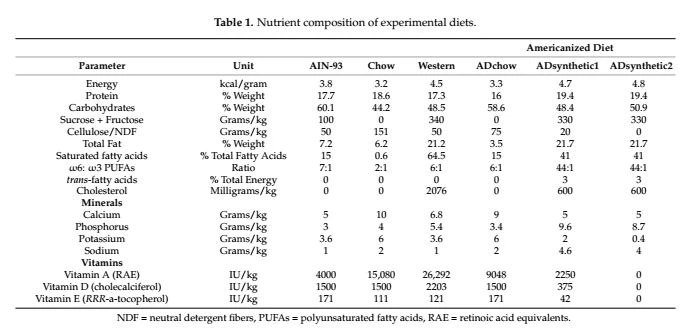
AD از دو گلوله تشکیل شده است که به عنوان AD chow (TD.170651) و ADsyn thetic (TD.170698 & TD.170699) نامیده می شود. پلت AD چو یک پلت اصلاح شده مبتنی بر چو با کاهش ویتامین های محلول در چربی (A، D و E) و فیبر نامحلول (فیبر شوینده خنثی) است. رژیم غذایی مصنوعی به گونهای فرموله شد که شامل ساکارز اضافی، فروکتوز، چربیهای اشباع، کلسترول، اسیدهای چرب غیراشباع امگا{5}}، اسیدهای چرب ترانس، سدیم و فسفر باشد در حالی که پتاسیم و امگا{7}} اسیدهای چرب غیراشباع را کاهش میدهد. . اسیدهای چرب ترانس در فرمولاسیون گنجانده شدند زیرا هنوز از منابع طبیعی (مانند گوشت گاو) مصرف می شوند، اما گنجاندن آن در گلوله ADSynthetic بسیار کمتر از آنچه در سایر مطالعات قبلی استفاده شده بود [13-16] بود. گنجاندن هر ماده مغذی بر اساس تطبیق درصد تفاوت مصرف واقعی و توصیه شده در موش و انسان (در جدول A1 ضمیمه A نشان داده شده است) بر اساس گزارش های اخیر وزارت کشاورزی ایالات متحده [5،12] بود. ترکیب مواد مغذی برای هر گلوله بر اساس اختلاف درصد محاسبهشده مقادیر دریافتی گزارششده و توصیهشده هر ماده مغذی در آمریکاییها بود، و این درصد تفاوت سپس برای نیازهای مواد مغذی موش اعمال شد [13]. سپس فرمول نهایی هر گلوله برای محاسبه میانگین مصرف روزانه 2 و 0.5 گرم AD مصنوعی و ADchow تنظیم شد. گلوله مصنوعی دیگر، ADsythetic2، برای سازگاری با تغییر ترجیحات رژیم غذایی بیش از 8 هفته، که در آن موش ها روزانه تقریباً مقادیر مساوی (1.5 گرم) ADchow و ADsynthetic2 را مصرف می کردند، فرموله شد. خلاصه ای از رژیم های غذایی مورد استفاده در این مطالعه در جدول 1 ارائه شده است.
2.2. مدل موش آسیب حاد کلیه (AKI)
موش ها به مدت 12 هفته قبل از القاء در رژیم غذایی آزمایشی خود باقی ماندندکلیهصدمهبا نفروپاتی ناشی از اسید فولیک (FAN) یا آسیب یک طرفه ایسکمی خونرسانی مجدد (uIRI). این مدلها از آنجایی انتخاب شدند که به طور معمول در ادبیات استفاده میشوند و استحکام را القا میکنندکلیهصدمهبه روشی وابسته به دوز [17]. مدل FAN بر اساس انتشارات قبلی [18-21] با تغییراتی انجام شد. با توجه به تفاوت وزن بدن بین گروههای غذایی، ما دوز 250 میلیگرم بر کیلوگرم را برای کوچکترین موش در مطالعه خود (25 گرم) محاسبه کردیم و همان دوز (6.25 میلیگرم/500 میکرولیتر) را به همه تزریق کردیم. موش ها تحت بیهوشی مختصر ایزوفلوران (3 درصد در اکسیژن 100 درصد، 600 میلی لیتر در دقیقه). موشهای کنترل (n=4 برای هر رژیم) حجم مساوی (500 میکرولیتر) از وسیله نقلیه بیکربنات سدیم 0.3 میلیمولار را به عنوان موشهای دریافت کننده FAN (n=4 برای هر رژیم) دریافت کردند. برای مدل uIRI، موشها (تعداد=5-6 برای هر رژیم) با ایزوفلوران بیهوش شدند و یک برش پهلو و شریان و ورید چپ ایجاد شد.کلیهاز بافت همبند و چربی اطراف جدا شده و با یک گیره میکروواسکولار مسدود شدند. پس از 45 دقیقه، گیره برداشته شد و بازیابی جریان خون به صورت بصری تایید شد. عضله با نخ ابریشم 4.{2}} بسته شد و برش پوست با منگنه جراحی بسته شد. دمای سطح بدن در 28-3{6}} ◦C با لامپ حرارتی و پد گرمایش (دمای طبیعی سطح بدن ~30 ◦C) حفظ شد. بوپرنورفین (0.1 میلی گرم در میلی لیتر، تزریق زیر جلدی 100 میکرولیتر) به عنوان ضد درد پس از شروع به دست آوردن هوشیاری حیوان تجویز شد.
سیستانچ می تواند آسیب کلیه را درمان کند
2.3. اتانازی حیوانی، آنالیز بافت شناسی و اندازه گیری های سرمی عملکرد کلیه
حیوانات 24 (uIRI) یا 48 ساعت (FAN) بعد با دررفتگی دهانه رحم در حالی که تحت بیهوشی مختصر ایزوفلوران بودند، معدوم شدند. قلب برداشته شد و خون تنه جمعآوری شد، به مدت 1{12}} دقیقه در دمای اتاق رها شد و به مدت 10 دقیقه در 2500 گرم سانتریفیوژ شد. سرم جمع آوری و در دمای 80- درجه سانتیگراد منجمد شد تا زمانی که برای کراتینین (Crystal Chem)، نیتروژن اوره خون (BUN، Arbor Assays)، یا اینترلوکین-6 (IL6، Biolegend) با استفاده از سنجش های تجاری موجود تجزیه و تحلیل شد. کلیه ها تشریح و کپسوله شدند و یک بخش ساژیتال مرکزی در فرمالین 10 درصد بافر فسفات تثبیت شد و در پارافین جاسازی شد و بخش های 5 میکرومتری برش داده شد و با H&E یا Picro Sirius Red (ABCAM) رنگ آمیزی شد. در مقاطع رنگ آمیزی شده با H&E، شدت نکروز حاد توبولار توسط یک فرد کور در طرح آزمایشی بر اساس مقیاس 0-4 ارزیابی شد، که در آن (0) به هیچ شواهدی از آسیب اشاره دارد، (1)<25% of="" the="" identifiable="" tissue="" area="" consists="" of="" injury,="" (2)="" 25–50%,="" (3)="" 50–75%,="" and="" (4)="">75 درصد. مشابه کار قبلی [22]، «آسیب لولهای» شامل اتساع لولهای، قالبهای پروتئینی و بازسازی ظاهری لولههای بینابینی بود. درجه فیبروز توبولو بینابینی در مقاطع رنگ آمیزی Picro Sirius بررسی شد.
2.4. سمیت نفروتوکسیسیته آرایه PCR
تقریباً 30 تا 100 میلی گرم قطعات کپسوله شدهکلیهبافتدر محلول RNAlater™ (Thermo) ذخیره شدند. یک نمونه نماینده واحد از هر گروه رژیم غذایی در مطالعه FAN انتخاب شد که شباهت زیادی به میانگین گروه برای کراتینین سرم، BUN و نمرات بافت شناسی در هر گروه درمانی داشت. سپس نمونه انتخاب شده برای تعیین کمیت بیان 84 ژن مرتبط با سمیت کلیوی با استفاده از RT2 ProfilerTM PCR Array—Mouse Nephrotoxicity (#PAMM-094Z) طبق توصیه سازنده (Qiagen) پردازش شد. RNA کل با استفاده از کیت RNeasy® جدا شد، DNA ژنومی با هضم DNA حذف شد و 0.5 Ugs از RNA کل برای سنتز cDNA با استفاده از کیت رشته اول RT2 استفاده شد. مخلوط cDNA با theRT2 SYBR® Green Mastermix و آب بدون نوکلئاز مخلوط شد و سپس روی صفحه RT2 اعمال شد و همانطور که توصیه شد با استفاده از ابزار Lightcycler™ 96 (روش) آنالیز شد. مقادیر ΔCt برای هر گروه درمانی بر اساس بیان ژن های خانه داری با استفاده از معادله زیر محاسبه شد: 2ˆ (∆CT)، که در آن ∆CT=(خانه داری (GAPDH)) -CT (ژن مورد علاقه)] . درصد تفاوت در بیان در مقایسه با موشهای کنترل (موشهای تغذیه شده با غذا با تیمار وسیله نقلیه) برای هر ژن محاسبه شد. برای شناسایی ژن هایی که به طور بالقوه تحت تأثیر FAN و رژیم غذایی هستند، تجزیه و تحلیل ارائه شده توسط سازنده (Qiagen) را اصلاح کردیم. ژنهایی با اختلاف بیشتر از 2-از موشهای کنترل شناسایی شدند و از این فهرست، ژنهایی را با اختلاف بیشتر یا مساوی ۲۵ درصد بین موشهای تغذیهشده با WD و AD شناسایی کردیم. شش ژن با استفاده از این روش شناسایی شدند و بیان mRNA کلیوی آنها با استفاده از RT-PCR بلادرنگ معمولی اندازهگیری شد.
2.5. RT-PCR برای ژن های مرتبط با سمیت کلیوی، التهاب، و بازسازی بافت
کلیه ها و طحال ها برای RT-PCR با استفاده از کیت های تجاری موجود (Qiagen و BioRad) به دنبال توصیه های سازنده پردازش شدند. پرایمرهای پوشاننده اینترون برای ژن های دخیل در سمیت کلیوی یا نشانگرهای اختصاصی لکوسیت از BioRad خریداری شدند یا با استفاده از نرم افزار Primer3 ایجاد شدند [23-25]. اطلاعات آغازگر در ضمیمه C جدول A2 ارائه شده است. سپس 10 میکرولیتر واکنش RT-PCR با استفاده از iTaq Universal SYBR Green Supermix (BioRad) انجام شد و مقادیر ΔCT برای هر ژن محاسبه شد. همه داده ها به صورت نرمال شده به میانگین گروه های کنترل برای هر کدام ارائه می شوندکلیهصدمهمدل (موشهای تغذیه شده با وسیله نقلیه برای FAN یا کلیه طرف مقابل موشهای تغذیه شده با غذا در IRI).

2.6. تحلیل آماری
تمامی مطالعات با استفاده از طرح کاملا تصادفی انجام شد. در مطالعه FAN، "رژیم غذایی" و "درمان" متغیرهای مستقل بودند که "رژیم غذایی" دارای 3 سطح (چو، WD، و AD) و "درمان" دارای 2 سطح (خودرو یا FAN) بود. تحلیلهای مشابهی در مطالعه uIRI استفاده شد، جایی که «درمان» با مقایسه دادههای بیان ژن در کلیه ایسکمیک با کلیه کنترل غیرایسکمیک و طرف مقابل تعیین شد. همه دادهها قبل از تجزیه و تحلیل GLM بررسی شدند و مقادیر پرت با استفاده از تابع Explore شناسایی شدند و با استفاده از روشهای مدل خطی عمومی در SPSS (IBM) تجزیه و تحلیل شدند. مقادیر با p کمتر یا مساوی 0 معنیدار در نظر گرفته شد.05 با تحلیل Tukey Post Hoc، و یک گرایش به صورت p کمتر یا مساوی 0.1 تعریف شد.
3. نتایج
3.1. رژیم غذایی نامناسب آسیب بافتی را در FAN تشدید می کند
موشهای تغذیه شده با WD بیشترین وزن کل بدن (4.1 ± 37.4 گرم) را در مقایسه با موشهای تغذیه شده با AD داشتند (1 ± .30.0، p=0). 17}}01) و موشهای تغذیه شده با غذا (26.8 ± 1.1، p < {{2{22}}}}.001).="" چاقی="" همچنین="" در="" بین="" گروههایی="" که="" موشهای="" تغذیه="" شده="" با="" wd="" دارای="" بالاترین="" وزن="" پد="" چربی="" اپیدیدیم="" بودند="" متفاوت="" بود="" (2.0="" ±="" {{3{32}}}}}.6،="" p=""><{36}}). 001)="" در="" مقایسه="" با="" موش="" های="" تغذیه="" شده="" با="" غذا="" (0.4="" ±="" 0.08،="" p=""><0.001) و="" ad="" (0.7="" ±="" 0.3،="" p=""><0.001). افزایش="" وزن="" بدن="" و="" چربی="" مشاهدهشده="" در="" موشهای="" تغذیهشده="" با="" ad="" نیز="" بیشتر="" از="" موشهای="" تغذیهشده="" با="" غذا="" بود="" (بهترتیب="" 0.001.0="0" و="" 001/0=""> p). وزن بافت چربی بین موشهای گروه تحت درمان با وسیله نقلیه یا FAN تفاوتی نداشت (6.6.{38}}).
جالب اینجاست که موشهایی که با AD تغذیه شدهاند، بیشترین وزن کلیه را در مقایسه با موشهای تغذیه شده با غذا (p < {0}}}.001)="" و="" wd="" (p="" {{2)="" داشتند.="" }}.01)="" (جدول="" 2).="" وزن="" کلیه="" بین="" موشهای="" تغذیهشده="" با="" غذا="" یا="" wd="" تفاوتی="" نداشت="" (p="0.1)" و="" این="" دادهها="" زمانی="" که="" وزن="" بدن="" بهعنوان="" متغیر="" کمکی="" استفاده="" میشد="" سازگار="" بود="" (p="0.52)." کراتینین="" در="" گردش="" (p=""><0.001) و="" bun="" (p=""><0.001) به="" طور="" قابل="" توجهی="" در="" پاسخ="" به="" fan="" افزایش="" یافت،="" اما="" هیچکدام="" به="" طور="" قابل="" توجهی="" تحت="" تأثیر="" رژیم="" غذایی="" قرار="" نگرفتند="" (به="" ترتیب="" 74.74="" و="" 0.67="" p="0)." با="" این="" حال،="" رژیم="" غذایی="" به="" طور="" قابل="" توجهی="" بر="" شدت="" آسیب="" بافت="" ارزیابی="" شده="" توسط="" میکروسکوپ="" با="" موش="" های="" تغذیه="" شده="" با="" wd="" (p="0.001)" و="" ad="" (p="0.004)" که="" آسیب="" بافتی="" شدیدتری="" نسبت="" به="" موش="" هایی="" که="" با="" غذا="" تغذیه="" می="" شوند="" (جدول="" 2="" و="" شکل="" 1).="" ویژگیهای="" بافتشناسی="" غالب="" آسیب="" کلیه،="" اتساع="" لولهای="" و="" نکروز="" حاد="" لولهای="" بود="" که="" در="" موشهای="" تغذیه="" شده="" با="" ad="" و="" wd="" در="" سراسر="" قشر="" شدیدتر="" و="" گستردهتر="" بود.="" هیچ="" تفاوتی="" در="" فیفیبروز="" کلیه="" بین="" گروه="" های="" رژیم="" غذایی="" در="" بخش="" های="" رنگ="" آمیزی="" شده="" picro="" sirius="" مشاهده="" نشد="" (پیوست="" c="" شکل="" a1).="" fan="" باعث="" افزایش="" قابل="" توجهی="" (p="0.005)" در="" اینترلوکین="" در="" گردش="" -6="" (il6)="" شد="" که="" با="" wd="" در="" مقایسه="" با="" موشهایی="" که="" با="" ad="" تغذیه="" شده="" بودند="" تشدید="" شد="" (p="0.01)" و="" چو="" (p="0.006،" جدول="" 2).="" به="" همین="" ترتیب،="" fan="" باعث="" افزایش="" شدید="" بیان="" mrna="" il6="" کلیوی="" شد=""><). با="" این="" حال،="" تفاوت="" معنی="" داری="" بین="" گروه="" های="" رژیم="" غذایی="" وجود="" نداشت="" (9.9.="">

3.2. رژیم غذایی به طور قابل توجهی بر بیان mRNA کلیوی ژن های نفروتوکسیک و لکوسیت خاص در FAN تأثیر می گذارد
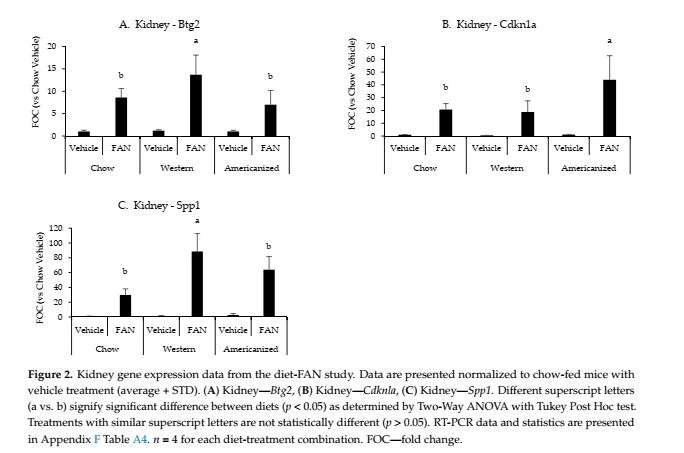
ما در مرحله بعد به شناسایی مکانیسمهای بالقوه مسئول تشدید آسیب بافتی در موشهای تغذیهشده با WD و AD پرداختیم. نمونه های نماینده از هر رژیم غذایی انتخاب شد و بیان 84 ژن مرتبط با سمیت کلیوی با استفاده از یک آرایه PCR تجاری موجود غربال شد (داده های خام در جدول A3 پیوست E ارائه شده است). در مقایسه با موش های تغذیه شده با وسیله نقلیه، 57 ژن نفروتوکسیک به عنوان دارای بیش از 50 درصد تغییر در بیان با FAN شناسایی شدند، و شش مورد از آنها براساس رژیم غذایی متفاوت بودند (پیوست F جدول A4). از شش ژن شناسایی شده توسط آزمایش سمیت کلیوی، بیان کلیه Btg2 (p=0.03)، Cdkn1a (p=0.01) و Spp1 (p=0.001) معنیدار بود. تحت تأثیر رژیم غذایی که با استفاده از RT-PCR معمولی تعیین می شود. موش های تغذیه شده با WD بیان بیشتری از Btg2 و Spp1 در مقایسه با موش های تغذیه شده با غذا و AD داشتند، در حالی که موش های تغذیه شده با AD بیان بیشتری از Cdkn1a در مقایسه با موش های تغذیه شده با غذا و WD داشتند (پیوست F جدول A4 و شکل 2). . ما همچنین بیان mRNA کلیوی 4 نشانگر اختصاصی لکوسیت (CD3e، CD19، CCR2، و Ly6G) را تعیین کردیم، که همه آنها به طور قابل توجهی تحت تأثیر FAN قرار گرفتند (ضمیمه F جدول A4). با این حال، رژیم غذایی هیچ اثر قابل توجهی بر بیان نشانگرهای اختصاصی لکوسیت در کلیه نداشت.
ما قبلا نشان داده بودیم که طحال به طور قابل توجهی بر آسیب شناسی ایمنی آسیب کلیه تأثیر می گذارد [26-28]. بنابراین، ما تصمیم گرفتیم تعیین کنیم که آیا رژیم غذایی بیان mRNA طحال همان نشانگرهای اختصاصی لکوسیت را در FAN تغییر میدهد یا خیر. FAN باعث کاهش قابل توجهی در بیان mRNA طحال نشانگر سلول T Cd3e (p=0.001) و نشانگر سلول B Cd19 (p <0.001) شد="" (شکل="" 3)="" و="" ضمیمه="" f="" جدول="" a4).="" با="" توجه="" به="" رژیم="" غذایی،="" موشهایی="" که="" با="" ad="" تغذیه="" شدهاند،="" بیان="" mrna="" طحال="" کمتری="" از="" cd3e="" (p="0.01)" و="" cd19="" (p="0.009)" در="" مقایسه="" با="" موشهایی="" که="" با="" غذا="" تغذیه="" شدهاند="" اما="" موشهایی="" که="" با="" wd="" تغذیه="" شدهاند،="" کمتر="" داشتند="" (p="" بزرگتر="" یا="" مساوی="" 0.2).="" هیچ="" اثر="" معنی="" داری="" رژیم="" غذایی="" (p="0.8)" یا="" fan="" (p="0.1)" بر="" بیان="" il6="" طحال="" (داده="" ها="" نشان="" داده="" نشده="" است)="" وجود="">

3.3. رژیم غذایی به طور قابل توجهی بر بیان ژن اختصاصی لکوسیت در uIRI تأثیر می گذارد
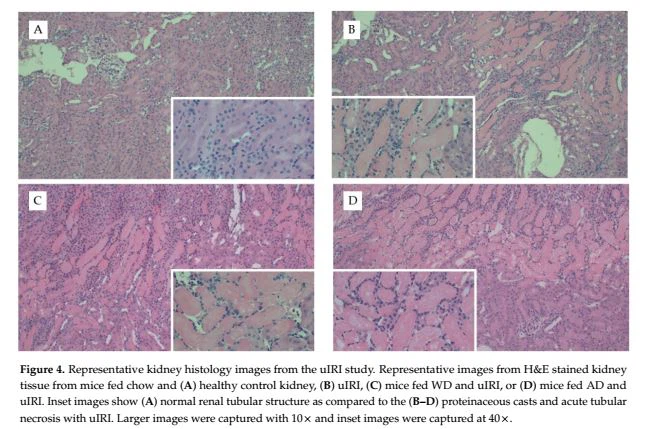
ما مطالعات رژیم غذایی خود را در مدل uIRI تکرار کردیم تا تعمیم پذیری داده های FAN را ارزیابی کنیم. علیرغم تفاوت معنی داری در میزان چاقی بین گروه های درمانی رژیم غذایی، تفاوت معنی داری در زمان جراحی (~ 5 دقیقه) بین گروه های درمان مشاهده نشد (5/0=0). رژیم غذایی بر شدت آسیب بافتی که با تعیین کمیت H&E- (p=0.7، شکل 4) یا اسلایدهای رنگ آمیزی شده با Picro Sirius (پیوست D شکل A2) تعیین می شود، تأثیری نداشت. در حالی که موشهای تغذیه شده با AD وزن کلیههای بیشتری در مطالعه FAN داشتند، در مطالعه uIRI فقط تمایل به رژیم غذایی برای تأثیرگذاری بر وزن کلیه وجود داشت (p=0.07). در کلیه طرف مقابل غیر ایسکمیک، موشهایی که با غذای خوراکی تغذیه میشدند، وزن کلیههای عددی کمتری داشتند (22 ± 160 میلیگرم) در مقایسه با موشهای تغذیهشده با AD (14 ± 168) و WD (15 ± 186). روندهای عددی مشابهی در کلیه های ایسکمیک مشاهده شد که در آن موش های تغذیه شده با غذا (24 ± 173 میلی گرم) یا موش های تغذیه شده با AD (12 ± 170) وزن کلیه عددی کمتری در مقایسه با موش های تغذیه شده با WD (32 ± 195) داشتند. این داده ها نشان می دهد که اثر رژیم غذایی بر وزن کلیه با آسیب به مدل مورد استفاده بستگی دارد.
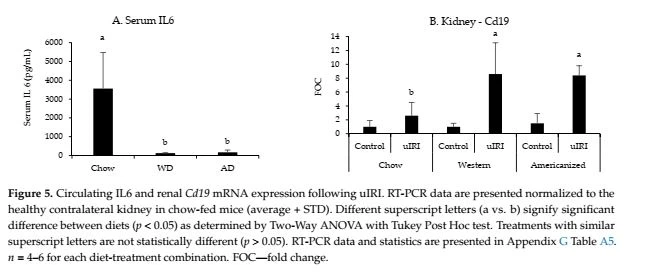
تمام ژنهای نفروتوکسیک و لکوسیتی خاص که در کلیهها کمیتسازی شدهاند، بهجز Cd3e به طور قابلتوجهی تحت تأثیر uIRI قرار گرفتند (p=0.1، ضمیمه G جدول A5). با این حال، هیچ یک از ژن های نفروتوکسیک شناسایی شده در مطالعه FAN به طور قابل توجهی تحت تاثیر رژیم غذایی قرار نگرفت. با توجه به بیان ژنهای اختصاصی لکوسیت، اثر uIRI بر بیان mRNA Cd19 کلیوی به شدت به تغذیه با رژیم غذایی وابسته بود (008/0 {{8}) و موشهایی که با WD و AD تغذیه شده بودند تقریباً چهار برابر بود. بیان بالاتر Cd19 کلیه پس از uIRI در مقایسه با موش های تغذیه شده با غذا (شکل 5). همچنین تمایلی برای موشهای تغذیهشده با غذا وجود داشت که بعد از uIRI بیان کلیوی Ly6g بیشتری داشته باشند (ص=0.06، ضمیمه G جدول A5). جالب توجه است، موشهایی که با WD (p=0.006) و AD (p=0.004) تغذیه شدهاند، غلظتهای IL6 در گردش خون بهطور قابلتوجهی در مقایسه با موشهای تغذیهشده با غذا کمتر بود (شکل 5).
رژیم غذایی به طور قابل توجهی بر بیان mRNA طحال Cd19 (p=0.008)، Ccr2 (p =0.004) و Ly6g (p {{7}) تأثیر گذاشت. }.03) به دنبال uIRI (شکل 6 و پیوست G جدول A5). موشهای تغذیه شده با غذا دارای بالاترین بیان طحالی این نشانگرها بودند، با Ccr2 نسبت به موشهایی که با WD (p=0.02) و AD (p=0.005) تغذیه میشدند، بیان Cd19 به طور قابلتوجهی بیشتر از موشهای تغذیهشده بود. AD (p=0.007)، اما نه WD (p=0.4)، و بیان Ly6g بیشتر از موشهایی که AD تغذیه کردند (p=0.04) و تمایل به بیان بیشتر در موش های تغذیه شده با WD (p=0.07). هیچ تفاوتی در بیان نشانگرهای اختصاصی لکوسیت بین موشهای تغذیهشده با WD یا AD وجود نداشت (به ترتیب برای Ccr2، Cd19 یا Ly6g، 0.9، 0.8، و 0.1=0).

4. بحث
در اینجا، ما دادههایی را ارائه میکنیم که نشاندهنده تأثیر رژیم غذایی بر شدت و آسیبشناسی ایمنی بیماری کلیوی در مدلهای موش بالینی است. موش های تغذیه شده با WD و AD هر دو درجات بالایی از آسیب بافتی و بیان متفاوت ژن های نفروتوکسیک را به دنبال FAN در مقایسه با موش های تغذیه شده با غذا داشتند. موشهایی که با WD تغذیه میشوند، اما نه AD، سطوح گردشی قابلتوجهی بالاتری از IL6 به دنبال FAN داشتند. در uIRI، ما اثر قابل توجهی از رژیم غذایی بر شدت آسیب بافتی یا بیان کلیوی ژنهای نفروتوکسیک مشابه مشاهده نکردیم. با این حال، کاهش قابل توجهی در IL در گردش و بیان ژنهای اختصاصی لکوسیت در کلیه و طحال موشهای تغذیه شده با WD و AD مشاهده کردیم. روی هم رفته، این داده ها نشان می دهد که رژیم غذایی به طور قابل توجهی بر آسیب شناسی ایمنی دو مدل مجزای آسیب کلیوی موش تأثیر می گذارد.
به طور شگفت انگیزی مطالعات کمی در مورد تأثیر رژیم غذایی بر پیامدهای آسیب کلیه وجود دارد. موشهای C57Bl/6 که به مدت 9 هفته از رژیم غذایی پرچرب تغذیه شدند، در مقایسه با موشهای تغذیه شده با غذا، آسیب کلیوی ناشی از سیس پلاتین بدتر داشتند [29]. لازم به ذکر است که دوز سیس پلاتین در این مطالعه بر اساس وزن بدن بود و منجر به دریافت مقدار مطلق سیس پلاتین در موش های پرچرب شد. این یک عارضه رایج در مطالعات رژیم غذایی است و دلیل منطقی برای تجویز همان حجم و مقدار مطلق FA به همه موش ها بود.
در حالی که تعداد محدودی مقاله در مورد تأثیر رژیم غذایی بر پیامدهای بیماری کلیوی توصیف میشود، ادبیات قابلتوجهی در مورد تأثیر دیابت بر حساسیت و پیشرفت آسیب کلیوی در جوندگان وجود دارد [3{14}}-33]. مطالعات در حال انجام (منتشر نشده) در آزمایشگاه ما نشان می دهد که موش هایی که با WD و AD تغذیه می شوند، کالری دریافتی روزانه بالاتری دارند (به ترتیب 16 و 15 کیلو کالری در روز) در مقایسه با موش های تغذیه شده با غذا (12 کیلو کالری در روز). جالب توجه است، تنها موشهایی که با WD شواهد مقاومت به انسولین را تغذیه کردند، هیپوگلیسمی ناشتا (12{17}}.3 میلیگرم در دسیلیتر) در اوایل 8 هفته پس از شروع رژیم مشاهده شد و افزایش چهار برابری در انسولین ناشتا در گردش مشاهده شد. 4.2 نانوگرم در میلی لیتر) پس از 24 هفته. موشهای تغذیه شده با غذا و AD دارای گلوکز ناشتا (به ترتیب 166 و 167 میلیگرم در دسیلیتر) و سطوح انسولین (به ترتیب 0.6 و 1.0) در مقاطع زمانی مشابه هستند. با توجه به سینتیک این دادهها، ما معتقدیم که AD با موفقیت نارساییهای تغذیهای متوسط را مدلسازی میکند و در بازه زمانی مطالعه کنونی فاقد اختلال متابولیک است، در حالی که موشهایی که با WD تغذیه میشدند احتمالاً مقاومت به انسولین داشتند.
Previous work has shown diabetic mice have altered renal hemodynamics [30], exacerbated inflflammatory response [31,32], and altered expression of cell-cycle regulators [33] following kidney injury. Interestingly, we also observed alterations in the immune response and cell-cycle regulators in both WD- and AD-fed mice. Regarding the immune response, mice fed the WD had greater circulating IL6 concentrations than mice fed chow and the AD. This suggests that the overt obesity and developing metabolic dysfunction that is likely developing in the WD-fed mice exacerbates the immune response in FAN. We did not observe a signifificant increase in renal or splenic mRNA expression of IL6 in either the FAN or uIRI model suggesting another tissue source (perhaps the liver [34]) is responsible. The spleen is a reservoir of deployable leukocytes [35,36] and we have previously shown the spleen to play a signifificant role in the pathophysiology of kidney injury with splenic size being inversely correlated with kidney injury [26–28]. Mice fed the WD and AD had a>کاهش 30 درصدی در بیان نشانگرهای لکوسیتی در طحال، که می تواند به عنوان افزایش گسترش لکوسیت ها از طحال تفسیر شود. این امر نشان دهنده افزایش التهاب در موش هایی است که با WD و AD تغذیه می شوند. با این حال، داده های IL6 در گردش تنها از این فرضیه در موش های تغذیه شده با WD پشتیبانی می کند. مطالعات اضافی با فلوسایتومتری و توصیف گستردهتر کموکاینها و سیتوکینهای در گردش برای درک بهتر چگونگی تأثیر رژیم غذایی بر ایمونولوژی و پاتوفیزیولوژی FAN مورد نیاز است.
با توجه به تنظیم کننده های پیشرفت چرخه سلولی، رژیم غذایی نیز به طور قابل توجهی بر بیان mRNA Btg2 و Cdkn1a (p21) به دنبال FAN تأثیر گذاشت. مطالعات حذفی نشان می دهد که نقش محافظتی Cdkn1a در بیماری کلیوی (در [37] بررسی شده است) و بیان Btg2 نیز در کلیه ایسکمیک، اما نه در کنترل مقابل، افزایش یافته است [38]. با این حال، عملکرد و اهمیت تنظیم مثبت Btg2 در آسیب و بیماری کلیه مشخص نشده است. Btg2 یک عامل پاییندستی NFκB و تنظیمکنندههای چرخه سلولی p53 و p19 است که با استفاده از مکانیسمهای سلولی مختلف منجر به محاصره چرخه سلولی میشود (در [39] بررسی شده است). با هم، ادبیات کنونی نشان میدهد که مهارکنندههای چرخه سلولی در کاهش آسیب اولیه کلیه مفید هستند، اما همچنین ممکن است پیشرفت بعدی به شکلهای مزمنتر بیماری را تقویت یا حتی تسهیل کنند [37،38،40-43]. تفاوت در بیان Btg2 و Cdkn1a در موش های تغذیه شده با WD و AD نشان می دهد که چاقی مرضی و نارسایی های تغذیه ای بر پاتوفیزیولوژی آسیب کلیه از طریق مکانیسم های سلولی مختلف تأثیر می گذارد و ممکن است پیامدهای طولانی مدت متفاوتی داشته باشد. علاوه بر این، تفاوت در بیان Btg2 و Cdkn1a ممکن است به هیپرتروفی کلیه مشاهده شده در مدل FAN کمک کند. نشان داده شده است که مدل FAN باعث ایجاد هیپرتروفی حاد کلیه می شود [20،21]، و AD دارای ترکیب معدنی غذایی است که همچنین نشان داده شده است که باعث ایجاد هیپرتروفی و آسیب کلیه در موش ها می شود [44،45]. بنابراین، ممکن است که محتوای مواد معدنی تغییر یافته (به ویژه کلسیم و فسفر) در AD مسئول تشدید هیپرتروفی کلیه در FAN باشد. مطالعات آینده برای تأیید این حدس و گمان و اینکه آیا Btg2 و Cdkn1a درگیر هستند، مورد نیاز است.
ما همچنین دریافتیم که بیان کلیوی Spp1 mRNA به طور قابلتوجهی تحتتاثیر FAN و رژیم غذایی قرار میگیرد، با بیان بالاتر در موشهایی که از WD تغذیه شدهاند در مقایسه با موشهایی که با غذا تغذیه میشوند، اما نه AD. Spp1 (استئوپنتین) یک گلیکوپروتئین است که به طور معمول در ادرار ترشح می شود و در کلیه ها، به ویژه در نفرون دیستال قشر، به شدت بیان می شود. Spp1 نقش کلیدی در تنظیم تشکیل کریستال کلسیم و رسوب در لوله های کلیه دارد [46-49]، فرآیندی که به رژیم غذایی، استروژن و FGF23 وابسته است [7،50،51]. به طور کلی به دنبال آسیب کلیوی تنظیم می شود [52]. با این حال، نقش Spp1 در آسیب ایسکمیک کلیه نامشخص است و مطالعات بیشتری برای روشن کردن اهمیت فیزیولوژیکی افزایش بیان آن با چاقی و بیماری مورد نیاز است.
ما همچنین نتایج را در یک مدل آسیب ایسکمی خونرسانی مجدد یک طرفه ارزیابی کردیم. ما تغییراتی را در بافتشناسی یا بیان mRNA ژنهای مرتبط با سمیت کلیوی شناساییشده در مطالعه FAN در مدل uIRI خود مشاهده نکردیم. فقدان تفاوت در بیان Btg2 و Cdkn1a کلیه در مطالعه uIRI ممکن است توضیح دهد که چرا هیپرتروفی کلیه در موش هایی که با AD در مطالعه FAN تغذیه شده بودند مشاهده نشد. با این حال، رژیم غذایی بر بیان نشانگرهای ایمنی در کلیه و طحال تأثیر داشت. بیان کلیوی نشانگر سلول B CD19 در موش های تغذیه شده با WD و AD در مقایسه با موش های تغذیه شده با غذا بیش از دو برابر شد. اهمیت این یافته نامشخص است، زیرا نقش سلولهای B در مدلهای موشی AKI ایسکمیک پیچیده است و پیامدها به عوامل مختلفی (نوع فرعی، کلاس آنتیبادی و غیره) وابسته هستند [53-56]. رژیم غذایی همچنین به طور قابل توجهی بر بیان mRNA نشانگرهای ایمنی در طحال (Ccr2، Cd19، و Ly6g) تأثیر گذاشت، که در آن موشهایی که با WD و AD تغذیه میشوند در مقایسه با موشهای تغذیه شده با غذا، بیان کمتری داشتند. همانطور که در بالا ذکر شد، این می تواند به عنوان افزایش استقرار لکوسیت ها از طحال و تشدید پاسخ ایمنی سیستمیک در موش های تغذیه شده با WD و AD تفسیر شود. با این حال، IL6 در حال گردش سرکوب شده در موشهایی که با WD و AD تغذیه شدهاند، یک اثر سرکوبکننده سیستم ایمنی این رژیمها را در مدل uIRI نشان میدهد. مکانیسمهای مولکولی مختلف آسیب سلولی در مدلهای بیماری کلیوی توصیف شده است [57-59]، و مطالعه ما نشان میدهد که رژیم غذایی ممکن است این مکانیسمها را اصلاح کند. مطالعات بیشتری برای تأیید این حدس و گمان و تعیین اینکه چگونه رژیم غذایی به طور قابل توجهی پاسخ التهابی و مسیرهای مرگ سلولی دخیل در آسیب کلیه را تغییر می دهد مورد نیاز است.
محدودیتهایی وجود دارد که باید هنگام مقایسه دادههای ما با دیگران در ادبیات، بهویژه در مطالعات uIRI در نظر گرفت. ما یک مدل یک طرفه را برای کاهش عوارضی که در حین جداسازی عروق کلیوی از بافت چربی بیش از حد در موشهای تغذیه شده با WD و AD با آن مواجه بودیم، انتخاب کردیم. بنابراین، معیارهای سرمی عملکرد کلیه در مطالعات uIRI با توجه به وجود کلیه سالم و غیر ایسکمیک طرف مقابل اندازه گیری نشد. ما همچنین از بیحسی ایزوفلوران استفاده کردیم زیرا موشهای چاق مخلوط بیهوشی کتامین/گزیلازین را که معمولاً در این مدل استفاده میشود، تحمل نمیکردند [60]. نشان داده شده است که ایزوفلوران آسیب کلیه را در IRI کاهش می دهد [61] و نیاز دارد که زمان ایسکمیک خود را از 30 به 45 دقیقه افزایش دهیم تا به آسیب مشاهده شده برسیم. این تجربیات باعث نگرانی در مورد نتایج مطالعات uIRI ما شد و دلیلی برای تمرکز ما بر مدل FAN بود. همچنین مهم است که تأکید شود تغییرات در بیان ژن با تغییر در تولید پروتئین برابری نمیکند و مطالعات بیشتری برای تأیید تغییرات در فراوانی پروتئین و تغییرات بعدی در سلامت و عملکرد سلولی مورد نیاز است.

سیستانچ می تواند آسیب کلیه را درمان کند
5. نتیجه گیری ها
در نتیجه، ما داده هایی را ارائه می دهیم که از اهمیت رژیم غذایی در حساسیت به آسیب کلیه حمایت می کند. یافتههای ما نشان میدهد که رژیم غذایی ایجاد شده برای مدلسازی صدک 50 دریافت مواد مغذی در آمریکاییها برای تشدید آسیب کلیوی در جوندگان به میزان مشابهی که در یک WD تجاری موجود مشاهده شده است، کافی است. دادههای ما همچنین نشان میدهد که ارتباط مکانیکی بین تغذیه، التهاب، و تنظیم چرخه سلولی در آسیبشناسی ایمنی آسیب کلیه وجود دارد که بهطور قابلتوجهی پیامدهای بیماری را تغییر میدهد. روی هم رفته، مطالعه ما نیاز به افزایش قدردانی و توجه به تغذیه در مطالعات پیشبالینی حیوانی مکانیکی را برجسته میکند.
مشارکت نویسنده:
مفهوم سازی، JCG; روش، JCG، JFH، JEB، RL. تجزیه و تحلیل رسمی، JCG; بررسی، JEB، DLQ، KJW، BB، HTH، RL، JFH. منابع، JCG، JFH; مدیریت داده، JCG، JFH. نوشتن - آماده سازی پیش نویس اصلی، JCG، JFH. نوشتن- بررسی و ویرایش، JEB، DLQ، KJW، BB، HTH، RL، JFH؛ نظارت، JCG، JFH; مدیریت پروژه، JCG، JFH؛ تأمین مالی، JCG همه نویسندگان نسخه منتشر شده نسخه خطی را خوانده و با آن موافقت کرده اند.
منابع مالی:
این تحقیق با کمک هزینه های داخلی از دانشگاه لیبرتی و کالج پزشکی استئوپاتی دانشگاه لیبرتی، کمک هزینه از انجمن استئوپاتی آمریکا (گرنت #19133749) و کمک هزینه از مؤسسه ملی بهداشت (1R01DK113632-01A1) پشتیبانی شد. .
بیانیه هیئت بررسی نهادی:
این مطالعه بر اساس راهنمای مراقبت و استفاده از حیوانات آزمایشگاهی [8] و تایید شده توسط کمیته مراقبت و استفاده از حیوانات سازمانی دانشگاه لیبرتی (#49.190710، 11 ژوئیه 2019) انجام شد.
قدردانی ها:
ما میخواهیم از جسیکا فلاورز در Teklad Diets (Envigo) برای کمک او در ایجاد مرکز بافتشناسی AD و دانشگاه ویرجینیا برای خدمات بافتشناسی قدردانی کنیم.
تضاد علاقه:
نویسندگان هیچ تضاد منافع را اعلام نمی کنند.
از: "رژیم غذایی به طور قابل توجهی بر آسیب شناسی ایمنی و شدت آسیب کلیه تاثیر می گذارد" توسطجان ای بروس و همکاران
---مواد مغذی 2021، 13، 1521
