اثرات فشارهای پرفیوژن بر از دست دادن پودوسیت در کلیه پرفیوژن ایزوله موش
Mar 13, 2022
خلاصه
زمینه/هدف: پودوسیت ها در اکثر بیماری های گلومرولی از بین می روند که منجر به گلومرولواسکلروز و پیشرونده می شود.بیماری کلیوی. به طور کلی فرض بر این است که پودوسیت ها در معرض جریان فیلتراسیون و در نتیجه نیروهای برشی قابل توجهی هستند که باعث جدا شدن آنها از غشای پایه گلومرولی (GBM) می شود. در این زمینه، رفع فرآیند پا به عنوان یک پاسخ تطبیقی بالقوه برای افزایش چسبندگی پودوسیت ها به GBM پیشنهاد شده است. روشها: ما این فرضیهها را با استفاده از پاکسازی نوری و تجزیه و تحلیل مورفومتریک ابعادی با وضوح بالا در موش پرفیوژن جدا شده آزمایش کردیم.کلیهما پویایی جدا شدن پودوسیت را در فشارهای پرفیوژن مختلف (50، 300 و بیش از 450 میلیمتر جیوه) در موشهای جوان یا مسن سالم (20 در مقابل 71 هفتگی) یا موشهایی که با سرم ضد GBM برای القای پای جهانی تزریق شده بودند، بررسی کردیم. حذف فرآیند یافتهها: نتایج نشان میدهد که پودوسیتهای سالم در موشهای جوان محکم به GBM چسبیدهاند و حتی فشارهای فوقمکزیمم باعث جدا شدن معنیدار نشدند. در مقایسه با موشهای جوان، در موشهای مسن و موشهای مبتلا به نفریت ضد GBM و از بین رفتن فرآیند پا، از دست دادن تدریجی سلولهای پادوسیت قبل از پرفیوژن رخ داده بود. فشار پرفیوژن بالا منجر به از دست دادن اضافی نسبتاً جزئی سلولهای بدن در موشهای مسن شد. در موشهای مبتلا به نفریت ضد GBM، از دست دادن پودوسیتهای اضافی قابلتوجهی در این نقطه اولیه زمانی که فشار خونرسانی به 300 میلیمتر جیوه یا بالاتر افزایش مییابد، رخ داد. نتیجهگیری: این کار اولین شواهد تجربی را ارائه میکند که نشان میدهد پودوسیتها به طور فوقالعادهای در برابر فشارهای پرفیوژن حاد افزایش یافته در محیط خارج شده از بدن مقاوم هستند.کلیهمدل پرفیوژن فقط در بیماری گلومرولی، تعداد قابل توجهی از پودوسیتهای آسیب دیده به دنبال افزایش حاد فشار خون جدا شدند.
کلید واژه ها:فشار خون گلومرولی؛ هایپرفیلتراسیون گلومرولی؛ استرس مکانیکی؛ پیشرفت؛ بیماری مزمن کلیوی

سیستانچ بیماری کلیوی/کلیوی را بهبود می بخشد
مقدمه
فشار خون و هایپرفیلتراسیون گلومرولی به گلومرول آسیب می رساند که منجر به بیماری پیشرونده گلومرولی می شود. به طور گسترده اعتقاد بر این است که افزایش فشار پرفیوژن توفت را در معرض افزایش استرس مکانیکی قرار می دهد که چسبندگی پودوسیت ها به غشای پایه گلومرولی (GBM) را به چالش می کشد و به جدا شدن آنها کمک می کند [1، 2]. پودوسیت ها سلول های بسیار متمایز و پس از میتوزی هستند که برای یک سد فیلتراسیون گلومرولی دست نخورده ضروری هستند. از دست دادن پودوسیت به احتمال زیاد نتیجه جدا شدن سلولهای زنده از GBM است نه آپوپتوز یا نکروز [3-6] زیرا کشت سلولهای پادوسیت بازیابی شده از ادرار بیماران امکانپذیر بوده است [4]. جدا شدن پودوسیتهای زنده از GBM ممکن است به دلیل اختلال در مکانیسمهای اتصال یا نیروهای آلتمکانیکی باشد. اختلال در اتصال به GBM ممکن است به دلیل آسیب سلولی یا کاهش بیان مولکول های چسبندگی باشد و عمدتاً با بیماری های التهابی گلومرولی مرتبط است. با توجه به نیروهای مکانیکی مربوط به پودوسیت، دو عامل تعیین کننده کلیدی وجود دارد، یعنی فشار فیلتراسیون و جریان فیلتر [7-9]. فشار فیلتراسیون فشار دیواره محیطی ایجاد می کند و به عنوان یک نیروی انبساط کننده بر روی GBM عمل می کند. تغییرات فشار هیدرواستاتیک بین دیواری به طور موثر با توانایی GBM برای عمل به عنوان یک غشاء الاستیک و انبساط یا کوچک شدن در سطح سطح جبران می شود [8، 10]. از سوی دیگر، جریان فیلتر در سراسر GBM نیروهای مماسی را بر روی سطح سلولهای پودوسیت اعمال میکند، یعنی تنش برشی. ما از مطالعات آزمایشگاهی میدانیم که پودوسیتها در مواجهه با تنشهای برشی بیش از 0.025 Pa [11] و اتخاذ یک فنوتیپ میانی که ممکن است به آنها در مقابله با نیروهای ناشی از جریان کمک کند، بسیار مستعد جدا شدن تنش برشی از بستر خود هستند [12]. اینکه فشار خون گلومرولی از طریق افزایش فشار فیلتراسیون و/یا افزایش فیلتراسیون بر سلولهای پادوسیت تأثیر میگذارد، هنوز مشخص نیست. در این مطالعه، ما اولین تحلیل از توانایی سلولهای پودوسیت برای مقاومت در برابر نیروهای مکانیکی افزایش یافته را در یک مدل ex vivo ارائه میکنیم. از دست دادن پودوسیت با وضوح بالا با استفاده از پاکسازی بافت و تجزیه و تحلیل مورفومتریک ابعادی در موشهای جوان و سالم اندازهگیری شد.
مواد و روش ها
همه آزمایشهای حیوانی بر اساس دستورالعملهای قانون آلمان برای رفاه حیوانات انجام شد و توسط Landesamt für Natur، Umwelt und Verbraucherschutz Nordrhein-Westfalen (Az 84-02.04. 2015.A469) تأیید شد. موشها در یک مرکز خاص بدون پاتوژن با دسترسی رایگان به غذا و آب و یک چرخه روز/شب 12-ساعت نگهداری شدند. اصلاح نژاد و ژنوتیپ بر اساس روش های استاندارد انجام شد. موشهای Pod-rtTA/LC1/R26R/H2BeGFP روی یک پسزمینه ژنتیکی FVB/N قبلاً شرح داده شدهاند [13]. برای فعال کردن بیان تراریخته Pod-rtTA-eGFP، موشها داکسیسایکلین را از طریق آب آشامیدنی بهطور آزاد به مدت 7 روز (2 گرم در لیتر، 5 درصد ساکارز، محافظتشده از نور) دریافت کردند و طبق گزارشهای قبلی، یک دوره شستشوی 1 هفتهای انجام شد. نفریت ضد GBM با یک تزریق داخل صفاقی 5 میلی گرم بر گرم سرم نفروتوکسیک وزن بدن همانطور که قبلاً توضیح داده شد القا شد [14].

CISTANCHE عملکرد کلیه/کلیه را بهبود می بخشد
پرفیوژن کلیه
منزوی هاکلیهمدل پرفیوژن همانطور که در جای دیگر توضیح داده شد استفاده شد [15]. به طور خلاصه، موشها با تزریق داخل صفاقی زایلازین/کتامین (0، 1 میلیلیتر/10 گرم وزن بدن داخل صفاقی)، و سپس کلیهها با یک محلول پیچیده اصلاحشده Krebs-Henseleit (جدول 1) همراه با 5 پرفیوژن شدند. درصد آلبومین سرم گاوی (BSA) در 37 درجه برای تقلید از محیط فیزیولوژیکی در طول آزمایش. حداکثر اتساع عروقکلیهعروق با 1. تزریق زیر جلدی وراپامیل (50 میکرولیتر) بلافاصله پس از القای بیهوشی و 2. افزودن پاپاورین به محلول پرفیوژن ایجاد شد. پس از پرفیوژن اولیه به مدت 5 دقیقه در 50 میلیمتر جیوه، یک لکتین نشاندار شده با فلورسنت (Communis I - RCA120؛ آزمایشگاههای وکتور: RL{8}}؛ 4 ul در 986 ul سالین) برای برچسبگذاری سلولهای اندوتلیال تزریق شد.کلیه هابه مدت 5 دقیقه دیگر با محلول اصلاح شده Krebs-Henseleit با 5 درصد BSA پرفیوژن شدند. پس از آن، سمت چپکلیهکه در هر آزمایش به عنوان کنترل جفتی عمل می کرد، پس از بستن دقیق سمت چپ حذف شدکلیهظروف، برش داده شده و مستقیماً در 3 درصد پارافورمالدئید (PFA) در سالین بافر فسفات (PBS) غوطه ور می شوند. حقکلیه was perfused either for additional 5 minutes at 300 mmHg or with supramaximal pressure (>>300 میلیمتر جیوه، فشارهای فیلتراسیون بسیار بالاتر از 400 میلیمتر جیوه تخمین زده شد، به صورت دستی اعمال شد، حجم کل 50 میلیلیتر محلول پرفیوژن. اینکلیه هابا فشار ثابت 50 میلیمتر جیوه یا 300 میلیمتر جیوه با استفاده از پمپ کنترلشده فشار (Universal Perfusion Systems UP{3}}، Hugo-Sachs Electronics، آلمان) پرفیوژن شدند. سپس سمت راستکلیهبرداشته شد، به برش های 2 میلی متری بریده شد و در 3 درصد پارافورمالدئید (PFA) در سالین بافر فسفات (PBS) غوطه ور شد.
تصویربرداری سه بعدی و تحلیل محاسباتی غوطه ور در PFAکلیهبرش ها روی شیکر مکانیکی به مدت 5 روز در دمای اتاق انکوبه شدند. پس از آن، نمونه های ثابت در 1x PBS شسته شده و در یک شیکر مکانیکی به مدت یک شب در دمای اتاق قرار داده شدند.کلیهسپس برش ها در اتانول 100 درصد با عیار بالا (Merck; 100983) به مدت 1 ساعت در دمای اتاق با تکان دادن ملایم (حداقل 1 تغییر به اتانول تازه)، و به دنبال آن غوطه ور شدن مستقیم در اتیل سینامات (ECi) (Sigma-Aldrich, سنت لوئیس، MO؛ 112372) و یک شبه در یک تکان دهنده ملایم در دمای اتاق و تحت حفاظت نور رها شدند. شفافیت بافت در کمتر از 1 ساعت به دست آمد. برای میکروسکوپ های عمودی، ما از محفظه های یکبار مصرف ساخته شده در خانه همانطور که قبلا توضیح داده شد استفاده کردیم [16]. بیشتر آزمایشها با استفاده از میکروسکوپ فوتونی 2- (LaVision BioTec TriMScope، "Medizinische Fakultät RWTH Aachen، IZKF Aachen، Core Facilities) انجام شد. از نرم افزار تصویربرداری فیجی برای حرکت در محور Z هر پشته از بخش های نوری سریال استفاده شد. و برای جداسازی گلومرول های فردی از طریق کشت سه بعدی [16]. 40 گلومرول در هرکلیه(20 ساب کورتیکال و 20 جناح مدولاری) برای تجزیه و تحلیل انتخاب شدند. بنابراین، در مجموع 1200 گلومرول در این مطالعه برای به دست آوردن نتایج با دقت کافی مورد تجزیه و تحلیل قرار گرفت. پودوسیت ها به عنوان سلول های eGFP به علاوه شناسایی شدند. کمی سازی حجم مویرگی، حجم گلومرولی و همچنین تعداد هسته (نقاط) و حجم با استفاده از یک نرم افزار رندر و تحلیل سه بعدی (Imaris v9.1; Bitplane AG، زوریخ، سوئیس) انجام شد. فاصله پودوسیت ها از قطب عروقی با استفاده از آن محاسبه شد. Bitplane XTension "نزدیکترین نقطه. فاصله". کمی سازی خودکار پودوسیت ها همانطور که قبلاً توضیح داده شد [17] انجام شد. تجزیه و تحلیل تصویر با استفاده از Imaris (Biplane AG Zurich، سوئیس) انجام شد. هر گلومرول توسط شریان آوران نشاندار شده با لکتین آن تعریف شد. 20 ساب کورتیکال و 20 جناحی (که با فاصله آنها از سطح قشر مغز مشخص می شود).

سیستانچ درد کلیه/کلیه را بهبود می بخشد
میکروسکوپ نوری و ایمونوفلورسانس
برای میکروسکوپ نوری، فرمالین بافر 4 درصد ثابت شدکلیهقطعات خشک شده، در پارافین جاسازی شده و با اسید پریودیک شیف (PAS) رنگ آمیزی شدند. درصد گلومرول های غیرطبیعی/آسیب دیده بر اساس شناسایی 50 سطح مقطع گلومرولی نماینده در هر موش انتخاب شده در طی یک پیاده روی سیستماتیک در سراسر ناحیه محاسبه شد.کلیهقشر پروتکل استاندارد ایمونوفلورسانس ما [18] بر روی مقاطع 2 میکرومتری تعبیه شده در پارافین انجام شد. آنتی بادی های زیر مورد استفاده قرار گرفت: مرغ پلی کلونال آنتی-GFP (ab13970؛ Abcam)، موش مونوکلونال آنتی-سیناپتوپودین (sc-515842؛ بیوتکنولوژی سانتا کروز)، خرگوش پلی کلونال ضد موش p57 (sc-8298)، سانتا -Cruz Biotechnology), rabbit polyclonal anti-WT1 (sc-192; Santa-Cruz Biotechnology), Cy2 Donkey Anti-Chicen (703-225-155; Dianova, Hamburg, Germany), Alexa Fluor546 goat anti-mouse IgG1 (A{21}}؛ ترمو فیشر)، ضد خرگوش چند کلونال AF555 (A31572; Life Technologies, Carlsbad, CA).
میکروسکوپ الکترونی
قطعات کوچک قشر در محلول کارنوفسکی ثابت شد و در Epon (Serva، هایدلبرگ، آلمان) جاسازی شد. مقاطع فوق نازک با میکروسکوپ الکترونی عبوری ZEISS Leo 906 در 6{26}} کیلوولت با بزرگنمایی 3597-6000x مورد بررسی قرار گرفت. نمونه ها در 0.1 مولار سورنسن فسفات (Merck، دارمشتات، آلمان)، پس از تثبیت در 1 درصد OsO 4 (راث، کارلسروه، آلمان) در بافر 17 درصد ساکارز (Merck، دارمشتات، آلمان) و آبگیری با افزایش سری اتانول (سری اتانول صعودی) شدند. 30، 50، 70، 90 و 100 درصد) هر کدام به مدت 10 دقیقه. مرحله آخر 3 بار تکرار شد. نمونه های خشک شده در پروپیلن اکسید (Serva، هایدلبرگ، آلمان) به مدت 30 دقیقه، در مخلوطی از رزین Epon (Serva، هایدلبرگ، آلمان) و پروپیلن اکسید (1:1) به مدت 1 ساعت و در نهایت در Epon خالص به مدت 1 ساعت انکوبه شدند. پلیمریزاسیون اپون در دمای 90 درجه به مدت 2 ساعت انجام شد. مقاطع بسیار نازک (70-100 نانومتر) توسط اولترامیکروتوم (Reichert Ultracut S، Leica با یک چاقوی الماسی (Leica) برش داده شد و بر روی شبکههای Cu/Rh (HR23 Maxtaform، Plano، Wetzlar Germany) برداشت شد. کنتراست با افزایش یافت. رنگآمیزی با 0.5 درصد اورانیل استات و 1 درصد سیترات سرب (هر دو EMS، مونیخ، آلمان) نمونهها با ولتاژ شتاب 60 کیلوولت با استفاده از میکروسکوپ الکترونی عبوری Zeiss Leo 906 (Carl Zeiss، Oberkochen، آلمان) مشاهده شدند.
تحلیل آماری
تجزیه و تحلیل های آماری با نرم افزار GraphPad Prism v8 انجام شد. همه مقادیر به صورت میانگین ± SD بیان می شوند. برای مقایسه دو گروه از آزمون t استفاده شد. مقایسه چند گروه با استفاده از تحلیل واریانس انجام شد. تصحیح Tukey post hoc برای مقایسه های چندگانه استفاده شد. همه آزمونها 2- دنبالهدار بودند و معنیداری آماری به صورت P < 0.05="" تعریف="">
نتایج
روش نیمه خودکار برای تعیین تعداد پودوسیت در هر گلومرول سه گروه، یعنی موش های سالم جوان و پیر و موش های مبتلا به گلومرولونفریت ضد GBM (♂:♀ 1:1) مورد مطالعه قرار گرفتند. موشهای سالم و جوان 15-21 هفته سن داشتند، در حالی که سن (سالمند) 74 هفته بود. پاکسازی فرآیند جهانی پا در موشهای 14-20 هفتهای از طریق یک تزریق سرم ضد GBM 3 روز قبل از راهاندازی پرفیوژن جدا شده القا شد.کلیهمدل (شکل 1A)، همانطور که قبلا توضیح داده شد [19].

برای تعیین تأثیر فشار پرفیوژن داخل کلیوی بر سلولهای بدن،کلیه هاتحت فشارهای پرفیوژن مختلف در جدا شده قرار گرفتندکلیهمدل پرفیوژن اول، هر دوکلیه هاهمیشه در 50 میلی متر جیوه به مدت 5 دقیقه پرفیوژن می شدند. برای آزمایش اینکه آیا محلول پرفیوژن ما یکپارچگی گلومرول را در حالت ثابت نشده حفظ می کند یا خیرکلیه ها2 موش با فشار ثابت 100 میلی متر جیوه به مدت 90 دقیقه پرفیوژن شدند. پرفیوژن، جریان ادرار (25 میکرولیتر/دقیقه/گرم وزن بدن) و همچنین کلیرانس اینولین (22 میکرولیتر در دقیقه) در تمام مدت ثابت ماندند (شکل تکمیلی 1 - برای همه مواد تکمیلی رجوع کنید بهwww.cellphysiolbiochem.com).در موش های آزمایشی، پس از پرفیوژن اولیه در 50 میلی متر جیوه، سمت چپکلیه was removed and served as a control in all experiments. Next, constant pressure of 300 mmHg or a pressure significantly higher than 300 mmHg (>>300 میلی متر جیوه؛ فشار فیلتراسیون فوق حداکثر در حدود 450 تا 500 میلی متر جیوه) به سمت راست باقی مانده اعمال شد.کلیهبه مدت 5 دقیقه (شکل 1B). در پرفیوژن جدا شدهکلیه هاپودوسیتها با استفاده از برچسبگذاری هستهای با eGFP-هیستون در موشهای تراریختهای که eGFP را تحت پروموتر پودوسین بیان میکنند (موشهای eGFP:Pod-rtTA) شناسایی شدند. تعداد پودوسیت ها با استفاده از ترکیبی از این برچسب گذاری متابولیک in vivo و مورفومتری سه بعدی (شکل 1C) اندازه گیری شد.
از دست دادن پودوسیت در موش های سالم و مسن
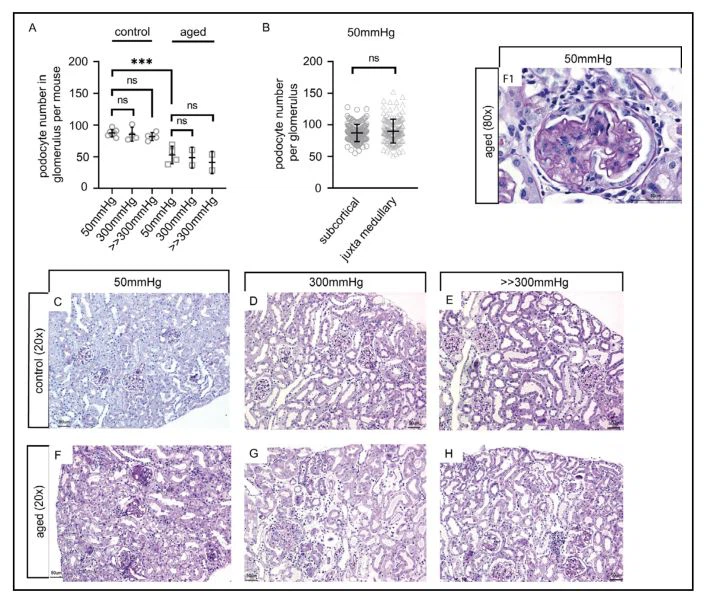
Healthy mice contained 87.46 ± 5.66 (SD) podocytes per glomerulus at baseline (i.e.at physiological perfusion pressure of 50 mmHg) (Fig. 2A). Juxtamedullary glomeruli were larger than those in the outer cortex (Supplementary Fig. 2), but this was not associated with higher podocyte numbers (87.0± 23.65 vs. 90.1 ± 18.49, respectively, Fib 2B). No differences in the number of podocytes related to sex were observed (see below). In young mice, there was no significant loss of podocytes at high (300 mmHg) or maximal (>>300 mmHg) perfusion pressures (85.62 ± 10.83 and 81.98 ± 6.45 podocytes per glomerulus, respectively) (Fig. 1A). On PAS sections, mild histological changwere observed particularly in aged mice (Fig. 2A), which were independent of perfusion pressures. In addition, tubular dilatation and interstitial edema were apparent as a result of perfusion. In humans, older age (53 ± 10 years) has been associated with absolute and relative podocyte depletion [20]. Compared to young mice, our mice aged 72 weeks contained significantly lower numbers of podocytes per glomerulus at baseline (52.81 ± 13.8 SD), indicating that about 40% of the podocytes had been lost. Perfusion at high or maximal pressures resulted in only a very mild reduction of podocyte numbers (48.65 ± 16.8 SD and 41.06 ± 17.7 SD, respectively). Because of the precision of the counting method (absolute podocyte numbers in 40 glomeruli per mouse) [21], the loss of podocytes of 7.9% and 22% after perfusion with 300 or >>300 میلیمتر جیوه به ترتیب در مقایسه با سطح پایه نشان میدهد که این افزایش جزئی در از دست دادن سلولهای بدن با فشار بالاتر، یافتهای تصادفی نیست. در مقاطع PAS، تغییرات خفیف گلومرولی در موشهای مسن در ابتدا مشاهده شد (انبساط مزانژیال و اسکلروز گاه به گاه، شکل 2F). آ
از دست دادن پودوسیت پس از آسیب حاد
سرم Anti-GBM روی موش های سالم جوان استفاده شد تا آسیب قابل توجه و اختصاصی به سلول های پادوسیت ایجاد کند. در نقطه زمانی بسیار اولیه (یعنی 3 روز) پس از القای گلومرولونفریت ضد GBM، از بین رفتن فرآیند عمومی پا در همه گلومرول ها با میکروسکوپ الکترونی عبوری مشاهده شد (شکل 3A-D). در پرفیوژن ایزولهکلیه هاobtained from these mice, at baseline (i.e. perfusion with 50mmHg) podocyte numbers per glomerulus were reduced by 20% compared to controls (69.76 ± 7.07 vs 87.46 ± 5.66, respectively) (Fig. 3E). Perfusion with higher pressures (300 and >>300 mmHg) resulted in significant further reductions of podocyte numbers per glomerulus (50.84 ± 7.82 and 53.18 ± 4.26, respectively), i.e. 27% and 24% additional reduction (Fig. 3E). When analyzing individual glomeruli, the anti-GBM mice, perfusion with >>300 میلی متر جیوه باعث از بین رفتن بیش از 80 درصد پودوسیت در تعداد کمی از گلومرول ها شد (شکل 3E). این با ماهیت کانونی مدل بیماری ضد GBM مطابقت دارد. در گلومرول های جانبی، از دست دادن پودوسیت در مقایسه با گلومرول های زیر قشری بارزتر بود (به ترتیب 16.9 ± 56.66 و 17.07 ± 47.35) (شکل 3F).

By transmission electron microscopy (TEM), specific changes were observed after high perfusion pressures, in particular focal podocyte detachment from the GBM and denuded basement membrane (Fig. 3D). Cellular debris was present within the capillaries as well as within Bowman's space (>>300 میلی متر جیوه)؛ اندوتلیوم تغییرات قابل توجهی را نشان نداد. رنگ آمیزی PAS اتساع لوله ای را مشخص کرد. سه روز پس از تزریق سرم ضد GBM، هنوز هیچ ضایعه هلالی ایجاد نشده بود (شکل 3G-I). نرها درجه بالاتری از از دست دادن پودوسیت را در مقایسه با مادهها نشان دادند (11/2 ± 71/63 در مقابل 83/3 ± 81/75 پودوسیت در هر گلومرول)، که با مشاهدهای که موشهای نر نسبت به آنتیسرم ضد GBM حساستر هستند و هلالهای سلولی بیشتری در دوره تشکیل میدهند مطابقت دارد. بیماری (شکل 3J). با این حال، از دست دادن اضافی پودوسیت ها پس از فشار خون بالا در مردان و زنان مشابه بود (شکل 3J).

شکل 3. از دست دادن پودوسیت پس از آسیب حاد. (AB) میکروسکوپ الکترونی عبوری از یک کنترلکلیه per- fused at a low pressure and after supramaximal pressure (>>300 mmHg) shows normal foot process architecture. (C-D) Transmission electron microscopy reveals the typical finding of foot process effacement after injection of anti-GBM serum at baseline. After perfusion with higher pressure, areas of denuded basement membrane were observed. (E) Total number of podocytes per mouse in anti-GBM mice at baseline and under higher (300 mmHg) or supramaximal pressures (>> 300 mmHg); (each circle represents 1 kidney; n=7 control kidneys with 50mmHg, n=8 anti-GBM kidneys with 50mmHg, n=4 kidneys with 300 mmHg or >> 300mmHg). (F) Total number of podocytes per glomerulus in juxtamedullary and subcortical glomeruli; each circle represents 1 subcortical glomerulus (n= 20 glomeruli pro mouse) and each triangle represents 1 juxtamedullary glomerulus (n= 20 glomeruli pro mouse). (G-I) Histologic staining of anti-GBM mice at baseline identified protein casts, whereas three days after injection of anti-GBM serum no crescentic lesions could be found. After perfusion with higher pressure, tubule-interstitial dilatation and edema were observed. (J) Total podocyte number per mouse between males and females; each circle represents 1 kidney (n=4 control kidneys with 50mmHg, n=4 anti-GBM kidneys with 50mmHg, n=2 kidneys with 300 mmHg or >>300 میلی متر جیوه). برای مقایسه چندگانه ANOVA. ****پ<0.0001, ***p ="" <="" 0,0001,=""><0.01,><0.05 and="" ns="" and="" ns="not" statistically="" significant;="" error="" bars="" represent="" means="" ±="">
ردیابی پودوسیت های از دست رفته در لوله ها
eGFP به علاوه پادوسیت ها به طور منظم در لومن لوله های پروگزیمال مشاهده می شدند، جایی که به نظر می رسید به مرز برس سلول های لوله پروگزیمال می چسبند (شکل 4A). این پادوسیت ها در پرفیوژن هایپرفیوژن شسته نشدندکلیهs، در عوض آنها به مرز برس چسبیده بودند تا در برابر جریان فوقالعاده ادرار اولیه در فشارهای پرفیوژن بسیار بالا مقاومت کنند. برای تأیید هویت آنها، پودوسیت ها با نشانگرهای اختصاصی پودوسیت (یعنی p57، سیناپتوپودین و WT{3}}) علاوه بر نشانگر ژنتیکی eGFP هسته ای (شکل 4B) رنگ آمیزی شدند. تعداد پودوسیتها در گلومرولهایی با پادوسیتهای چسبنده در توبول پروگزیمال مرتبط به طور قابلتوجهی کمتر بود، و حضور پودوسیتها در لولهها با تعداد پودوسیتها در هر گلومرول ارتباط معکوس داشت (شکل 4C).

از دست دادن ترجیحی پودوسیت ها در محل اطراف
Finally, we investigated whether podocyte loss driven by an acute increase in perfusion pressures might occur in preferential locations of the glomerulus (i.e. at the vascular pole vs. the tubular pole of the glomerular tuft). To analyze the spatial distribution of podocyte detachment, the vascular pole was marked in each glomerulus (acquired in 3D) based on the lectin signal and the distance of each podocyte from the vascular pole was determined semi-automatically. The individual distances from the vascular pole were separated into quartiles (Fig. 4E). As depicted in Fig. 4E, the majority of podocytes clustered in the 2 middle quartiles (i.e. quartile 2 and 3). Less than 12 % of the podocytes localized to either in the first, i.e. vascular pole, or the fourth quartile, i.e. most distant from the vascular pole. Upon perfusion with pressures >>300 میلیمتر جیوه، هیچ تغییر معنیداری در توزیع فضایی پودوسیتها در موشهای جوان و سالم مشاهده نشد. در موش های مسن، فاصله پودوسیت ها از قطب عروقی به طور کلی افزایش یافته بود که به احتمال زیاد منعکس کننده هیپرتروفی گلومرولی است، در حالی که پرفیوژن خون منجر به جدا شدن ترجیحی پودوسیت ها در نزدیکی قطب عروقی شد (چارک اول از 11.5 به 4.9 درصد در موش های مسن کاهش یافت، شکل 4E. ). به طور مشابه، جدا شدن ترجیحی پودوسیت ها نزدیک به قطب عروقی در پودوسیت های محو شده مشاهده شد (ضد GBM، چارک اول از 25 به 5 درصد کاهش یافت).
بحث
در این مطالعه، ما اثرات حاد افزایش فشار فیلتراسیون و جریان فیلتراسیون را بر از دست دادن سلولهای پودوسیت در کلیه موش پرفیوژن جدا شده، با استفاده از دقیقترین روش فعلی برای تعیین تعداد پودوسیتها بررسی کردیم. اولین یافته اصلی مطالعه ما این بود که پودوسیت های سالم به تنش برشی حاد در داخل بدن حساس نیستند، همانطور که قبلاً توسط مطالعات کشت سلولی پیشنهاد شده بود [11]. در کمال تعجب، حتی فشارهای فوق فیزیولوژیکی شدید (بیش از 450 میلیمتر جیوه) باعث جداشدگی قابل توجه پودوسیتها نشد. در عوض، میکروسکوپ الکترونی عبوری نشان داد که هر سه لایه مانع فیلتراسیون نسبتاً به خوبی حفظ شدهاند. موشهای مسنتر تعداد پودوسیتها را کاهش دادند (همانطور که قبلاً گزارش شد) و این فقط با افزایش حساسیت بسیار محدود به فشارهای پرفیوژن بالا همراه بود. دومین یافته اصلی این بود که آسیبهای پودوسیت قبلی، سلولهای پادوسیت را مستعد جدا شدن در فشارهای پرفیوژن بالا میکرد. موشهای Anti-GBM سه روز پس از تزریق آنتیسرم ضد GBM، فرآیندهای جهانی پا را از بین بردند و تعداد قابلتوجهی در فشارهای پرفیوژن بالا جدا شدند. در موشهای مسن، ما فرض میکنیم که فیزیولوژی پودوسیت نسبتاً به خوبی حفظ شده است و آنها را کمتر مستعد جدا شدن میکند. با استفاده از روش شمارش نیمه خودکار، هر گلومرول به طور جداگانه مورد تجزیه و تحلیل قرار گرفت (در مجموع 1200 گلومرول تجزیه و تحلیل شد). ما تایید کردیم که گلومرول های کنار هم دارای حجم بالاتری نسبت به گلومرول های زیر قشری هستند. جالب توجه است که تعداد پودوسیت ها یکسان بود و نشان می دهد که تراکم پودوسیت در گلومرول های جانبی کاهش می یابد. علاوه بر این، گلومرول های juxtamedullary نیز در برابر افزایش فشار فیلتراسیون در مقایسه با گلومرول های زیر قشری آسیب پذیرتر بودند. این یافته ها می تواند تا حدی توضیح دهد که چرا ضایعات FSGS را می توان با فرکانس بالاتر در چنین گلومرول های بزرگتر مشاهده کرد [22، 23].

شکل 4. تشخیص پودوسیت ها در پروکس مجاور. لوله (الف) تصویری نشاندهنده eGFP به علاوه پادوسیتها (سبز) در لولهها. (ب) رنگآمیزی ایمونوفلورسانس پودوسیتهایی که توسط ترانس ژن هیستون eGFP (سبز) و نشانگرهای پودوسیت درونزا p57 (قرمز)، wt{3}} (قرمز) و سیناپتوپودین (بنفش) نشانگذاری شدهاند. (C) ارتباط تعداد پودوسیت ها در هر گلومرول با تعداد پودوسیت های شناسایی شده در توبول (n=81 گلومرول از موش های کنترل، n= 41 گلومرول از موش های مسن، و n= 81 گلومرول های موش ضد GBM). برای مقایسه چندگانه، از ANOVA استفاده شد. ****پ<0.0001,>< 0.01="" and="" ns="not" statistically="" significant;="" error="" bars="" represent="" means="" ±="" sd;="" in="" the="" graph,="" each="" circle="" represents="" 1="" podocyte;="" (d)="" schematic="" showing="" how="" the="" distance="" of="" podocytes="" from="" vascular="" pole="" was="" calculated.="" (e)="" distances="" of="" individual="" podocytes="" from="" the="" vascular="" pole.="" the="" individual="" distances="" from="" the="" vascular="" pole="" were="" separated="" into="">
محدودیت این مطالعه دوره مشاهده کوتاه است، زیرا هیچ نتیجهگیری در مورد سازگاری طولانیمدت پودوسیتها با افزایش فشار فیلتراسیون نمیتوان انجام داد. پیشنهاد شده است که اولین پاسخ پودوسیتهایی که در معرض تنش برشی قرار میگیرند، دستخوش تغییرات ساختاری محافظ است [8، 24]. این تغییرات شامل از بین رفتن شکاف های فیلتراسیون (به عنوان مثال FPE) و جایگزینی شکاف-دیافراگم ها با اتصالات مسدود شده یا محکم است. اتصالات مسدود شده قبلاً در چندین مدل بیماری گلومرولی [25-28] توضیح داده شده است. با این حال، در مطالعه ما، مشاهده کردیم که سلولهای پودوسیت با FPE بیشتر در معرض فشارهای پرفیوژن بالاتر هستند. از این رو، نتایج ما نشان داد که این تغییرات تطبیقی برای محافظت در برابر جداشدگی کافی نیست یا به طور بالقوه حتی برعکس آن، که پودوسیتها را مستعدتر به جدا شدن میکنند. بعد، ممکن است استدلال شود که جدا شده پرفیوژن شده استکلیهیک سیستم فیزیولوژیکی نیست و فشارهای اعمال شده بسیار بیشتر از شرایط in vivo بود. تا آنجا که ما می دانیم، هیچ مدل دیگری از یک موجود زنده دست نخورده استفاده نمی کندکلیهوجود دارد که امکان بررسی مستقیم اثرات افزایش فشار پرفیوژن را فراهم می کند. با استفاده از وازودیلاتورها قبل و در حین پرفیوژن، حداکثر اتساع عروق پیش گلومرولی القا می شود تا جریان نامحدود (هیپرفیلتراسیون) و حداکثر انتقال افزایش فشار پرفیوژن به گلومرول ایجاد شود. در مطالعه حاضر، اثرات حاد فشارهای پرفیوژن بالاتر مورد بررسی قرار گرفت. اثرات طولانی مدت هیپرپرفیوژن پاتولوژیک می تواند مضرتر باشد و حتی منجر به از دست دادن سلول های بدن شود. با این حال، مطالعه ما نشان می دهد که این از دست دادن مزمن پودوسیت ها توسط نیروی محض جریان فیلتراسیون به خودی خود هدایت نمی شود، بلکه بیشتر به دلیل تغییرات (نادرست) تطبیقی در پودوسیت ها است که باعث کاهش پایبندی آنها به GBM می شود. بیماران مبتلا به بیماری های گلومرولی با جلوگیری از تغییرات ساختاری (نادرست) تطبیقی پودوسیت ها از درمان ضد فشار خون سود می برند.
نتیجه
این کار اولین شواهد in vivo را ارائه میکند که نشان میدهد پودوسیتهای سالم به طور فوقالعاده محکمی به GBM در کلیههای سالم موش متصل هستند و میتوانند حتی در برابر فشارهای پرفیوژن بسیار بالا مقاومت کنند. افزایش سن یا آسیب حاد پودوسیت با محو شدن جهانی، پودوسیت ها را مستعد جدا شدن در فشارهای پرفیوژن افزایش می دهد.
