ضعف در پیوند کلیه: مروری بر ارزیابی، تنوع و تأثیر بلندمدت آن
May 30, 2023
خلاصه
مشکل شکنندگی در پیوند کلیه موضوعی است که به طور فزاینده ای در زمینه پیوند مورد بحث قرار می گیرد، که تا حدی نیز ناشی از بیماری های همراه متعددی است که این بیماران تحت تأثیر آن قرار می گیرند. معیارهایی که در حال حاضر برای تعیین وجود و درجه ضعف مورد استفاده قرار می گیرند، می توانند به سرعت در عمل بالینی، حتی در بیماران مبتلا به بیماری مزمن کلیوی (CKD) ارزیابی شوند. اهداف اصلی این کار عبارتند از: (1) توصیف روش ارزیابی و تأثیری که ضعف در بیماران مبتلا به CKD دارد، (2) بررسی نحوه بررسی ضعف در ارزیابی قبل از پیوند، (iii) چگونه تغییرات ضعف پس از پیوند و (IV) تأثیر ضعف در دراز مدت بر بقای بیماران پیوند کلیه.
کلید واژه ها
بیماری مزمن کلیه، ضعف، بقای پیوند، پیوند کلیه.
معرفی
ضعف در پیوند کلیه موضوعی است که به طور فزاینده ای در زمینه پیوند مورد بحث قرار می گیرد. در عمل بالینی، نفرولوژیست ها به طور مکرر از بیماران ضعیفی که تحت تاثیر چند بیماری همراه هستند مراقبت می کنند [1-3]. مهم است که به یاد داشته باشید که «شکستگی» همیشه با پیری مرتبط نیست و حتی بیماران نسبتاً جوان ممکن است تا حدی تحت تأثیر قرار گیرند [4]. وضعیت ضعف در بیماران مبتلا به بیماری مزمن کلیه (CKD) امروزه نسبت به گذشته شیوع بیشتری دارد [5] که نشان دهنده توانایی بهتر نفرولوژیست برای بهبود بقای بیمار است. همانطور که اخیرا گزارش شده است، مرگ و میر جمعیت CKD بالای 65 سال به تدریج کاهش یافته است [6]. علاوه بر این، بیماریهای با تأثیر بالای ضعف به طور فزایندهای شایع هستند و به طور فزایندهای افراد مسن را درگیر میکنند [7، 8].
هدف این کار توصیف تأثیر ضعف بر بیماران CKD است. ارزیابی شکنندگی قبل از پیوند، سیر آن پس از پیوند کلیه (RTx) و تأثیر آن بر بقای طولانی مدت بیماران نیز مورد بحث قرار خواهد گرفت.

برای خرید اینجا کلیک کنیدمکمل های سیستانچ
ضعف: واقعاً در مورد چیست؟
در طول سال ها، تلاش های زیادی برای به دست آوردن تعریف دقیق تر از ضعف در جمعیت عمومی انجام شده است [9-11]. متأسفانه، اجماع در مورد تعریف دقیق عملیاتی شکنندگی هنوز وجود ندارد. به همین دلیل، ارزیابی جامع سالمندی هنوز به عنوان استاندارد طلایی برای تعریف ضعف در نظر گرفته می شود. در محیط های تحقیقاتی، شکنندگی عمدتاً توسط فنوتیپ فرید یا شاخص شکنندگی (FI) عملیاتی می شود [12، 13].
این جنبه در بیماران CKD و حتی کمتر در بیماران RTx مورد بررسی قرار گرفته است. هارهای و همکاران [14] بیشتر ابزارهای شکنندگی موجود را که برای جمعیت های مبتلا به CKD، وابستگی به دیالیز و RTx به کار رفته اند، خلاصه کرده اند. ابزارهای مختلف به طور متغیر از اندازهگیریهای عینی و/یا ذهنی وضعیت سلامت عمومی و عوارض، عملکرد عملکردی و ناتوانیها، با برخی مقیاسها از جمله حمایت اجتماعی، مصرف دارو، تغذیه و شناخت تشکیل شدهاند. به طور خاص، وجود شکنندگی که با مقیاس شکنندگی بالینی، فنوتیپ شکنندگی فیزیکی (PFP)، شاخص شکنندگی گرونینگن (GFI)، FI، مقیاس FRAIL، و SF{1}} PCS اندازهگیری شد، به طور قابل توجهی با عوارض و/ یا مرگ و میر در بیماران دیالیزی یا RTx [15-19].
در حال حاضر، در زمینه نفرولوژی، در غیاب دستورالعمل های روشن، تعریف عملیاتی شکنندگی معمولاً توسط فرید و همکاران ارائه شده است. [12] در سال 2001، به اصطلاح فنوتیپ شکنندگی، یکی از متداولترین فنوتیپها در ادبیات استفاده شد. در این مدل، ضعف از طریق ارزیابی پنج معیار (شکل 1) ارزیابی می شود: کاهش وزن غیر ارادی، خستگی، ضعف عضلانی، سرعت پایین راه رفتن و فعالیت بدنی کم. بنابراین شکنندگی به طور فنوتیپی به عنوان یک سندرم چند جزئی توصیف می شود که عوامل عینی و ذهنی را در نظر می گیرد و با افزایش آسیب پذیری در برابر عوامل استرس زا مشخص می شود.

هر جزء در صورت منفی دارای امتیاز {{0}} و در صورت وجود 1 است. مجموع امتیازهای به دست آمده از هر عامل امتیاز نهایی را از 0 تا 5 تشکیل می دهد:
• غیر ضعیف: امتیاز برابر با 0.
• پیش ضعیف: امتیاز 1 یا 2.
• ضعیف: بین 3 تا 5 امتیاز بگیرید.
نقطه قوت اصلی این ارزیابی این است که می توان آن را به راحتی در عمل بالینی در کمتر از 10 دقیقه به دست آورد زیرا مبتنی بر ارزیابی فنوتیپی و اندازه گیری های ساده است [20].
شایان ذکر است، تعاریف بسیاری از ضعف در ادبیات وجود دارد. FI، متفاوت از امتیاز فرید، از 30 تا 70 کسری تشکیل شده است. آنها با علائم بالینی، اختلالات عملکردی، یافته های آزمایشگاهی، ناتوانی ها و بیماری های همراه اندازه گیری می شوند. نسبت تعداد کسری های موجود به تعداد کل اقلام ارزیابی شده امتیاز شاخص را می دهد. بنابراین، اندازه گیری ذهنی کمتری از شدت ضعف را ارائه می دهد [13].
سارکوپنی، که به عنوان توده و عملکرد عضلانی کم تعریف می شود، همچنین به عنوان یک شاخص عینی شکنندگی استفاده شده است. می توان آن را از طریق جذب سنجی اشعه ایکس با انرژی دوگانه ارزیابی کرد یا با توموگرافی کامپیوتری، تصویربرداری رزونانس مغناطیسی یا بیوامپدانس تخمین زد [21].
باتری عملکرد فیزیکی کوتاه بر روی اندازه گیری عملکرد اندام تحتانی متمرکز است که با توده ماهیچه ذخیره فیزیولوژیکی مرتبط است و بنابراین برای ارزیابی شکنندگی نیز استفاده شده است. با این حال، در حال حاضر، هیچ کاربردی از باتری عملکرد فیزیکی کوتاه در CKD تایید نشده است [22].
امتیاز Clegg بر اساس 36 متغیر از داده های مراقبت های اولیه، از جمله علائم، علائم، بیماری ها، ناتوانی ها و مقادیر غیرطبیعی آزمایشگاهی است که به عنوان کمبود شناخته می شود. امتیاز تعداد کسری های موجود است که به عنوان نسبت وزنی یکسان از کل بیان می شود [23].
مقیاس فعالیت در اوقات فراغت مینه سوتا پرسشنامه ای است که توسط جمعیت عمومی استفاده می شود. استفاده از آن در جمعیت نارسایی اندام پیشرفته قابل اعتماد نیست زیرا عمدتاً بر فعالیت های متوسط تا قوی متمرکز است [24].

سیستانچه توبولوزا
ضعف در بیماران مبتلا به CKD
برای سالها، تلاشهایی برای شناسایی شیوع و تأثیر ضعف در بیماران مبتلا به CKD انجام شده است [25، 26].

جدول 1 مرتبط ترین و متعدد ترین مطالعات مربوط به ارزیابی شکنندگی در بیماران CKD را خلاصه می کند و آنها را بر اساس زیرجمعیت مورد مطالعه (بیماران مبتلا به CKD مرحله 1 تا 5، در گیرندگان دیالیز یا پیوند کلیه) و ابزار ارزیابی شکنندگی مورد استفاده، متمایز می کند.
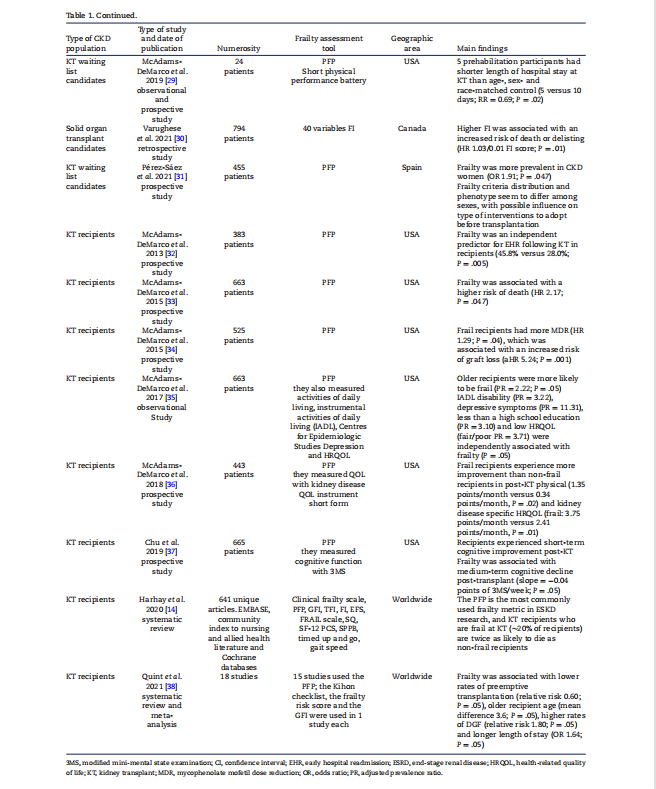
در سال 2009، ویلهلم لین و همکاران. [27] شیوع ضعف را در بیماران CKD حدود 2.8 درصد تخمین زد. با این حال، ذکر این نکته ضروری است که در میان افراد مبتلا به CKD متوسط تا شدید (GFR < 45 میلی لیتر در دقیقه)، تا 20.9 درصد افزایش یافته است. یک تحلیل فرعی، که شیوع متفاوت معیارهای ضعف جسمانی را در مراحل مختلف CKD مشاهده کرد، رفتار بیتحرک و ضعف عضلانی را به عنوان بیشترین نشاندهنده شناسایی کرد. وجود ضعف نیز به طور مستقل و به طور قابل توجهی خطر مرگ و میر کوتاه مدت را در بیماران CKD افزایش داد.
همچنین تلاش هایی برای ارزیابی تأثیر ضعف در جمعیت همودیالیز انجام شد [39، 40]. به طور خاص، بائو و همکاران. [28] نشان داد که چگونه وجود ضعف با افزایش قابل توجهی در خطر بستری شدن در بیمارستان و مرگ و میر طولانی مدت در گروهی از 1576 بیمار همودیالیزی مرتبط است. مطالعه ای از Chao و همکاران. [18] شش نوع پرسشنامه خودگزارشی را برای ارزیابی ضعف در بیماران دیالیزی مزمن مقایسه کردند [پرسشنامه Strawbridge (SQ)، مقیاس Frail ادمونتون (EFS)، مقیاس FRAIL ساده (SFS)، GFI، پرسشنامه G8 و Tilburg Fail Indicator (TFI) ]. نتایج نشان داد که مقیاس ساده FRAIL ممکن است رابطه نزدیک تری با عوارض دیالیز داشته باشد، که با سن (02/0 =)، آلبومین سرم پایین (03/0. P {{10}) و سطح کراتینین همبستگی ثابتی دارد. (P <.01)، و سطوح فریتین بالاتر (P=0.02). امروزه دانش عمومی این است که توده عضلانی، قدرت عضلانی و التهاب همگی پیشبینیکنندههای مهم پیامدها در جمعیت CKD هستند، با آلبومین سرم پایین و کراتینین پایین سرم که ارتباط مستقیمی با مرگ و میر دارند [41، 42].

هربا سیستانچ
پیوند کلیه و ضعف
اگرچه RTx اغلب به رفع تقریباً کامل اورمی کمک می کند، اما اغلب قادر به رفع کامل برخی از عوارض متابولیک، معمولی CKD پیشرفته نیست [43، 44]. علاوه بر این، از همان ابتدای تاریخ پیوند، گیرنده پیوند شرایط ایمونولوژیک، متابولیک و روانشناختی را ارائه می دهد که باید در زمان پذیرش در لیست انتظار RTx در نظر گرفته شود [45، 46]. این عوامل همچنین باید به طور منظم مورد ارزیابی مجدد قرار گیرند و در نهایت (در صورت امکان) در طول عمر پیوند درمان شوند. برای پیچیده تر کردن این موضوع، هنوز هیچ دستورالعملی برای کمک به پزشکان در تصمیم گیری برای پذیرش بیمار مسن ضعیف در لیست انتظار پیوند وجود ندارد. این بدان معنی است که تصمیم گیری در مورد اینکه آیا بیمار ضعیف را مناسب برای RTx در نظر بگیریم یا نه، عمدتاً به نظرات ذهنی یا سیاست های متفاوت در مراکز مختلف مربوط می شود.
ضعف در زمان قبل از پیوند
مشکل ارزیابی ضعف در جمعیت دیالیزی شده و اینکه چگونه می تواند بر هر RTx تأثیر بگذارد هنوز مورد بحث است [30]. در سال 2019، یک نشست بین المللی برای گزارش شواهد موجود در مورد ضعف در بیمارانی که منتظر پیوند عضو جامد بودند، تشکیل شد. هدف این جلسه نیز توسعه و اعتبار بخشیدن به یک تعریف استاندارد و خصوصیات برای بیماران ضعیف بود تا در این عمل بالینی خاص اعمال شود. در پایان این جلسه اما تصمیم بر این شد که اطلاعات در مورد چنین موضوع مهمی هنوز نسبتاً اندک و محدود باشد. تأیید شد که ضعف نشان دهنده یک وضعیت شایع در بیماران مبتلا به بیماری عضو مرحله نهایی است که منتظر پیوند هستند و با پیش آگهی ضعیف در افرادی که در لیست پیوند فعال باقی مانده اند همراه است. با این حال، به ویژه تأکید شد که روش بهینه برای اندازهگیری ضعف در این بیماران هنوز تا تعییننشده فاصله دارد و درجه خاصی از آزادی در انتخاب ابزارهای مورد استفاده باقی میماند [47].
In a paper published by McAdams-DeMarco et al. [33], 537 patients on the RTx waiting list were evaluated and classified according to the PFP. A state of overt frailty was present in ∼20% of patients. Pre-frailty was found in 33% of this population, meaning that >50 درصد از بیماران در لیست فعال RTx آسیب پذیری بیشتری نسبت به عوامل استرس زای درون زا و/یا برون زا نشان دادند. در زیر ارزیابی خواهیم کرد که چگونه این ضعف می تواند بر موفقیت پیوند و بقای کوتاه مدت و بلندمدت بیمار تأثیر بگذارد.

سیستانچ استاندارد شده
اما عوامل بالقوه تعیین کننده ایجاد شکنندگی در بیماران RTx چیست؟
برخی از عوامل جهانی هستند، مانند پیری سلولی و زوال میتوکندری، که معمولاً در سنین بالا مشخص میشود، که میتواند به ایجاد یک وضعیت ضعف کمک کند. با این حال، بیماران CKD دارای برخی از ویژگیهای خاص هستند (شکل 2). برای مثال، ضعف به طور قابل توجهی با زمان دیالیز قبل از پیوند مرتبط است [48]. پلی داروسازی، سوءتغذیه و ورزش بدنی کم عواملی هستند که در درازمدت مطمئناً می توانند به نفع، حفظ و افزایش ضعف باشند. علاوه بر این، نباید فراموش کرد که این بیماران اغلب دارای بیماری های همراه مانند بیماری های عروق محیطی، دیابت شیرین و افسردگی هستند. نتیجه همه اینها افزایش عمده در درجه التهاب زمینه ای و در نتیجه یک محرک بیشتر برای ایجاد شکنندگی است. از سوی دیگر، گاهی اوقات درک آنچه قبل یا بعد از آن می آید دشوار است. به عنوان مثال، بسیاری از بیماری ها یک بستر بیماری زا بر اساس التهاب دارند. التهاب مزمن همچنین اساس «التهاب پیری» است و همچنین میتواند یک عامل تعیینکننده قوی برای شرایط ایجاد شکنندگی باشد.

تأثیر التهاب بر شکنندگی اخیراً در 2300 بیمار مبتلا به CKD نشان داده شد و به رابطه بین ضعف، عملکردهای شناختی و بیومارکرهای ادراری آسیب لولهای اشاره شد. بیماران ضعیف سطوح بالاتری از سیتوکین های التهابی در مقایسه با گروه کنترل داشتند که از ارتباط بین التهاب و شکنندگی حمایت می کند [49]. کارهای اخیر از پرز-سائز و همکاران. [31] همچنین شیوع بالاتری از ضعف را در زنان مبتلا به CKD نشان داد (47.2 درصد زنان ضعیف در مقابل 22.5 درصد مردان ضعیف؛ P <.001)، همانطور که در جمعیت عمومی توصیف شد. این امر به دلیل داشتن توده بدون چربی کمتر و سطح بالاتر سارکوپنی و تأثیر عوامل اجتماعی (مثلاً درآمد کمتر) امکان پذیر است. در عوض، بیماری های همراه در مردان ضعیف بیشتر بود. این پدیده نیاز به ارزیابی بیشتر دارد، به ویژه به این دلیل که شیوع بیشتر شکنندگی در بیماران زن در مقابل مرگ و میر کمتر آنها در مراحل پیشرفته CKD است.
به عنوان دلیلی بر این که مفهوم شکنندگی فقط به پیری مربوط نمی شود، ضعف ممکن است در افراد جوان و بزرگسال نیز وجود داشته باشد. اثری که در 2{11}}17 بر اساس 663 بیمار RTx منتشر شد، علائم ضعف را به ترتیب در 45 درصد و 4{13}} درصد از افراد 46 تا 65 سال و 18 تا 45 سال نشان داد. عوامل اصلی در تعیین وضعیت بیمار ضعیف بی تحرکی و ضعف عضلانی بود. علاوه بر این، بیماران پیوند ضعیف بدون در نظر گرفتن سن، در معرض خطر بیشتری برای بستری شدن مجدد زودهنگام پس از پیوند قرار داشتند [35]. همچنین به نظر میرسد که وضعیت ضعف قدرت تمایز مدلهای ثبت آماری منتشر شده قبلی را در تخمین خطر بستری شدن مجدد در بیمارستان پس از پیوند بهبود میبخشد. پس از افزودن شکنندگی به 11 عامل سنتی، سطح زیر منحنی مدلهای مشخصه عملکرد گیرنده از 0.63 به 0.70 افزایش یافت. این دادهها بیشتر نشان میدهند که ضعف ممکن است یک پیشبینیکننده مستقل از سن عوارض بالقوه در پس از پیوند، حتی در کوتاهمدت در نظر گرفته شود. بنابراین، ارزیابی شکنندگی قبل از پیوند میتواند به پزشکان اجازه دهد تا بیمارانی را که در بالاترین خطر ابتلا به عوارض پس از پیوند قرار دارند، شناسایی کنند [32].
با این حال، دو سوال مهم همچنان باز است: آیا به نوعی می توان وضعیت شکنندگی را در دوره قبل از پیوند کاهش داد؟ و در صورت امکان، آیا این موضوع می تواند تاثیری بر نتیجه بعد از عمل بیمار داشته باشد؟
در سال 2019، مطالعهای در رابطه با نقش «پیشسازی» قبل از RTx در بیماران در لیست انتظار فعال منتشر شد. پیش آماده سازی به عنوان فرآیند افزایش ظرفیت عملیاتی برای بهبود تحمل به رویدادهای استرس زا تعریف شد. این مطالعه با هدف ارزیابی امکانسنجی یک برنامه هفتگی پیش از توانبخشی مبتنی بر مرکز و اثرات آن بر بستری شدن در بیمارستان پس از پیوند انجام شد. بیماران تنها پس از 2 ماه از برنامه بهبود قابل توجهی در ظرفیت فیزیکی و حرکتی خود نشان دادند. علاوه بر این، بیماران همچنین بهبود قابل توجهی در وضعیت سلامت کلی خود گزارش کردند. از 18 بیمار مورد مطالعه، 5 نفر RTx در دوره پیگیری دریافت کردند. این بیماران در مقایسه با بیمارانی که از نظر سن، جنس و نژاد همسان بودند، مدت اقامت کوتاهتری در بیمارستان پس از پیوند (5 در مقابل 10 روز) داشتند [29]. این مطالعه اهمیت فیزیوتراپی هدفمند و حفظ فعالیت بدنی را برای بیماران در لیست پیوند، با هدف تأثیر مثبت بر نتایج کوتاه مدت نشان می دهد. این نتایج با آنچه در جمعیت عمومی مشاهده شده است مطابقت دارد [50].
1. آیا پیوند کلیه وضعیت شکنندگی را اصلاح می کند؟
همانطور که قبلا ذکر شد، شکنندگی در زمان پیوند یک اتفاق نسبتاً مکرر در بیماران مبتلا به CKD است. ارزیابی اینکه آیا می تواند در دوره پس از پیوند تغییر کند یا خیر، مهم است. یک کار منتشر شده در سال 2015 نشان داده است که 50 درصد (از 349 بیمار پیوندی) در زمان RTx تحت تأثیر درجاتی از ضعف (20 درصد آشکارا ضعیف) قرار گرفتند. ارزیابی مجدد ضعف پس از 1، 2 و 3 ماه انجام شد. اگرچه اولین ارزیابی افزایش شیوع ضعف را نشان داد (از 20 درصد به 33 درصد)، شکنندگی در ماه های بعد از RTx کاهش یافت (بیماران ضعیف، 17 درصد). این کار به صراحت نشان می دهد که ضعف ممکن است به زودی پس از پیوند بدتر شود، اما اثرات مثبت مداخله در طولانی مدت قابل مشاهده است. علاوه بر این، این مطالعه ماهیت برگشت پذیر وضعیت شکنندگی را تأیید می کند [51]
ارزیابی اثرات RTx بر کیفیت زندگی خود گزارش شده (QOL) به همین ترتیب مهم است. در کار اخیر، کیفیت زندگی (در هر دو حوزه فیزیکی و ذهنی درک شده) در 443 بیمار RTx ضعیف مورد ارزیابی قرار گرفت. ارزیابی به ویژه بار CKD را در نظر گرفت. در این مورد، ارزیابی ها پس از 1 و 3 ماه پس از پیوند انجام شد. نتایج بهبود قابل توجهی در کیفیت زندگی درک شده، به ویژه پس از ماه سوم نشان داد. همچنین لازم به ذکر است که بهبود قابل توجهی (به ویژه در حوزه ذهنی) پس از 1 ماه مشاهده شد. این نتایج پیامدهای ویژه ای برای نامزدهای RTx در شرایط ضعف و تحمل ناکافی دیالیز دارد [36].
اگر نتایج به دست آمده از حالت ضعف به طور کلی و از کیفیت زندگی دلگرم کننده باشد، نمی توان همین را برای عملکرد شناختی بلندمدت گفت. در یک کار اخیر منتشر شده توسط چو و همکاران. [37] 665 بیمار پیوند کلیه از نظر عملکرد شناختی در 3 ماه، 6 ماه، 1 سال، و سپس تا 4 سال پس از پیوند (متوسط پیگیری 1.5 سال پس از پیوند) مورد ارزیابی قرار گرفتند. 15 درصد از آنها پس از پیوند، حالت ضعف داشتند. بهبودی در عملکردهای شناختی عمومی هم در گروه ضعیف و هم در گروه غیر ضعیف مشاهده شد. متأسفانه، بین 1 تا 4 سال پس از پیوند، بیماران ضعیف کاهش عمده ای در عملکرد شناختی داشتند، رویدادی که در گروه غیر ضعیف وجود نداشت.

قرص سیستانچ
2. آیا ضعف بر بقا تأثیر می گذارد؟
موضوع مورد بحث دیگر تأثیر شکنندگی قبل از پیوند بر بقای طولانی مدت RTx است. سه حوزه اصلی ضعف به ویژه مورد بررسی قرار گرفته است و باید مورد توجه قرار گیرد: درمان سرکوب کننده سیستم ایمنی. بهبود عملکردی RTx و بقای طولانی مدت بیماران ضعیف
در سال 2015، مک آدامز دیمارکو و همکاران. [34] رابطه بین درمان با مایکوفنولات موفتیل (MMF)، ضعف و از دست دادن کلیه را در 525 بیمار پیوندی بررسی کردند (شیوع ضعف: 19.5 درصد). در طول سال اول RTx، کاهش یا قطع MMF در نیمی از بیماران ضروری شد. این بیماران مسن تر بودند و شیوع RTx اهداکننده فوت شده بیشتر بود. در 4 سال پس از RTx، MMF بیشتر در بیماران ضعیف در مقایسه با بیماران غیر ضعیف کاهش یافت. در واقع، ضعف یک عامل خطر مهم و مستقل برای کاهش یا قطع دارو بود [نسبت خطر (HR) 1.29]. علاوه بر این، بیمارانی که سرکوب کننده ایمنی را کاهش داده یا قطع کردند، در طول سال اول پیگیری، خطر رد پیوند را افزایش دادند. مکانیسمی که درمان سرکوب کننده ایمنی و ضعف را به هم مرتبط می کند نامشخص است. به احتمال زیاد، تحمل ضعیف نسبت به سرکوب سیستم ایمنی و کاهش ذخایر فیزیولوژیکی در بیماران مبتلا به ضعف دخیل است.
گزارش شده است که بیماران ضعیف 80 درصد افزایش خطر ابتلا به تاخیر در بهبود عملکرد کلیه پس از پیوند دارند، که در هفته اول به دیالیز نیاز دارند، به اصطلاح "عملکرد پیوند تاخیری" (DGF). با این حال، قابل توجه است که تنها چهار مقاله، تا به امروز، این رابطه را مورد بررسی قرار داده اند، بنابراین موضوع را برای نیاز به مطالعات بیشتر باز گذاشته است [38]. آسیب سلولی و مرگ سلولی ناشی از آسیب ایسکمیک و خونرسانی مجدد، که معمولاً مربوط به دوره بلافاصله پس از پیوند است، ممکن است منجر به انتشار واسطه های التهابی شود. سناریوی پیش التهابی ممکن است سلول های ایمنی را فعال کند و التهاب بیشتر را تعیین کند که آسیب سلول های اپیتلیال لوله های کلیوی را تعیین می کند. در این زمینه، پس زمینه التهابی مشخصه شکنندگی می تواند به طور فعال کمک کند. در عین حال، التهاب با کاهش پاسخ ایمنی موثر به تحریک ایمنی و ناتوانی در دفع مؤثر زباله های سلولی همراه است [52-54]. این جنبه ها ممکن است ارتباط بین ضعف و خطر DGF را توضیح دهد.
The role played by frailty in mortality in RTx patients is particularly relevant. Data published in 2015 showed 5-year survivals of 91.5%, 86.0%, and 77.5% for non-frail, mildly frail, and frail recipients of RTx, respectively. Furthermore, being frail was independently associated with a >2-برابر افزایش خطر مرگ [48].
دادههای جدیدتر که تقریباً از 20 000 کاندیدای RTx به دست میآیند، ماندگاری طولانیتری در لیست انتظار پیوند برای بیماران ضعیف نشان دادهاند. این یافته ممکن است با بدتر شدن احتمالی وضعیت بالینی و بدتر شدن ضعف همراه باشد. با این حال، کاهش قابل توجهی در مرگ و میر در بیماران ضعیفی که RTx دریافت کردند، در اوایل ماه ششم پس از پیوند، در مقایسه با بیمارانی که تحت دیالیز باقی مانده بودند، قابل توجه بود [55]. این واقعیت از مفید بودن و اهمیت اجرای RTx در تمام موارد ممکن پشتیبانی می کند.
نتیجه گیری
در نتیجه، RTx باید همیشه در طیف گزینه های درمانی برای بیماران ضعیف در نظر گرفته شود (شکل 3).

ارزیابی ضعف در عمل بالینی باید به طور معمول در ارزیابی نامزدهای بالقوه RTx گنجانده شود. اطلاعات تکمیلی را برای تخمین بهتر ذخایر فرد و شناسایی بهتر کسانی که ممکن است از پیوند سود بیشتری ببرند، ارائه می دهد. ارزیابی ضعف در جمعیت دیالیز به برنامههای پیوند و پزشکان این امکان را میدهد تا بیمارانی را که ممکن است به دلیل شرایطشان یا به دلیل خطر بالای عوارض برای دریافت RTx مناسب نباشند، راحتتر تشخیص دهند. علاوه بر این، شناسایی ضعف ممکن است بیمار را با برنامههای چند رشتهای با هدف ارائه پروتکلها/راهحلهای سازگار آشنا کند. اینها ممکن است شامل راهبردهای قبل از توانبخشی یا مدیریت بیماریهای همراه باشد که بر نمایه ریسک فرد تأثیر منفی می گذارد. به این ترتیب به هر بیمار بدون در نظر گرفتن سن تقویمی او مناسب ترین راه حل برای شرایط وی ارائه می شود.
منابع
1. مورتون ام، گاف-لگت دی، بابروسکا آ و همکاران. بار بیماری مزمن کلیه توسط دسته های KDIGO میزان فیلتراسیون گلومرولی و آلبومینوری: یک بررسی سیستماتیک. Adv Ther 2021؛ 38:180–200.
2. Fried LF، Folkerts K، Smeta B و همکاران. بررسی ادبیات هدفمند بار بیماری در بیماران مبتلا به بیماری مزمن کلیه و دیابت نوع 2. Am J Manag Care 2021؛ 27: S168–77.
3. Fraser SD, Roderick PJ, May CR et al. بار همبودی در افراد مبتلا به بیماری مزمن کلیه مرحله 3: یک مطالعه کوهورت. BMC Nephrol 2015؛ 16:193
4. Loecker C، Schmaderer M، Zimmerman L. ضعف در بزرگسالان جوان و میانسال: یک بررسی یکپارچه. J Frailty Aging 2021؛ 10:327-33.
5. Chowdhury R، Peel NM، Krosch M، و همکاران. ضعف و بیماری مزمن کلیه: یک بررسی سیستماتیک Arch Gerontol Geriatr 2017؛ 68:135–42.
6. Foster BJ، Mitsnefes MM، Dahhou M et al. تغییرات در مرگ و میر بیش از حد ناشی از مرحله نهایی بیماری کلیوی در ایالات متحده از 1995 تا 2013. Clin J Am Soc Nephrol 2018؛ 13: 91-9.
7. Wild S، Roglic G، Green A و همکاران. شیوع جهانی دیابت: برآوردها برای سال 2000 و پیش بینی ها برای سال 2030. مراقبت از دیابت 2004؛ 27: 1047-53.
8. مورلی جی. دیابت، سارکوپنی و ضعف. Clin Geriatr Med 2008؛ 24:455-69، vi
9. مورلی جی، ولاس بی، آبلان ون کان جی، و همکاران. اجماع ضعف: فراخوانی برای اقدام J Am Med Dir Assoc 2013؛ 14:392-7.
10. Fried LP، Ferrucci L، Darer J et al. گرهگشایی مفاهیم ناتوانی، ضعف، و بیماری همراه: پیامدهایی برای بهبود هدفگیری و مراقبت J Gerontol A Biol Sci Med Sci 2004؛ 59:255-63.
11. Collard RM، Boter H، Schoevers RA و همکاران. شیوع ضعف در افراد مسن ساکن جامعه: یک بررسی سیستماتیک J Am Geriatr Soc 2012؛ 60:1487-92.
12. Fried LP، Tangen CM، Walston J et al. ضعف در افراد مسن: شواهدی برای یک فنوتیپ J Gerontol A Biol Sci Med Sci 2001؛ 56: M146-56.
13. Mitnitski AB، Mogilner AJ، Rockwood K. تجمع کمبودها به عنوان معیاری برای سنجش پیری. Sci World J 2001؛ 1:323-36.
14. Harhay MN، Rao MK، Woodside KJ و همکاران. مروری بر ضعف در پیوند کلیه: اندازه گیری، مدیریت و ملاحظات آینده Nephrol Dial Transplant 2020؛ 35:1099-1112.
15. Alfaadhel TA، Soroka SD، Kiberd BA و همکاران. ضعف و مرگ و میر در دیالیز: ارزیابی مقیاس ضعف بالینی Clin J Am Soc Nephrol 2015؛ 10:832-40.
16. Garonzik-Wang JM، Govindan P، Grinnan JW و همکاران. عملکرد ضعیف و تاخیری پیوند در گیرندگان پیوند کلیه Arch Surg 2012؛ 147:190-3.
17. Van Munster BC, Drost D, Kalf A et al. ارزش تمایز ابزار غربالگری شکنندگی در مرحله نهایی بیماری کلیوی کلین کلین J 2016؛ 9:606-10.
18. Chao CT، Hsu YH، Chang PY، و همکاران. یک مقیاس ساده خود گزارشی FRAIL ممکن است بیشتر از سایر ابزارهای غربالگری ضعف در بیماران دیالیزی مزمن روستایی با عوارض دیالیز مرتبط باشد. نفرولوژی (کارلتون) 2015؛ 20: 321-8.
19. Reese PP, Shults J, Bloom RD, et al. وضعیت عملکردی، زمان تا پیوند، و مزایای بقای پیوند کلیه در میان نامزدهای فهرست انتظار. Am J Kidney Dis 2015؛ 66:837-45.
20. Gandolfini I، Regolisti G، Bazzocchi A و همکاران. ضعف و سارکوپنی در بیماران مسن دریافت کننده پیوند کلیه. Front Nutr 2019; 6:169
21. Beaudart C، McCloskey E، Bruyère O و همکاران. سارکوپنی در تمرین روزانه: ارزیابی و مدیریت BMC Geriatr 2016؛ 16:170
22. سینگر جی پی، دیاموند جی ام، اندرسون ام آر و همکاران. فنوتیپ های ضعف و مرگ و میر پس از پیوند ریه: یک مطالعه کوهورت آینده نگر Am J Transplant 2018؛ 18:1995-2004.
23. Clegg A, Bates C, Young J, et al. توسعه و اعتبار سنجی یک شاخص شکنندگی الکترونیکی با استفاده از داده های پرونده الکترونیکی سلامت اولیه مراقبت های اولیه. سن پیری 2016؛ 45:353-60.
24. Taylor HL، Jacobs DR Jr، Schucker B، و همکاران. پرسشنامه سنجش فعالیت بدنی اوقات فراغت. J Chronic Dis 1978؛ 31:741-55.
25. Chowdhury R، Peel NM، Krosch M، و همکاران. ضعف و بیماری مزمن کلیه: یک بررسی سیستماتیک Arch Gerontol Geriatr 2017؛ 68:135–42.
26. Shen Z، Ruan Q، Yu Z و همکاران. ضعف فیزیکی و اختلال شناختی مرتبط با بیماری مزمن کلیوی: یک بررسی سیستمیک Geriatr Gerontol Int 2017؛ 17:529–44.
27. Wilhelm-Leen ER، Hall YN، K Tamura M و همکاران. ضعف و بیماری مزمن کلیه: سومین نظرسنجی ملی سلامت و ارزیابی تغذیه. Am J Med 2009؛ 122:664-71.e2.
28. Bao Y، Dalrymple L، Chertow GM و همکاران. ضعف، شروع دیالیز و مرگ و میر در مرحله نهایی بیماری کلیوی. Arch Intern Med 2012؛ 172:1071-7.
29. McAdams-DeMarco MA، Ying H، Van Pilsum Rasmussen S et al. پیش آمادگی قبل از پیوند کلیه: نتایج یک مطالعه آزمایشی پیوند کلین 2019؛ 33: e13450
30. Varughese RA، Theou O، Li Y et al. شاخص شکنندگی کسری تجمعی نتایج را برای نامزدهای پیوند عضو جامد پیشبینی میکند. پیوند مستقیم 2021؛ 7: e677
31. Pérez-Sáez MJ، Arias-Cabrales CE، Dávalos-Yerovi V و همکاران. ضعف در میان بیماران بیماری مزمن کلیه در لیست انتظار پیوند کلیه: پارادوکس ضعف جنسی کلین کلین J 2021؛ 15:109-18.
32. McAdams-DeMarco MA, Law A, Salter ML, et al. ضعف و بستری مجدد در بیمارستان پس از پیوند کلیه Am J Transplant 2013؛ 13:2091-5.
33. McAdams-DeMarco MA, Law A, King E, et al. ضعف و مرگ و میر در گیرندگان پیوند کلیه Am J Transplant 2015؛ 15:149-54.
34. McAdams-DeMarco MA, Law A, Tan J, et al. ضعف، کاهش مایکوفنولات و از دست دادن پیوند در گیرندگان پیوند کلیه. پیوند 2015؛ 99: 805-10.
35. McAdams-DeMarco MA، Ying H، Olorundare I و همکاران. اجزای ضعف فردی و مرگ و میر در گیرندگان پیوند کلیه پیوند 2017؛ 101: 2126-32.
36. McAdams-DeMarco MA، Olorundare IO، Ying H و همکاران. ضعف و کیفیت زندگی مرتبط با سلامت پس از پیوند کلیه پیوند 2018؛ 102: 291-9.
37. Chu NM، Gross AL، Shaffer AA و همکاران. ضعف و تغییرات در عملکرد شناختی پس از پیوند کلیه. J Am Soc Nephrol 2019؛ 30:336-45.
38. Quint EE, Zogaj D, Banning LBD et al. ضعف و پیوند کلیه: یک مرور سیستماتیک و متاآنالیز پیوند مستقیم 2021؛ 7: e701
39. لی اچ جی، سون وای جی. شیوع و عوامل مرتبط با ضعف و مرگ و میر در بیماران مبتلا به بیماری کلیوی مرحله نهایی تحت همودیالیز: یک بررسی سیستماتیک و متاآنالیز. Int J Environ Res Health عمومی 2021؛ 18: 3471
40. Garcia-Canton C، Rodenas A، Lopez-Aperador C و همکاران. ضعف در همودیالیز و پیشبینی پیامد کوتاهمدت ضعیف: مرگومیر، بستری شدن در بیمارستان و مراجعه به خدمات اورژانس بیمارستانی. رن فایل 2019؛ 41:567–75.
41. Isoyama N، قریشی AR، Avesani CM و همکاران. ارتباط مقایسه ای توده عضلانی و قدرت عضلانی با مرگ و میر در بیماران دیالیزی. Clin J Am Soc Nephrol 2014؛ 9: 1720-8.
42. Gill TM، Gahbauer EA، Han L et al. مسیرهای ناتوانی در سال آخر زندگی. N Engl J Med 2010؛ 362:1173-80.
43. Abecassis M، Bartlett ST، Collins AJ، و همکاران. پیوند کلیه به عنوان درمان اولیه برای مرحله نهایی بیماری کلیوی: کنفرانس بنیاد ملی کلیه / ابتکار کیفیت پیامدهای بیماری کلیوی (NKF/KDOQITM). Clin J Am Soc Nephrol 2008؛ 3:471-80.
44. Alfieri C، Mattinzoli D، Messa P. ترشیاری و هیپرپاراتیروئیدیسم پس از پیوند. Endocrinol Metab Clin North Am 2021؛ 50:649-62.
45. فیلیپس اس، هوبرگر آر. اختلالات متابولیک بدنبال پیوند کلیه. J Ren Nutr 2012؛ 22:451-60.e1.
46. De Pasquale C، Pistorio ML، Veroux M et al. جنبه های روانشناختی و آسیب شناختی پیوند کلیه: یک بررسی سیستماتیک روانپزشکی جبهه 2020؛ 11:106
47. Kobashigawa J, Dadhania D, Bhorade S, et al. گزارشی از انجمن پیوند آمریکا در مورد ضعف در پیوند اعضای جامد. Am J Transplant 2019؛ 19:984-94.
48. Kosoku A, Uchida J, Iwai T et al. ضعف با مدت زمان دیالیز قبل از پیوند در گیرندگان پیوند کلیه مرتبط است: یک مطالعه مقطعی تک مرکزی ژاپنی. Int J Urol 2020؛ 27:408-14.
49. Miller LM, Rifkin D, Lee AK et al. ارتباط بیومارکرهای ادرار آسیب و اختلال عملکرد لوله کلیه با شاخص شکنندگی و عملکرد شناختی در افراد مبتلا به CKD در SPRINT. Am J Kidney Dis 2021؛ 78:530–40.e1.
50. Izquierdo M، Merchant RA، Morley JE و همکاران. توصیه های ورزشی بین المللی در افراد مسن (ICFSR): دستورالعمل های اجماع کارشناسان J Nutr Health Aging 2021؛ 25:824-53.
51. McAdams-DeMarco MA, Isaacs K, Darko L et al. تغییر در ضعف بعد از پیوند کلیه J Am Geriatr Soc 2015؛ 63:2152-7.
52. Zhao H، Alam A، Soo AP و همکاران. آسیب ایسکمی-پرفیوژن مجدد بقای طولانی مدت پیوند کلیه را کاهش می دهد: مکانیسم و فراتر از آن. EBioMedicine 2018؛ 28:31-42.
53. Ferrucci L، Fabbri E. Inflammageing: التهاب مزمن در پیری، بیماری های قلبی عروقی، و ضعف. Nat Rev Cardiol 2018؛ 15:505–22.
54. Nieuwenhuijs-Moeke GJ، Pischke SE، Berger SP و همکاران. ایسکمی و آسیب خونرسانی مجدد در پیوند کلیه: مکانیسم های مرتبط در آسیب و ترمیم جی کلین مد 2020؛ 9: 253
55. Sawinski D، Forde KA، Lo Re V III و همکاران. مرگ و میر و پیامدهای پیوند کلیه در بیماران دیالیز نگهدارنده سرم مثبت ویروس هپاتیت C: یک مطالعه کوهورت گذشته نگر. Am J Kidney Dis 2019؛ 73: 815–26.
کارلو آلفیری 1،2، سیلویا مالویکا 1، ماتئو سزاری 2،3، سیمون وتورتی 1، متئو بندتی 1، الیزا سیسرو 1، روبرتا میگلیو 1، لارا کالدیرولی 1، الساندرو پرنا 4، آنجلا سروساتو کاستل 4 و جوزپه 4
1 گروه نفرولوژی، دیالیز و پیوند کلیه، Fondazione IRCCS Ca' Granda Ospedale Policlinico Milan، میلان، ایتالیا،
2 گروه علوم بالینی و سلامت جامعه، دانشگاه میلان، میلان، ایتالیا،
3 واحد سالمندان، IRCCS Istituti Clinici Scientifici Maugeri، میلان، ایتالیا
4 گروه علوم پزشکی ترجمه، دانشگاه کامپانیا 'L. وانویتلی، ناپل، ایتالیا






