اسید لیپوئیک سنتز و رسوب کلاژن را در کلیه های موش صحرایی غیردیابتی و دیابتی افزایش می دهد.
Mar 18, 2022
نونا گردوویچ و همکاران
اسید لیپوئیک (ALA) به طور گسترده ای به عنوان یک مکمل غذایی و عامل درمانی در مدیریت دیابت استفاده می شود. اثرات آنتی اکسیدانی و هیپوگلیسمی ثابت ALA در مبارزه با عوارض دیابت از جمله مهم است.کلیهصدمه. مطالعه حاضر پتانسیل ALA را برای تأثیرگذاری بر وقایع پروفیبروتیک در بدن ارزیابی کردکلیهکه می تواند ساختار و عملکرد آن را تغییر دهد. ALA به صورت داخل صفاقی (10 میلی گرم بر کیلوگرم) به موش های صحرایی نر ویستار دیابتی غیردیابتی و دیابتی ناشی از استرپتوزوتوسین به مدت 4 و 8 هفته تجویز شد. اثرات ALA از تغییرات ساختاری/مورفولوژیکی از طریق تغییراتی که فرآیندهای پروفیروتیک را مشخص می کند تا تنظیم بیان ژن کلاژن درکلیه. در اینجا، ما نشان دادیم که ALA سطح گلوکز و اوره سیستمیک را بهبود میبخشد و تشکیل آن را کاهش میدهدکلیهمحصولات نهایی گلیکاسیون پیشرفته (AGEs)، و حفظ یکپارچگی ساختاری کلیه در موشهای دیابتی. با این حال، رویدادهای پروفیبروتیک ایجاد شده در دیابت توسط ALA کاهش نمی یابد زیرا سنتز/رسوب کلاژن و بیان فاکتور رشد تبدیل کننده- 1 (TGF- 1) و اکتین عضلات صاف (-SMA) در ALA- بالا باقی مانده است. موش های دیابتی تحت درمان، به ویژه پس از 8 هفته از شروع دیابت. علاوه بر این، 8 هفته درمان موشهای غیر دیابتی با ALA منجر به ایجاد ویژگیهای پروفیبروتیک شد که در افزایش سنتز/رسوب کلاژن منعکس شد. علاوه بر سیگنالدهی پاییندست TGF، مکانیسم اضافی زیربنای تنظیم مثبت کلاژن IV در موشهای غیردیابتی تحت درمان با ALA، شامل کاهش متیلاسیون DNA پروموتر آن است که میتواند از افزایش بیان Tet1 ناشی شود. این یافته ها بر احتیاط درمانی در استفاده از ALA، به ویژه در بیماران مبتلا به آن تاکید می کندکلیهدیابتیعوارض
برای اطلاعات بیشتر: ali.ma@wecistanche.com

روی پودر عصاره سیستانچ برای بیماری کلیوی کلیک کنید
1. مقدمه
دیابتیکلیهبیماری (DKD) یا نفروپاتی دیابتی یکی از عوارض میکروواسکولار با بروز 20-40 درصد در بین بیماران دیابتی است که با تغییرات ساختاری پیشرونده و از دست دادن عملکرد کلیه همراه است [1]. مکانیسم پاتوفیزیولوژیکی که زمینه DKD را تشکیل می دهد پیچیده است و با هیپرگلیسمی مزمن شروع می شود که به نوبه خود باعث ایجاد استرس اکسیداتیو، تشکیل محصولات نهایی گلیکوزیشن پیشرفته (AGEs)، فعال شدن مسیرهای سیگنالینگ MAPK/PKC و متعاقب آن بیان چندین واسطه پیش التهابی و پروفیبروتیک می شود [2, 3]. گفتگوی متقابل بین این رویدادها منجر به تجمع پروتئین های ماتریکس خارج سلولی (ECM) در مزانژیوم و توبولواینترستیتیوم با الگوی هیستوپاتولوژیکی کلاسیک می شود.کلیهفیبروز. با تغییرات ساختاری مانند ضخیم شدن غشای پایه و انبساط مزانژیال شروع می شود و به تدریج به گلومرولواسکلروز و فیبروز بینابینی پیشرفت می کند و در نهایت به اوج می رسد.کلیهشکست[4, 5].
سیگنال دهی پایین دستی فاکتور رشد (TGF{1}}) بخشی از فرآیند بهبود زخم است که بر اثر التهاب مداوم، هیپرگلیسمی یا استرس اکسیداتیو که مشخصه دیابت است، به فیبروز پاتوفیزیولوژیک تبدیل می شود [6] . TGF{4}} یک واسطه مرکزی پاتوژنز DKD است که تنظیم کننده اصلی بیان پروتئین ECM در بیماران مبتلا به دیابت است که احتمالاً در نتیجه هیپرگلیسمی و محیط اکسیداتیو مختل است [7-10]. TGF با تحریک کلاژن نوع I و IV، اکتین ماهیچه صاف (-SMA)، لامینین و سنتز فیبرونکتین و همچنین با مهار آنزیم های تجزیه کننده ECM باعث تجمع ECM می شود [11].
کلاژن نوع IV فراوان ترین ماده تشکیل دهنده غشای پایه [12] است که در غشای پایه گلومرولی و لوله ای تحت شرایط فیزیولوژیکی بیان می شود [13]. با این حال، نفروپاتی دیابتی با بیان نابجای کلاژن نوع IV همراه است که شامل تولید بیش از حد و توزیع نامنظم از طریق بینابینی و مزانژیوم است [14-16]. از میان شش ایزوفرم کلاژن نوع IV (1- 6)، 1 (IV) و 2 (IV) به طور جهانی در تمام غشاهای پایه وجود دارد. زنجیره های کلاژن 1 (IV) و 2 (IV) توسط ژن های Col4a1 و Col4a2 کدگذاری می شوند که تنظیم رونویسی آنها بر تعاملات سیس-ترانس به خوبی توصیف شده رله می کند [17]، اما یافته های اخیر نقش مهم مکانیسم های اپی ژنتیکی از جمله متیلاسیون DNA را برجسته می کند. تنظیم بیان آنها [18-20].
با توجه به مکانیسم های پاتوفیزیولوژیکی که در پشت DKD نهفته است، استراتژی های درمانی ساده هستند و هیپرگلیسمی و استرس اکسیداتیو را هدف قرار می دهند. پتانسیل هیپوگلیسمی و آنتی اکسیدانی ALA، که یکی از آنتی اکسیدان های پرمصرف است، بهبود می یابد.کلیهتغییرات پاتولوژیک مرتبط با نفروپاتی دیابتی [21-23]. با این حال، در ارتباط با پیری پوست، اثرات مفید ALA از طریق افزایش سنتز کلاژن نوع I در فیبروبلاست های پوستی انسان گزارش شده است [24]. با توجه به پاتوفیزیولوژی DKD، یک اثر مشابه ALA می تواند برای بیماران دیابتی مضر باشد.کلیهعوارض با این پیشینه، مطالعه حاضر به بررسی اثرات ALA بر ویژگیهای ساختاری/مورفولوژیکی کلیه و فرآیندهای پروفیبروتیک با تاکید بر بیان ژن کلاژن نوع IV در موشهای دیابتی و غیردیابتی پرداخته است.

2. مواد و روشها
2.1. حیوانات، درمان ها و تنظیمات آزمایشی.همه آزمایشها بر روی موشهای صحرایی نر 2 ماهه آلبینو ویستار با وزن بین 220 تا 250 گرم انجام شد. همه رویه های حیوانی تایید شده توسط کمیته اخلاقی برای استفاده از حیوانات آزمایشگاهی موسسه تحقیقات بیولوژیکی "Siniša Stan-ković"، دانشگاه بلگراد، مطابق با دستورالعمل 2010/63/EU در مورد حمایت از حیوانات مورد استفاده برای آزمایش و سایر اهداف علمی حیوانات در این مطالعه با روش فیزیکی اتانازی با استفاده از گیوتین، طبق تمام توصیههای دستورالعملهای اتانازی حیوانات، قربانی شدند. مرگ فورا رخ می دهد و حیوانات رنج نمی برند. اتانازی در اتاق عمل، جدا از اتاق خواب، یک به یک حیوان انجام شد (بقیه حیوانات حاضر در آزمایش در اتاق آزمایش که جدا از اتاق عمل است که در آن اتانازی انجام شده است نگهداری میشوند تا از استرس برای دیگری جلوگیری شود. حیوانات). اتانازی توسط افراد با تجربه و آموزش دیده انجام شد. تجهیزات مورد استفاده برای بریدن سر از وضعیت خوبی برخوردار بودند (خدمات به طور منظم برای ارائه تیزی تیغه ها انجام می شود).
دیابت با دوز پایین (4{2}} mg/kg) تزریق استرپتوزوتیسین (STZ) (MP Biomedicals) برای پنج روز متوالی القا شد. موش های کنترل تنها با وسیله نقلیه (بافر سدیم سیترات 0.1 مولار، pH 4.5) تزریق شدند. سطح گلوکز خون 24 ساعت پس از آخرین تزریق STZ با گلوکومتر Accu-Chek Active خون اندازه گیری شد و حیوانات دیابتی در نظر گرفته شدند که سطح گلوکز خون ناشتا از 20 میلی مول در لیتر فراتر رفت. موشها به طور تصادفی به چهار گروه آزمایشی تقسیم شدند: کنترل (کنترل، n=8)، کنترل تحت درمان با ALA (ALA، n=8)، دیابتی (STZ، n=10) و گروه دیابتی تحت درمان با ALA (STZ/ALA، n=10). ALA (Ivančić i synovial، بلگراد، صربستان) به صورت داخل صفاقی (10 میلی گرم بر کیلوگرم) هر روز به مدت 4 و 8 هفته، شروع از آخرین تزریق STZ تزریق شد. پس از قربانی و خونگیری، یک برش شکمی و هر دو ایجاد شدکلیه هاحذف شدند. یکیکلیهدر نیتروژن مایع منجمد شد، در درجه {0}} نگهداری شد و برای جداسازی پروتئین، DNA و RNA استفاده شد، در حالی که دیگری در فرمالین 10 درصد بافر برای بررسیهای بافتشناسی تثبیت شد.
2.2. تجزیه و تحلیل بیوشیمیایی.موش ها قبل از قربانی یک شبه روزه گرفته اند. سرم خون پس از لخته شدن خون و سانتریفیوژ در 2،{1}} گرم به مدت 10 دقیقه جمع آوری شد. سرم برای تعیین غلظت گلوکز با کیت تجاری (Gluco-quant Glucose/HK; Boehringer)، سطح تری گلیسیرید سرم به روش GPO-PAP با استفاده از کیت آنزیمی (Randox Laboratories، UK)، سطح اوره با روش اوره استفاده شد. کیت (Abcam، ایالات متحده آمریکا) و غلظت کراتینین با استفاده از سنجش کراتینین Cayman طبق دستورالعمل سازنده.
2.3. تجزیه و تحلیل بافت شناسی و رنگ آمیزی ایمنی.فرمالین ثابت شدکلیهبافتها در یک سری کاهشیافته از زایلول و الکلها برای گنجاندن خلفی در بلوکهای پارافین آبگیری شدند. بلوک های بافت در 5 میکرومتر بر روی یک میکروتوم چرخشی (RM 2125RT؛ Leica Microsystem) برش داده شدند. به منظور مشاهده تغییرات در مورفولوژی کلیه، مقاطع بافتی با استفاده از روش اسید دوره ای - شیف (PAS) رنگ آمیزی شدند. بعلاوه، مقاطع رنگآمیزی شده با استفاده از میکروسکوپ Olympus (BX{3}}) مجهز به میکرومحرک، استیج موتوردار و دوربین، که توسط بسته نرمافزاری استریولوژیکی newCAST کنترل میشود، تجزیه و تحلیل شدند. نواحی لومن لوله ای با بزرگنمایی عینی 40 برابر به دست آمد و به صورت درصد (درصد) در هر ناحیه مورد بررسی بیان شد. کسر ماتریکس مزانژیال به عنوان ناحیه رنگ آمیزی PAS مثبت ارزیابی شد که به صورت درصد در کل ناحیه گلومرولی بیان می شود (بزرگنمایی عینی 100x).
برای تشخیص فیبر کلاژن، مقاطع بافتی با رنگ آمیزی تری کروم ماسون رنگ آمیزی شدند. پس از رنگ آمیزی، مقاطع زیر یک میکروسکوپ نوری مشاهده شدند (DM RB Photomicroscope Leica Microsystems GmbH، Wetzlar، آلمان، مجهز به دوربین Leica DFC 320 CCD؛ بزرگنمایی شیئی 40x). تجزیه و تحلیل تصویر توسط نرم افزار ImageJ (نسخه 1.52p، موسسه ملی بهداشت) انجام شد. تصاویر به پشته های RGB تبدیل شدند و آستانه دستی برای ارزیابی نسبت سطح کلاژن در هر ناحیه بافت اعمال شد.
آنالیز ایمونوهیستوشیمی همانطور که در [25] توضیح داده شد با استفاده از آنتی بادی پلی کلونال ایجاد شده علیه N(?)-(کربوکسی متیل) لیزین (CML) (رقت 1: 50) (سانتا کروز بیوتکنولوژی، CA، ایالات متحده آمریکا) و آنتی بادی ثانویه ترب کوهی پراکسیداز (1: 100) (بیوتکنولوژی سانتا کروز). مقاطع بافت با 3،3'-دی آمینوبنزیدین (DAB) رنگآمیزی شدند، با هماتوکسیلین رنگآمیزی شدند و در زیر میکروسکوپ نوری نصب و مشاهده شدند (فتومیکروسکوپ Leica DM RB؛ بزرگنمایی عینی 40x). تجزیه و تحلیل تصویر توسط نرم افزار ImageJ (نسخه 1.52p، موسسه ملی بهداشت) انجام شد. تصاویر با دکانولوشن رنگ با گزینه بردار H DAB پردازش شدند. سیگنالینگ CML به عنوان میانگین شدت خاکستری رنگآمیزی DAB به تعداد هستهها (بهدستآمده با استفاده از گزینه Analyze Particles) نرمال شده محاسبه شد.
2.4. تجزیه و تحلیل وسترن بلات.25 گرم ازکلیههموژن ها توسط SDS-PAGE جدا شدند، روی غشاهای پلی وینیلیدین دی فلوراید منتقل شدند و با آنتی بادی پلی کلونال علیه GAPDH (FL{0}}) و آنتی بادی های مونوکلونال علیه TGF{1}} موش صحرایی (3C11) و SMA (CGA7) همه از بیوتکنولوژی سانتا کروز و همه در نسبتهای 1: 1،000 رقیق شدهاند. تشخیص توسط یک سیستم تشخیص لومینسانس شیمیایی (سانتا کروز بیوتکنولوژی) انجام شد. کمیسازی باندهای واکنشگر ایمنی با استفاده از نرمافزار الکتروفورز TotalLab (Phoretix) (نسخه 1.10) انجام شد و به GAPDH که بهعنوان کنترل بارگذاری استفاده میشود، نرمال شد.
2.5. Real-Time Quantitative PCR (RT-qPCR).RNA کل ازکلیه هابا استفاده از کیت کوچک RNeasy (Qiagen). برای سنتز cDNA، 1 میکروگرم از RNA کل با DNase I تیمار شد و با کیت سنتز cDNA رشته اول RevertAid (فرمنتاس، برلینگتون، کانادا) با استفاده از ترکیبی از پرایمرهای تصادفی هگزامر و الیگو (dT) رونویسی معکوس شد. سطوح mRNA با استفاده از 2x Maxima SYBR Green/- ROX qPCR Master Mix (Fermentas) روی یک سیستم Real-Time PCR QuantStudio 3 (Applied Biosystems, Carlsbad, CA, USA) اندازهگیری شد. Primer-BLAST (https://www.ncbi.nlm.nih.gov/tools/ primer-blast/) برای طراحی پرایمرها (فهرست شده در جدول تکمیلی S1) برای ارزیابی Col4a1، Dnmt1، Dnmt3a، Dnmt3b و بیان ژن Tet1 چرخه های حرارتی شامل دناتوراسیون اولیه در 95 درجه / 10 دقیقه و 40 سیکل PCR دو مرحله ای در 95 درجه / 15 ثانیه و 60 درجه / 60 ثانیه بود. سطوح بیان mRNA ژن های مورد نظر با روش 2-dCT به سطح بیان mRNA ژن Actb به عنوان یک ژن مرجع نرمال شد.
2.6. جداسازی DNA ژنومی و تبدیل بی سولفیت DNA.DNA ژنومی با استفاده از روش Bio-On-Magnetic-Beads (BOMB) [26]، طبق پروتکل استخراج DNA از بافت پستانداران (به صورت آنلاین در https://bomb.bio/protocols/ موجود است) جدا شد. DNA ژنومی تحت پروتکل تبدیل بی سولفیت BOMB قرار گرفت (به صورت آنلاین در https://bomb.bio/protocols/ موجود است) [26].
2.7. اندازه گیری سطوح جهانی متیلاسیون DNA.سطوح متیلاسیون DNA جهانی با استفاده از کیت 5-mC DNA ELISA (Zymo Research، کالیفرنیا، ایالات متحده آمریکا) طبق دستورالعمل سازنده اندازهگیری شد. DNA ژنومی خالص شده (100 نانوگرم) جدا شده ازکلیه هااز تمامی گروه های آزمایشی استفاده شد و هر نمونه در دو نسخه مورد سنجش قرار گرفت. اهمیت آماری با استفاده از آنالیز واریانس یک طرفه با مسدود کردن، در نظر گرفتن هر صفحه ELISA به عنوان یک بلوک برآورد شد.
2.8. PCR اختصاصی متیلاسیون (MSP).جفت های پرایمر برای تجزیه و تحلیل MSP، طراحی شده در ناحیه پروموتر Col4a1 که محل شروع رونویسی (TSS) را در بر می گیرد، با استفاده از MethPrimer (http://www.urogene.org/cgi-bin/methprimer/methprimer.cgi) طراحی شدند (جدول تکمیلی S2) ). موقعیت پرایمرها (نسبت به TSS برای Col4a1، علامت گذاری شده به عنوان مثبت 1) مورد استفاده برای تجزیه و تحلیل MSP به شرح زیر است: M fw (-35، -14)، M rev (به علاوه 44، به علاوه 64)، U. fw (-35، -14)، و U rev (به علاوه 45، به علاوه 69). از آنجایی که هر آغازگر 2 CpG را پوشش می دهد، در مجموع 4 CpG برای وضعیت متیلاسیون در هر جفت آغازگر مورد آزمایش قرار گرفت. مخلوط واکنش برای MSP حاوی Maxima SYBR Green/ROX qPCRqRT-PCR Master Mix (Fermentas)، 2{19}} نانوگرم DNA تبدیل شده به بی سولفیت، و 0.5 میکرومولار از هر پرایمر ویژه برای DNA متیله (M) و غیر متیله (U) در حجم نهایی 10 میکرولیتر. MSP بر روی سیستم QuantStudio 3 Real-Time PCR (Applied Biosystems) انجام شد. شرایط چرخه PCR به شرح زیر بود: مراحل اولیه دناتوراسیون در 95 درجه / 10 دقیقه و به دنبال آن 40 چرخه دناتوراسیون در 95 درجه / 15 ثانیه، و بازپخت و ازدیاد طول در 58 درجه / 60 ثانیه. سطح نسبی DNA متیله با استفاده از شاخص متیلاسیون که به صورت 2 (سیکل متیله Ct) - (سیکل متیله Ct) تعریف شده است، بیان شد [27].
2.9.تحلیل آماری.داده ها به عنوان میانگین ± انحراف استاندارد برای تمام پارامترهای مورد مطالعه بیان شد. برای مقایسه میانگین متغیرهای توزیع شده نرمال بین دو گروه از آزمون t دانشجویی استفاده شد. تفاوتهای آماری بین گروهها با استفاده از آنالیز واریانس یکطرفه (ANOVA) و سپس آزمون مقایسه چندگانه توکی با استفاده از نرمافزار GraphPad Prism، ver. 5. 00 (نرم افزار GraphPad، سن دیگو، کالیفرنیا، ایالات متحده آمریکا).

3. نتایج
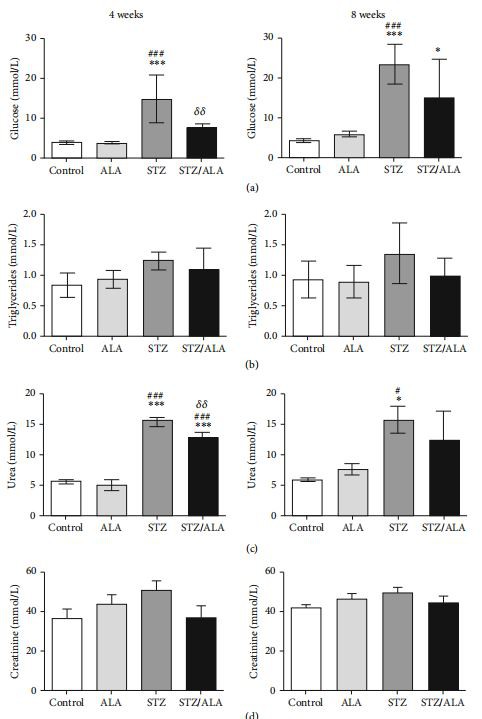
3.1. تأثیر ALA بر شاخص های بیوشیمیایی در موش های صحرایی دیابتی.گلوکز، تری گلیسیرید، اوره و کراتینین در سرم موش های صحرایی کنترل، دیابتی و غیردیابتی و دیابتی تحت درمان با ALA تعیین شد (شکل 1). وضعیت دیابت 4 هفته و 8 هفته پیگیری شد تا دوره زمانی لازم برای تظاهر فرآیندهای مضر در نظر گرفته شود. هر دو گروه از موش های دیابتی با هیپرگلیسمی، روند افزایشی تری گلیسیرید و سطح کراتینین اما بدون اهمیت آماری، و با افزایش قابل توجه سطوح اوره مشخص شدند. در موش های دیابتی، 4 هفته درمان با ALA منجر به کاهش سطح گلوکز سرم به مقدار کنترل شد، در حالی که پس از 8 هفته سطح گلوکز کاهش یافت اما همچنان به طور قابل توجهی در مقایسه با گروه شاهد افزایش یافت. در هر دو گروه دیابتی تحت درمان با ALA، تری گلیسیرید و کراتینین تغییر قابل توجهی نداشتند. درمان با ALA به طور قابل توجهی سطح اوره موشهای دیابتی را پس از 4 هفته کاهش داد، در حالی که پس از 8 هفته سطح سرمی اوره موشهای دیابتی نسبت به گروه کنترل دیابتی کاهش یافت اما بدون معنیداری آماری. تجویز ALA به موش های کنترل به طور قابل توجهی بر پارامترهای بیوشیمیایی بررسی شده تأثیری نداشت.
3.2. ارزیابی مورفولوژیکی ساختار کلیه و تشکیل CML پس از درمان ALA.رنگ آمیزی PAS ویژگی های هیستوپاتولوژیک کلیوی مرتبط با دیابت را برجسته کرد (شکل 2(a)). ضخیم شدن غشای پایه گلومرولی پس از 4 هفته از شروع دیابت ظاهر شد در حالی که انبساط ماتریکس مزانژیال و لوله های با لومن گشاد شده پس از 8 هفته از شروع دیابت مشاهده شد. تجزیه و تحلیل بافت شناسی نشان داد که ناحیه لومن لوله ای، گلومرولی و ماتریکس مزانژیال به طور قابل توجهی در موش های دیابتی 8 هفته ای نسبت به گروه کنترل و کنترل تحت درمان با ALA افزایش یافته است. با این حال، پس از درمان ALA، اتساع لولهای و گسترش ماتریکس مزانژیال به طور قابلتوجهی کاهش یافت، اما همچنان بالاتر از مقادیر کنترل باقی ماند، در حالی که ناحیه گلومرولی به طور کامل به سطوح کنترل برگردانده شد. در موشهای کنترل تحت درمان با ALA، کسر ماتریکس مزانژیال افزایش یافته است که نشان میدهد استفاده طولانیمدت از ALA میتواند بر برخی از ویژگیهای ساختاری تأثیر بگذارد.کلیه ها(شکل 2 (الف)).
AGE ها عوامل بیماری زایی هستند که به آسیب کلیوی در دیابت کمک می کنند. به منظور بررسی اینکه آیا ALA بر تجمع محصولات AGE در بدن تأثیر می گذارد یا خیرکلیه هادر موشهای دیابتی، محتوای کلیوی CML با رنگآمیزی ایمونوهیستوشیمی در گروه شاهد، موشهای دیابتی (هفتههای 4 و 8) و گروه کنترل تحت درمان با ALA و موشهای دیابتی (4 و 8 هفته) ارزیابی شد (شکل 2 (ب)). رنگآمیزی برای CML در هر دو گروه موشهای دیابتی مثبت بود و نشان داد که CML عمدتاً در توبولو اینترستیتیوم و به میزان کمتری در گلومرولها تجمع مییابد. با توجه به کمی سازی محتوای CML، این تغییرات در مقایسه با کنترل های مربوطه از نظر آماری معنی دار بود (شکل 2(b)). پس از درمان با ALA موشهای دیابتی (4 و 8 هفته)، هم رنگپذیری CML لولهای بینابینی و گلومرولی به طور قابلتوجهی کاهش یافت در حالی که در موشهای کنترل تحت درمان با ALA، مثبت بودن CML مانند گروه کنترل غیرقابل تشخیص باقی ماند.

3.3. تأثیر ALA بر رسوب کلاژن و بیان ژن Col4a1.رنگ آمیزی تری کروم ماسون رسوب کلاژن را در نواحی توبولو بین بافتی و درون گلومرول ها، به ویژه در غشای پایه هر دو بخش در گروه دیابتی (4 و 8 هفته) موش نشان داد (شکل 3(a)). درمان ALA (هفته های 4 و 8) موش های غیر دیابتی نیز با افزایش رسوب کلاژن همراه بود که مشخصه آن مناطق گلومرولی و توبولو بینابینی اشغال شده توسط ماتریکس رنگ آمیزی شده با کلاژن اما بدون اهمیت آماری بود. در موش های دیابتی تحت درمان با ALA (هفته های 4 و 8)، رسوب کلاژن به طور مداوم باقی ماند زیرا کاهش قابل توجهی در مقایسه با موش های دیابتی مشاهده نشد. برای تأیید افزایش سنتز کلاژن، سطح بیان ژن Col4a1 توسط RT-PCR ارزیابی شد (شکل 3 (b)). افزایش قابلتوجهی در بیان ژن Col4a1 در کلیههای موشهای دیابتی در هر دو مقطع زمانی و همچنین در کلیههای موشهای دیابتی و غیردیابتی تحت درمان با ALA از هر دو گروه آزمایشی (4 و 8 هفته)، در مقایسه با گروه کنترل مربوطه مشاهده شد. .

3.4. تغییرات پروفیبروتیک مرتبط با دیابت و درمان ALA.تجزیه و تحلیل وسترن بلات نشان داد که سطح پروتئین TGF- 1 بدون توجه به درمان، پس از 4 هفته به طور قابل توجهی تغییر نمی کند (شکل 4(a)). با این حال، القای آماری معنیدار پروتئین TGF{3}} پس از 8 هفته دیابت تشخیص داده شد که با درمان ALA اندکی کاهش یافت، اما در مقایسه با کنترل به طور قابلتوجهی افزایش یافت. علاوه بر این، القای مشابهی از TGF- 1 در حیوانات غیر دیابتی تحت درمان با ALA مشاهده شد (شکل 4(a)). برای بررسی اینکه آیا القای TGF{8}} با وقوع نشانگرهای فیبروتیک همراه است یا خیر، حضور SMA با استفاده از وسترن بلات آنالیز شد (شکل 4(b)). حالت دیابتی باعث تحریک بیان SMA شد که از هفته چهارم پس از شروع دیابت و به بعد تشخیص داده شد. درمان ALA در موشهای دیابتی پس از 4 هفته SMA را به سطح کنترل کاهش داد، اما پس از 8 هفته بیاثر بود. درمان ALA بعد از 4 هفته بر SMA در موشهای غیردیابتی تأثیری نداشت، در حالی که پس از 8 هفته، منجر به افزایش بیان SMA در مورد کنترل شد، اما این افزایش از نظر آماری معنیدار نبود (شکل 4 (ب)).
درمان موشهای غیردیابتی با ALA منجر به آثار مشابهی در خصوص ویژگیهای پروفیبروتیک در مقایسه با موشهای دیابتی شد، که نشاندهنده نیاز به آشکارسازی مکانیسمهایی است که زمینهساز تغییرات مشاهدهشده شبه فیبروتیک در کلیههای موشهای غیردیابتی تحت درمان با ALA است. به منظور بررسی این امکان که تغییرات اپی ژنتیکی مکانیسمهای دیگری را نشان میدهد که در چشمانداز پروفیبروتیک مشاهدهشده ناشی از ALA در موشهای غیردیابتی، در افزایش خاصی از بیان Col4a1، کلیههای موشهای غیردیابتی کنترل و تحت درمان با ALA بیشتر تحت آنالیز وضعیت متیلاسیون DNA قرار گرفتند. .
3.5. تأثیر ALA بر وضعیت متیلاسیون DNA.سطح جهانی متیلاسیون DNA و بیان ژن بازیگران اصلی درگیر در متیلاسیون DNA (Dnmt1، Dnmt3a و Dnmt3b) و دی متیلاسیون (Tet1) در کلیه های موش های کنترل غیر دیابتی و موش های تحت درمان با ALA به مدت 4 و 8 هفته ارزیابی شد (شکل 5). ). فقط سطح mRNA Tet1 بعد از 8 هفته درمان با ALA از نظر آماری افزایش معنی داری نشان داد، در حالی که بیان Dnmts و سطح جهانی متیلاسیون DNA تفاوت معنی داری را پس از 4 یا 8 هفته درمان با ALA در مقایسه با گروه شاهد نشان نداد.
آزمایش بعدی به بررسی سطح محلی متیلاسیون DNA ژن Col4a1 انجام شد. شکل اصلی کلاژن IV شامل دو زنجیره 1 (IV) و یک زنجیره 2 (IV) است که توسط ژنهای Col4a1 و Col4a2 کدگذاری شدهاند که در جهت سر به سر قرار گرفتهاند و یک واحد رونویسی منحصربهفرد را تشکیل میدهند و در جهتهای مختلف رونویسی میشوند. مروج [17]. Col4a1 از ناحیه بین ژنی با طول 130 جفت باز حاوی دو مکان Sp1، جعبه های CAAT و CTC [17] رونویسی شده است (شکل 6(a)). وضعیت متیلاسیون DNA پروموتر Col4a1/Col4a2 با استفاده از آنالیز MSP ارزیابی شد و موقعیت پرایمرها در شکل 6(a) نشان داده شده است. هر دو جفت آغازگر، ویژه برای DNA متیله و غیر متیله، 2 CpG را در هر آغازگر پوشش دادند. نتایج MSP نشان داد که ALA بر وضعیت متیلاسیون پروموتر Col4a1/Col4a2 پس از {27}}درمان یک هفتهای تأثیری نمیگذارد (شکل 6 (b)). با این حال، کاهش معنیدار آماری در شاخص متیلاسیون DNA پس از 8 هفته درمان با ALA مشاهده شد (شکل 6 (b))، که پتانسیل ALA را برای تعدیل بیان Col4a1 در سراسر تغییر الگوی متیلاسیون DNA پروموتر آن نشان میدهد.

4. بحث
با توجه به نسبت اپیدمی دیابت، DKD شایع ترین علت بیماری کلیوی در مرحله نهایی در سراسر جهان و شاخص ترین عامل برای مرگ و میر زودرس در بیماران مبتلا به دیابت است [28، 29]. بروز DKD در بیماران دیابتی در دهه های گذشته علیرغم درمان شدید برای کنترل قند خون کاهش نیافته است [28، 30]. از جمله راهبردهای درمانی بالقوه ای که در برابر DKD سودمند است، هدف قرار دادن استرس اکسیداتیو است و در آن اصطلاح مشخص شد که ALA می تواند عملکرد کلیه را در دیابت بهبود بخشد [29، 31، 32]. نتایج بهدستآمده در مطالعه حاضر اثرات هیپوگلیسمی ALA را تأیید کرد، اما نشاندهنده ناکارآمدی ALA در برابر سطوح اوره مختل در دیابت طولانیمدت بود.
افزایش قند خون به تنهایی یا همراه با استرس اکسیداتیو یکی از مکانیسمهای دخیل در تشکیل AGE است که تجمع آن در بخشهای گلومرولی و لولهای بینابینی با درجه آسیب کلیوی در یک سیستم مدل تجربی نفروپاتی دیابتی مرتبط است [33، 34] . CML یکی از AGE های اصلی در داخل بدن [35] است که سطح آن در گردش خون و اندام ها از جمله کلیه بیماران دیابتی [36] افزایش می یابد و نقش مهمی در پاتوژنز نفروپاتی دیابتی دارد [37]. نتایج ما نشان داد که رسوب CML عمدتاً در توبولو بینابینی و به میزان کمتری در محفظه گلومرولی کلیه موش صحرایی دیابتی تجمع مییابد که به طور قابل توجهی پس از درمان ALA کاهش یافته است. طبق دادههای منتشر شده، لولههای غنیشده با CML میتوانند آسیبپذیرترین بخش کلیوی باشند [38-40]. در مغایرت با نتایج ما، اثرات محدود ALA بر محتوای CML در موشهای دیابتی، که هم با رنگآمیزی ایمونوهیستوشیمی و هم با تجزیه و تحلیل شیمیایی شناسایی شدهاند، توصیف شدهاند [40] و این تناقض ممکن است از طراحی تجربی این مطالعه ناشی شود.
تجزیه و تحلیل بافت شناسی ساختار کلیه با رنگ آمیزی PAS، اثرات محافظتی ALA در دیابت را تأیید کرد. اثرات آنتی اکسیدانی مفید ALA در برابر آسیب اکسیداتیو ناشی از دیابت در کلیه ها به خوبی ثابت شده است [22، 31، 32]. درمان با ALA برای جلوگیری از نارسایی کلیوی و کاهش تغییرات پاتولوژیک ساختاری کلیه از جمله گسترش ماتریکس مزانژیال گلومرولی و گلومرولواسکلروز به دلیل ترکیب آنتی اکسیدانی و پتانسیل هیپوگلیسمی آن [21، 22] مشخص شد. با توجه به اینکه گلوکز بالا، استرس اکسیداتیو و تشکیل AGE ها به عنوان عوامل مهم برای القای تغییرات سودمند در کلیه شناخته می شوند [41]، اثرات آنتی اکسیدانی و هیپوگلیسمی به خوبی تثبیت شده، و توانایی ALA در کاهش محتوای CML به شدت از این موضوع حمایت می کنند. پتانسیل ALA برای کاهش فرآیند فیبروتیک در کلیه های دیابتی با این حال، نتایج ما نشان داد که در بخشهای بافت کلیه رنگآمیزی شده با ماسون، میزان رسوب فیبر کلاژن پس از درمان ALA در موشهای دیابتی تغییر قابلتوجهی نداشت. علاوه بر این، درمان ALA تمایل به افزایش سنتز کلاژن / محتوای در موش های غیر دیابتی را نشان داد. مطابق با یافته های ما، اثرات مضر ALA بر کلیه های کنترل/سالم گزارش شده است [42]. نویسندگان با مطالعه مکانیسمهای محافظت مجدد ALA در نفروپاتی دیابتی، به طور غیرمنتظرهای دریافتند که درمان با ALA با ایجاد گلومرولواسکلروز، فیبروز توبولو بینابینی و کاهش عملکرد کلیه در کلیههای غیر دیابتی مرتبط است. مطالعات مستقل نشان داد که دوزهای بالاتر ALA باعث آسیب پروتئین اکسیداتیو در موشهای مسن و حتی کاهش عملکرد کلیه در دیابت میشود [40]. در همین راستا، اثر پرواکسیدانی ALA نه تنها در مطالعات حیوانی، بلکه در بیمارانی که از مرحله نهایی بیماری کلیوی که آهن داخل وریدی دریافت میکردند، نیز مشاهده شد [44].
در زمینه اثرات مشاهدهشده ALA بر رسوب کلاژن، نتایج ما بهعلاوه نشان داد که ALA سطح دو نشانگر فیبروتیک TGF- 1 و -SMA را در موشهای دیابتی پس از 8 هفته کاهش نداد و حتی TGF را القا کرد. بیان - 1 در موشهای صحرایی غیردیابتی پس از 8 هفته درمان. در همین راستا، بیان ژن کلاژن نوع IV در موشهای دیابتی و همچنین در موشهای دیابتی و غیردیابتی تحت درمان با ALA به طور قابلتوجهی بالاتر از گروه کنترل بود. قبلاً نشان داده شده بود که استرس اکسیداتیو TGF{6}} و ژن های هدف پایین دست آن مانند کلاژن انواع I، III و IV و همچنین فیبرونکتین را القا می کند [9، 45] و آنتی اکسیدان ها TGF را سرکوب می کنند. 10}} بیان [46]. برخلاف ایده کلی نقش محافظتی و ضد فیبروتیک آنتی اکسیدان ها، نتایج ما نشان می دهد که ALA می تواند اثرات متعددی بر عوامل دخیل در فرآیند فیبروتیک در کلیه های دیابتی داشته باشد. به نظر می رسد که ALA به طور خاص بیان برخی از ژن های مرتبط با فیبروز مانند TGFB1 و به خصوص Col4a1 را القا می کند که بیان افزایش یافته آنها قبلاً پس از 4 هفته درمان با ALA در کلیه های دیابتی و غیردیابتی مشاهده شد. افزایش بیان و رسوب کلاژن نوع I پس از درمان ALA در فیبروبلاست های پوستی انسان مشاهده شده است [24]. این مطالعه نشان داد که تنظیم مثبت کلاژن نوع I ناشی از سیگنال دهی پایین دستی گیرنده TGF-I است، بنابراین اثر دارویی جدید ALA در پیری پوست را نشان می دهد. با توجه به نتایج ارائه شده در اینجا، تنظیم دخیل کلاژن ها ممکن است یک پاسخ سلولی رایج به ALA باشد تا یک مکانیسم خاص برای فیبروبلاست های پوستی.
سنتز کلاژن نوع IV در سطوح رونویسی، پس از رونویسی، و پس از ترجمه به خوبی تنظیم می شود، اما داده های بیشتری در مورد نقش متیلاسیون DNA در بیان Col4a1 در حال ظهور است. مطالعه ای که 40 سال پیش انجام شد نشان داد که درمان سلول های تراتوکارسینومای F9 با عامل دی متیل کننده DNA 5-آزاسیتیدین منجر به افزایش بیان Col4a1 می شود که برای اولین بار نشان می دهد که متیلاسیون DNA ممکن است نقش مهمی در بیان آن ایفا کند [47]. مطالعات متیلوم انسانی و ترانسکریپتوم ارتباط متیلاسیون پروموتر Col4a1 با بیان آن در سلول های سالم و کبد فعال شده برای تولید پروتئین های ECM را نشان داد [20، 48]. همین مورد در سلولهای مزانژیال یافت شد که در آنها به دنبال درمان با آزاسیتیدین، سطح mRNA Col4a1 بهطور قابلتوجهی افزایش یافت [49]. علاوه بر این، در بیماران مبتلا به بیماری مزمن کلیوی، سطح متیلاسیون DNA ژن های Col4a1 و Col4a2 در مقایسه با افراد سالم و در ارتباط با افزایش بیان mRNA و پروتئین به طور قابل توجهی پایین تر بود [50]. نتایج ما شواهد قوی از تنظیم بیان Col4a1 از طریق متیلاسیون DNA را تأیید کرد زیرا دریافتیم که بیان Col4a1 با وضعیت متیلاسیون پروموتور آن در کلیه ارتباط دارد. لازم به ذکر است که تغییرات مشاهده شده در وضعیت متیلاسیون پروموتر Col4a1 احتمالاً بر بیان Col4a2 نیز تأثیر می گذارد، زیرا دو ژن از طریق ناحیه پروموتر دو طرفه متقابل تنظیم می شوند. آغازگرهای MSP مورد استفاده در آزمایشهای ما به گونهای طراحی شدند که تا حدی با دو محل اتصال Sp1 همپوشانی داشته باشند و کاهش متیلاسیون DNA که ما بعد از درمان ALA مشاهده کردیم، میتواند بر بهبود اتصال Sp1 و تنظیم مثبت بیان Col4a1 منعکس شود.
یافتههای ما مبنی بر اینکه بیان Col4a1 و وضعیت متیلاسیون آن مستعد فعالیت ALA در حیوانات غیر دیابتی پس از 8 هفته درمان با ALA است، علاوه بر این، پتانسیل ALA را برای عمل به عنوان یک تنظیمکننده اپی ژنتیک نیز نشان میدهد. با توجه به نتایج ما، ALA آنزیم Tet1 را پس از 8 هفته درمان تحت تأثیر قرار داد، بهسوی افزایش بیان آن که نشاندهنده این احتمال است که دیمتیلاسیون اختصاصی ژن میتواند بدون هیچ اثر خالص قابل تشخیص روی متیلاسیون DNA در کل ژنوم رخ دهد. اگرچه ارتباطی بین افزایش بیان Col4a1 و کاهش متیلاسیون پروموتر آن پس از 8 هفته درمان با ALA وجود دارد، با این حال، دشوار است به طور واضح در نظر بگیریم که دی متیلاسیون DNA تنها ارتباط علت بین درمان ALA و افزایش بیان ژن کلاژن است. در 4 هفته، افزایش بیان Col4a1 با تغییر در وضعیت متیلاسیون آن همراه نبود. توانایی ALA برای تنظیم ژنهای خاص به صورت اپی ژنتیکی برای ژنهای IL{13}} و IL{14}} پیشنهاد شده است که سطوح mRNA و پروتئین کاهشیافته با هیپرمتیلاسیون نواحی پروموتور آنها مرتبط است [51، 52]. اگرچه هایپرمتیلاسیون به عنوان یکی از مکانیسم های عمل ALA پیشنهاد شد، مسیرهای دقیق تنظیم اپی ژنتیکی که توسط ALA هدایت می شود هنوز مشخص نشده است و منتظر می ماند تا برای سایر ژن ها نیز تایید شود. از این رو، ارتباط بین افزایش سنتز/رسوب کلاژن که ممکن است منجر به فنوتیپ پاتولوژیک و دی متیلاسیون DNA با واسطه Tet پروموتر Col4a1 شود که توسط درمان ALA تحریک شده است، نیاز به اثبات بیشتری دارد و باید بستری را برای مطالعات آینده فراهم کند.

5. نتیجه گیری ها
نقش محافظتی ALA در برابر عملکرد نادرست مرتبط با دیابت در ارگان های مختلف از جمله کلیه ها بیشتر به اثرات آنتی اکسیدانی و هیپوگلیسمی آن نسبت داده شده است. با این حال، نتایج ارائه شده در این مطالعه نشان می دهد که حفاظت کلیوی در دیابت توسط ALA می تواند به دلیل افزایش سنتز / رسوب کلاژن در کلیه ها محدود شود. با تجزیه و تحلیل اثرات ALA بر فرآیندهای پروفیبروتیک در کلیه موش های دیابتی، متوجه شدیم که ALA باعث کاهش سنتز کلاژن یا نشانگرهای پروفیبروتیک نمی شود. علاوه بر این، درمان با ALA به رویدادهای پروفیبروتیک و سنتز کلاژن حتی در کلیههای موش صحرایی غیردیابتی کمک کرد که تا حدی با تغییرات در وضعیت متیلاسیون DNA ژن Col4a1 مرتبط است. در نتیجه، در بیماران مبتلا به فیبروز کلیه، احتیاط در مورد استفاده از ALA برای جلوگیری از تشدید عارضه کلیوی موجود ضروری است. علاوه بر این، زمانی که قرار است از ALA برای تقویت پتانسیل آنتی اکسیدانی در یک فرد سالم یا در مدیریت سایر عوارض دیابت استفاده شود، احتیاط لازم است زیرا اثرات مفید یک عارضه می تواند برای دیگری مضر باشد.

1گروه بیولوژی مولکولی، موسسه تحقیقات بیولوژیکی "Siniša Stanković، " موسسه ملی جمهوری صربستان، دانشگاه بلگراد، Bulevar Despota Stefana 142، 11060 بلگراد، صربستان
2 دپارتمان سیتولوژی، موسسه تحقیقات بیولوژیکی "Siniša Stanković"، موسسه ملی جمهوری صربستان،
دانشگاه بلگراد، Bulevar Despota Stefana 142، 11060 بلگراد، صربستان
مکاتبات باید به الکساندرا اوسکوکوویچ ارسال شود. auskokovic@ibiss.bg.ac.rs
دریافت شده در 4 نوامبر 2020؛ بازبینی شده در 19 فوریه 2021؛ پذیرش در 27 فوریه 2021؛ منتشر شده در 12 مارس 2021
ویراستار آکادمیک: آلین چیوبیکا
حق چاپ © 2021 Nevena Grdović et al. این یک مقاله با دسترسی آزاد است که تحت مجوز Creative Commons Attribution توزیع شده است، که اجازه استفاده، توزیع و تکثیر نامحدود در هر رسانه را می دهد، مشروط بر اینکه اثر اصلی به درستی ذکر شده باشد.
در دسترس بودن داده ها
تمام داده های مرتبط مورد استفاده برای حمایت از یافته های این مطالعه در مقاله گنجانده شده است.
تضاد علاقه
نویسندگان اعلام می کنند که هیچ تضاد منافعی در مورد انتشار این مقاله وجود ندارد.
مشارکت نویسندگان
مفهوم و طراحی آزمایش ها: MM، NG، AU. نگهداری و درمان حیوانات: MĐ, JAJ, AU, SD. انجام تجزیه و تحلیل بافت شناسی، ایمونوهیستوشیمی و کمی سازی نتایج: JAJ، MĐ، ST. تجزیه و تحلیل وسترن بلات انجام شده: AU، SD، NG. آزمایشهای RTqPCR را انجام داد: JR، MĐ. آزمایشهای متیلاسیون DNA را انجام داد: JR، AT، MV. تجزیه و تحلیل آماری: NG; تفسیر داده ها و تهیه ارقام: NG, MM; مقاله را نوشت: NG, AU; بازبینی انتقادی نسخه خطی: MV, SD. همه نویسندگان نسخه نهایی را برای انتشار تأیید کردند.
قدردانی
این کار توسط وزارت آموزش، علم و توسعه فناوری جمهوری صربستان (Grant No. 451-03-9/{1}}/200007) پشتیبانی شده است.
مواد تکمیلی
جدول تکمیلی S1: توالی پرایمرهای مورد استفاده برای تجزیه و تحلیل کمی PCR در زمان واقعی Col4a1 (کلاژن نوع IV زنجیره آلفا 1)، Dnmt1 (DNA متیل ترانسفراز 1)، Dnmt3a (DNA متیل ترانسفراز 3 آلفا)، Dnmt3b (DNA متیل ترانسفراز) (Tet methylcytosine dioxygenase 1) و بیان ژن Actb (Actin، بتا). جدول تکمیلی S2: توالی پرایمرها برای آنالیز MSP متیلاسیون DNA ناحیه پروموتر ژن Col4a1. شکل تکمیلی S1: تصاویر نشان دهنده ایمونوبلات. سطح پروتئین TGF{17}} (A) و SMA (B)، دو پروتئین مرتبط با فیبروز، در کلیههای ALA تحت درمان یا درمان نشده، کنترل و موشهای دیابتی، 4 و 8 هفته پس از القای دیابت، تعیین شده توسط Western تجزیه و تحلیل لکه (مواد تکمیلی)
منابع
[1] RC Atkins، "اپیدمیولوژی بیماری مزمن کلیه"، کلیه بین المللی. متمم، ج. 67، صفحات S14–S18، 2005.
[2] AB Oyenihi، AO Ayeleso، E. Mukwevho، و B. Masala، "راهبردهای آنتی اکسیدانی در مدیریت نوروپاتی دیابتی"، BioMed Research International, vol. 2015، شناسه مقاله 515042، 15 صفحه، 1394.
[3] M. Lv، Z. Chen، GY Hu، و QB Li، "راهبردهای درمانی نفروپاتی دیابتی: پیشرفت اخیر و چشم اندازهای آینده"، Drug Discovery Today، جلد. 20، شماره 3، صص 332-346، 2015.
[4] الف. کاریهالو، «درمان ضد فیبروز و نفروپاتی دیابتی»، گزارشهای کنونی دیابت، جلد. 12، شماره 4، صفحات 414-422، 2012.
[5] S. Yamagishi و T. Matsui، "محصولات نهایی گلیکاسیون پیشرفته، استرس اکسیداتیو، و نفروپاتی دیابتی"، داروی اکسیداتیو و طول عمر سلولی، جلد. 3، نه 2، صص 414-108، 2010.
[6] F. Genovese، AA Manresa، DJ Leeming، MA Karsdal و P. Boor، "ماتریکس خارج سلولی در کلیه: منبع بیومارکرهای جدید غیر تهاجمی فیبروز کلیه؟"، Fibrogenesis & Tissue Repair، جلد. 7، نه 1، ص. 4، 2014.
[7] S. چن، SW Hong، MC Iglesias-dela Cruz، M. Isono، A. کازارتو و اف. 23، صفحات 471-481، 2001.
[8] BB Hofman, K. Sharma, Y. Zhu, and FN Ziyadeh, "Transcriptional activation of transforming growth factor- 1 in themesangial cell cells by high glucose غلظت" Kidney International, vol. 54، شماره 4، صص 1107-1116، 1998.
[9] M. Gonzalez-Ramos, S. de Frutos, M. Griera, et al., "کیناز مرتبط با اینتگرین واسطه افزایش تنظیم فاکتور رشد تبدیل کننده وابسته به پراکسید هیدروژن است"، Free Radical Biology & Medicine, vol. 61، صفحات 416-427، 2013.
[10] K. Sharma و TA McGowan، "TGF- در بیماری کلیوی دیابتی: نقش مسیرهای سیگنالینگ جدید"، بررسیهای سیتوکین و فاکتور رشد، جلد. 11، نه 1-2، صفحات 115-123، 2000.
[11] FJ Lopez-Hernandez و JM Lopez-Novoa، "نقش TGF- در بیماری مزمن کلیه: ادغام اثرات لوله ای، گلومرولی و عروقی" Cell and Tissue Research، جلد. 347، شماره 1، صفحات 141-154، 2012.
[12] PD Yurchenco و JJ O'Rear، "مجموعه لایه پایه"، دیدگاه فعلی در بیولوژی سلولی، جلد. 6، نه 5، صص 674-681، 1994.
[13] الف. Nerlich و E. Schleicher، "محلی سازی ایمونوهیستوشیمی اجزای ماتریکس خارج سلولی در ضایعات گلومرولی دیابتی انسان،" The American Journal of Pathology, vol. 139، شماره 4، صص 889-899، 1991.
[14] RM Mason و NA Wahab، "متابولیسم ماتریکس خارج سلولی در نفروپاتی دیابتی"، مجله انجمن نفرولوژی آمریکا، جلد. 14، شماره 5، صص 1358-1373، 2003.
[15] RE Gilbert, A. Cox, LL Wu et al., "بیان تبدیل فاکتور رشد بتا 1 و کلاژن نوع IV در لوله بینابینی کلیوی در دیابت تجربی - اثرات مهار ACE" Diabetes, vol. 47، شماره 3، صفحات 414-422، 1998.
[16] MS Razzaque, T. Koji, Y. Horita, et al., "Synthesis of type III collagen and type IV collagen by سلول های اپیتلیال لوله ای در نفروپاتی دیابتی" Pathology, Research and Practice, vol. 191، شماره 11، صفحات 1099-1104، 1995.
[17] JP Grande، DC Melder، DL Kluge، و ED Wieben، "ساختار پروموتر کلاژن IV موش"، Biochimica et Bio- Physica Acta، جلد. 1309، شماره 1-2، صفحات 85-88، 1996.
[18] E. Verdura, D. Hervé, F. Bergametti, et al., "Disruption of a miR-29 site binding lead to COL4A1 upregulation باعث ایجاد میکروآنژیوپاتی اتوزومال غالب پونتین با لکوآنسفالوپاتی می شود." Annals of Neurology, vol. 80، شماره 5، ص 741- 753، 2016.
[19] م. Grifiths، M. Van Sinderen، K. Rainczuk و E. Dimitriadis، "بیان بیش از حد miR{{1}c و کاهش COL4A1 در آندومتر نابارور انسان ظرفیت چسبندگی سلول های اپیتلیال آندومتر را _در شرایط آزمایشگاهی{5} کاهش می دهد. دلالت بر نقشهایی در پذیرش، "گزارشهای علمی، جلد. 9، نه 1، ص. 8644، 2019.
[20] الف. El Taghdouini، AL Sørensen، AH Reiner، و همکاران، "تجزیه و تحلیل گسترده ژنوم متیلاسیون DNA و الگوهای بیان ژن در سلول های کبد انسان خالص، کشت نشده و سلول های ستاره ای کبدی فعال شده،" Oncotarget، جلد. 6، نه 29، ص 26729– 26745، 2015.
