قسمت 1: درمان نارسایی قلبی در بیماران مبتلا به بیماری مزمن کلیه: تردیدها و تحولات جدید از آخرین دستورالعمل ESC
Jul 04, 2022
برای اطلاعات بیشتر. مخاطبtina.xiang@wecistanche.com
چکیده: بیماران مبتلا بهنارسایی قلبی(HF) و مرتبطبیماری مزمن کلیوی(CKD) جمعیتی هستند که کمتر در کارآزماییهای بالینی حضور دارند. علاوه بر این، افراد با شدیدتر برآورد شده استنرخ فیلتراسیون گلومرولیکاهش اغلب از مطالعات بزرگ حذف می شوند. در این تنظیمات، بیشتر دادهها از تحلیلهای تعقیبی و مطالعات گذشتهنگر به دست میآیند. بر این اساس، در بیماران مبتلا به CKD پیشرفته، هیچ مطالعه خاصی برای ارزیابی اثرات طولانی مدت داروهای سنتی که معمولاً در HF تجویز می شوند، وجود ندارد. نگرانیهای کنونی ممکن است روی رویکرد عملی به درمان سنتی تأثیر بگذارد، و در این شرایط، پزشکان اغلب تمایلی به تجویز و تیتراسیون برخی از داروهایی که بر روی سیستم رنین-آنژیوتانسین-آلدوسترون و فعالیت سمپاتیک اثر میگذارند، ندارند. بنابراین، کاربرد گسترده در زیرگروه های مختلف HF با شرایط مرتبط گسترده و علل مختلف اختلال عملکرد کلیوی موضوع بحث باقی می ماند. به نظر میرسد نقش داروهای جدید، مانند مهارکنندههای مسدودکننده گیرنده آنژیوتانسین، مهارکنندههای نپریلیزین و مهارکنندههای انتقالدهنده مرتبط با سدیم-گلوکز 2، دیدگاه جدیدی را در بیماران مبتلا به CKD ارائه میکند. با توجه به اثرات محافظتی عروقی و هورمونی، استفاده از این عوامل ممکن است با خیال راحت در بیماران مبتلا بهاختلال عملکرد کلیهدر بلند مدت. در این مرور، ما بزرگترین کارآزماییهایی را که دادهها را بر روی افراد مبتلا به HF و CKD گزارش میکنند، مورد بحث قرار دادیم، در حالی که یک الگوریتم گامبهگام عملی را برای جلوگیری از عوارض کلیوی و قلبی پیشنهاد کردیم.
کلمات کلیدی: نارسایی قلبی; بیماری مزمن کلیوی؛ تخمین نرخ فیلتراسیون گلومرولی. ناقلین مرتبط با سدیم-گلوکز 2 بازدارنده. رفتار؛ مهارکننده های گیرنده آنژیوتانسین مهارکننده های نپری لیزین

برای اطلاع از فروش سیستانچ اینجا را کلیک کنید
1. مقدمه
جدیدترین دستورالعملهای HF الگوریتم تجدیدنظر شدهای را برای درمان نارسایی قلبی با کسر جهشی کاهشیافته (HFrEF)، با رویکرد "چهار درمانی" با استفاده از مهارکنندههای SGLT{0}}، مهارکنندههای مسدودکننده گیرنده آنژیوتانسین (ARN) پیشنهاد میکنند. (به عنوان جایگزینی برای مهارکنندههای آنزیم مبدل آنژیوتانسین (ACE-I) و مسدودکنندههای گیرنده آنژیوتانسین (ARBs) یا در بیماران HFrEF جدید با کلاس توصیهشده llb)، در راس بلوکرهای B و آنتاگونیستهای گیرنده مینرالوکورتیکوئید (MRAs) ، با بهبود قابل توجهی در نتایج بالینی از نظر بستری شدن در بیمارستان و مرگ و میر [1]. با این حال، مهارکنندههای سیستم رنین-آنژیوتانسین (RAAS)، MRAها، مهارکنندههای مسدودکننده گیرنده آنژیوتانسین، مهارکنندههای نپریلیزین (ARNI) و مهارکنندههای انتقالدهنده متصل به سدیم-گلوکز 2 (SGLT2) بهدلیل تغییرات در فیزیولوژی کلیوی، به طور قابلتوجهی بر عملکرد کلیه تأثیر میگذارند. این داروها ریست می شوندعملکرد کلیهمنحنی، بر رابطه فشارهای هیدرواستاتیک داخل گلومرولی-ناتریورز از طریق مکانیسم بازخورد توبول-گلومرولی و با تضاد اثرات بر روی شریان های گلومرولی آوران و وابران ناشی از عوامل مختلف تأثیر می گذارد. این اثرات کسر فیلتراسیون فیزیولوژیکی را تغییر میدهند، پیامدهای پیشگیرانه و کموتاکتیک متفاوتی روی ماکولا دنسا دارند و ممکن است بر عملکرد لولهای تأثیر بگذارند (شکل 1). استفاده همزمان از مهارکنندههای RAAS، MRAها، و داروهای جدید مانند مهارکنندههای SGLT2 و ARNI ممکن است روند نارسایی گذرا کلیوی را که پس از تجویز اولیه رخ میدهد، تقویت کند و منجر به اینرسی شروع و افزایش تیتراسیون این درمانهای نجاتبخش شود. در بیشتر موارد، نارسایی کلیوی گذرا است و عملکرد کلیه تمایل دارد به شرایط قبلی خود بازگردد یا در طولانی مدت ثابت بماند [2]. با این حال، اثر بر عملکرد کلیه ناشی از پلی تراپی به اندازه کافی مورد تجزیه و تحلیل قرار نمی گیرد. بنابراین، بیماران HF با اختلال عملکرد کلیوی همزمان با احتمال کمتری درمانهای توصیهشده توسط دستورالعمل را دریافت میکنند، حتی اگر این همیشه موجه نباشد. در این بررسی، ما اثرات داروهای نارسایی قلبی کلیه (HF) را در بیماران مبتلا به HF و بیماری مزمن کلیوی (CKD) گزارش کردیم و کاربرد صحیح این درمانهای نجات دهنده را در عمل بالینی پیشنهاد کردیم.


2. ویژگی های بالینی بیماران مبتلا به بیماری مزمن کلیه و نارسایی قلبی
مطالعات قبلی بر روی بیماران سرپایی مبتلا به HF مزمن نشان داد که یکی از بالاترین شیوع در بین بیماری های غیر قلبی عروقی مربوط به نارسایی کلیوی بین 30 تا 50 درصد است [3]. قلب و کلیه ها کاملاً مرتبط بودند؛ اختلال عملکرد هر یک از آن اندام ها به دلیل مکانیسم های مختلف مانند التهاب، استرس اکسیداتیو، اختلال در هموستاز هیدرو نمکی و مقاومت ادرارآور منجر به زوال عملکردی دیگر شد [4،5]. در HF مزمن، برون ده قلبی کاهش یافته است، عمدتا به دلیل HFrEF که منجر به کاهش پرفیوژن اندام می شود. در بیماران مبتلا به HFpEF، فشارهای پرشدگی بالا ویژگی اصلی همودینامیک بود و کاهش پر شدن سیستولیک منجر به ذخیره ناکافی حجم سکته مغزی شد که در نهایت باعث کاهش برون ده قلبی شد. نشان داده شده است که کاهش برون ده قلبی در بیماران مبتلا به HF مزمن منجر به کاهش جریان خون کلیوی می شود. علاوه بر این، در پاسخ به کاهش برون ده قلبی، کلیه مکانیسم هایی را ترویج می کند که منجر به احتباس آب و سدیم می شود و در نهایت باعث احتقان تحت بالینی می شود که به نوبه خود باعث اختلال بیشتر عملکرد کلیه می شود. هم در محیط های تجربی و هم در بیماران مبتلا به HF مزمن یا حاد، افزایش فشار ورید مرکزی یا فشار شکمی با افزایش خطر بدتر شدن عملکرد کلیه همراه بود. در سندرم قلب و عروق نوع 2، CKD در 45 تا 63 درصد بیماران مشاهده شده است. احتقان کلیه، هیپوپرفیوژن و افزایش فشار دهلیز راست نشانههای بارز این وضعیت بالینی است [6]. بیماران HF و CKD کیفیت زندگی پایینی داشتند و به دلیل چندین عامل خطر رایج مانند دیابت، فشار خون بالا و بیماری عروق کرونر (CAD) بار بالایی از خطر قلبی عروقی (CV) را نشان دادند. فنوتیپ کردن بیماران مبتلا به اختلال عملکرد کلیوی یک چالش واقعی است. مکانیسم های پاتوفیزیولوژیک و نقش پیش آگهی اختلال عملکرد کلیه ممکن است در HFrEE، HFmrEF و HFpEF متفاوت باشد. CKD اغلب با شرایط و مراحل HF شدیدتر، مستقل از کسر جهشی بطن چپ (LVEF) همراه است. روابط بین CKD، سن بالاتر، جنس مونث، دیابت و مرحله HF در سه گروه HF مشابه بود، اما مطالعات متعدد نشان دادند که CKD در نارسایی قلبی با کسر جهشی حفظ شده (HFpEF) بیشتر از نارسایی قلبی با کاهش خفیف بود. کسر جهشی (HFmrEF) و HFrEF [8،9]. مطالعات دیگر شیوع بالاتری از CKD را در بیماران HFrEF نشان داد [10]. ارتباط بین HFpEF و بدتر شدن عملکرد کلیه مستقل از وجود CKD در ابتدا بود. اختلال عملکرد کلیه در HFpEF ممکن است به عنوان یک همبودی عمده در نظر گرفته شود، با یک تاثیر پیش آگهی کلی بدون هیچ ارتباطی با وضعیت بدتر HF: برعکس، در بیماران HFrEF، اختلال عملکرد کلیه ممکن است منعکس کننده پیشرفت HF باشد، شاید به دلیل برون ده قلبی پایین، هیپوپرفیوژن همودینامیک، و فعال سازی سمپاتیک و عصبی هورمونی [11].
در میان بیماریهای همراه غیر CV، بیماری مزمن کلیه بیشتر با بستری شدن در بیمارستان همراه بود[12]. اختلال عملکرد کلیه، صرف نظر از تعریف و روش غربالگری آن، خطر بالینی قابل توجهی را برای مرگ و میر بیش از حد در بیماران مبتلا به HF ایجاد می کند [13]. CKD با پیامدهای بدتر در تمام فنوتیپ های HF همراه بود. با این حال، ادبیات در مورد مرگ و میر در HFpEF و CKD نتایج متناقضی را نشان می دهد. در متاآنالیزهای بزرگتر، که شامل گروهی از بیماران HFpEF بود، CKD پیش بینی کننده قوی تری برای مرگ بود [14]. برعکس، یک متاآنالیز از گروه جهانی در نارسایی مزمن قلب (MAGGIC) میزان مرگ و میر کمتر و ارتباط کمتری بین CKD و مرگ در بیماران مبتلا به HFpEF نسبت به بیماران مبتلا به HFrEF نشان داد [15]. این نتیجه در ثبت نارسایی قلب سوئد تأیید شد، که در آن ارتباط بین CKD و خطر مرگ و میر در بیماران HFpEF کمتر مشخص بود [16].
در بیماران مبتلا به نارسایی حاد قلبی (AHF)، ما میتوانیم دو فنوتیپ متمایز را تشخیص دهیم: بیماران مبتلا به اختلال عملکرد کلیوی اولیه، که به عنوان CKD تعریف میشود، و بیمارانی که در طول بستری شدن در بیمارستان دچار بدتر شدن عملکرد کلیوی (WRF) میشوند [17]. طبقه بندی جدیدی از WRF با توجه به وضوح یا ماندگاری چارچوب زمانی پیشنهاد شده است. اولین سناریوی بالینی، بیمار با عملکرد کلیوی خوب و بروز WRF "شبه" در طول بستری شدن در بیمارستان برای HF حاد بود که ثانویه به درمان رفع احتقان در نظر گرفته شد. افزایش کراتینین در بیمارستان معمولاً پس از ترخیص باقی نمی ماند، بدون عواقب برای پیش آگهی اگر بیمار به خوبی درمان می شد، با رفع احتقان کارآمد در هنگام ترخیص. سناریوی دوم بیمار مبتلا به WRF واقعی به دلیل احتقان (افزایش فشار وریدی کلیوی) و هیپوپرفیوژن (کاهش پرفیوژن شریانی) بود که در آن بدتر شدن کلیه ادامه داشت، با افزایش کراتینین نیز در دوره پس از ترخیص و با بار بیشتر بستری مجدد HF [18]. در نهایت، در سناریوی سوم، WRF می تواند در حضور CKD مربوط به کاهش جریان خون قشر مغز و گلومرولواسکلروز مزمن با کاهش دیواره قشر رخ دهد. این زیرگروه در بیماران مسنتر با چندین بیماری همراه رایج بود، جایی که WRF منعکسکننده زوال واقعی عملکرد کلیه بود، با ارزش پیش آگهی بدتر. طبقه بندی فعلی تکمیل نشده بود زیرا ارزیابی سریال کلیه پس از ترخیص و شدت اختلال تخمین زده شده موثر در نرخ فیلتراسیون گلومرولی (eGFR) را در نظر نمی گرفت (جدول 1).
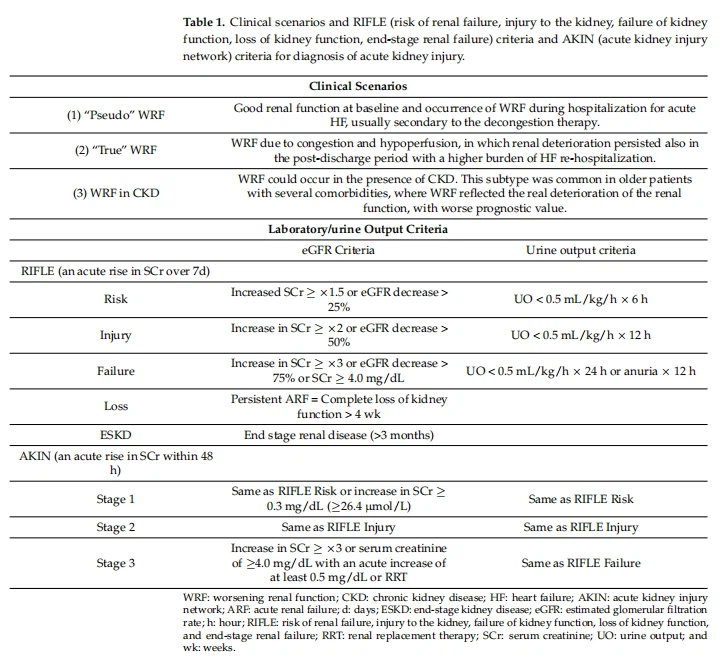

3. هدف و محدودیت های درمانی در بیماران مبتلا به نارسایی قلبی و بیماری مزمن کلیه
تمام داروهای مورد استفاده در بیماران HF اثرات بالقوه مضری بر عملکرد کلیه دارند و بیماران HF با اختلال عملکرد کلیه را در معرض خطر بیشتری از عوارض جانبی کلیوی مانند هیپرکالمی و دیالیز قرار می دهند. از نظر تاریخی، دادههای حاصل از کارآزماییهای تصادفیسازی و کنترلشده در مورد تأثیر داروهای HF در بیماران HF و CKD، به دلیل حذف بیماران مبتلا به CKD، محدود بود.
مطالعات کارآزمایی اختلال عملکرد بطن چپ (SOLVD) 36 درصد از بیماران مبتلا به CKD و eGFR را مورد بررسی قرار دادند.<60 ml/min/1.73="" m;33%="" of="" all="" patients="" presented="" a="">0.5 mg/dL increase in serum creatinine; in the final analyses, the benefits on all-cause mortality were maintained across the entire CKDspectrum [19]. This finding was confirmed by the survival and ventricular enlargement (SAVE) trial, which demonstrated the improvement in survival and reduced morbidity in patients with asymptomatic left ventricular dysfunction treated with captopril vs. placebo regardless of CKD(exclusion criteria Cr>2.5 mg/dL,33%of patients with CKD). After 42 months of follow-up, the risk for death associated with renal events was a hazard ratio (HR) of 1.63 (95%CI 1.05-2.52)in the placebo group, versus HR of 1.33 (95% CI 0.81-2.21) in the captopril group (p=0.49 for interaction)[20]. Similar findings were found in the trandolapril cardiac evaluation (TRACE)study group, in which 40% of patients with post-myocardial infarct LV dysfunction had CKD. In this group, trandolapril significantly reduced the risk of CV mortality and HF progression [21]. More recently, in the NETWORK and ATLAS trials, patients with Cr>2.3 mg/dL and Cr>2.5 mg/dL were excluded, and no specific therapeutic data on advanced CKD could be extrapolated. The valsartan heart failure trial (Val-HeFT) included a higher percentage of patients with HF and CKD (58% of the entire cohort); valsartan significantly reduced the combined endpoint of mortality and morbidity and improved HF symptoms also in HF patients with CKD[22]. Notably, candesartan in heart failure assessment of reduction in mortality and morbidity (CHARM)-added and CHARM-alternative trials, which included a significant proportion of the CKD population, confirmed the previous data. However, patients with more severe CKD (creatinine>3. 0 میلی گرم در دسی لیتر) حذف شدند. در این مطالعه، درصد قابل توجهی از بیماران (7.1 درصد) درمان را به دلیل افزایش کراتینین، در غیاب اطلاعات کافی در مورد تأثیر دائمی بر نتیجه کلیوی، قطع کردند [23].
مدلهای رگرسیون خطرات متناسب کاکس در کارآزمایی SOLVD نشان داد که در مقایسه با دارونما، ACE-I کاهش eGFR را کاهش نداد، که در هر دو گروه مشابه بود. با این حال، این مطالعه اجتناب از قطع ACE-I را در بیماران مبتلا به کاهش eGFR کم و متوسط به دلیل تأثیر مفید بر نتیجه کلی CV توصیه کرد [24]. علاوه بر این، هر دو ACE-I و ARB به دلیل اثر فیزیولوژیکی مطلوبشان به طور قابل توجهی کاهش eGFR را در دیابت و نفروپاتی کاهش دادند [25] (جدول 2).



در بیماران دارای ریتم سینوسی با HF و LVEF<50%, b-blockers="" reduced="" mortality="" versus="" placebo="" without="" any="" deterioration="" in="" renal="" function="" over="" time="" in="" patients="" with="" moderate="" or="" moderate="" to="" severe="" renal="" impairment="" [26].="" these="" beneficial="" results="" were="" lost="" in="" patients="" with="" hf="" and="" atrial="" fibrillation(af)at="" any="" level="" of="" egfr.="" metoprolol="" was="" analyzed="" in="" three="" renal="" function="" subgroups="" and="" demonstrated="" an="" effective="" reduction="" in="" all-cause="" death="" and="" hospitalizations="" for="" worsening="" hif="" in="" patients="" with=""><45 ml/min/1.73="" m²="" and="" egfr="" 45="" to="" 60ml/min/1.73="" m²,="" as="" in="" those="" with="" egfr="">60 میلی لیتر در دقیقه / 1.73 متر مربع【27】. متاآنالیز مطالعات CAPRICORN (کنترل بقای کارودیلول پس از انفارکتوس در مطالعه اختلال عملکرد بطن چپ) و COPERNICUS (مطالعه تصادفی بقای آینده نگر کارودیلول) نشان داد که کارودیلول در بیماران مبتلا به و بدون CKD با افزایش نسبی نسبی به خوبی تحمل می شود. افزایش کراتینین سرم، بدون عوارض جانبی جدی کلیه و تغییرات الکترولیت در بیماران CKD. درمان با کارودیلول نتیجه ترکیبی مرگ و میر CV یا بستری در بیمارستان HF را کاهش داد، بدون اینکه اثرات قابل توجهی بر مرگ ناگهانی در حضور CKD خفیف تا متوسط داشته باشد[28]. کارودیلول عوارض و مرگ و میر را در بیماران دیالیزی شده با کاردیومیوپاتی دیلاته کاهش داد [29]. یافتههای متضاد کنونی نشان میدهد که استفاده از B-blockerها در دیالیز یا در بیماران مبتلا به زوال شدید کلیه نیاز به بررسی بیشتر دارد (جدول 3).



از نظر تاریخی، MRAها در بیماران مبتلا به اختلال عملکرد کلیوی منع مصرف در نظر گرفته می شدند، زیرا خطر بالای هیپرکالمی وجود داشت. اثر مفید اسپیرونولاکتون و اپلرنون بر نتایج بیماران HF اخیراً به بیماران مبتلا به اختلال عملکرد کلیوی گسترش یافته است. با این حال، هیچ کارآزمایی بر روی اثرات MRA ها بر پیامد کلیوی و مرگ و میر مرتبط در بیماران مبتلا به HF و eGFR متمرکز نبود.<30ml in/1.73m2="" [30].="" a="" recently="" published="" secondary="" analysis="" of="" the="" eplerenone="" in="" mild="" patients="" hospitalized="" and="" a="" survival="" study="" in="" heart="" failure="" (emphasis-hf)="" examined="" the="" beneficial="" and="" adverse="" effects="" of="" eplerenone="" on="" renal="" function.="" even="" though="" patients="" with="" an=""><50 ml/min/1.73m2="" were="" assigned="" lower="" target="" doses="" of="" eplerenone="" (25="" mg="" versus="" 50="" mg),="" the="" drug="" showed="" a="" beneficial="" effect="" on="" the="" outcome="" versus="" placebo;="" however,="" patients="" with="" egfr="" 30-49ml/min/1.73m²="" experienced="" higher="" incidences="" of="" hyperkalemia,="" renal="" failure,="" and="" drug="" discontinuation="" [31]patients="" with="" moderate="" renal="" dysfunction="" should="" be="" monitored="" closely="" after="" the="" initiation="" of="" an="" mras,="" with="" frequent="" k="" analyses="" and="" a="" slower="" up-titration="" of="" therapy,="" due="" to="" the="" higher="" risk="" of="" hyperkalemia="" and="" the="" potential="" arrhythmic="" and="" renal="" consequences.="" mras="" treatment="" did="" not="" affect="" renal="" function="" in="" subjects="" without="" evidence="" of="" hf;="" finerenone,="" a="" non-steroidal="" selective="" mra,="" resulted="" in="" a="" lower="" risk="" of="" ckd="" progression="" and="" cv="" events="" than="" placebo="" in="" patients="" with="" ckd="" and="" type="" two="" diabetes="" [32].="" the="" aforementioned="" data="" reinforced="" the="" use="" of="" mras="" in="" patients="" with="" either="" hf="" and="" mild="" to="" moderate="" ckd,="" or="" in="" patients="" with="" high="" cv="" risk="" associated="" with="" renal="" dysfunction,="" but="" a="" larger="" use="" in="" more="" advanced="" hf="" and="" ckd="" stages="" was="" not="" extensively="" carried="" out,="" and="" it="" deserves="" specific="">
در بیماران مبتلا به HF، اثر سودمند ARNI مکانیسمهای فیزیولوژیکی متعددی را نشان داد، از جمله افزایش GMP حلقوی درون سلولی که با اثرات انقباضی بازخورد لوله-گلومرولی بر شریان آوران مقابله میکند. در یک تحلیل گذشته نگر از مقایسه آینده نگر ARNI با ACE-i برای تعیین تاثیر بر مرگ و میر جهانی و عوارض در کارآزمایی نارسایی قلبی (PARADIGM-HF)، ساکوبیتریل و والزارتان نتایج CV را بهبود بخشیدند و منجر به کاهش سرعت کاهش eGFR در مقایسه با انالاپریل شدند. (تفاوت 0.4 میلیلیتر/دقیقه/1.73 متر مربع در سال). کاهش خطر نسبی مرتبط با ساکوبیتریل و والزارتان در بیماران با و بدون اختلال عملکرد کلیوی مشابه بود، علیرغم اینکه باعث افزایش متوسط آلبومین ادرار به کراتینین شد. نسبت [33]. میزان سود در بیماران مبتلا به دیابت بیشتر از افراد بدون [34] بود. این اثر در بیماران HFpEF نیز تأیید شد، که در آنها ساکوبیتریل و والزارتان خطر ابتلا به دیابت را بیش از یا مساوی 50 درصد کاهش دادند. کاهش eGFR، مرحله نهایی بیماری کلیوی، یا مرگ ناشی از علت کلیوی، و کاهش کاهش eGFR در طول پیگیری در مقابل والزارتان. مزایای کلیوی در بیماران مبتلا به LVEF بین 30-60 درصد مشهودتر بود. با این حال، کل جمعیت شرکتکننده در مطالعه، بدون توجه به LVEF، کاهش eGFR را به میزان 1.8 میلیلیتر/دقیقه/73/1 متر مربع در سال در گروه ساکوبیتریل و والزارتان تجربه کردند، در مقابل 2.4 میلیلیتر/دقیقه/1.73 متر مربع در سال در گروه مهارکنندههای RAAS، بدون در نظر گرفتن LVEF[35]. ].
انتقال دهنده های SGLT{0}} عمدتاً در لوله پیچیده پروگزیمال کلیه قرار دارند. با مهار Na plus و بازجذب گلوکز، مهارکنندههای SGLT{2}} باعث افزایش گلوکوزوری و ناتریورز میشوند و مایع خارج سلولی و حجم پلاسما را کاهش میدهند. این اثرات باعث کاهش پس بار و پیش بار بطن چپ و کاهش فشار خون و سفتی شریانی شد و در عین حال جریان خون درون قلب را بهبود بخشید [36]. اثرات همودینامیک کلیه ناشی از مهار SGLT به کاهش فشار داخل گلومرولی نسبت داده شد. اثر SGLT برای متعادل کردن فشار خون و هایپرفیلتراسیون گلومرولی در دیابت نوع دو (T2DM)، که در آن هیپرگلیسمی منجر به بازجذب سدیم کلیوی میشود، که از طریق بازخورد توبولوگلومرولی باعث ایجاد پاسخ گشادکننده عروقی کلیه آوران میشود، بسیار مهم بود [37] امپاگلیفوزین باعث بهبود بیماری کلیه دیابتی با کاهش شکافت میتوکندری از طریق مسیر AMPK/SP1/PGAM5 [38،39]. با تمام این اثرات مطلوب، مهارکنندههای SGLT{14}} منجر به محافظت از نفرون و کاهش پیشرفت نفروپاتی دیابتی شد. علاوه بر این، مبدل سدیم-هیدروژن 3 (NHE3) در لوله پروگزیمال بیان میشود و Na plus را با صادرات پروتون به سلول مبادله میکند [40]. NHE3 بیان SGLT{20}} را در غشای نفرون افزایش میدهد که منجر به فعالسازی سمپاتیک/RAAS و اسیدوز میشود. بازیابی هموستاز Na به علاوه به مهار NHE3 کلیه توسط مهارکنندههای SGLT{22}} نیز بستگی دارد. در نهایت، در یک متاآنالیز کارآزماییهای تصادفیسازی و کنترلشده، SGLT{24}} آلبومینوری را کاهش داد، پیشرفت میکروآلبومینوری به ماکروآلبومینوری را کاهش داد و خطر بیماری کلیوی در مرحله نهایی را کاهش داد.
در سالهای اخیر، کارآزماییهای شاخص مزایای CV و پیامدهای کلیوی مهارکنندههای SGLT-2 را در جمعیت HFrEF نشان دادند. کارآزمایی نتیجه امپاگلیفلوزین در بیماران مبتلا به نارسایی مزمن قلبی و کاهش کسر جهشی (EMPEROR-Reduced) نشان داد که امپاگلیفلوزین هم مرگ CV و هم بستری شدن HF را در بیماران مبتلا به HFrEF، علیرغم OMT کاهش میدهد. این کارآزمایی شامل بیمارانی با eGFR بالاتر از 20 میلیلیتر در دقیقه/1.73 متر بود و 48 درصد از افراد ثبتنام شده دارای eGFR بودند.<60 ml/min/1.73="" m².="" empagliflozin="" reduced="" the="" primary="" outcome="" and="" the="" total="" number="" of="" hf="" hospitalizations="" in="" patients="" with="" and="" without="" ckd,="" and="" had="" the="" beneficial="" effect="" of="" reducing="" the="" decline="" of="" renal="" function,="" regardless="" of="" the="" severity="" of="" renal="" function="" at="" baseline="" [43].="" the="" analyses="" of="" the="" credence="" (canagliflozin="" and="" renal="" events="" in="" diabetes="" with="" established="" nephropathy="" clinical="" evaluation)trial="" showed="" the="" effects="" of="" canagliflozin="" in="" reducing="" the="" incidence="" of="" kidney-related="" adverse="" events="" in="" patients="" with="" t2dm="" and="" ckd[44].="" moreover,="" the="" dapagliflozin="" and="" prevention="" of="" adverse="" outcomes="" in="" heart="" failure="" (dapa-hf)="" trial="" included="" 41%of="" patients="" with=""><60 ml/min/1.73="" m²="" and="" excluded="" those="" with=""><25 ml/min/1.73="" m².="" the="" results="" of="" the="" trial="" showed="" that="" the="" benefits="" of="" dapagliflozin="" on="" morbidity="" and="" mortality="" in="" hfref="" did="" not="" differ="" by="" egfr="" category="" or="" by="" examining="" egfr="" as="" a="" continuous="" variable,="" with="" a="" significantly="" slower="" rate="" of="" decline="" in="" egfr,="" regardless="" of="" the="" presence="" of="" diabetes="" [46].="" in="" the="" dapa-ckd(dapagliflozin="" and="" prevention="" of="" adverse="" outcomes="" in="" chronic="" kidney="" disease)="" trial,="" properly="" designed="" for="" patients="" with="" ckd,="" dapagliflozin="" significantly="" reduced="" the="" decline="" in="" egfr,="" the="" end-stage="" kidney="" disease,="" or="" death="" from="" renal="" or="" cv="" causes="" [47](table="">


در عمل بالینی، همانطور که در چندین کارآزمایی نشان داده شد، شروع مهارکنندههای SGLT{0}}با کاهش خفیف اولیه تخممریخنورد در هفتههای اول همراه بود. این کاهش در eGFR برگشت پذیر بود، و عملکرد کلیه به تدریج به سطح اولیه خود بازگشت، با تثبیت عملکرد کلیه در طول پیگیری. کاهش خفیف اولیه در eGFR نباید منجر به قطع زودرس درمان با مهارکنندههای SGLT{2}} شود.
اخیراً درمان های جدیدی در HFrEF پیشنهاد شده است. مطالعه جهانی vericiguat در افراد مبتلا به نارسایی قلبی با کاهش کسر جهشی (VICTORIA) اثر وریسیگوات، یک محرک محلول گوانیلات سیکلاز، را در کاهش پیامد ترکیبی اولیه مرگ CV یا بستری در بیمارستان HF نشان داد. برای اولین بار در درمان های HF، این مطالعه شامل بیماران با eGFR بالاتر از 15 میلی لیتر در دقیقه / 1.73 متر مربع بود. اثرات سودمند vericiguat در کل محدوده eGFR، صرف نظر از WRF، ثابت بود [48].
استفاده از هیدرالازین و ایزوسورباید دینیترات (H-ISDN) در HFrEF به ندرت در عمل بالینی استفاده می شود. با این حال، درمان با H-ISDN در آخرین دستورالعملها برای بیماران HFrEF که نسبت به مهارکنندههای RAAS عدم تحمل دارند، و در بیماران آفریقایی-آمریکایی HFrEF که علیرغم درمان بهینه عصبی-هومورال علامتدار هستند، توصیه شد. درمان با H-ISDN در بیماران مبتلا به CKD ایمن است. با این حال، در یک کارآزمایی اخیر، H-ISDN در بالای درمان پزشکی استاندارد، ظرفیت ورزش را در بیماران مبتلا به سندرم قلب و عروق و HFrEF بهبود نداد [49]. این یافتهها با دادههای دنیای واقعی در مورد گروه بزرگی از بیماران HFpEF و HFmrEF که در ثبت نارسایی قلب سوئد ثبتنام کردهاند، مطابقت دارد، جایی که بیماران در زیرگروه با HF و CKD (eGFR 30-59 میلیلیتر در دقیقه/1.73) آنالیز میکنند. m² و eGFR<30 ml/min/1.73="" m²)benefitted="" from="" nitrate="">
