بخش دوم: درمان نارسایی قلبی در بیماران مبتلا به بیماری مزمن کلیوی: شک و تردید و تحولات جدید از آخرین دستورالعمل ESC
Jul 04, 2022
برای کسب اطلاعات بیشتر. تماسtina.xiang@wecistanche.com
4. آزمون های تشخیصی کلیه و مقایسه بین معیارهای مختلف
روش های متعدد و روش های تشخیصی برای ارزیابی پیشنهاد شده استعملکرد کلیهدر شرایط مزمن. تا کنون هیچ تعریف و طبقه بندی جهانی وجود ندارد و این امر به پیچیده کردن تعریف و شدت CKD کمک می کند.
اصلاح ساده شده رژیم غذایی دربیماری کلیویفرمول MDRD محدودیت های کمی را نشان داد، مانند استفاده از توده بدن و سن بیماران که رابطه نادرستی بین کراتینین سرم و تغییر پذیری توده عضلانی نشان می دهد. فرمول Cockcroft-Gault بدترین دقت را در اندازه گیری eGFR نشان داد؛ با این حال، آن را در بهبود کاهش خطر برای مرگ و میر در بیماران HF دقیق بود، شاید به دلیل گنجاندن وزن در فرمول آن (در MDRD گنجانده نشده است). اصلاح ساده شده رژیم غذایی در بیماری کلیویکلیه مزمنفرمول همکاری اپیدمیولوژی (CKD-EPI) بر اساس کراتینین سرم و سیستاتین C سرم، eGFR واقعی را در تمام بیماران HF، به ویژه در کسانی که عملکرد کلیوی حفظ شده یا متوسط مختل شده اند [52.53] دقیق تر تخمین زد. غلظت سیستاتین C کمتر تحت تاثیر سن قرار گرفت،جنسیت، توده عضلانی ، و یا رژیم غذایی نسبت به کراتینین. به طور مفصل، CKD-EPIcrea/cys و CKD-EPIys(CKD-EPI کراتینین و سیستاتین فرمول:177.6×(کراتینین سرم(mg dL))-0.. 65×(سرم سیستاتین C (میلی گرم L))-0.57×age-0.2)ارائه سوگیری کمتر و برآورد دقیق تر از eGFR نسبت به CKD-EPlcrea [54]. به تازگی معادله جدید کنسرسیوم عملکرد کلیه اروپا دقت و دقت بهبود یافته ای را با سوگیری مربوط به سن پایین تر در مقایسه با معادلاتی که معمولاً برای تخمین GFR از سطوح کراتینین سرم (SCr) استفاده می شود، نشان داد.

اینجا را کلیک کنید برای کسب اطلاعات در مورد مزایای عصاره سیستانچه توبولوسا
محدودیت eGFR و کراتینین در ارزیابی عملکرد کلیه باید منجر به اضافه شدن چندین نشانگر و امتحانات آزمایشگاهی، به منظور نظارت عمیق بر عملکرد کلیه شود. نیتروژن اوره خون معمولاً در ارتباط با عملکرد کلیوی مورد ارزیابی قرار گرفت و تصفیه گلومرولار، جذب مجدد لوله ای و فعال سازی نوروهورمونال را منعکس کرد. تفاوت اصلی بین sCr و BUN جذب مجدد BUN در سطح لوله ای بود. اخیراً نسبت BUN به کراتینین توانست بیماری های کلیوی پیش کلیوی و ذاتی را از هم متفاوت کند؛ به طور خاص، فعال سازی نوروهورمونال منجر به جذب مجدد نامتناسب BUN در مقایسه با کراتینین شد. هر دو BUN و نسبت BUN به کراتینین بیماران HF را با افزایش خطر پیامدهای نامطلوب شناسایی کردند. همچنین نسبت BUN ادرار به کراتینین کارایی مدر و تفاوت معنی داری در بستری مجدد HF و میزان مرگ و میر در 180 روز [56] پیش بینی کرد. آلبومینوری عمدتاً نشانگر افزایش ترامر پذیری گلومرولار و شکست جذب لوله ای بود و حدود ۲۰ تا ۳۰٪ از بیماران مبتلا به HF، به ویژه بیماران مبتلا به CKD مرتبط را تحت تأثیر قرار داد. آلبومینوری نشانگر اختلال عملکرد آندوتلیال، التهاب، آسیب پودوسیت، جذب مجدد لوله ای مختل، و ازدحام بود و اطلاعات اضافی در مورد مکانیسم اختلال کلیوی در بالای نسبت eGFR یا BUN به کراتینین [57l. میکرو و ماکرو آلبومینوری با افزایش مرگ و میر در جمعیت HF، به طور مستقل از eGFR همراه بود، در نتیجه برجسته کردن این مفهوم است که آلبومینوری خود می تواند پیشرفت اختلال عملکرد کلیوی از طریق اختلال در سلول های بازیابی در فضای بومن و اضافه بار مزمن و آسیب به سیستم حمل و نقل مکعب مگالین در توبول پروگزیمال شتاب.
آسیب توبولواینتراستیتال در HF، همانطور که با افزایش غلظت لیپوکالین مرتبط با نوتروفیل ادراری ژلاتیناز (NGAL) اندازه گیری می شود، ممکن است نشان دهنده آسیب کلیوی، حتی در حضور تصفیه گلومرولار طبیعی باشد. Poniatowski و همکاران به رسمیت شناخته شده سرم و ادرار NGALas به عنوان نشانگرهای حساس اولیه اختلال عملکرد کلیه در بیماران مبتلا به HF مزمن و کراتینین سرم طبیعی اما کاهش eGFR [58]. به طور مفصل، گسترش آسیب لوله ای مربوط به افزایش غلظت ادراری سه نشانگر ادراری آسیب لوله ای بود: NGAL، N-استیل بتا-D-گلوکوسامینیداز(NAG)، وآسیب کلیهمولکول ۱ (KIM-1). افزایش این نشانگرهای لوله ای مربوط به نتیجه ضعیف تری در بیماران HF بود، حتی زمانی که eGFR طبیعی بود.
اخیرا, سدیم ادراری ارزیابی شده در نمونه های ادراری نقطه—نشان داد داده های جالب در هر دو بیماران حاد و مزمن HF; اندازه گیری ناتریورسیس در اوایل پس از بستری شدن در بیمارستان می تواند به طور قابل اعتمادی بیماران مبتلا به پاسخ دیورتیک ضعیف در طول بستری شدن در بیمارستان را شناسایی کند، که ممکن است نیاز به تنظیم استراتژی های دیورتیک خود داشته باشند [59]. در یک مطالعه تک مرکزه از سرپاتیون های HF، یک هفته قبل از بستری شدن در بیمارستان برای HF، افت غلظت سدیم لکه ادراری یافت شد. ارزیابی سرپایی سدیم ادراری نقطه بنابراین ممکن است یک نشانگر به آسانی قابل اجرا برای هدایت یا شروع درمان و جلوگیری از بستری شدن در بیمارستان برای AHF [60]. اتیولوژی هیپوکلرامی در بیماران مبتلا به HF نه تنها مربوط به مدر مورد استفاده بود بلکه با فعال شدن RAAS و اثر تحریکی بر کینازهای بدون lysine نیز همراه بود که ممکن است فعالیت هم حمل کننده سدیم-کلرید کلیوی را افزایش دهد [61]. یک تجزیه و تحلیل فرعی از ارزیابی بتا مسدود کننده از بقا (BEST) کارآزمایی نشان داد که هر دو هیپوکلمی ادراری و هیپوناترمی مربوط به پیش آگهی ضعیف در بیماران HF، نشان می دهد استفاده معمول از نمونه های ادراری نقطه ای برای نظارت بر پاسخ کلیوی و تنظیم درمان HF [62].

5. استراتژی بالقوه برای استفاده صحیح از درمان های مهار عصبی هورمونی با توجه به شدت اختلال عملکرد کلیه
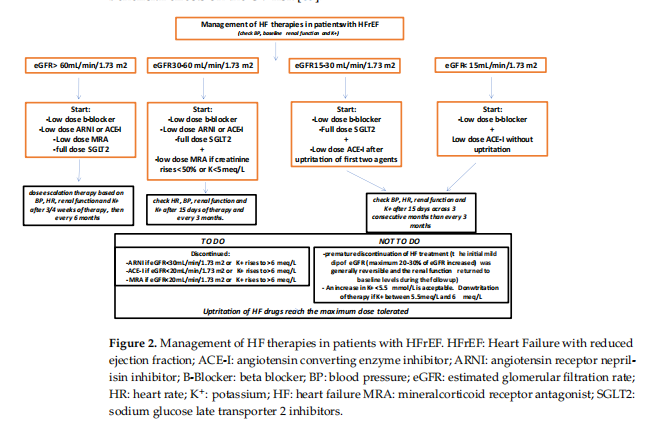
از لحاظ تاریخی، CKD نشان دهنده یک "کابوس" واقعی در هنگام خیاطی و بهینه سازی درمان HF است. اگر چه آخرین دستورالعمل ESC استفاده همسو از چهار عامل پس از تشخیص HF را توصیه کرد، اما استراتژی درمان بالقوه در سراسر CKDspectrum روشن نشد. بر اساس تجزیه و تحلیل یک کارآزمایی بزرگتر ارزیابی خصومت سمپاتتیک و درمان با مهارکننده های RAAS، استفاده از درمان بازدارنده عصبی-هورمونی رایج در CKD خفیف تا متوسط توصیه شد، حتی اگر برخی مطالعات به نظر می رسید نقش حفاظتی مسدودکننده های B را در بیماران مبتلا به اختلال عملکرد شدیدتر کلیوی پیشنهاد می کنند. دستورالعمل های جدید ESC درمان چهارگانه را در بیماران مبتلا به eGFR>60 میلی L/min/1.73 m² توصیه کرد. مهارکننده های SGLT-2 علاوه بر ACE-I/ARNI، بتا بلاکر و MRA برای همه بیماران مبتلا به HFrEF توصیه شد. این رویکرد ترکیبی ممکن است به طور ناگهانی فیزیولوژی کلیوی را تغییر دهد که می تواند منجر به خطر بالاتر کاهش پیشرونده eGFR، حتی در بیمارانی که عملکرد کلیوی طبیعی دارند، شود. در آن دسته از بیماران، نظارت دقیق بر عملکرد کلیه و الکترولیت ها باید ۳ یا ۴ هفته پس از شروع درمان انجام شود، تا از زوال ناگهانی eGFR و افزایش پتاسیم (K) جلوگیری شود. در بیماران مبتلا به eGFR 30-60 میلیL/min/1.73 m²، درمان سه گانه با دوز پایین B-blocker، RAASinhibitors، یا ARNI و دوز کامل SGLT-2inhibitors باید تجویز شود. در طول پیگیری، ما می توانیم MRAs با دوز پایین اضافه کنید اگر سطح کراتینین پایدار باقی می ماند—و یا افزایش کمتر از 30٪—و اگر K است<5 meq/l.="" more="" attention="" should="" be="" paid="" to="" patients="" with="" egfr="" 15-30="" ml/min/1.73="" m-,="" where="" we="" suggest="" starting="" with="" low-dose="" b-blockers="" and="" sglt-2="" inhibitors,="" adding="" raas="" inhibitors="" after="" the="" up-titration="" of="" the="" first="" two="" agents="" only="" if="" creatinine="" increases="" by=""><30% or="" k+=""><5 mmol/l.="" in="" patients="" with="" severe="" renal="" dysfunction,="" the="" multi-drug="" approach="" may="" become="" deleterious.="" the="" administration="" of="" lower="" dosages="" of="" b-blocker="" with="" the="" subsequent="" addition="" of="" ace-i="" without="" up-titration="" may="" be="">
به طور کلی در بیماران مبتلا به اختلال عملکرد کلیه، بررسی عملکرد کلیه و Kt را پس از 15 روز شروع درمان و سپس هر 2 تا 3 ماه یک بار به منظور رسیدن به حداکثر دوز تحمل شده توصیه می کنیم. اگر کراتینین سرم افزایش می یابد>50٪یا بالاتر از 3.5mg/dL. درمان باید قطع شود. هیپرکلمی شایع ترین عامل قطع دارو بود؛ کاهش تیتراسیون داروهای HF توصیه شد اگر K بین 5.5 meq/L و 6 meq/L بود، و قطع موقت توصیه شد اگر پتاسیم بالاتر از 6 meg/L (شکل 2) بود. در هنگام تنظیم برای قطع ACE-I/ARB، هیپرکلمی دیگر با مرگ و میر همراه نبود و پیشنهاد می کرد که ممکن است یک نشانگر خطر برای قطع ACE-I/ARB باشد تا یک عامل خطر برای پیامدهای بدتر. در بیماران مبتلا به عملکرد طبیعی کلیه و افزایش K جدا شده، بایندر K رمان مانند پاسیرومر و سدیم زیرکونیوم سیکلوزیلیکات به طور قابل ملاحظه ای کاهش سطح Kf سرم در دراز مدت، اجازه می دهد تا تیتراسیون و نگهداری از مهارکننده های RAASinhibitors و درمان ARNI. بنابراین، هر دو عامل با خیال راحت در بیماران مبتلا به HF مزمن به عنوان ارائه اثرات مفید بر خطر CV آزمایش شده است.
بنابراین، ترکیب داروهای نجات غریق HF فعلی به طور قابل توجهی نقاط پایانی سخت در جمعیت HF را بهبود بخشید؛ بنابراین، هدف استفاده از یک تیتراسیون پی در پی از عوامل تنها در حالی که چک کردن عملکرد کلیه، الکترولیت ها، و فشار خون، در نتیجه اجتناب از خطرات ناشی از عوارض جانبی درمان بود.

6. نتیجه گیری
CKD در HF با پیش آگهی بدتر در سراسر کل طیف eGFR همراه است. درمان چهارگانه HF که به تازگی پیشنهاد شده است، مرگ و میر و بستری شدن HF را نیز در بیماران مبتلا به HF و CKD به طور قابل توجهی کاهش می دهد. با وجود اثرات مطلوب این داروهای HF، مطالعات خاص بررسی تاثیر درمان با eGFR پایین تر از 30 میلی L/min/m² کمیاب باقی می ماند، و ایمنی آنها باید در طول یک دوره مشاهده ای طولانی تایید شود. برعکس، اساطاط کاذب تجویز دوز هدف ناکافی یا برداشت درمان های HF برای جلوگیری از بیماری کلیوی مرحله پایانی منجر به استفاده کمتر از این درمان های نجات غریق، با تاثیر قابل توجهی بر پیش آگهی HF شد. کاربرد گسترده عوامل متعدد HF نیاز به احتیاط و نظارت مکرر از الگوهای آزمایشگاهی خاص، با توجه خاص در طول مرحله تیتراسیون و عود HF.

