گیاهان تایلندی با سطوح آنتی اکسیدانی بالا، فعالیت پاکسازی رادیکال آزاد، فعالیت ضد تیروزیناز و آنتی کلاژناز
Mar 19, 2022
مخاطب:
مخاطب:joanna.jia@wecistanche.com/ واتساپ: 008618081934791
Moragot Chatatikun1 و Anchalee Chiabchalard2
خلاصه
زمینه:اشعه ماوراء بنفش نور خورشید باعث تولید بیش از حد گونه های فعال اکسیژن (ROS) می شود که منجر به پیری پوست و اختلالات هیپرپیگمانتاسیون می شود. ترکیبات جدید سفید کننده و ضد چروک حاصل از محصولات طبیعی اخیراً مورد توجه قرار گرفته است. هدف از این مطالعه یافتن محصولاتی بود که ROS را در 14 عصاره گیاهی تایلندی کاهش میدهند.
مواد و روش ها:برای تعیین فنول کل وفلاونوئیدمحتوا،آنتی اکسیدانفعالیت،ضدتیروزینازفعالیت، و فعالیت ضد کلاژناز، ما عصاره های 14 گیاه تایلندی تهیه شده با استفاده از حلال های مختلف (پترول اتر، دی کلرومتان و اتانول) را مقایسه کردیم.آنتی اکسیدانفعالیت ها با سنجش DPPH و ABTS تعیین شد.
نتایج:محتوای فنلی کل 14 عصاره گیاه تایلندی به ترتیب در اتانول و سپس عصاره دی کلرومتان و نفت اتر در بالاترین سطح یافت شد.فلاونوئیدمحتوای آن به طور معمول در بخش دی کلرومتان یافت شد. فعالیت مهاری در محدوده 7 تا 99 درصد مهار با سنجش DPPH و ABTS بود. عصاره اتانولی برگ Ardisia elliptica Thunb. بالاترین محتوای فنلی، فعالیت آنتی اکسیدانی و مهار کلاژناز را داشت، در حالی که Cassia alata (L.) Roxb. عصاره غنی ترین بودفلاونوئیدمحتوا. جالب توجه است که سه عصاره گیاهی، که فراکسیونهای اتانولی Annona squamosa L.، Ardisia elliptica Thunb بودند. و سنا آلاتا (L.) Roxb. بالا داشتآنتی اکسیدانمحتوا و فعالیت و به طور قابل توجهی هر دو را مهار کردتیروزینازو کلاژناز
نتیجه:یافتههای ما نشان میدهد که بخشهای اتانولی Annona squamosa L.، Ardisia elliptica Thunb. و سنا آلاتا (L.) Roxb. به عنوان مواد تشکیل دهنده بالقوه برای محصولات آرایشی مانند عوامل ضد چروک و محصولات سفید کننده پوست امیدوار کننده است.
کلید واژه ها:Ardisia elliptica Thunb.،آنتی اکسیدانمحتوا، فعالیت پاکسازی،ضد تیروزینازفعالیت، فعالیت ضد کلاژناز

فلاونوئید یکی از عناصر استسیستانچ
زمینه
اشعه ماوراء بنفش (UVR) از نور خورشید مهم ترین عامل خطر برای سرطان های غیر ملانوم و ملانوما پوست است [1]. قرار گرفتن بیش از حد در معرض نور خورشید، به ویژه UVA و UVB، باعث بیان بیش از حد گونه های فعال اکسیژن (ROS) می شود که به لیپیدها، پروتئین ها و اسیدهای دئوکسی ریبونوکلئیک آسیب می رساند. کلاژن پایه اصلی ماتریکس خارج سلولی در لایه درم پوست است. ROS بیش از حد بیان کلاژناز را افزایش می دهد، پروتئازی که کلاژن را تجزیه می کند که می تواند منجر به پیری و چروک شدن پوست شود [2]. علاوه بر این، قرار گرفتن در معرض اشعه ماوراء بنفش باعث تولید ملانین می شود و در نتیجه هیپرپیگمانتاسیون ایجاد می شود.تیروزینازآنزیم کلیدی شروع کننده رنگدانه پوست است. در مرحله اول، L-تیروزین به شکل 3،{2}}دی هیدروکسی فنیل آلانین (L-DOPA) توسط تیروزیناز هیدروکسیله می شود. متعاقباً، L-DOPA توسط تیروزیناز به DOPA کینون اکسید می شود. کینون DOPA بیشتر به DOPAchrome تبدیل میشود که میتواند به اسید کربوکسیلیک 5،6-دی هیدروکسیاندول (DHI) یا 5،6-دی هیدروکسیاندول-2- (DHICA)[3] تبدیل شود. درمان های فعلی برای پیری پوست شامل هیدروکسیل اسید برای لایه برداری لایه اپیدرمی، رتینوئیدها برای کاهش پوست زبر و پرکننده پوست با تزریق کلاژن به پوست است. با این حال، این درمان ها دارای اثرات نامطلوبی مانند هایپرپیگمانتاسیون، التهاب، سمیت سلولی، تحریک و عفونت باکتریایی هستند [4]. محبوب ترین عامل سفید کننده پوست هیدروکینون است که مهار می کندتیروزینازاما عوارض جانبی آن شامل درماتیت، ادم، واکنش های آلرژیک و اکرونوز است [5]. اخیراً، محققان بر روی محصولات طبیعی متمرکز شدهاند که ROS ناشی از اشعه ماوراء بنفش، سرکوب آنزیمها، و کاهش تشکیل ملانین را بهعنوان جایگزین درمانهای فعلی کاهش میدهند. به عنوان مثال، ترکیبات گیاهی فعال، مانند آربوتین، آلوئزین، اسید جنتیزیک،فلاونوئیدهاهسپریدین، شیرین بیان، نیاسینامید، مشتقات مخمر و پلی فنل ها، ملانوژنز را بدون سمیت سلولی توملانوسیت ها مهار می کنند [6]. بنابراین، گیاهان ممکن است تشکیل چین و چروک و هایپرپیگمانتاسیون ناشی از قرار گرفتن در معرض نور خورشید را کاهش دهند.
هدف از این مطالعه تجزیه و تحلیل 14 گیاه تایلندی استخراج شده با سه حلال مختلف از نظر پتانسیل ترکیبات ضد چروک و سفید کننده پوست آنها بود. سپس تعدادآنتی اکسیدانفنل ها وفلاونوئیدهابرای ارتباط با فعالیت های مهار رادیکال های آزاد و ضد کلاژناز وضد تیروزینازفعالیت ها. عصاره داشتآنتی اکسیدان هاکه رادیکال های آزاد را از بین می برد و آنزیم های دخیل در تشکیل چین و چروک و رنگدانه را مهار می کند. ما Ardisia elliptica Thunb.، Annona squamosa L.، و Senna alata (L.) Roxb را یک نامزد بسیار امیدوارکننده برای استفاده در محصولات آرایشی و بهداشتی شناسایی کردیم.

بدنسازی سیستانچ
مواد و روش ها
مواد شیمیایی و معرف ها
معرف فنل Folin Ciocalteu، کربنات سدیم (Na2CO3)، اسید گالیک، کورستین، کلرید آلومینیوم 10 درصد، اتانول، 2، 2-دی فنیل-1-پیکریل هیدرازیل (DPPH)، اسید اسکوربیک، 2،2'-Azino- بیس ({10}}اتیل بنزتیازولین-6-سولفونیک اسید) (ABTS)، پرسولفات پتاسیم، اسید کوجیک، تیروزیناز قارچ (EC 1.14.18.1)، 3،4-دی هیدروکسی-L- فنیل آلانین (L- DOPA)، N-[3-(2-فوریل) آکریلول]-Leu-Gly-Pro-Ala (FALGPA)، کلاژناز از کلستریدیوم هیستولیتیکوم (EC3.4.24.3)، اپی گالوکاتچین گالات (EGCG) کلرید سدیم، کلرید کلسیم و دی متیل سولفوکساید (DMSO) از شرکت شیمیایی سیگما آلدریچ (سنت لوئیس، MO، ایالات متحده آمریکا) خریداری شد. نفت اتر، دی کلرومتان، اتانول مطلق، متانول، دی سدیم هیدروژن فسفات و سدیم دی هیدروژن فسفات از Merck (دارمشتات، آلمان) خریداری شد. تمام مواد شیمیایی و معرف ها دارای درجه تجزیه و تحلیل بودند.
مواد گیاهی و استخراج
سیزده گونه از برگ های تایلندی از باغ گیاهی HRH Princess Sirindhorn، استان رایونگ، تایلند جمع آوری شد. منگوستین از استان چانتابوری تایلند به دست آمد. این گیاهان احراز هویت شدند و در هرباریوم، دپارتمان گیاه شناسی، دانشکده علوم، دانشگاه چولالانگکورن، تایلند قرار گرفتند. اسامی علمی، شماره کوپن و قطعات گیاه در جدول 1 نشان داده شده است. گیاهان با استفاده از دستگاه سوکسله استخراج شدند. به طور خلاصه، 10 گرم از گیاه خشک شده به طور جداگانه با پترولیومتر، دی کلرومتان و اتانول استخراج شد. حلال ها با استفاده از یک اواپراتور چرخشی خلاء تحت فشار کاهش یافته با استفاده از متمرکز کننده MiVac Quattro حذف شدند. نمونههای غلیظ در DMSO با غلظت 100 میلیگرم بر میلیلیتر حل و تا زمان استفاده در دمای {3}} درجه نگهداری شدند. بازده عصاره خشک در جدول 1 به صورت درصد وزنی بر وزن مواد گیاهی خشک ارائه شده است.
تعیین محتوای فنلی کل
محتوای فنلی کل عصاره های گیاهی با استفاده از روش Folin-Ciocalteu [7] ارزیابی شد. به طور خلاصه، 5{8} میکرولیتر عصاره با غلظت 1 میلیگرم در میلیلیتر در آب مقطر با 50 میکرولیتر معرف فولین-سیوکالتیو 10 درصد و 50 میکرولیتر Na2CO3 0.1 مولار مخلوط شد. مخلوط واکنش به مدت 1 ساعت در دمای اتاق در تاریکی انکوبه شد. جذب در 750 نانومتر با دستگاه میکروپلیت ریدر (Biotek، ایالات متحده آمریکا) اندازه گیری شد. اسید گالیک از 1.56 تا 100 میکروگرم بر میلی لیتر به عنوان استاندارد استفاده شد. محتوای فنلی کل عصاره ها به صورت میلی گرم معادل اسید گالیک (GAE) در هر گرم ماده گیاه خشک بیان می شود. تمام نمونه ها در سه تکرار آنالیز شدند.

تعیین محتوای فلاونوئید
جمعفلاونوئیدمحتوای (TFC) با استفاده از روش رنگ سنجی کلرید آلومینیوم (AlCl3) تعیین شد [7]. به طور خلاصه 50 میکرولیتر از عصاره ها با غلظت 1 میلی گرم بر میلی لیتر در اتانول 80 درصد با 50 میکرولیتر از محلول AlCl3 2 درصد در چاهک دیواره 96 مخلوط شد. پلیت به مدت 15 دقیقه در دمای اتاق انکوبه شد. جذب در 435 نانومتر با استفاده از دستگاه میکروپلیت ریدر اندازه گیری شد. کوئرستین از 1.56 تا 100 ug/ml به عنوان استاندارد استفاده می شود. محتوای فلاونوئید کل به صورت میلی گرم معادل کوئرستین (QE) در هر گرم ماده گیاه خشک بیان می شود. نمونه ها در سه تکرار مورد تجزیه و تحلیل قرار گرفتند.
فعالیت پاکسازی DPPH
سنجش فعالیت مهار DPPH همانطور که توسط Yamasaki و همکارانش توصیف شد انجام شد. [8]. محلول DPPH برای هر سنجش تازه تهیه شد. به طور خلاصه، 100 ug/ml عصاره یا 1.56 تا 100 ug/ml اسید اسکوربیک استاندارد در متانول مطلق با 180 ul معرف DPPH در یک بشقاب چاهک 96 مخلوط شد. مخلوط حاصل به مدت 30 دقیقه در دمای اتاق در تاریکی انکوبه شد. سپس، جذب در 517 نانومتر با دستگاه میکروپلیت خوان اندازه گیری شد. آزمایش ها در سه تکرار انجام شد. جذب در 517 نانومتر DPPH 02/0 ± 70/0 بود و میزان جذب را کاهش داد. توانایی مهار به عنوان فعالیت مهارکننده (درصد )=100 درصد × [(훥A517 ofcontrol - 훥A517 از نمونه)/ 훥A517 از کنترل] محاسبه شد. درصد فعالیت مهار DPPH عصاره ها با اسید اسکوربیک مقایسه شد و به عنوان معادل میلی گرم ویتامین C بیان شد.آنتی اکسیدانظرفیت (VCEAC) در هر ماده گیاهی گرما. IC5{1}} از نمودار درصد مهار غلظت (از 0.78-100 ug/ml از هر عصاره) تعیین شد.
فعالیت پاکسازی ABTS
فعالیت مهار رادیکال آزاد ABTS همانطور که قبلاً توضیح داده شد [9] انجام شد. معرف ABTS• plus با مخلوط کردن 7 میلی مولار ABTS• و 2.45 میلی مولار پرسولفات پتاسیم در نسبت حجم/حجم 8:12 تهیه شد. محلول کار به مدت 16 تا 18 ساعت در دمای اتاق در تاریکی نگهداری شد. محلول ABTS• پلاس با اتانول مطلق رقیق شد تا جذبی در 734 نانومتر 0.02 ± 7.7{0 بدهد. سپس، 100 میکروگرم بر میلیلیتر عصاره یا 1.56 تا 100 میکروگرم بر میلیلیتر اسید اسکوربیک استاندارد در اتانول مطلق به 180 میکروگرم ABTS بعلاوه معرف کار در چاهکهای یک صفحه 96 چاهی اضافه شد. صفحه به مدت 45 دقیقه در دمای اتاق انکوبه شد و جذب در طول موج 734 نانومتر اندازهگیری شد. آزمایش ها در سه تکرار انجام شد. قابلیت مهار به عنوان فعالیت مهار (درصد)=100 × [(훥A734 از شاهد - 훥A734 از نمونه)/ 훥A734 از کنترل] محاسبه شد. درصد فعالیت مهاری ABTS عصاره ها با اسید اسکوربیک مقایسه شد و معادل ویتامین C ارائه شد.آنتی اکسیدانظرفیت (VCEAC) در گرم ماده خشک گیاهی. IC50 از نمودار درصد مهار در برابر غلظت (از 15.62-1000 ug/ml از هر عصاره) تعیین شد.
تعیین مهار تیروزیناز قارچ
روش دوپاکروم با اندکی اصلاح [10] انجام شد. به طور خلاصه، 20 میکرولیتر عصاره گیاهی یا DMSO (به عنوان شاهد)، 20 میکرولیتر از 203.3 واحد در میلی لیتر تیروزیناز قارچ و 140 میکرولیتر بافر فسفات 20 میلی مولار در pH 6.8 به مدت 10 دقیقه در دمای 25 درجه پیش انکوبه شدند. پس از انکوباسیون، 20 ul از 2.5 میلی مولار L-DOPA اضافه شد و نمونه ها به مدت 20 دقیقه دیگر در دمای 25 درجه انکوبه شدند. مقدار دوپاکروم در طول موج 492 نانومتر با دستگاه میکروپلیت خوان اندازه گیری شد. اسید کوجیک (KA) به عنوان یک کنترل مثبت برای مهار عمل کرد. درصد مهار فعالیت تیروزیناز (درصد) اکسپرس درصد بودتیروزینازبازداری {{0}} × [(훥A492 کنترل – 훥A492 نمونه)/ 훥A492 از کنترل]. غلظت نهایی عصاره ها و اسید کوجیک به ترتیب 1 و 0.1 میلی گرم در میلی لیتر بود. IC50 از گراف درصد تعیین شدتیروزینازمهار غلظت (از 15.62-1000 ug/ml از هر عصاره).

بدنسازی سیستانچ
تعیین مهار کلاژناز
مهار کلاژناز با روشی که قبلاً توصیف شده بود [11] تعیین شد. به طور خلاصه، 40 ul کلاژناز از کلستریدیوم هیستولیتیکوم با مقدار 0.25 واحد در میلیلیتر در بافر 50 میلیمولار Tricine حاوی 10 میلیمولار CaCl2 و 400 میلیمولار NaCl، و 10 میکرومولار بافر 50 میلیمولار Tricine با 10 مخلوط شد. از عصاره ها یا DMSO (به عنوان شاهد). اپی گالوکاتچین گالات (EGCG) به عنوان کنترل مثبت استفاده شد. پس از 15-دقیقه انکوباسیون در دمای اتاق، 50 ul N-[3-(2-فوریل)اکریلویل]-Leu-Gly-Pro-Ala (FALGPA) اضافه شد. جذب بلافاصله و به طور مداوم به مدت 20 دقیقه در 340 نانومتر اندازه گیری شد. فعالیت آنزیم با کاهش جذب در طول بازه زمانی ارزیابی شد. درصد مهار فعالیت کلاژناز 100 × [(فعالیت کنترل – فعالیت نمونه) / فعالیت کنترل] محاسبه شد. غلظت نهایی عصاره ها و اپی گالوکاتچین گالات به ترتیب 1 و 0.1 میلی گرم در میلی لیتر بود. IC50 از نمودار درصد مهار کلاژناز در برابر غلظت (از 15.62-1000 ug/ml از هر عصاره) تعیین شد.
تجزیه و تحلیل های آماری
تمام آزمایش ها در سه تکرار انجام شد و نتایج به صورت میانگین ± خطای استاندارد بیان شد. ضریب همبستگی (R2) بینآنتی اکسیدانمحتویات و فعالیت آنتی اکسیدانی با استفاده از نرم افزار SigmaPlotversion 12.2 تعیین شد. تفاوت بین این دو میانگین با استفاده از آزمون t-test مورد ارزیابی قرار گرفت. زمانی که P-value کمتر از 0.05 بود، تفاوت ها معنی دار در نظر گرفته شد.
نتایج
استخراج بازده
جدول 1 اسامی علمی، شماره کوپن و قسمت های گیاهی 14 گیاه تایلندی مورد استفاده در این مطالعه را نشان می دهد. درصد بازده عصاره ها از 73/0/2 {{2} درصد تا 11/31 درصد وزنی متغیر بود (جدول 1). Ardisia elliptica Thunb. بیشترین بازده را در عصاره نفتی اتر (89/19 درصد) آنداتانولی (11/31 درصد) و Garcinia mangostanaL داشت. بیشترین درصد عملکرد را از استخراج دی کلرومتان (07/11 درصد) داشت.
محتوای فنلی ۱۴ گیاه تایلندی
بنابراین، محتوای فنلی کل در گیاهان با روش فولین-سیوکالتئو تعیین شد. همانطور که در جدول 2 نشان داده شده است، عصاره ها دارای محدوده وسیعی از نظر تعداد فنل ها بودند و مقادیر بین عصاره ها به میزان 33-برابر متغیر بود. Ardisiaelliptica Thunb. در هر سه نوع عصاره دارای بیشترین میزان فنل بود، در حالی که کمترین محتوای فنلی در قلاب Stemona curtissi وجود داشت. f. عصاره اتر نفتی
محتوای فلاونوئید 14 گیاه تایلندی
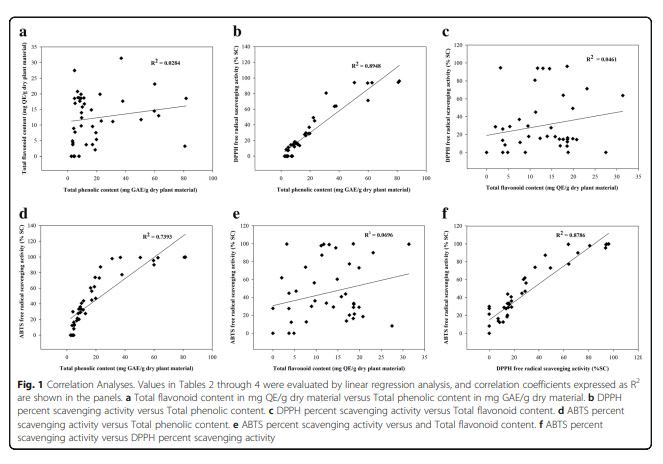
مشابه فنل ها، کلفلاونوئیدمحتوا به طور قابل ملاحظه ای در بین گونه های گیاهی متفاوت بود، از 2.04 ± 0.16 تا 31.38 ± 0.81 میلی گرم QE در هر گرم ماده خشک (جدول 2). به طور کلی، استخراج دی کلرومتان بیشترین بازده را داشتفلاونوئیدسطح در مقایسه با حلال های دیگر. از بین همه عصارهها، بالاترین مقدار فلاونوئید در عصاره اتانولی از برگ سنا آلاتا (L.) Roxb (31.38 ± 0.81 mg QE perg ماده خشک) یافت شد. از سوی دیگر، Ardisia elliptica Thunb. (23.14 ± 1.10 میلی گرم QE در هر گرم ماده خشک). دارای غنی ترین فلاونوئید در بخش دی کلرومتان بود. علاوه بر این، Ipomoea pes-caprae (L.) R.br. بالاترین محتوای فلاونوئید را در بین عصارههای نفتی اتر (27.48 ± 2.59 میلیگرم QE در هر گرم ماده خشک) داشت. کمترین سطح فلاونوئید قابل تشخیص در عصاره اتانولی Daturametel L بود.فلاونوئیدهادر عصارههای نفتی اتر و دی کلرومتان از Stemona curtisii Hook.f. و عصارههای نفتی اتر از Streblus asper Lour یافت نشد. و Phyllanthus acidus (L.) Skeels. محتوای کل فلاونوئیدها با محتوای فنلی کل همبستگی نداشت (R{0}}.0284، شکل 1a).
فعالیت مهار رادیکال DPPH در عصاره های مختلف از 14 گیاه تایلندی
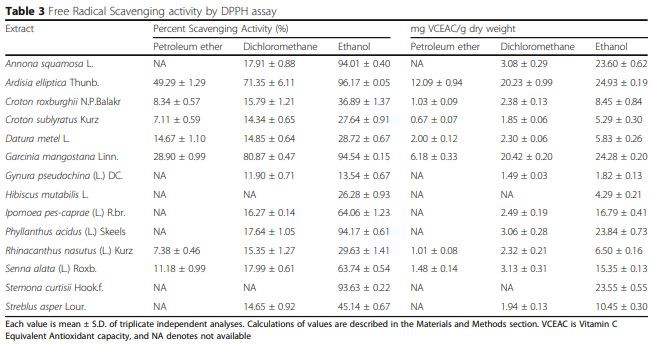
فعالیت مهار رادیکال های آزاد با استفاده از DPPH به عنوان یک شاخص اساسی استآنتی اکسیدانسنجش [12]. همانطور که در جدول 3 نشان داده شده است، فعالیت های پاکسازی عصاره ها بسیار متفاوت بوده و از 7.11 ± 0.59 درصد تا 96.17 ± 0.05 درصد متغیر است. عصاره اتانولی Ardisia ellipticaThunb با 96 درصد بیشترین فعالیت مهاری را داشت. علاوه بر این، قوی ترین بعدی استآنتی اکسیدان activities (>90 درصد) در فراکسیون های اتانولی از Stemonacurtisii Hook.f.، Annona squamosa L.، Phyllanthus acidus (L.) Skeels مشاهده شد. و Garcinia mangostana Linn. از نظر حلالهای دیگر، Ardisia elliptica Thunb نیز غنیترین فعالیت کاوشکننده را در میان فراکسیونهای نفتی اتر داشت و Garcinia mangostana L. بالاترین فعالیت آنتیاکسیدانی را در فراکسیونهای دی کلرومتان داشت. کمترین توانایی حذف در Croton sublyratus Kurz در بخش نفتی اتر مشاهده شد. هیچ فعالیت مهاری در 7 عصاره نفتی اتر و 2 عصاره دی کلرومتان شناسایی نشد.

فعالیت مهار رادیکال ABTS در عصاره های مختلف از 14 گیاه تایلندی
آنتی اکسیدانفعالیت فازهای آبی و لیپیدی در گیاهان نیز با سنجش رنگ زدایی ABTS ارزیابی شده است [13]. مجدداً، اسید اسکوربیک به عنوان استاندارد عمل کردآنتی اکسیدان. As with the DPPH assay, scavenging activity in the ABTS assay varied greatly among the plant preparations with a similarly broad range from 8.03 ± 0.54% to 99.84 ± 0.07% (Table 4). Furthermore, the next strongest scavenging activities (> 90%) were observed in the same 4 ethanol fractions as shown by the DPPH assay. In addition, no scavenging activity was found in the same 5 petroleum ether extracts. In general, the values obtained with the ABTS assay were higher than the DPPH values. Hence, activity in the ethanol extract from Senna alata (L.) Roxb. was now observed as >90 درصد، و فعالیت روبنده در تمام عصارههای دی کلرومتان و عصارههای نفتی اتری از Annona squamosa L. و Ipomoea pes-caprae(L.) R.br شناسایی شد. که توسط سنجش DPPH شناسایی نشد.
مهار فعالیت تیروزیناز توسط عصاره های گیاهی
توانایی ترکیبات گیاهان تایلندی در مهار قارچتیروزینازفعالیت با استفاده از یک روش آزمایشگاهی با L-DOPA به عنوان بستر مورد بررسی قرار گرفت. اسید کوجیک به عنوان یک مهار کننده شناخته شده استفاده می شود و باعث مهار حداکثر آنزیمی 1.63 ± 93.38 درصد می شود. همانطور که در جدول 5 نشان داده شده است، تنها عصاره های اتانولی به طور قابل توجهی فعالیت تیروزیناز را با Ardisia elliptica Thunb مهار کردند. آماده سازی استثنا هستند. فراکسیون های نفتی اتر و دی کلرومتان Ardisia elliptica Thunb. فعالیت تیروزیناز را تقریباً 20 درصد مهار کرد. فراکسیون اتانول از Rhinacanthus nasutus (L.) Kurz (مقدار IC50 271.50 ug/ml) قوی ترین مهارکننده تیروزیناز بود که به دنبال آن عصاره اتانولی از Ardisia ellipticaThunb قرار گرفت. و Phyllanthus acidus (L.) Skeels. سایر فراکسیون های اتانولی به طور قابل توجهی فعالیت آنزیمی را بیش از 20 درصد کاهش دادند (جدول 5)، در حالی که عصاره های باقی مانده فعالیت بازدارندگی قابل تشخیصی نداشتند (داده ها نشان داده نشده است).
مهار فعالیت کلاژناز توسط 14 گیاه
عصاره ها برای فعالیت ضد کلاژناز با استفاده از کلستریدیوم هیستولیتیکوم کلاژناز، و N-[3-(2-furyl)acryloyl]-Leu-Gly-Pro-Ala (FALGPA) به عنوان بستر مورد آزمایش قرار گرفتند. Epigallatecatechin gallate یک مهارکننده کلاژناز شناخته شده و فعالیت آنزیمی را به میزان 79/2 ± 51/90 درصد کاهش داد. همانطور که در جدول 5 نشان داده شده است، تنها 4 عصاره اتانولی دارای فعالیت مهاری کلاژناز قابل تشخیص بودند. از آنهایی که باعث مهار می شوند، Ardisia elliptica Thunb. (مقدار IC50 157.78 میکروگرم بر میلیلیتر) بالاترین سطح مهار کلاژناز را نشان داد و پس از آن Annona squamosa L. (مقدار IC50 426.67 میکروگرم بر میلیلیتر)، سنا آلاتا (L.) Roxb. و Croton sublyratusKurz در رتبهبندی قرار گرفتند. سفارش. سایر عصاره های گیاهی به طور قابل توجهی فعالیت کلاژناز را تحت شرایط واکنش مورد استفاده در این مطالعه مهار نکردند (داده ها نشان داده نشده است).
بحث
تشعشعات خورشیدی یک عامل محیطی مهم در آسیب پوست است و می تواند باعث ایجاد سرطان پوست شود [14]. اشعه ماوراء بنفش باعث پاسخ پیش التهابی، تخریب ماتریکس خارج سلولی وآنتی اکسیدانتخلیه [15، 16]. UV باعث تشکیل گونههای اکسیژن فعال (ROS) میشود که باعث افزایش رنگدانه و بیان کلاژناز میشود [17، 18]. مطالعه ما 14 گیاه تایلندی استخراجشده با سه حلال مختلف را برای پتانسیل آنها به عنوان مواد ضدچروک و سفیدکننده پوست مورد بررسی قرار داد. در این مطالعه از اتر نفتی، دی کلرومتان و اتانول برای استخراج گیاهان با استفاده از دستگاه سوکسله استفاده شد. Ardisia elliptica Thunb. بالاترین عملکرد را در عصاره نفتی اتر و اتانولی داشت، در حالی که Garcinia mangostana L. بالاترین درصد عملکرد را از استخراج دی کلرومتان داشت. این حلال ها مجموعه ای از حلال های آلی با افزایش قطبیت هستند. تنوع در درصد عملکرد به گونه گیاهی بستگی دارد و احتمالاً منعکس کننده تفاوت در ترکیب شیمیایی گیاهان است.


فنولیک ها بزرگترین گروه فیتوکمیکال های موجود در گیاهان هستند و فعالیت های بیولوژیکی مختلفی در حیوانات از جمله انسان دارند [19]. محتوای فنلی کل در گیاهان با روش Folin Ciocalteu تعیین شد. به طور کلی، بخش اتانول دارای غنیترین محتوای فنلی و به دنبال آن دی کلرومتان بود، در حالی که اتر نفتی با قطبیت پایین کمترین محتوای فنلی را در مقایسه با سایر حلالها داشت. در این مطالعه، Ardisia elliptica Thunb. بالاترین محتوای فنلی را در هر سه نوع عصاره داشت. در مطالعات قبلی، عصاره برگ دی کلرومتان Ardisia elliptica Thunb دارای محتوای فنلی 1{7}} 1 ± 1.3 میلی گرم GAE در گرم ماده گیاه خشک است که بیشتر از محتوای عصاره شاخه می باشد [20]. علاوه بر این، عصاره متانولی میوه آردیسیای رسیده حاوی 37/0 ± 64/5 گرم GAE در هر 100 گرم عصاره بود [21]. از این رو، برگ و میوه Ardisia ellipticaThunb. دارای محتوای فنلی بالا است که می توان آن را به راحتی با متانول، دی کلرومتان و اتانول استخراج کرد.
فلاونوئیدهارنگدانه هایی در گل ها، برگ ها، میوه ها و دانه ها هستند. این ترکیبات متابولیت های ثانویه گیاهان هستند و به طور گسترده در بین گونه های گیاهی توزیع می شوند [22]. سپس، محتوای فلاونوئید در گیاهان تایلندی با استفاده از روش رنگ سنجی کلرید آلومینیوم ارزیابی شد. نتایج ما نشان داد که بیشترین مقدار فلاونوئید در عصاره اتانولی از Senna alata (L.) Roxbleaves یافت شد. در مطالعه قبلی، محتوای بالای فلاونوئید در آب (25/4 میلیگرم QE در 100 گرم) و فراکسیون متانولی (97/3 میلیگرم QE در هر 100 گرم) سنا آلاتا (L.) Roxb یافت شد.[23]. بنابراین، آمادهسازی سنا آلاتا (L.) Roxb دارای محتوای فلاونوئید بالایی است که با حلالهایی با قطبیت بالا از جمله اتانول، متانول و آب استخراج شود. Ardisiaelliptica Thunb. غنی ترین محتوای فلاونوئید را در بخش دی کلرومتان داشت. میوه این گیاه همچنین دارای محتوای فلاونوئیدی 36.91 ± 2.37 میلی گرم QE در گرم عصاره است [24]. از این رو، میوه و برگ Ardisia elliptica Thunb. فلاونوئیدهای غنی هستند. محتوای فلاونوئید کل با محتوای فنلی کل ارتباطی نداشت. با این حال،فلاونوئیدهافعالیت های بیولوژیکی زیادی مانند محافظت در برابر اشعه UVB [25]، ضد التهاب [26]، ضد سمیت کبدی [27] و ضد سرطان [28] دارند.
فعالیت مهار رادیکال های آزاد با استفاده از DPPH و ABTSassay. در سنجش DPPH، DPPH یک هیدروژناتوم را از یکآنتی اکسیدان[29]. ما دریافتیم که عصاره اتانولی Ardisiaelliptica Thunb بالاترین فعالیت مهاری را داشت. سایر محققین همچنین بخش دی کلرومتان Ardisia elliptica Thunb را گزارش کرده اند. برگ ها و ساقه ها دارای سطوح بالایی ازآنتی اکسیدانفعالیت توسط سنجش DPPH تعیین میشود، و از این رو، این گیاه برای بررسی بیشتر به عنوان یک درمان گیاهی بسیار جالب است [20]. عصاره از بخش اتانول با قطبیت بالا به وضوح بهتر نشان دادآنتی اکسیدانفعالیت نسبت به فراکسیون های با قطبیت کمتر حاوی دی کلرومتان و اتر نفت. عصاره های اتانولی دارای بالاترین سطح فعالیت مهار رادیکال های آزاد در مقایسه با سایر عصاره ها بودند و تمام عصاره های اتانولی فعال بودند. در روش ABTS، ABTS با افزودن پرسولفات پتاسیم به رادیکال کاتاسیون آن تبدیل می شود. در حضور یک آنتی اکسیدان، کاتیون واکنش پذیر ABTS (یا ABTS• plus) به شکل طبیعی بی رنگ خود تبدیل می شود [9]. در توافق با روش DPPH، عصارههای اتانولی دارای بالاترین سطوح فعالیت روبنده در مقایسه با عصارههای دیگر بودند. باز هم، بالاترین فعالیتهای مهارکننده عصارههای اتانول، دی کلرومتان و اتر نفت از همان گیاهانی بودند که در روش سنجش DPPH نشان داده شد.
با این حال، کلفلاونوئیدمحتوای عصارههای گیاه با فعالیت پاککننده رادیکالهای آزاد که با سنجش DPPH (شکل 1c) یا با سنجش ABTS (شکل 1e) شناسایی شد، ارتباطی نداشت. یافته های ما هیچ رابطه معنی داری بینفلاونوئیدمحتوا و فعالیت روبنده با استفاده از روش ABTS با نتایج سایر محققین مطابقت دارد [30]. در مقابل، محتوای فنلی کل آمادهسازی گیاه به طور مثبتی با قابلیت جمعآوری اندازهگیری شده توسط هر دو سنجش (شکل 1b و d) همبستگی مثبت داشت که با مطالعه قبلی مطابقت نداشت [31]. به طور قابل توجهی، این فعالیت مهاری به محتوای فنلی کل و حلال هایی با قطبیت بالا، مانند اتانول و دی کلرومتان بستگی دارد. این نتایج نشان میدهد که محتوای فنلی جزء اصلی تشکیلدهنده آن استآنتی اکسیدانفعالیت در 14 گیاه تایلندی
ملانین، رنگدانه اصلی رنگ پوست و مو، توسط ملانوسیت های درون ملانوزوم سنتز می شود. تولید بیش از حد و تجمع ملانین در پوست ممکن است منجر به اختلالات پوستی و مشکلات زیبایی شود. هایپرپیگمانتاسیون در نواحی در معرض آفتاب پوست رخ می دهد [32]. در ملانوژنز،تیروزینازآنزیم کلیدی در مرحله محدود کننده سرعت است که در آن L-تیروزین به L-DOPA هیدروکسیله می شود که بیشتر به DOPAquinone اکسید می شود. پس از آن، به DOPAchrome تبدیل می شود که بستری برای سنتز ملانین است [3]. کاهش مقرراتتیروزینازفعالیت به عنوان مسئول کاهش تولید ملانین پیشنهاد شده است. توسعه ترکیبات فیتوشیمیایی سفیدکننده جدید از محصولات طبیعی اخیراً به یک روند رو به رشد تبدیل شده است. یافتههای ما نشان داد که کسر اتانولی از Rhinacanthus nasutus (L.) Kurz قویترین مهارکننده تیروزیناز است و به دنبال آن عصاره اتانولی از Ardisia elliptica Thunb قرار دارد. و Phyllanthus acidus (L.) Skeels. بدیهی است که 7 گیاه از 14 گیاه دارای محتوای فنلی بالا به ویژه Ardisiaelliptica Thunb بودند. و Annona squamosa L. علاوه بر این، Senna alata (L.) Roxb. ثروتمندترین ها را داشتفلاونوئیدمحتوایی که می تواند فعالیت تیروزیناز را مهار کند. ترکیبات فعال از گیاهان مانند آربوتین، آلوئزین، اسید جنتیزیک، فلاونوئیدها، هسپریدین، شیرین بیان، نیاسینامید، مشتقات مخمر و پلی فنول ها می توانند ملانوژنز را بدون سمیت سلولی برای ملانوسیت ها مهار کنند [6].
کلاژناز یک پپتیداز روی گذرنده است که پیوند X-Gly کلاژن را جدا می کند. کلاژن یک پروتئین ساختاری فراوان و جزء ماتریکس خارج سلولی است [33]. کاهش الیاف کلاژن و الاستین با افزایش سن و آسیب ناشی از اشعه ماوراء بنفش افزایش می یابد که باعث ایجاد چین و چروک پوست می شود[34]. مهار کلاژناز برای جلوگیری از پیری پوست پیشنهاد شده است. از آنهایی که باعث مهار در مطالعه ما می شوند، Ardisiaelliptica Thunb. بالاترین سطح مهار کلاژناز را نشان داد و پس از آن Annona squamosa L.، Senna alata(L.) Roxb. و Croton sublyratus Kurz به ترتیب رتبهبندی شدند. در مطالعه قبلی، عصاره غلاف کاکائو دارای اسید فنولیک وفلاونوئیدهاکه فعالیت الاستاز و کلاژناز را مهار کرد [35]. به ویژه، سه عصاره اتانولی (Ardisia elliptica Thunb.، Annona squamosa L. و Senna alata (L.) Roxb. هر دو را مهار کردند.تیروزینازو کلاژناز این گیاهان همچنین دارای سطح بالایی از فنل و فلاونوئید بودند وآنتی اکسیدانجالب توجه است که این عصاره ها به عنوان مواد تشکیل دهنده محصولات آرایشی کاربردهای احتمالی دارند.
نتیجه
نتایج ما نشان می دهد که عصاره 14 گیاه تایلندی دارای درجات مختلفی از کل فنولیک وفلاونوئیدمحتوا و همچنین فعالیت های مهار رادیکال های آزاد، بستگی به حلال های استخراج دارد. همبستگی بالایی بین محتوای فنلی کل و فعالیت مهار رادیکال آزاد ارزیابی شده توسط سنجش DPPH و ABTS وجود داشت. کسر اتانولی Ardisia ellipticaThunb. هر دو گیاه به طور قابل توجهی فعالیت تیروزیناز و کلاژناز را مهار کردند، در حالی که Rhinacanthusnasutus (L.) Kurz بالاترین مهار تیروزیناز را نشان داد. علاوه بر این، سنا آلاتا (L.) Roxb. غنی ترین از نظر محتوای فلاونوئید بود، و همچنین به نمایش گذاشته شدتیروزینازو رفتار مهاری کلاژناز. کسر اتانولی از سه گیاه، یعنی Annona squamosa L.، Ardisia elliptica Thunb، و Senna alata (L.) Roxb.، پتانسیل این را دارند که در محصولات آرایشی برای ضد چروک و همچنین سفید کننده پوست باشند. مطالعات بیشتر برای بررسی اجزای فعال و ایمنی این عصاره ها ضروری است.

بدنسازی سیستانچ
منابع
1. Moehrle M. ورزش در فضای باز و سرطان پوست. کلین درماتول. 2008؛ 26 (1): 12-5.
2. Lopez-Camarillo C، Ocampo EA، Casamichana ML، Perez-Plasencia C، Alvarez-Sanchez E، Marchat LA. پروتئین کینازها و فعالسازی فاکتورهای رونویسی در پاسخ به اشعه ماوراء بنفش پوست: پیامدهایی برای سرطانزایی. Int J Mol Sci. 2012؛ 13 (1): 142-72.
3. Iwata M، Corn T، Iwata S، Everett MA، Fuller BB. رابطه بین فعالیت تیروزیناز و رنگ پوست در پوست ختنه گاه انسان J Investig Dermatol.1990;95(1):9-15.
4. استرن آر اس. درمان پیری نوری N Engl J Med. 2004؛ 350 (15): 1526-34.
5. Levin CY، Maibach H. اگزوژن ochronosis. به روز رسانی در مورد ویژگی های بالینی، عوامل ایجاد کننده، و گزینه های درمانی. درماتول جی کلین هستم. 2001؛ 2 (4): 213-7.
6. Zhu W, Gao J. استفاده از عصاره های گیاهی به عنوان عوامل روشن کننده موضعی پوست برای بهبود اختلالات رنگدانه پوست. J Investig DermatolSymp Proc. 2008؛ 13 (1): 20-4.
7. Zongo C، Savadogo A، Ouattara L، Bassole IHN، Ouattara CAT، Ouattara AS، Barro N، Koudou J، TraoreI AS. محتوای پلی فنول ها، فعالیت های آنتی اکسیدانی و ضد میکروبی Ampelocissus grandii (بکر) Planch. (Vitaceae): گیاه دارویی از بورکینافاسو. Int J Pharmacol. 2010؛ 6 (880-887)
8. Yamasaki K, Hashimoto A, Kokusenya Y, Miyamoto T, Sato T. روش الکتروشیمیایی برای تخمین اثرات آنتی اکسیدانی عصاره متانولی داروهای خام. Chem Pharm Bull (توکیو). 1994؛ 42 (8): 1663-5.
9. Re R، Pellegrini N، Proteggente A، Pannala A، Yang M، Rice-Evans C. فعالیت آنتی اکسیدانی با استفاده از یک سنجش رنگ زدایی کاتیونی رادیکال ABTS بهبود یافته. رادیک آزاد بیول مد. 1999؛ 26 (9-10): 1231-7.
10. Nithitanakool S، Pithayanukul P، Bavovada R، Saparpakorn P. مطالعات مولکولی داکینگ و فعالیت ضد تیروزیناز عصاره هسته دانه انبه تایلندی. مولکول ها. 2009؛ 14 (1): 257-65.
11. Bonvicini F، Antognoni F، Iannello C، Maxia A، Poli F، Gentilomi GA. فعالیت انتخابی و مرتبط Pancratium Illyricum L. در برابر جدایه های بالینی Candida Albicans: اثر ترکیبی بر رشد مخمر و حدت. BMCComplement Altern Med. 2014؛ 14 (1): 409.
12. Sharma OP، Bhat TK. سنجش آنتی اکسیدانی DPPH دوباره مورد بررسی قرار گرفت. مواد شیمیایی مواد غذایی 2009؛ 113 (4): 1202-5.
13. MacDonald-Wicks LK، Wood LG، Garg ML. روش شناسی برای تعیین ظرفیت آنتی اکسیدانی بیولوژیکی در شرایط آزمایشگاهی: یک بررسی J Sci Food Agric. 2006؛ 86(13): 2046-56.
14. آرمسترانگ BK، کریکر A. اپیدمیولوژی سرطان پوست ناشی از UV. JPhotochem Photobiol B Biol. 2001؛ 63 (1-3): 8-18.
15. بشیر MM، شرما ام.آر، ورث معاون. UVB و سیتوکینسنرژیک پیش التهابی تولید TNF- در کراتینوسیت ها را از طریق رونویسی افزایش یافته ژن فعال می کنند. J Investig Dermatol. 2009؛ 129 (4): 994-1001.
16. Watson RE، Gibbs NK، Griffiths CE، Sherratt MJ. آسیب به ماتریکس خارج سلولی پوست ناشی از قرار گرفتن در معرض UV. سیگنال ردوکس آنتی اکسیدان 2014؛ 21 (7): 1063-77.
17. D'Orazio J، Jarrett S، Amaro-Ortiz A، Scott T. اشعه UV و پوست. Int JMol Sci. 2013؛ 14 (6): 12222-48.
18. Pittayapruek P، Meephansan J، Prapapan O، Komine M، Ohtsuki M. نقش متالوپروتئینازهای ماتریکس در پیری نوری و سرطان زایی. Int J MolSci. 2016؛ 17 (6): 868.
19. Sulaiman CT, Balachandran I. کل فنول ها و فلاونوئیدهای کل گیاهان دارویی هندی انتخاب شده. هند جی فارم Sci. 2012؛ 74 (3): 258-60.
20. Mamat N، Jamal JA، Jantan I، Husain K. فعالیت های مهار رادیکال DPPH و مهار رادیکال DPPH برخی از گونه های Primulaceae. ساینس مالزی. 2014؛ 43 (12): 1827-33.
21. Wetwitayaklung P، Charoenteeraboon J، Limmatvapirat C، Phaechamud T. فعالیت های آنتی اکسیدانی برخی از میوه های تایلندی و عجیب و غریب کشت شده در تایلند. Res J Pharm، Biol Chem Sci. 2012؛ 3 (1): 12-21.
22. Falcone Ferreyra ML، Rius SP، Casati P. فلاونوئیدها: بیوسنتز، عملکردهای بیولوژیکی، و کاربردهای بیوتکنولوژیکی. علوم گیاهی جلویی 2012؛ 3:222.
23. Devendra K, Kiran D, Ritesh V, Satyendra B, Abhishek K. برای ارزیابی کل فنولیک ها و فلاونوئیدها در گیاهان مختلف چاتیسگر. JPharmacognosy Phytochem. 2013؛ 2 (4): 116-8.
24. Siti-Azima AM، Northam A، Nurhuda M. فعالیت های آنتی اکسیدانی SyzygiumCumini و ArdisiaElliptica در رابطه با ترکیبات فنلی و خواص کروماتیک تخمین زده شده آنها. Int J Biosci Biochem Bioinform. 2013؛ 3 (4): 314-7.
25. Solovchenko A, Schmitz-Eiberger M. اهمیت فلاونوئیدهای پوست برای محافظت از UV-B در میوه های سیب. J Exp Bot. 2003؛ 54 (389): 1977-84.
26. Gonzalez-Gallego J, Sanchez-Campos S, Tunon MJ. خواص ضد التهابی فلاونوئیدهای رژیمی بیمارستان نوتر. 2007؛ 22 (3): 287-93.
27. Sudha A، Sumathi K، Manikandaselvi S، Prabhu NM، Srinivasan P. فعالیت ضد کبدی بخش فلاونوئید خام Lippia Nodiflora L. آسیب کبدی ناشی از انتانول در موش صحرایی. آسیایی J Anim Sci. 2013؛ 7 (1): 1-13.
28. Sak K. سمیت سلولی فلاونوئیدهای رژیم غذایی بر روی انواع مختلف سرطان انسان. Pharmacogn Rev. 2014؛ 8 (16): 122-46.
29. Kedare SB، Singh RP. پیدایش و توسعه روش DPPH سنجش آنتی اکسیدانی. J Food Sci Technol. 2011؛ 48 (4): 412-22.
30. Boo HO، Kim TS، Koshio K، Shin JH، Chon SU. سطوح فنول کل و خواص آنتی اکسیدانی در عصاره متانولی چندین گیاه وحشی ویتنامی کره ای J Plant Res. 2011؛ 24 (6): 659-65.
31. Dudonne S، Vitrac X، Coutiere P، Woillez M، Merillon JM. بررسی مقایسه ای خواص آنتی اکسیدانی و محتوای فنلی کل 30 عصاره گیاهی مورد علاقه صنعتی با استفاده از سنجش DPPH، ABTS، FRAP، SOD و ORAC. جی AgricFood Chem. 2009؛ 57 (5): 1768-74.
32. Slominski A، Tobin DJ، Shibahara S، Wortsman J. رنگدانه ملانین در پوست پستانداران و تنظیم هورمونی آن. Physiol Rev. 2004؛ 84 (4): 1155-228.
33. Shoulders MD، Raines RT. ساختار و پایداری کلاژن Annu RevBiochem. 2009؛ 78:929-58.
34. Cua AB، Wilhelm KP، Maibach HI. خواص ارتجاعی پوست انسان: نسبت به سن، جنس و ناحیه آناتومیکی. Arch Dermatol Res. 1990؛ 282 (5): 283-8.
35. کریم AA، ازلان A، اسماعیل A، هاشم P، گانی SSA، زین الدین BH، عبدالله NA. ترکیب فنلی، آنتی اکسیدان، ضد چین و چروک و فعالیت مهاری تیروزیناز عصاره غلاف کاکائو. BMC Complement Altern Med. 2014؛ 14 (381): 1-13.
