تحمل به NADH/NAD به علاوه عدم تعادل، مداخلات پیری و ضد پیری را پیش بینی می کند
Jun 13, 2022
لطفا تماس بگیریدoscar.xiao@wecistanche.comبرای اطلاعات بیشتر
خلاصه
زوج های ردوکس عملکرد سلولی را هماهنگ می کنند، اما پیامدهای عدم تعادل آنها نامشخص است. این تا حدودی با محدودیت های کمی سازی تجربی آنها مرتبط است. در اینجا ما با ارائه رویکردی که پروفایل های تحمل مبتنی بر تناسب اندام را برای عدم تعادل زوج ردوکس با استفاده از ارائه سیلیکونی متابولیسم مشخص می کند، این مشکلات را دور می زنیم. با تمرکز بر روی زوج ردوکس NADH/NAD1 در مخمر، نشان میدهیم که عدم تعادل تقلیلی باعث ایجاد سندرمهای متابولیک قابل مقایسه با موارد مشاهده شده در سلولهای سرطانی میشود.فواید عصاره سیستانچتحمل جهش مخمرها به عدم تعادل ردوکس همچنین می تواند 30 درصد از تنوع در طول عمر زمانی اندازه گیری تجربی آنها را توضیح دهد. علاوه بر این، با پیشبینی اهمیت برخی از متابولیتها برای کمک به عدم تعادل، مواد مغذی را به درستی شناسایی میکنیم که مکانیسمهای آسیبشناسی، مولکولهای محافظ طول عمر، یا تقلیدهای محدودیت کالری را تشکیل میدهند. تحمل در برابر عدم تعادل ردوکس، به این ترتیب، به صدایی تبدیل میشود که چارچوبی برای تشخیص ویژگیهای فنوتیپ پیری ارائه میکند، در حالی که با یک منطق بیولوژیکی برای ارزیابی مداخلات ضد پیری سازگار است.
مقدمه
تحقیقات در مورد هموستاز ردوکس در دو دهه گذشته به طور قابل توجهی گسترش یافته است و به طور مداوم مفاهیم کلاسیک آسیب سلولی اکسیداتیو را تغییر می دهد (Halliwell and Gutteridge, 2015). در میان پارادایماتیکترین عوامل مولکولی زیربنای این هموستاز، نسبتهای زوجهای ردوکس، مانند فرمهای مزدوج گلوتاتیون، NADPH، و NADH ظاهر میشوند. گلوتاتیون و NADPH هر دو به عنوان مکانیسمهای مهارکننده ضروری گونههای اکسیژن فعال (ROS) در میتوکندری عمل میکنند، در حالی که NADPH و NADH به ترتیب مسیرهای آنابولیک و کاتابولیک را با حالت ردوکس سلول همراه میکنند.

لطفا برای دانستن بیشتر اینجا را کلیک کنید
با این حال، مکانیسمهای جدیدی که جفتهای NADPH/NADP* و NADH/NAD* را به هموستاز ردوکس مرتبط میکند همچنان شناسایی میشوند. به عنوان مثال، تعادل NADPH/NADP به علاوه تا حدی پیامدهای بقای پروتئین کیناز فعال شده با AMP را توضیح می دهد (She et al., 2014). همچنین، زمان سنجی شبانه روزی را با حالت های ردوکس مرتبط می کند (ری و همکاران، 2016). در حال حاضر تصور می شود که نسبت NADH/NAD پلاس در هماهنگی عملکرد میتوکندری و هسته، تنظیم اپی ژنتیکی ترمیم DNA و هویت سلولی، و تنظیم متابولیسم انرژی با متغیرهای محیطی نقش دارد (Canto et al., 2015; Gomes et al. al. 2013). در شرایط غیر پاتولوژیک، نسبت NADH/NAD* با تنش اکسیژن، با شرایط هیپوکسیک و در دسترس بودن اکسیژن بالاتر به ترتیب با انحرافات کاهنده و اکسیداتیو همراه است (کلانتون، 2007؛ گراف و همکاران، 1999).
اما علاقه فزاینده به نسبت زوج های ردوکس عمدتاً از پیامدهای آنها در آسیب شناسی ناشی می شود.سیستانچ چنگیز خانظهور ROS در هر دو حس تقلیل دهنده (هیپوکسیک، مستعد NADH) و اکسیداتیو (هیپراکسیک، NAD به علاوه مستعد) به واگرایی از یک پتانسیل ردوکس بهینه مربوط می شود که بهترین عملکرد میتوکندری را تضمین می کند (Aon et al., 2010). ؛ کلنتون، 2007). با توجه به سرطان، کاهش NADH/NAD پلاس ممکن است زمینه ساز کشندگی گلیوبلاستوما باشد (گوجار و همکاران، 2016) و پیشرفت سرطان روده بزرگ را ارتقا دهد (هنگ و همکاران، 2019)، با این حال، می تواند برخی از فنوتیپ های سالم را به درجات مختلف در سلول ها نجات دهد. سایر انواع تومور (گاریدو و جودر، 2017).

سیستانچ می تواند ضد پیری باشد
NADH همچنین به یک نقطه مورد توجه در زیست شناسی تورنتو تبدیل شده است. در این زمینه، افزایش استخر NAD پلاس منجر به معکوس شدن جزئی پیری و سایر فنوتیپهای پاتولوژیک مرتبط در سراسر موجودات شد (داس و همکاران، 2018؛ مندلسون و لاریک، 2014؛ وی و همکاران، 2017؛ ژو و همکاران. ، 2017) و سلول های پیر و نئوپلاستیک نشان دهنده عدم تعادل نسبت NADH/NAD پلاس هستند (Braidy et al., 2011; Schwartz and Passonneau, 1974; Wiley et al, 2016). علاوه بر این، نقشهای تازه کشفشده NADPH و مفهوم نوظهور NADH/NADH بهعنوان یک تنظیمکننده اصلی هموستاز ردوکس و پیری، همگی در راستای تئوری پایداری متابولیک پیری هستند (Demetrius, 2004). این نظریه پیشنهاد میکند که علت پیری آسیبپذیری سطوح حالت پایدار زوجهای ردوکس در برابر اختلالات محیطی تصادفی در نرخ واکنش آنزیمی است و چندین پیشبینی جالب را انجام میدهد که برای انسانها اعمال میشود.
با توجه به همه این پیامدها، بسیاری از مطالعات پدیدارشناسی نسبتهای زوج ردوکس را با گزارش غیرفعال سطوح آنها یا با اصلاح فعالانه آنها بررسی کردهاند. با این حال، دستکاری های تجربی چالش برانگیز هستند. سنتیترین اخطارهای تجربی عمیق (سان و همکاران، 2012) و موارد جدیدتر هنوز شرایط بیولوژیکی خاصی را به دلیل محدود شدن به دما و فواصل pH از دست میدهند (هنگ و همکاران، 2011؛ ژائو و همکاران، 2015). علاوه بر این، نظارت بر طیف وسیعی از فنوتیپها به دنبال تغییر مخزنهای کوآنزیمی توسط مکملهای متابولیت (Hou et al., 2010) و جهش یا بیان بیش از حد آنزیمهای مصرفکننده NAD(H) از نظر تجربی گران است (Bait al., 2011; فیلیپ و همکاران، 1998). بنابراین، نیاز به استراتژیهای جایگزین برای رسیدگی به کنترل هموستاز ردوکس از طریق دستکاری زوجهای ردوکس، و همچنین درک ما از پیامدهای بیولوژیکی این کنترل وجود دارد.
در مدلهای سیلیکونی، هر زمان که رویکردهای تجربی محدود میشوند، به یک استراتژی تحقیقاتی عملی تبدیل میشوند، با این مزیت که امکان یک حساب مکانیکی کامل از پدیدههای مشاهدهشده را فراهم میکند. مدل های متابولیک در مقیاس ژنوم، که می توانند از طریق تجزیه و تحلیل تعادل شار (FBA) مورد مطالعه قرار گیرند (Orth et al, 2010) به استانداردی در زیست شناسی سیستم ها برای مطالعه پیامدهای اختلالات متابولیک بر عملکرد سلولی تبدیل شده اند (روش S1). از جمله کمکهای دیگر، آنها در کشف آنتیبیوتیکها و شیمیدرمانهای جدید، طراحی سویههای باکتریایی بهینهسازی شده برای تولید صنعتی مواد مورد علاقه، و درک بهتر بیماریهای متابولیک انسانی کمک کردهاند (بورگارد و همکاران، 2003؛ پاگلارینی و همکاران. 2016؛ رامان و همکاران، 2009). استفاده از FBA دارای مزیت اضافی ارائه بینش به پدیده های متابولیک بدون تأثیر عوامل مخدوش کننده غیر متابولیک (ژنتیکی، اپی ژنتیکی، مکانیکی و غیره) است. بنابراین، مدلهای متابولیکی در مقیاس ژنوم برای بررسی عواقب متابولیکی انحراف از هموستاز ردوکس بسیار مناسب هستند.
در اینجا، ما از FBA برای بررسی تعادل زوجهای ردوکس در بازسازی مقیاس ژنوم یوکاریوت تک سلولی ساکارومایسس سرویزیه استفاده میکنیم که به موجب آن پیامدهای متابولیکی و مرتبط با طول عمر یک اختلال کنترلشده NADH/NAD به علاوه شار موجود در ژنتیکهای مختلف را مشخص میکنیم. پس زمینه ها به طور خاص، نتایج ما نشان میدهد که تحمل به این عدم تعادل منجر به تغییر مسیر متابولیکی خاص میشود که یادآور آسیبشناسی است و همچنین بیش از یک چهارم تنوع دروناختصاصی در طول عمر پس از میتوزی را توضیح میدهد. علاوه بر این، این چارچوب به ما کمک میکند تا یک پروتکل محاسباتی (که در مدلهای متابولیک حیوانی و انسانی نیز اعمال میکنیم) برای شناسایی متابولیتها و آنزیمهای بالقوه بهعنوان اهداف درمانی در زمینه آسیبشناسیهای مرتبط با سن، ترسیم کنیم.
نتایج
یک پروفایل تحمل مبتنی بر تناسب اندام، اختلالات زوج ردوکس را مشخص می کند
برای نشان دادن عدم تعادل بین اشکال مزدوج یک زوج ردوکس، ما یک واکنش برگشتپذیر مصنوعی - "واکنش عدم تعادل" - را در بازسازی مقیاس ژنوم شبکه متابولیک مربوطه (روشهای STAR) وارد کردیم. این واکنش با در نظر گرفتن بخشهای سلولی خاص (مانند سیتوزول، میتوکندری و غیره) زوج را اکسید یا کاهش میدهد و فعالیت آن را میتوان به هر مقدار نرخ دلخواه ثابت کرد. برای هر یک از این مقادیر، می توان نرخ رشد ("تناسب") را محاسبه کرد که به عنوان نماینده ای برای تحمل سلول مخمر به آن شرایط خاص عمل می کند. در نهایت، یک پروفایل تحمل با محاسبه نرخ رشد برای یک محدوده تعریف می شود. مقادیر عدم تعادل (شکل 1A؛ توجه داشته باشید که شرایط کاهشی/اکسیداتیو به ترتیب به رنگ آبی/قرمز در سراسر مقاله نشان داده شده است).
پروفیل های تحمل معمولاً حداکثر رشد را در اطراف نقطه عدم تعادل صفر نشان می دهند، تقریباً هر انحرافی (یعنی مقدار غیر صفر واکنش) منجر به کاهش تناسب می شود. این امر بر این واقعیت تأکید دارد که برای اینکه متابولیسم کار کند، فعالیت واکنشهایی که نسبت زوج ردوکس را تنظیم میکنند از یک جهت باید متناسب با فعالیت واکنشهایی باشد که آن را در دیگری تنظیم میکنند. به طور خاص، عدم تعادل سیتوزولی NADH/NADt در S.افزایش عمر cistancheسرویزیههایی که در شرایط گلوکز و هوازی رشد میکنند، نمایهای با حداکثر رشد بهطور قابلتوجهی به سمت سمت اکسیداتیو در نقطهای از پروفایل عدم تعادل که در آن ~50 میلیمول در DW/ساعت NADH به NADH تبدیل میشود، ایجاد میکند (شکل 1B). هنگام در نظر گرفتن عدم تعادل در میتوکندری، ما حداکثر را در نقطه عدم تعادل صفر مشاهده کردیم (شکل 1C)، الگویی که به طور مشابه در پروفایل های دیگر مشاهده کردیم (شکل S1). به طور کلی، شرایط تقلیل تبدیل می شود

شکل 1. پروفایل تحمل پاسخ به عدم تعادل ردوکس را مشخص می کند
(الف) بالا. ما یک واکنش مصنوعی را در مدل بازسازی متابولیک یک ارگانیسم (در این مورد مخمر) برای تبدیل دو شکل مزدوج یک کوآنزیم ردوکس (در اینجا جفت NADH/NADH) معرفی کردیم. تحت هر یک از یک سری از شرایط عدم تعادل، به عنوان مثال، مقادیر نرخ واکنش مصنوعی، ما تجزیه و تحلیل تعادل شار را برای محاسبه نرخ رشد اعمال می کنیم. پایین. مقادیر پیشبینیشده رشد در برابر مقادیر نرخ عدم تعادل ترسیم میشوند که نمایه تحمل را مشخص میکند. پروکسی برای تحمل متابولیسم در هنگام مواجهه با اختلال انتخابی.cistanche nz(ب) مشخصات تحمل در مخمر مرتبط با عدم تعادل واقع در سیتوزول.
(C) مشخصات تحمل در مخمر مرتبط با عدم تعادل واقع در میتوکندری. سایه آبی/قرمز به ترتیب نشان دهنده رژیم های عدم تعادل کاهش یافته و اکسید شده است و نقاط خاکستری مقادیر مربوط به عدم تعادل یا عدم تعادل کاهنده/اکسیداتیو شدید را نشان می دهد که رشدی ایجاد نمی کند. مضر و کشنده تر از رژیم های اکسیداتیو است. در دو مورد (جفت های کونژوگه NADH سیتوزولی یا تیوردوکسین میتوکندریایی)، اکسیداسیون مصنوعی خفیف زوج رشد را بهبود می بخشد (شکل S1).
اختلالات NADH/NAD* باعث ایجاد سندرم های متابولیک می شود که یادآور آسیب شناسی است
متابولیسم انرژی مخمر بدون عدم تعادل با یک متابولیسم هوازی مشخص در حضور گلوکز (شرایط رشد مورد مطالعه) مطابقت دارد که در آن گلیکولیز با چرخه اسید تری کربوکسیلیک (TCA) و فسفوریلاسیون اکسیداتیو همراه است. مسیر پنتوز فسفات، گلوکز را اکسید می کند و ریبوز-5P را برای سنتز نوکلئوتید و قدرت کاهشی ناشی از NADPH برای آنابولیسم فراهم می کند، در حالی که مسیرهای آناپلروتیک چرخه TCA را ترک می کنند، مشابه متابولیسم گلوتامین، به طور متوسط برای تغذیه و تغذیه اولیه پیریمیدین استفاده می شود. سنتز اسید آمینه FBA ما را قادر میسازد تا تغییرات در این مسیرها و چگونگی جزئیات آنها در نهایت ویژگیهای متابولیک زیربنای هر رژیم عدم تعادل خاصی را تعیین کنیم.
به طور خاص، شکل 2A نشان می دهد که چگونه عدم تعادل کاهشی NADH/NADH سیتوزولی باعث افزایش شار گلیکولیتیک، کاهش فعالیت چرخه TCA و زنجیره انتقال الکترون و افزایش متابولیسم گلوتامین می شود. این علامت متابولیک کاذب هیپوکسیک - در حضور اکسیژن - شبیه متابولیسم بی هوازی است، جایی که گلیکولیز با تخمیر الکلی یا لاکتیک همراه است تا مسیرهای میتوکندریایی را به خطر بیندازد. بخش اکسیژنی مسیر پنتوز فسفات بسته میشود و متابولیسم گلوتامین که فعالتر است، ممکن است برای تولید پیرووات تغییر مسیر داده و به آنابولیسم کمک کند. قابل توجه است که این فنوتیپ برخی از ویژگیهای متابولیسمهای عملکرد متناقض مشاهده شده در انواع مختلف سلولهای سرطانی (اثر Warburg) را نشان میدهد (Potter et al., 2016).

شکل 2. شارهای مسیرهای اصلی مدیریت انرژی که زیربنای مشخصات تحمل در مخمر هستند (A) عدم تعادل سیتوزولی NADH/NAD (بالا) و مقادیر شار پنج مسیر نماینده (پایین). i/گلیکولیز (گلیکولیز، هسته)، چرخه ii/Krebs (TCA، صورتی)، ili/pentose فسفات (Penphos، سبز)، فسفوریلاسیون IV/اکسیداتیو (Oxphos، خاکستری)، و متابولیسم گلوتامین (گلوتامین، بنفش). بردارهای شار نشاندادهشده نتیجه میانگینگیری شار تمام واکنشهای یک مسیر خاص هستند.

(ب) مانند (A) با توجه به عدم تعادل میتوکندری. توجه داشته باشید که وجود شارهای منفی در گلیکولیز (پانل A، پایین) نشان دهنده افزایش گلوکونئوژنز است. برای جزئیات بیشتر به متن اصلی مراجعه کنید.
در مقابل، متابولیسم انرژی زیربنای تحمل اکسیداتیو (با توجه به سیتوزول، شکل 2A) پیکربندی هوازی بیشتری را نشان داد اما با ویژگیهایی مانند متابولیسم پلیآمین به ویژه فعال. و خواص فوق العاده، از جمله افزایش گلوکونئوژنز، فسفوریلاسیون اکسیداتیو، و فعالیت چرخه TCA، و همچنین شار بسیار بالا (تا 12- برابر سطح نرمال) از طریق مسیر پنتوز فسفات. با این حال، دومی ممکن است مصنوع تفاوت در واکنش شبه زیست توده، تحت عدم تعادل اکسیداتیو بسیار بالا (55 میلی مول/gDW/h گذشته) باشد (به روش S1 مراجعه کنید).
هنگامی که واکنش عدم تعادل در میتوکندری قرار می گیرد، کاهش NADH دوباره یک رفتار شبه هیپوکسیک خاص را ایجاد می کند، با یک تفاوت (شکل 2B). شار از طریق گلیکولیز و متابولیسم گلوتامین افزایش یافته است، با از دست دادن همزمان بخشهایی از چرخه TCA و مسیر پنتوز فسفات. با این حال، بر خلاف در مورد سیتوزولی، فسفوریلاسیون اکسیداتیو به طور قابل توجهی افزایش یافته است. از سوی دیگر، سمت اکسیداتیو پروفایل میتوکندری خاصتر بود: فعالیت گلیکولیتیک به موازات چرخه TCA افزایش یافت، اما فسفوریلاسیون اکسیداتیو در بیشتر موارد در سطوح پایینتر از حد طبیعی کار میکرد و متابولیسم گلوتامین اهمیت کمی داشت.
سندرم های متابولیک ناشی از مصالحه بین تعادل اکسیداسیون و کاهش، تولید زیست توده و معاوضه ATP/NADH است.
ما چندین عنصر کلیدی را شناسایی کردیم که سندرم های قبلی را شکل دادند.اندازه آلت تناسلی سیستانچاغتشاش اکسیداتیو با یک پاسخ هوازی تشدید شده به عنوان سازشی بین حفظ رشد و بافر اختلال عدم تعادل مواجه شد. این شامل تغییر مسیر شار از طریق حداکثر تعداد ممکن واکنش بود که NAD پلاس را کاهش داد و در عین حال توزیع شار جهانی را حفظ کرد که قادر به تولید اجزای زیست توده بود. این دو عنصر مکانیکی (بافر اغتشاش و به حداکثر رساندن زیست توده) مرتبطترین الزامات مسئله بهینهسازی هستند و برای توصیف رژیم اکسیداتیو پروفایل تحمل کافی هستند.

شکل 3. مکانیسم های رقابتی باعث رفتار شبه هیپوکسیک مخمر می شود
(الف) تعادل بین NADH، ATP و تولید پیش سازهای زیست توده به نفع ماژولهای واکنشی است که به همان اندازه ATP تولید میکنند و NAD کمتر ممکن است برای جبران عواقب رژیمهای تقلیلدهنده، به عنوان مثال، استفاده از گلیکولیز به TCA. در اینجا توجه داشته باشید که فلش های بنفش نشان دهنده تولید ATP، فلش های زرد نشان دهنده تولید NAD(H) و دایره های سفید نشان دهنده تولید پیش سازهای زیست توده است، (B) یک اختلال NADH/NADt مستعد NADH (محور x) با یک ADP مصنوعی همپوشانی دارد. واکنش فسفوریلاسیون (محور y) که به زور قدرت تقلیل را به شکل ATP به متابولیسم نامتعادل وارد می کند. یک گرادیان رنگ سبز نشان دهنده نسبت بین شار گلیکولیتیک و چرخه کربس است که با مقدار نرمال آن نرمال شده است (تا 100- برابر). می توان دریافت که فسفوریلاسیون ADP فنوتیپ شبه هیپوکسیک را کاهش می دهد و سکون را به تاخیر می اندازد.

با این حال، سمت تقلیل به یک بینش اضافی نیاز داشت. هر چه بیشتر و بیشتر NADH به واکنشهای NADH که از NADt استفاده میکنند و به طور مستقیم یا غیرمستقیم برای تولید ترکیبات زیست توده ضروری هستند، محدود میشود، بیشتر و بیشتر محدود میشود، بنابراین متابولیسم انرژی باید تغییر مسیر داده شود تا تبدیل NADH به NAD' افزایش یابد و مقدار آن محدود شود. کاهش NAD' به NADH. این هنوز برای رویارویی با اغتشاش کافی نیست، زیرا بیشتر قدرت تقلیل به شکل NADH اساساً برای بسیاری از اهداف متابولیکی، واکنش ها و رشد بی فایده است: انرژی ذخیره شده در NADH باید دوباره به ADP تخصیص داده شود. بنابراین، متابولیسم باید ماژولهای واکنشی را در اولویت قرار دهد که تا آنجا که ممکن است ATP و NADH کمتری تولید میکنند. باید بر روی شانت ها و مسیرهایی تکیه کند که بازده ATP/NADH بالایی دارند، به عنوان مثال، گلیکولیز و فسفوریلاسیون اکسیداتیو.
این نتایج از جمله در کاهش چرخه TCA و افزایش شار گلیکولیتیک (شکل 3A). برای بررسی بیشتر تأثیر این مبادله ATP/NADH، ما یک اغتشاش کاهشی NADH/NAD را با یک واکنش مصنوعی همپوشانی کردیم که امکان فسفوریلاسیون ADP را فراهم می کند. . شبیهسازیها نشان داد که افزایش نسبت شار گلیکولیز به چرخه TCA که متابولیسم کاهشی را مشخص میکند به بازده ATP/NADH بستگی دارد.

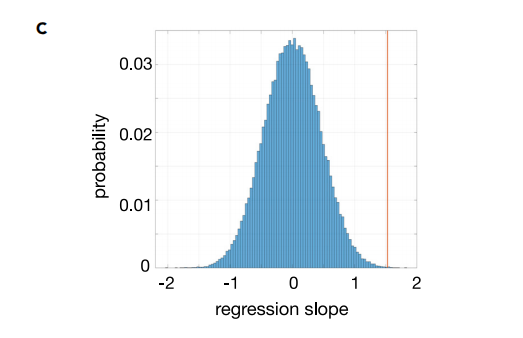
شکل 4. امتیاز تحمل به عنوان پیش بینی کننده طول عمر زمانی در مخمر
(الف) پروفایل های تحمل به دست آمده برای جهش مخمر. بخش های آبی/قرمز منحنی نشان دهنده رژیم کاهشی/اکسیداتیو عدم تعادل NADH/NADH است.
(ب) ارتباط بین نمره تحمل نرمال شده (متناسب با وسعت مقادیر عدم تعادل در هر دو رژیم اکسیداتیو و کاهشی، روش STAR) و طول عمر زمانی. این همبستگی 30 درصد از واریانس کل را توضیح می دهد (R'= 0). 29، p-value=3.2x 10-4، N= 41).
(C) به عنوان یک روش جایگزین برای مشاهده این ارتباط، ما یک هیستوگرام از مقادیر شیب رگرسیون به دست آمده از ده هزار ارتباط تصادفی بین نمره تحمل و طول عمر به دست آوردیم. از این نمونه، ما تنها 3 مورد را پیدا می کنیم که در آنها ارتباط بین امتیاز تحمل و داده های طول عمر قوی تر از مورد یافت شده است (که با خط عمودی قرمز مشخص می شود).
(شکل 3B). ADP با فسفریله کردن اجباری این علامت کاذب هیپوکسیک را حتی در مواجهه با نرخ های عدم تعادل بسیار قوی مستعد NADH کاهش می دهد.
Tolerance تفاوت های طول عمر زمانی تجربی بین جهش یافته های مخمری مختلف را توضیح می دهد
با توجه به اینکه زوجهای ردوکس بهعنوان عوامل بالقوه تعیینکننده طول عمر مورد بحث قرار گرفتهاند، ما پرسیدیم که پروفایل تحمل تا چه اندازه میتواند به عنوان پیشبینیکننده طول عمر عمل کند. یکی از راههای مطالعه این موضوع، محاسبه پروفایل در جهشیافتههای مختلف است (شکل 4A) و سپس تعیین کمیت چگونگی مطابقت آن با معیارهای دقیق طول عمر، طول عمر زمانی نرمالشده (CLS)، که از منحنیهای بقای جهشیافته به صورت تجربی اندازهگیری شده است (Garay et al., 2014). CLS ها از این منحنی های بقای جهش یافته به عنوان افزایش بقای فاز ثابت نسبت به نوع وحشی محاسبه می شوند.
در FBA، جهش در ژنهای خاص با محدود کردن شار واکنشهای مرتبط با آنها از طریق قوانین بولی شبیهسازی میشود که هر واکنش شیمیایی را به ORFهایی که آنزیم واکنش را ترجمه میکنند (روشهای STAR) مرتبط میکند. برای هر یک از این جهشیافتهها، ما یک پروفایل تحمل جهشیافته (شکل 4A) محاسبه کردیم و از مجموع مقادیر مطلق عدم تعادل که در آن نرخ رشد به نصف کاهش مییابد (هم در رژیمهای کاهشی و هم در رژیمهای اکسیداتیو) به عنوان یک نمره اسکالر تحمل (STAR) استفاده کردیم. مواد و روش ها).
مجموعه جهش یافته ما با برخی محدودیت ها (روش های STAR) محدود شد. قابلتوجه، ما قادر به تشخیص تفاوتها در تحمل کمتر از 10 ppm از مقدار نوع وحشی نبودیم، بدون اینکه به زمانهای محاسباتی غیرمجاز دست یابیم، و بسیاری از جهشیافتهها هم تفاوتهای ناچیز در طول عمر و هم تفاوتهای ناچیز در تحمل ارائه کردند. علاوه بر این، به طور کلی در نظر گرفته میشود که FBA قادر به توصیف حذفهای افزایش عملکرد نیست و کاملاً قابل پیشبینی است که هیچ تحمل جهشی بیش از تحمل نوع وحشی نیست.
فراتر از این محدودیتها، پروفایلهای تحمل سیلیکو قادر به توضیح -30 درصد از تغییرات طول عمر آزمایشی اندازهگیری شده بودند (شکل 4B، R2= 0.29، N{4}}، مقدار p{{5 }}.2x 10-) با اهمیت زیاد:10،000 تصادفیسازی جفتهای داده تنها به 3 مورد با شیب رگرسیون بزرگتر منجر شد (شکل 4C).
مواد مغذی معمولی تحمل به عدم تعادل NADH/NADH را امکان پذیر می کنند
در نهایت، ما بررسی کردیم که آیا متابولیت های رژیم غذایی خاص در پاسخ به عدم تعادل ردوکس تعیین کننده هستند یا خیر. برای این هدف، ما از یک ویژگی اضافی مدلهای FBA استفاده کردیم که امکان دسترسی به استفاده از یک متابولیت خاص است (تعریف شده به عنوان نرخ مصرف در روشهای STAR حالت پایدار). ما نحوه تغییر این نرخ را با افزایش مقادیر NADH/NAD احیا کننده و اکسیداتیو به اضافه عدم تعادل بررسی کردیم.
استفاده در هر دو طرف نمایه و برای اکثر متابولیت ها نسبتاً خطی بود. بنابراین، ما این الگوی در حال تغییر را به یک مدل خطی برازش کردیم و شیب (مطلق) را به عنوان نماینده مقیاسی از ارتباط متابولیت مربوطه برای تحمل عدم تعادل ردوکس در نظر گرفتیم (شکل 5A). در میان مواد مغذی پاسخگوی برتر iAZ900، ما متوجه متابولیتهای رژیمی شدیم که نقش مهمی در تنظیم طول عمر مخمر ایفا میکنند، مانند استات (برتنر و همکاران، 2009)، و همچنین بسیاری از این متابولیتها که به طور تجربی باعث افزایش طول عمر در مخمرها، کرمها میشوند. یا حتی سلول های انسانی (مادئو و همکاران، 2018؛ میشور و همکاران، 2016) از جمله مالات، هیدروکسی بوتیرات، اسپرمیدین یا اگزالواستات (شکل های 5B-5، جدول S1).
برخی از مواد مغذی برای تحمل به کاهش NAD، برخی دیگر به NADHoxidation، و تعداد کمی برای هر دوی این رژیمها مرتبطتر بودند. مهم ترین متابولیت های غذایی برای تحمل کاهشی به ترتیب استات، بتا هیدروکسی بوتیرات (BHB)، گلوتامات و گلوتامین بودند (شکل 5B)، در عین حال، مهم ترین متابولیت های غذایی برای تحمل اکسیداسیون NADH استات، NADP پلاس، پوترسین و اسپرمیدین بود. (شکل 5D). در میان آنهایی که از تحمل در هر دو طرف نمایه شرکت کردند، مرتبط ترین آنها به ترتیب استات، گلوتامات، اگزالواستات و اگزگلوتارات بود (شکل 5C).
ما مدلهای متابولیک را در سایر موجودات در نظر گرفتیم تا بیشتر تأیید کنیم که کدام مواد مغذی در پاسخ به عدم تعادل تعیینکننده هستند (روشهای S1، همچنین برای چگونگی تغییر جریان مسیرهای اصلی به شکل S2 مراجعه کنید). همه این عوامل اصلی تغییر کردند، البته نه به طور گسترده، با اسیدهای آلفا کتو، زوج های ردوکس، ویتامین های خاص و اسیدهای آمینه خاص که به طور قابل توجهی برای کنترل اختلالات NADH/NADt در C.elegans و بازسازی انسان ضروری بودند. شایع ترین واکنش به عدم تعادل ردوکس در این موجودات مربوط به متابولیت هایی است که واسطه هموستاز pH هستند، مانند استات، بی کربنات، بی فسفات، سدیم، آب و موارد مشابه. به طور مشابه، ارتباط گلوتامات، گلوتامین، آسپارتات، ترئونین، سرین و گلیسین آنها را از سایر اسیدهای آمینه و بیشتر متابولیت ها متمایز می کند. اسیدهای متوسط و اکسید شده مانند اگزگلوتارات، مالات و اگزالواستات نیز به طور مداوم در تحمل نقش دارند، همانطور که تمایل به بیوتین و برخی فولات ها دارند (جدول S1 را برای فهرست کامل ببینید).
بحث
ما در اینجا یک رویکرد جایگزین برای درک پیامدهای بیولوژیکی گسترده تغییرات در زوجهای ردوکس پیشنهاد میکنیم. این رویکرد مبتنی بر مدلهای متابولیک سیلیکونی است و مفهوم پروفایل تحملپذیر را بهعنوان معیاری معرفی میکند که انعطافپذیری سلولی را در برابر این تغییرات کمیت میکند.

شکل 5. مواد مغذی هموستاتیک در مخمر
(الف) نمونهای از مشخصات استفاده از یک ماده مغذی با رگرسیونهای خطی تقلیلدهنده (آبی) و اکسیداتیو (قرمز) مربوط به آن که به ترتیب با شیبهای m و m (در مقادیر مطلق) مشخص میشوند. ما پروفایل تحمل سیتوزولی را در پسزمینه بهعنوان مرجع درج کردیم.
(ب) شیب های رگرسیون خطی (متر) از 4 ماده مغذی هموستاتیک برتر به معنای تقلیل NADH/NAD به علاوه اغتشاش.
(C) شیب رگرسیون خطی از مواد مغذی top4 که هموستاتیک در هر دو حس اختلال هستند. آبی: شیب رگرسیون خطی تقلیلی. قرمز: شیب رگرسیون خطی اکسیداتیو.
(D) شیب های رگرسیون خطی (متر) از 4 ماده مغذی هموستاتیک برتر در مفهوم اکسیداتیو NADH/NAD به علاوه اغتشاش.
تنظیمات متابولیک زیربنایی نمایه حضور یک فنوتیپ شبه هیپوکسیک مرتبط با رژیمهای NADH تقلیلی را نشان میدهد. این فنوتیپ یادآور برخی از متابولیسم های انرژی کم بازده ظاهرا متناقض است که در سرطان ها مشاهده شده است (اثر Warburg) و همچنین در سلول های مخمر (اثر Crabtree) و باکتری (متابولیسم سرریز) شناخته شده است (Basan et al., 2015; Mori et al., 2016؛ پاتر و همکاران، 2016). این احتمال که این رفتار میتواند ناشی از محدودیتهای تخصیص منابع ناشی از رشد نسبتاً بالا یا نرخ جذب گلوکز باشد، در سالهای اخیر مطرح شده است (باسان و همکاران، 2015؛ موری و همکاران، 2016). با این حال، فنوتیپ کاذب هیپوکسی که مشاهده می کنیم مستقل از سرعت رشد و جذب گلوکز است و در واقع با نرخ رشد پایین (روش های STAR) همزمان رخ می دهد. ما نشان دادهایم که علت آن در یک مبادله اساسی ATP/NADH نهفته است، منطقی که توسط یک مطالعه تجربی اخیر پشتیبانی میشود (Maldo-nado و Lemasters، 2014).
علاوه بر این، تجزیه و تحلیل شار ما نشان می دهد که نگهداری ATP می تواند به طور منفی تحت تاثیر NADH/NAD تقلیل دهنده به علاوه عدم تعادل قرار گیرد. تصور می شود افزایش NADH ارتباطی با کاهش در دسترس بودن ATP باشد، زیرا اختلال در فسفوریلاسیون اکسیداتیو ممکن است منجر به افزایش NADH/NAD پلاس و کاهش ATP/ADP شود. ما نشان میدهیم که عدم تعادل NADH که بهصورت بیرونی تولید میشود، میتواند دلیل کاهش در دسترس بودن انرژی از طریق مکانیسمهای متابولیک متعامد باشد، حتی در حالی که فسفوریلاسیون اکسیداتیو بیش از سطوح طبیعی کار میکند. این در زمینه تحقیقات پیری بسیار مهم است، زیرا کاهش در دسترس بودن انرژی و نسبت های ATP/ADP نشانه بارز پیری سلولی و آسیب شناسی های مرتبط با سن هستند (Moreira و همکاران، 2003؛ Pall، 1990؛ Yaniv و همکاران، 2013). و ممکن است با کاهش گردش پروتئین و در نتیجه افزایش نیمه عمر پروتئین، تجمع مواد زائد سمی و از دست دادن پروتئوستاز (یکی دیگر از علائم پیری) را افزایش دهد (Anisimova et al., 2018).
هدف ما در مرحله بعد تعیین اعتبار چارچوب خود به عنوان پیش بینی کننده طول عمر و متابولیت های رژیم غذایی است که عدم تعادل ردوکس را بافر می کند. Tolerance طول عمر سلولی را پیش بینی می کند، با برخی محدودیت ها به دلیل مجموعه داده های موجود. با کنترل این محدودیتها (Garay و همکاران، 2014)، متوجه میشویم که همبستگیهای حاصل هنوز شواهد کافی از رابطه بین واریانس تحمل و CLS هستند.
بر خلاف انتظارات ما، متمایزترین درسی که از تجزیه و تحلیل ما از متابولیت های رژیم گرفته می شود این است که ماده اصلی که پاسخ به عدم تعادل را هدایت می کند، به ویژه به شبکه نجات NADt متکی نیست. در واقع، "مواد مغذی هموستاتیک" برتر، واسطههای چرخه TCA و سایر بخشهای متابولیسم مرکزی هستند که عملکرد آنها بسیار بیشتر از پیشسازهای NAD است. علاوه بر این، ارتباط واکنشهایی که NAD(H) را کاهش یا اکسید میکنند، در حالی که به عنوان پل بین جفت ردوکس و مسیرهای متابولیکی اصلی عمل میکنند، بسیار برتر از آنزیمهای محدودکننده نجات NADt (مانند نیکوتین آمید مونونوکلئوتید آدنیل ترانسفراز) است.
به عنوان مثال، اگزالواستات و اکساگلوتارات در مدل مخمر در میان چهار متابولیت اصلی موثر در تحمل در هر دو شرایط احیا کننده و اکسیداتیو امتیاز می گیرند، یک ویژگی ثابت که نتایج تجربی قبلی را تایید می کند (چین و همکاران، 2014؛ ویلیامز و همکاران، 2009). . متابولیت های مهم دیگر عبارتند از هیدروکسی بوتیرات که به طور مداوم نشان داده شده است که طول عمر را افزایش می دهد، NAD را تنظیم می کند و پاسخ به گرسنگی را واسطه می کند (ادواردز و همکاران، 2014؛ نیومن و وردین، 2014)، و اسپرمیدین، که به خانواده پلی آمین ها تعلق دارد و شناخته شده است. در فرآیندهای مرتبط با سن، اتوفاژی و محافظت از DNA نقش دارند (ایزنبرگ و همکاران، 2009؛ مینویس و همکاران 2011: پیتروکولا و همکاران 2015).
ما از C.elegans و مدلهای انسانی برای تقویت ارزیابی قبلی استفاده کردیم و تصویر وسیعتری را نشان دادیم که حول هموستاز pH، زوجهای ردوکس و چرخه TCA متمرکز است. این نشان می دهد که راه هایی که در آن pH (برتنر و همکاران، 2009) و عدم تعادل NADH (آیر و همکاران، 2014) پیری در سلول ها را تعیین می کنند عمیقاً در هم تنیده هستند. فراتر از pH، فراگیرترین و مهم ترین مواد مغذی برای تنظیم NADH/NAD به علاوه عدم تعادل، اسیدهای آلفا کتو اگزالواستات و اگزگلوتارات، اشکال آمیخته آنها و سایر متابولیت های مرتبط با میتوکندری مانند مالات، پیرووات و فومارات هستند، یعنی هاب اصلی کنترل تعادل ردوکس چرخه TCA است.
تا به امروز، مکانیسمهایی که از طریق آن اسیدهای آمینه و واسطههای چرخه TCA بر افزایش طول عمر در مخمرها و C. elegans تأثیر میگذارند مبهم باقی ماندهاند. متابولیت هایی مانند مالات، اگزالواستات، فومارات، والین، سرین یا ترئونین در واقع می توانند طول عمر ارگانیسم ها را افزایش دهند، اما فرآیندهایی که منجر به این اثرات می شوند بحث و گفتگو و پیچیده هستند (ادواردز و همکاران، 2013، 2015). نتایج ما نشان میدهد که یک توضیح مشترک برای همه این پدیدههای افزایش طول عمر در اثر مواد مغذی بر ظرفیت سلولها برای تحمل اختلالات در نسبت NADH/NAD به علاوه نهفته است.
با این حال، می توان استدلال کرد که برخی از متابولیت های در نظر گرفته شده بدیهی به نظر می رسند زیرا در نهایت در واکنش هایی دخیل هستند که NADH و NAD پلاس را به یکدیگر تبدیل می کنند. سوال این است که چرا متابولیت های دیگری که به صورت پیشینی بدیهی به نظر می رسند در نتایج ما ظاهر نمی شوند. پاسخ در مکانیسم هایی نهفته است که پیش بینی های واقع بینانه در FBA را تضمین می کند. برای اینکه یک ماده مغذی "هموستاتیک" در برابر عدم تعادل ردوکس باشد، نه تنها باید تولید NADt NADHor را افزایش دهد، بلکه باید در مرکز یک مسیر یا مدول با بازده ATP/NADH و/یا ظرفیت بالا برای تامین مواد تشکیل دهنده زیست توده قرار گیرد.
در نهایت، دو بینش دیگر از نتایج ما قابل توجه است. از یک طرف، آنها پیشنهاد میکنند که در پاسخ به عدم تعادل ردوکس، شبکههای متابولیک به طور فزایندهای آماده تولید و/یا مصرف برخی متابولیتها هستند که توسط شبکههای سیگنالینگ بهعنوان جلوگیری از نیاز به اتوفاژی، آنتیاکسیدانی و پاسخهای هورمتیک، و همچنین بسیاری از متابولیتهایی که بیش از حد هستند، تفسیر میشوند. یا مشخص شده است که مکملها طول عمر را افزایش میدهند و/یا اثرات محدودیت کالری (CR) را به شیوهای وابسته به مسیرهای سیگنالی که در افزایش طول عمر با واسطه CR دخیل هستند، تقلید میکند. این شواهد قبلی را تقویت می کند که CR و تعادل NADH/NADH را به عنوان بخشی از یک فرآیند افزایش طول عمر و ارتقاء سلامت مرتبط می کند (Lin et al., 2004).
از سوی دیگر، مطالعه ما نشان می دهد که در پاسخ به نسبت های تغییر یافته، متابولیسم همچنین از مواد خاصی استفاده می کند که می توانند از نظر شیمیایی به سلول آسیب بزنند، مانند استات، پوترسین یا استالدئید. و همچنین برخی که می توانند از طریق سیم کشی مجدد متابولیک باعث ایجاد تومور شوند، مانند گلوتامین، سوکسینات و فومارات (Sciacovell et al., 2016). این میتواند تا حدودی آسیبشناسی مرتبط با عدم تعادل ردوکس و فرآیندهای ماکروسکوپی را توضیح دهد، مانند بیماریهای دژنراتیو و انکولوژیک: اگر عدم تعادل ردوکس باید با مواد سمی بافر شود، پس این مواد احتمالاً مکانیسمهایی از آسیبشناسی هستند که در آن نقش دارند. - با عدم تعادل ردوکس رخ می دهد.
ما متوجه میشویم که رویکرد ما به عدم تعادل ردوکس را میتوان به عنوان یک تغییر غیرمعمول از مطالعه استحکام شبکه متابولیک درک کرد و ممکن است هشدارهای خاصی را متهم کند که فضای زیادی برای بهبود باقی میگذارد. با توجه به استحکام، مطالعات با استفاده از FBA به طور سنتی آن را بهعنوان تغییر راهحل هدف (معمولاً رشد) در پاسخ به کاهشهای متفاوت در نرخهای واکنش تعریف میکنند، به عنوان مثال (ادواردز و پالسون، 2000)، به جای یک اختلال خاص (عدم تعادل ردوکس). ) در متابولیت ها همانطور که ما انجام می دهیم. با توجه به محدودیت های تجزیه و تحلیل ما، آنها را می توان به محدودیت های ذاتی خود FBA، مانند عدم وجود ژن های تنظیم کننده، مرتبط کرد. در نهایت، قابلیت اطمینان نتایج ما به قدرت پیشبینی بازسازیهای متابولیک بستگی دارد: مدلهای مخمر فعلی پیشبینیکننده و پیشرفته هستند، اما کامل نیستند (هونر و پرایس، 2015)، و با این حال، حتی از مدلهای دیگر بسیار بهتر هستند. بازسازی های چند سلولی دقیق موجود است. با وجود تمام این نگرانی ها، شواهد زیادی وجود دارد که وفاداری فزاینده مدل های متابولیک به رفتار طبیعی را تضمین می کند.
در حال حاضر، پژوهش غالب تمایل دارد که پیامدهای منفی بالقوه کاهش بی رویه نسبت NADH/NADH را نادیده بگیرد. این تا حدی به دلیل مزایای امیدوارکننده ناشی از کاهش خفیف بهدستآمده بهطور تجربی است که شامل کاهش فنوتیپهای نئوپلاستیک، طول عمر و افزایش طول عمر میشود. با این حال، شواهد نوظهوری وجود دارد که احتیاط شدید را در مورد این نتایج مثبت توصیه میکند (Gujarat al., 2016; Hong et al., 2019) و همچنین یک چارچوب نظری ثابت و پایدار تجربی که پیامدهای منفی ناشی از کاهش نسبت NADH/NADH را فراتر از آن پیشبینی میکند. یک آستانه (Aon et al., 2010). پروفایل های تحمل عدم تعادل NADH/NADt ما به این تصویر در حال ظهور پاسخ می دهد، زیرا انحرافات اکسیداتیو خفیف می تواند مفید باشد، اما موارد بالاتر به همان اندازه مضر هستند.
به طور خاص، پروفایل های تحمل ما نشان می دهد که علاوه بر ایجاد مشکلات شیمیایی یا فیزیولوژیکی، نسبت NADH/NADH پایین و بالا نیز باید با معایب صرفاً متابولیکی، از جمله کاهش در دسترس بودن انرژی و/یا بازده بیوسنتزی مواجه شود. علاوه بر این، و همانطور که اشاره کردیم، مشاهدات تجربی محدودی که در مورد برخی از سوالاتی که ما به آنها رسیدگی می کنیم، به نظر می رسد یادآور نتایجی است که در اینجا گزارش می کنیم.
محدودیت های مطالعه
نتایج ارائه شده در اینجا زمانی بهبود می یابد که مدل های به کار رفته بیشتر اصلاح شوند. کار ما همچنین از محدودیت های ذاتی FBA به عنوان یک تکنیک رنج می برد. به عنوان مثال، با توجه به اینکه نسخه های موجود در حال حاضر تجزیه و تحلیل شار پویا بسیار کاهش یافته اند، اطلاعات پویا به دست نمی آید. به طور مشابه، فقدان محدودیت های انرژی ضمنی در تعادل شار، پیش بینی آن را برای نرخ های رشد بالا کاهش می دهد. این ضعف انگیزه افزودن تکنیک هایی مانند CAFBA را فراهم کرده است، همانطور که در نسخه خطی در نظر گرفتیم. در نهایت، دسترسی به اطلاعات نظارتی که به راحتی قابل کنترل و روشن یا خاموش کردن است، جالب خواهد بود. در حال حاضر، هیچ رویکرد استانداردی برای اجرای تنظیم ژن در FBA وجود ندارد. استفاده از امتیاز فعالیت واکنش در محدوده محدودیت در این زمینه امیدوارکننده است.
این مقاله از iScience 24, 102697, 23 ژوئیه 2021 استخراج شده است.
