قرار گرفتن حاد پوست در معرض اشعه ماوراء بنفش باعث التهاب کلیه با واسطه نوتروفیل می شود
Mar 08, 2022
حساسیت به نور به اشعه ماوراء بنفش (UV) تا حدود 80 درصد از بیماران لوپوس را تحت تاثیر قرار می دهد. قرار گرفتن در معرض نور خورشید میتواند تظاهرات موضعی و همچنین سیستمیک لوپوس، از جمله نفریت را با مکانیسمهایی تشدید کند که ناشناخته هستند. در اینجا، ما گزارش میکنیم که قرار گرفتن در معرض حاد پوست در برابر نور UV باعث ایجاد پاسخ آسیب وابسته به نوتروفیل در پوست میشود. کلیه با بیان تنظیمشده مولکولهای چسبندگی اندوتلیال و همچنین نشانگرهای التهابی و آسیب مرتبط با پروتئینوری گذرا مشخص میشود. ما نشان دادیم که نور ماوراء بنفش مهاجرت نوتروفیل ها را نه تنها به پوست بلکه به پوست نیز تحریک می کندکلیهبه روشی وابسته به IL- 17. با استفاده از یک رویکرد ردیابی اصل و نسب فعال کننده نور، مشاهده کردیم که زیر مجموعه ای از نوتروفیل ها درکلیهاز پوست در معرض نور UV عبور کرده بود که نشان دهنده انتقال معکوس است. علاوه بر اینکه برای القای کلیوی ژنهای کدکننده میانجیهای التهاب (vcam{1}}، s100A9 و Il-1b) و آسیب (لیپوکالین-2 و kim-1) مورد نیاز است. نوتروفیل ها به طور قابل توجهی در ایجادکلیهامضای اینترفرون نوع I که توسط نور UV ایجاد می شود. با هم، این یافته ها نشان می دهد که نوتروفیل ها واسطه تحت بالینی هستندکلیهالتهاب و آسیب به دنبال قرار گرفتن پوست در معرض نور UV. جالب اینجاست که بیماران مبتلا به لوپوس دارای زیرجمعیتهایی از نوتروفیلهای خون و گرانولوسیتهای کم چگالی با فنوتیپهای مشابه به نوتروفیلهای انتقال معکوس هستند که در موشها پس از قرار گرفتن در معرض اشعه ماوراء بنفش مشاهده شد، که نشان میدهد این سلولها ممکن است از بافت ملتهب مانند پوست منتقل شده باشند.
کلید واژه ها:نور فرابنفش؛ مهاجرت نوتروفیل ها؛ کلیه; التهاب؛ کلیه

CISTANCHE عملکرد کلیه/کلیه را بهبود می بخشد
حساسیت به اشعه ماوراء بنفش (UV) نور خورشید یک ویژگی شناخته شده لوپوس اریتماتوز سیستمیک (SLE) است (1). قرار گرفتن پوست در معرض اشعه ماوراء بنفش باعث التهاب موضعی و سیستمیک می شود و با عود بیماری های سیستمیک، از جمله نفریت لوپوس (LN)، در بیماران SLE مرتبط است (2-4). اینکه چگونه حساسیت به نور در پوست منجر به تظاهرات سیستمیک می شود هنوز به خوبی شناخته نشده است. امضای ژن مشترک در پوست وکلیه هااز بیماران SLE (5) پاتوژنز شایع را نشان می دهد. ما اخیراً مشاهده کردیم که قرار گرفتن پوست در معرض نور UV باعث ایجاد پاسخ موضعی و سیستمیک اینترفرون نوع I (IFN-I) می شود (6)، که نشان می دهد پاسخ های التهابی به نور UV محدود به پوست نیست. دقیقاً قرار گرفتن پوست در معرض اشعه ماوراء بنفش چگونه بر روی پوست تأثیر می گذاردکلیهشناخته نشده است.
ما و دیگران نشان دادهایم که نور UV باعث نفوذ سریع نوتروفیلها به پوست میشود (6، 7). اگرچه نوتروفیلها عامل اصلی التهاب در محلهای آسیب موضعی هستند، اخیراً مشخص شده است که نوتروفیلها همچنین میتوانند محل ارگانهایی باشند که از محل اولیه التهاب (8 تا 10) دور هستند، جایی که از طریق تولید اکسیژن واکنشی به آسیب بافت ریه کمک میکنند. گونه ها (ROS) (11) یا سیستم ایمنی تطبیقی را در غدد لنفاوی و مغز استخوان فعال می کند (9، 12). در SLE، تصور می شود که نوتروفیل ها نقش مهمی در بیماری های موضعی و سیستمیک دارند. نوتروفیل ها در ضایعات پوستی بیماران SLE (13، 14) و درکلیهبافت بیماران مبتلا به LN (15، 16). بیان بالای یک امضای ژن نوتروفیل یک پیش بینی کننده قوی بیماری فعال، از جمله LN و شعله های پوستی است (17، 18). گرانولوسیت های کم چگالی پیش التهابی (LDGs) به ویژه در بیماران مبتلا به بیماری پوستی افزایش می یابد (19). در حالی که این یافتهها نوتروفیلها را در آسیب بافتی موضعی در SLE دخیل میدانند، آیا نوتروفیلها ارتباط بیماریزایی بین التهاب پوست وآسیب کلیهدرک نمی شود.
برای روشن شدن چگونگی تاثیر قرار گرفتن پوست در معرض اشعه ماوراء بنفشکلیهو نقش نوتروفیل ها در این فرآیندها، ما تغییرات را ارزیابی کردیمکلیهبیان ژن در هماهنگی با مهاجرت نوتروفیل ما دریافتیم که قرار گرفتن حاد پوست در معرض نور UV باعث تحریک فرآیندهای التهابی در پوست می شودکلیه،از جمله بیان مولکول های چسبندگی اندوتلیال، واسطه های التهابی، نشانگرهای آسیب و پروتئینوری گذرا. به طور قابل توجهی، ما متوجه شدیم که نوتروفیل ها به آن مهاجرت کردندکلیهپس از قرار گرفتن در معرض اشعه ماوراء بنفش به روشی وابسته به IL{0}}، که در نواحی لوله بینابینی (TI) که در آن فنوتیپهای پیش التهابی را نشان میدهند، قرار میگیرد. مسدود کردن قاچاق نوتروفیل توسط درمان با ایمونوگلوبولین ضد G-CSF (IgG) لغو شدکلیهالتهاب و جلوگیری از تنظیم بالا نشانگر آسیب لوله. این یافته ها با هم نشان می دهد که قرار گرفتن پوست در معرض اشعه ماوراء بنفش باعث تحریک تحت بالینی می شودکلیهفرآیندهای التهابی و آسیب ناشی از نوتروفیل ها.
نتایج
قرار گرفتن پوست در معرض نور UV باعث آسیب کلیوی تحت بالینی می شود.قرار گرفتن در معرض نور خورشید با تشدید علائم سیستمیک و بروز عود بیماری در بیماران SLE، از جمله نفریت همراه است (2-4). بنابراین، ابتدا پرسیدیم که آیا التهاب استریل حاد در پوست ناشی از یک بار قرار گرفتن در معرض اشعه ماوراء بنفش B (UVB) (500 mJ/cm2) در موشهای سیاه 6 (B6) منجر به تغییراتی در پوست میشود.کلیهاز جمله التهاب، آسیب و پروتئینوری (شکل 1A). ریه به عنوان یک عضو کنترل انتخاب شد، زیرا هیچ ارتباطی بین حساسیت به نور و بیماری بالینی ریه در SLE گزارش نشده است. مجموعاً 500 mJ/cm2 نور UVB در موشهای B6 به عنوان دو دوز حداقل اریتماتوز (20)، دوز مرجع مورد استفاده برای اعتراض انسان تعریف شده است (21). تجزیه و تحلیل بیان ژن پرفیوژنکلیه tissues (Fig. 1A) revealed up-regulation in the gene expression of adhesion molecules vcam- 1 and e-selectin on days 1 and 2 after UVB light exposure (Fig. 1 B and C). In contrast, vcam-1 and e-selectin expression demonstrated a downward trend in the lung (SI Appendix, Fig. S1). We also observed a >10-تا کنیدکلیهالقایی در s100A9، یک واسطه نوتروفیل مرتبط باآسیب کلیه(22)، و همچنین افزایش بیان s100A6، یک پروتئین متصل به کلسیم مرتبط با آسیب لوله ای (23) (شکل 1 D و E). در حالی که القای s100A9 در ریه تشخیص داده شد، بیان ژن s100A6 در ریه بدون تغییر باقی ماند (ضمیمه SI، شکل S1). پاسخ التهابی درکلیههمچنین با افزایش اولیه بیان il{0}} (روزهای 1 و 2 پس از UV) همراه بود، در حالی که در tnf یا il{3}} حداقل یا بدون تغییر وجود داشت (شکل 1F). بیان Il{5}} تا 6 روز پس از قرار گرفتن در معرض پوست در معرض نور UVB در ریه تشخیص داده نشد (ضمیمه SI، شکل S1). القای سریع در بیان cxcl12، یک کموکاین که توسط گلومرول ها و لوله ها ترشح می شود و درآسیب کلیوی(24)، نیز در یافت شدکلیهاما نه ریه (شکل 1G و ضمیمه SI، شکل S1). بنابراین، آسیب پوستی ناشی از نور UVB به سرعت ایجاد می کندکلیهفرآیندهای پیش التهابی، در حالی که تغییرات کمتری در ریه مشاهده می شود.

علاوه بر پاسخ پیش التهابی مشاهده شده درکلیه،هم پروتئینوری و هم نسبت آلبومین/کراتینین ادراری در چند روز اول پس از قرار گرفتن پوست در معرض نور UVB افزایش یافت (شکل 1 H و I). این اثر سریع برعملکرد کلیهبا تنظیم بالا در بیان لیپوکالین-2 وآسیب کلیهمولکول 1 (کیم{1}}) (شکل 1 J و K)، نشانگرهای لوله ایآسیب کلیهکه در LN نیز مشاهده می شود (25، 26). با وجود ماهیت گذرا پروتئینوری، بیان اینهاآسیب کلیهنشانگرها تا روز 6 باقی ماندند (شکل 1 J و K)، که احتمالاً منعکس کننده ترمیم بافت هستند.
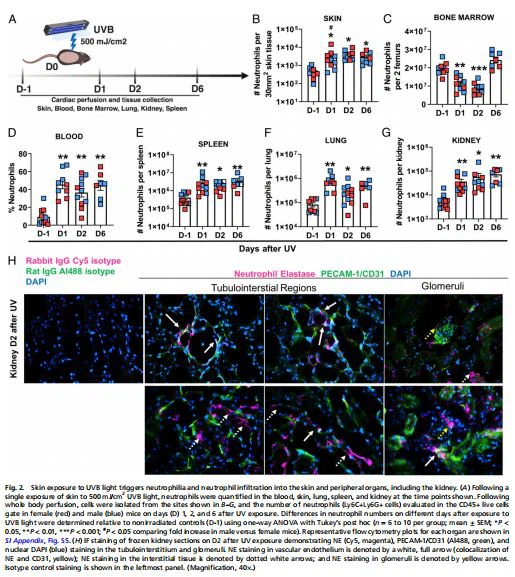
التهاب ناشی از نور UV در پوست منجر به مهاجرت نوتروفیل به کلیه می شود.برای بررسی اینکه آیا نوتروفیل ها در پاسخ التهابی سیستمیک به نور UVB شرکت می کنند، ما سینتیک تجمع نوتروفیل ها را در پوست تحت تابش اشعه UV و همچنین در طحال بررسی کردیم.کلیه،و ریه موش های C57BL/6 J (B6)، سویه ای که به بهترین وجه از تغییرات پوستی به نور UVB در پوست انسان تقلید می کند (شکل 2A) (27). به دنبال قرار گرفتن حاد پوست در معرض نور UVB، تعداد نوتروفیل ها در پوست در عرض 24 ساعت هفت برابر شد و در مقایسه با سطوح اولیه قبل از UV (D-1) به مدت 6 روز افزایش یافت (شکل 2B). این با کاهش تعداد نوتروفیل ها در مغز استخوان و افزایش پنج برابری نوتروفیل های خون در گردش در روزهای 1 تا 6 همراه بود (شکل 2 C و D). به طرز جالبی، در همان بازه زمانی، نوتروفیل ها در طحال، ریه وکلیه(شکل 2 E-G و پیوست SI، شکل S2A). سینتیک دقیق بین اندامها متفاوت بوده و در روز اول در ریه و روزهای 2 تا 6 در ریه به اوج خود میرسد.کلیهو طحال (شکل 2 E-G). درکلیه هانوتروفیلها عمدتاً در ناحیه لولههای بینابینی، از جمله عروق، که با رنگآمیزی نوتروفیل الاستاز (NE) در مجاورت با مولکول چسبنده پلاکت/سلول اندوتلیال (PECAM{1}}/CD31) یا کلوکالیزاسیون با آن مشخص میشود، موضعی دارند. ) (شکل 2H). تصاویر نشاندهنده در شکل 2H نوتروفیلها را در داخل یا اطراف عروق بینابینی (فلشهای سفید کامل) و در بینابینی (فلشهای سفید نقطهدار)، همراه با نوتروفیلهای گاه به گاه که در گلومرولها نیز یافت میشوند (فلشهای زرد) نشان میدهند. محلی سازی مشابه با رنگ آمیزی ایمونوفلورسانس anti-Ly6G (IF) تشخیص داده شد (ضمیمه SI، شکل S2B).
برای تعیین اینکه آیا سایر سلولهای ایمنی ذاتی پاسخهای موضعی و سیستمیک مشابه نوتروفیلها را نشان میدهند، توزیع مونوسیتها (CD11b به علاوه Ly6C به علاوه Ly6G-) را در همان نقاط زمانی پس از قرار گرفتن در معرض نور UVB بررسی کردیم. در حالی که مونوسیت ها نیز به داخل پوست جذب شدند، تنها تعداد کمی از مونوسیت های نفوذی در پوست شناسایی شدند.کلیهدر روز 6 پس از قرار گرفتن در معرض UVB (~2-برابر ~10.5-برابر افزایش درکلیهنوتروفیل ها) (شکل 2F و ضمیمه SI شکل، S3). هیچ افزایشی در تعداد مونوسیت ها در ریه یا طحال مشاهده نشد (ضمیمه SI، شکل S3)، که نشان می دهد پاسخ سیستمیک به آسیب UV نسبتاً انتخابی برای نوتروفیل ها بود.
نفوذ نوتروفیل ها به داخل پوست با تغییرات بافت شناسی همراه بود، از جمله التهاب زودرس درم و مرگ سلول های اپیدرمی (روزهای 1 و 2)، به دنبال آن ایجاد آکانتوز و هیپرکراتوز همراه با تشکیل پوسته سروسلولی در برخی موارد (روز 6) (SI) پیوست، شکل S4). قابل ذکر است، هیچ ضایعه پوستی باز پس از قرار گرفتن در معرض نور UVB ظاهر نشد، که نشان می دهد نفوذ سلول های ایمنی مشاهده شده در شرایط استریل رخ داده است، اگرچه نقش یک میکروبیوم پوست تغییر یافته را نمی توان رد کرد (20).
این یافتهها روی هم نشان میدهند که قرار گرفتن پوست در معرض یک دوز نور UVB، نوتروفیلها را هم به محل التهاب و هم به اندامهای داخلی، از جملهکلیه،همراه با نوتروفیلی خون در حالی که الگوهای مهاجرت کلی در موشهای نر و ماده مشابه بود، نفوذ نوتروفیل به پوست در مادهها در مقایسه با نرها سریعتر بود (شکل 2B). در مقابل، آسیب اپیدرم توسط نوار نوار منجر به مهاجرت نوتروفیل بهکلیهعلیرغم سطوح مشابه نفوذ نوتروفیل و پاسخ التهابی و آسیب بافتی که با قرار گرفتن در معرض اشعه ماوراء بنفش دیده می شود (ضمیمه SI، شکل S5)، که نشان می دهد انتشار سیستمیک نوتروفیل در همه اشکال آسیب پوستی استریل رایج نیست.

سیستانچ بیماری کلیوی/کلیوی را بهبود می بخشد
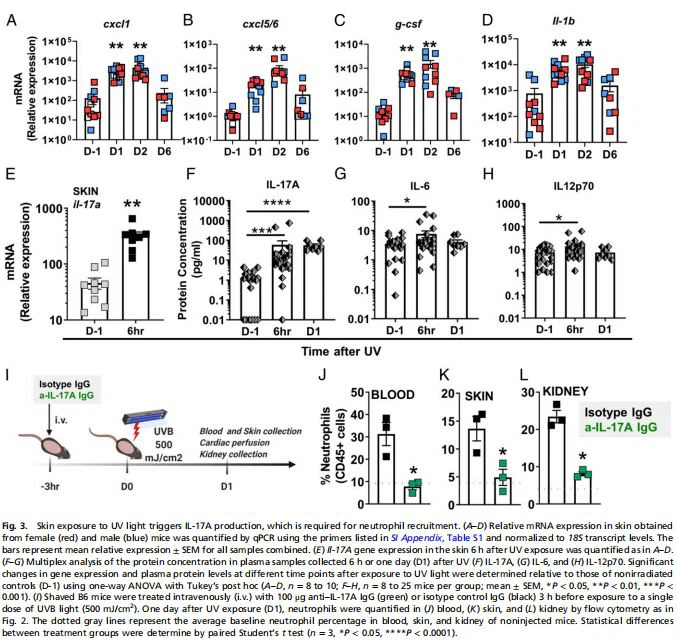
IL-17A جذب نوتروفیل را به دنبال قرار گرفتن پوست در معرض نور UV ترویج میکند.بررسی میانجیهای کموتاکتیک و التهابی در پوست نشان داد که بیان ژن کموکاینهای نوتروفیل و سیتوکینهای التهابی cxcl1، cxcl5/6، g-csf و il{5}} تا 2 روز پس از قرار گرفتن در معرض اشعه ماوراء بنفش افزایش قابلتوجهی دارد (شکل . 3 A-D). افزایش سریع و مداوم بیان s100A9 با سینتیک نفوذ نوتروفیل به پوست مطابقت داشت (شکل 2B و ضمیمه SI، شکل S6)، در حالی که سیتوکینهای il{12}}، tnf و il{13}} به طور موقت افزایش یافتند و تا روز 6 به بیان پایه بازگشتند (ضمیمه SI، شکل S6). در مقابل، il{16}}a فقط در روز 6 افزایش یافت (ضمیمه SI، شکل S6)، شاید منعکس کننده یک عملکرد ترمیمی باشد. حضور گذرا (1 تا 2 روز) مونوسیت ها در پوست (ضمیمه SI، شکل S3) به موازات افزایش تنظیم کموکاین های ccl4 و ccl2 اختصاصی مونوسیت بود (ضمیمه SI، شکل S6). مشابه تجمع نوتروفیلها در پوست موشهای ماده (شکل 2B)، تجمع مونوسیتها در پوست نیز در مادهها زودتر از نرها اتفاق افتاد (ضمیمه SI، شکل S3).
UV skin exposure was accompanied by rapid (6 h) 12-fold induction in il-17a gene expression in the skin (Fig. 3E) as well as >1،000-برابر کردن القای پوستی در بیان g-csf در روزهای 1 و 2 پس از UV (شکل 3C). برای تعیین اینکه آیا القای این سیتوکینها با بسیج نوتروفیل مرتبط است یا خیر، ابتدا غلظت پروتئین سیتوکین را در خون کمی کردیم، که افزایش قوی و پایدار (10- تا 100- برابر) در غلظت پلاسما را نشان داد. IL-176 تا 24 ساعت پس از قرار گرفتن در معرض نور ماوراء بنفش (شکل 3F)، همراه با افزایش گذرا (اوج در 6 ساعت) در IL-6 و IL-12، سیتوکین هایی که ممکن است پایین دست IL{15}}A (28) باشد (شکل 3 G و H). هیچ افزایشی در غلظت پلاسمایی IFN، GM-CSF، TNF، IL{19}}، IL{20}}، IL{21}}، یا IL1 مشاهده نشد. برای تعیین اینکه آیا IL{23}}A برای جذب نوتروفیل ناشی از UVB ضروری است، ما قبل از قرار گرفتن در معرض اشعه ماوراء بنفش، اثر IL{25}}A را با یک آنتی بادی خنثی کننده مسدود کردیم (شکل 3I). Anti-IL{27}}یک IgG به طور قابل توجهی نوتروفیلی خون (شکل 3J) را کاهش داد و هجوم نوتروفیل ها را به هر دو بافت پوست در معرض کاهش داد (شکل 3K و SI ضمیمه، شکل S7A) وکلیه(شکل 3L و پیوست SI، شکل S7B). این یافتهها نشان میدهند که استخدام نوتروفیل در پاسخ به اشعه ماوراء بنفش، حداقل تا حدی، توسط IL{2}}A انجام میشود.
نوتروفیل ها واسطه التهاب کلیه پس از قرار گرفتن پوست در معرض UV هستندسبک.برای تعیین اینکه آیا نوتروفیل ها مسئول تغییرات التهابی در هستند یا خیرکلیه following skin UVB light exposure, we blocked neutrophil recruitment prior to UV light exposure. Since cutaneous g-csf expression was up-regulated >1،000-بعد از قرار گرفتن در معرض اشعه ماوراء بنفش، نقش کموتاکتیکی را برای G-CSF در جذب نوتروفیل در پاسخ به نور UV نشان میدهد، ما با مسدود کردن G-CSF همانطور که در شکل 4A مشخص شده است، حرکت نوتروفیل را از مغز استخوان مهار کردیم. خنثی سازی G-CSF از نوتروفیلی خون و همچنین جذب نوتروفیل بهکلیهپس از قرار گرفتن پوست در معرض نور UVB (شکل 4 B و C). قابل توجه است، همانطور که قبلا در مدل های مختلف گزارش شده است (29، 30)، مسدود کردن G-CSF باعث تغییر تعداد مونوسیت ها درکلیه(شکل 4D). کاهش مهاجرت نوتروفیل ها بهکلیهبا کاهش قابل توجهی همراه بودکلیهبیان مولکول های چسبنده vcam-1 و e-selectin (شکل 4 E و F) و همچنین واسطه های التهابی s100A9 و il{5}} d پس از قرار گرفتن در معرض UVB (شکل 4 G و H). علاوه بر این، نشانگرهای آسیب بافتی لیپوکالین-2 و کیم-1 درکلیهدر موشهایی که در معرض نور UV قرار گرفتهاند، تحت درمان با آنتیبادی مسدودکننده G-CSF نسبت به حیوانات در معرض اشعه ماوراء بنفش تحت درمان با ایزوتیپ کاهش یافت (شکل 4 I و J). همانطور که قبلا گزارش کردیم (6)، قرار گرفتن پوست در معرض نور UVB باعث واکنش اینترفرون نوع I درکلیه(شکل 4K). مسدود کردن G-CSF به طور قابل توجهی امتیاز IFN را کاهش داد، اما به طور کامل لغو نکرد (شکل 4K). در حالی که وجود نوتروفیل ها درکلیهبرای پاسخ های التهابی و آسیب حاد مشاهده شده 1 روز پس از قرار گرفتن در معرض اشعه ماوراء بنفش پوست مورد نیاز بود (شکل 4)، هیچ تفاوتی در پروتئینوری در این زمان مشاهده نشد، زیرا اوج پروتئینوری در حدود روز 4 پس از قرار گرفتن در معرض UV رخ داد (شکل 1 H و من). این داده ها با هم نشان می دهد که نوتروفیل ها مسئول پاسخ التهابی هستند و به طور مستقیم یا غیرمستقیم در القای اینترفرون نوع I درکلیهبه دنبال قرار گرفتن در معرض اشعه ماوراء بنفش پوست مشابه نتایج بهدستآمده با IgG ضد G-CSF، تجویز آنتیبادی خنثیکننده ضد IL{1}} تا حدی مهاجرت نوتروفیلها را سرکوب کرد.کلیهو منجر به کاهش بیان ژن شدکلیهنشانگرهای التهابی (vcam-1 و s100A9) و آسیب (lipocalin-2 و kim-1)، اگرچه فقط کاهش بیان کیم-1 از نظر آماری معنیدار بود (ضمیمه SI، شکل S7 C–F)
یک زیرجمعیت از نوتروفیل های کلیه به طور معکوس منتقل می شود، یک فنوتیپ که همچنین در خون بیماران SLE شناسایی شده است.در حالی که مدتها تصور میشد که نوتروفیلهایی که وارد محلهای عفونت یا التهاب استریل میشوند متعاقباً تحت آپوپتوز قرار میگیرند و به سرعت توسط ماکروفاژها حذف میشوند، تعدادی از مطالعات نشان دادهاند که برخی از نوتروفیلها به صورت دوطرفه تردد میکنند، یعنی پس از ورود به بافت، انتقال مییابند. به جریان خون برگشته و به مکان دیگری نفوذ می کند، فرآیندی که به آن انتقال معکوس (rTEM) گفته می شود (8، 10، 11، 31-34). برای بررسی اینکه آیا نوتروفیلهایی که در خانه قرار دارند یا خیرکلیهپس از قرار گرفتن پوست در معرض نور UVB که از طریق پوست در معرض گذر قرار گرفت، مهاجرت نوتروفیل ها را در یک مدل موش B6 فعال کننده نوری (پروتئین فلورسنت سبز رنگ یوبیکوئیتین C [UBC]-photoactivated [PA] [GFP]) مورد مطالعه قرار دادیم.
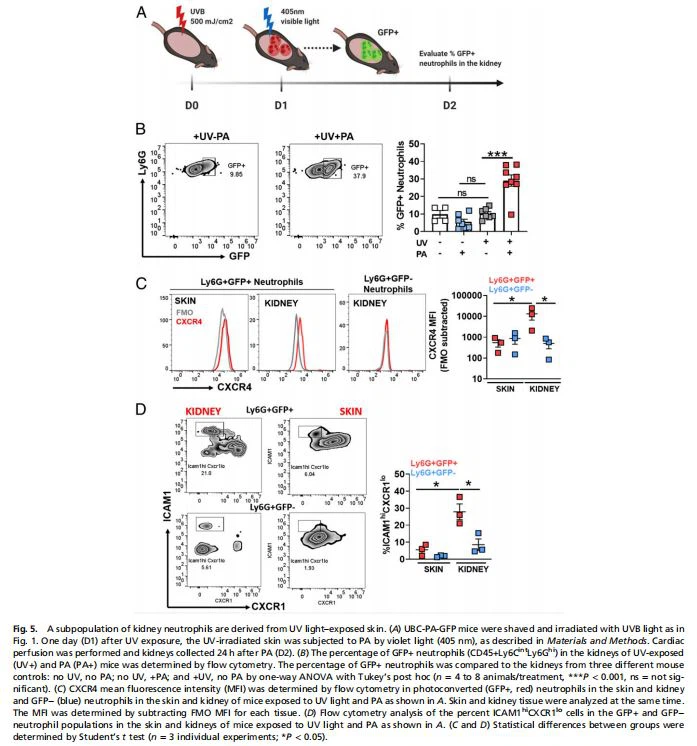
طرح تجربی در شکل 5A نشان داده شده است. 1 روز پس از قرار گرفتن پوست در معرض یک دوز نور UVB، پوست در معرض نور بنفش (405 نانومتر) قرار گرفت به طوری که سلولهای ایمنی نفوذی به سلولهای GFP مثبت تبدیل شدند. سپس نوتروفیل های تبدیل شده به نور (GFP به علاوه Ly6G پلاس) در پرفیوژن اندازه گیری شدند.کلیه هاروز بعد. آنالیز فلوسایتومتری نشان داد که حدود 20 درصد از نوتروفیل های نفوذ کننده کلیه پس از تفریق سیگنال پس زمینه (تقریبا 10 درصد) GFP مثبت بودند (شکل 5B). برخلاف مدلهای التهاب استریل در کبد یا عضله کرمستر (8، 10)، ما نوتروفیلهای تبدیلشده نوری را در ریه شناسایی نکردیم، احتمالاً به این دلیل که تعداد کمی نوتروفیل در ریه در روز 2 یافت شد (شکل 2F). برای آزمایش اینکه آیا GFP به اضافه نوتروفیل درکلیهخارج شده از بافت پوست در معرض اشعه ماوراء بنفش یا PA داخل عروقی، ما تغییرات در تعداد GFP به اضافه نوتروفیل های بدست آمده ازکلیه هااز موش هایی که همان پوستی که در معرض اشعه ماوراء بنفش قرار گرفته بود یک روز بعد PA با نور بنفش بود (گروه I) در مقابل موش هایی که پوست مجاور آن قرار گرفتن در معرض نور UV یک روز بعد با نور بنفش PA بود (گروه دوم، نمودار در پیوست SI، شکل S8A). اگرچه تفاوتی در درصد نوتروفیل های در گردش بین گروه ها وجود نداشت (ضمیمه SI، شکل S8B)، افزایش بیشتر در GFP به اضافه نوتروفیل ها در گروه ها مشاهده شد.کلیه هااز موش هایی که پوست در معرض اشعه ماوراء بنفش نیز PA (گروه I) بود در مقایسه با عدم افزایش GFP به علاوه نوتروفیل در موش هایی که پوست در معرض اشعه ماوراء بنفش PA (گروه II) بود (ضمیمه SI، شکل S7B). در گروه دوم، تعداد نوتروفیلها مشابه پسزمینه مثبت بودن GFP بود که در شکل 5B (ضمیمه SI، شکل S8B) دیده میشود.
در حالی که سطوح پایین GFP plusکلیهنوتروفیلهای گروه دوم نشان میدهند که نور بنفش سلولهای گردشکننده PA را در پوستی که در معرض اشعه ماوراء بنفش قرار نمیگیرد، انجام نمیدهد.کلیهدسترسی داشته باشید. برای تعیین نسبتهای نسبی نوتروفیلهای TEM، بیان نشانگرهای سطحی مورد استفاده برای مشخص کردن نوتروفیلهایی که تحت rTEM قرار گرفتند را کمی کردیم: CXCR4hi (8) و ICAM1hiCXCR1lo (11، 35). در واقع، GFP پلاسکلیهنوتروفیل ها سطوح بالاتری از CXCR4 را در مقایسه با GFP به اضافه نوتروفیل ها در پوست یا نوتروفیل های GFP- در پوست بیان کردند.کلیه(شکل 5C). از

علاقه،کلیهبیان لیگاند CXCR4، cxcl12، 1 تا 2 روز پس از مواجهه پوست با نور UVB همزمان با حضور نوتروفیل های CXCR4hi درکلیه(شکل 1G)، احتمالاً محرک کموتاکتیکی را برای جذب این نوتروفیل ها در کلیه فراهم می کند. جالب توجه است، ما نوتروفیلهای CXCR4hi و ICAM1- hiCXCR1lo را در اواخر پس از قرار گرفتن در معرض اشعه ماوراء بنفش در مغز استخوان شناسایی کردیم (روز 6، ضمیمه SI، شکل S9 B و C)، که نشان میدهد برخی از این نوتروفیلها نیز به مغز استخوان بازمیگردند. مغز استخوان مشابه آنچه برای rTEM به دنبال آسیب کبدی یا عفونت ویروسی پوست گزارش شده است (12، 36). مطابق با این مشاهدات، ما بیان CXCR4 بالاتری را در نوتروفیلهای خون در روز دوم پس از قرار گرفتن در معرض اشعه ماوراء بنفش شناسایی کردیم، که احتمالاً سلولها را در مسیر به سمتکلیهو مغز استخوان (ضمیمه SI، شکل S9D). به طور مشابه، درصد قابل توجهی بیشتری از سلول های ICAM1hiCXCR1lo در میان GFP به علاوه نوتروفیل ها درکلیهدر مقایسه با GFP به علاوه نوتروفیل در پوست و GFP- نوتروفیل در پوستکلیه(شکل 5D). فنوتیپ ICAM1hiCXCR1lo بر روی 20 تا 35 درصد از GFP به علاوه نوتروفیل ها درکلیه(شکل 5D)، نشان می دهد که زیرمجموعه ای از نوتروفیل ها به سمتکلیهاز طریق پوست در معرض اشعه ماوراء بنفش این کار را با انتقال معکوس انجام دهید، در حالی که بقیهکلیهنوتروفیل ها احتمالاً در هنگام گردش در پوست ملتهب در معرض اشعه ماوراء بنفش فعال می شوند. زیرجمعیت نوتروفیل ICAM1- hiCXCR1lo نیز درکلیه هاموشهای B6 معمولی که در معرض نور UV قرار گرفتند و PA دریافت نکردند (ضمیمه SI، شکل S9A).
در حالی که هر دو فنوتیپ نوتروفیل CXCR4hi و ICAM1hiCXCR1lo با عملکردهای التهابی و آسیب بافتی در مدلهای مختلف موش همراه بودهاند (11، 31، 37)، مطالعات کمی روی این جمعیتهای سلولی در بیماریهای انسانی انجام شده است. با توجه به نقش نوتروفیل ها در SLE (13، 17، 18) و ناهمگنی ظاهری آنها (19)، ما بررسی کردیم که آیا سلول های پلی مورفونوکلئر با چگالی طبیعی (PMNs) یا LDGs از بیماران SLE
فنوتیپ های مهاجرت معکوس را نشان داد: CXCR4hi (37، 38) و ICAM1hiCXCR1lo. پروفایل فلوسیتومتری PMN و LDG بیان CXCR4 بالاتری را در سطح این سلول ها در بیماران SLE در مقایسه با افراد سالم نشان داد (شکل 6 A و C). علاوه بر این، درصد کوچک اما به طور قابل توجهی بالاتری از ICAM1hiCXCR1lo PMNs در خون SLE (میانگین، 3.5 درصد) نسبت به افراد سالم (میانگین، 1.4 درصد) یافتیم (شکل 6B). جالب توجه است که جمعیت نوتروفیل LDG (CD15 به علاوه CD14loCD10 به علاوه در سلولهای تک هستهای خون محیطی [PBMCs]) حاوی درصد بیشتری از سلولهای ICAM1hiCXCR1lo نسبت به PMN در خون سالم (میانگین 7.1 درصد) و خون SLE (میانگین، 29 درصد) بود (شکل 29). . 6 B و D). جمعیت مشابه rTEM به طور قابل توجهی در LDGهای بیماران SLE نسبت به افراد سالم بیشتر نشان داده شد (شکل 6D). این دادهها حضور فنوتیپهای نوتروفیل مانند rTEM را در PMN و بهویژه LDGs در بیماران SLE شناسایی میکنند.
بحث
اثرات سیستمیک قرار گرفتن پوست در معرض اشعه ماوراء بنفش به خوبی درک نشده است. شناسایی این مسیرها در شرایط پایه طبیعی ممکن است مکانیسمهای درگیری بافت سیستمیک پس از قرار گرفتن در معرض نور خورشید را که در بیماریهایی مانند SLE رخ میدهد، اطلاع دهد (2-4). در اینجا، چندین یافته در مورد چگونگی تأثیر قرار گرفتن در معرض نور خورشید بر کلیه ها را گزارش می کنیم. اول، ما نشان دادیم که قرار گرفتن پوست در معرض نور UVB باعث ایجاد پاسخ های التهابی و آسیب در پوست می شود.کلیه،از جمله پروتئینوری تحت بالینی. جالبه ایناکلیهتغییرات با نفوذ نوتروفیل به کلیه به دنبال التهاب پوستی ناشی از نور UVB همراه بود. پاسخ نوتروفیل به IL-17A و G-CSF وابسته بود. نوتروفیلها در کلیه دارای فنوتیپهای پیشالتهابی بودند، همانطور که بوسیله محلیسازی خارج سلولی NE مشهود است، نسبت بیشتری از rTEM (CXCR4hi) که بهعنوان سلولهای پیر و ICAM1hiCXCR1lo نیز شناخته میشود. نوتروفیل ها به طور مستقیم در تحت بالینی دخیل بودندآسیب کلیه،به عنوان کاهش نوتروفیل منجر به کاهش قابل توجهی در بیان مولکول های چسبندگی، سایتوکین های التهابی، امضای IFN-I و نشانگرهای آسیب کلیه پس از قرار گرفتن در معرض UV پوست شد.
سایر انواع آسیب های پوستی، مانند برداشتن نوار و استفاده موضعی از آگونیست TLR7، گزارش شده است که باعث افزایشآسیب کلیهدر برخی از مدلهای لوپوس، اگرچه تصور میشد که افزایش بیماری توسط ماکروفاژها و سلولهای دندریتیک به جای نوتروفیلها انجام میشود (39، 40). پس از نشان دادن که سلب نوار منجر به استخدام نوتروفیل بهکلیه، ما پیشنهاد می کنیم که قرار گرفتن در معرض اشعه ماوراء بنفش با سایر انواع التهاب پوستی استریل متفاوت است. این ممکن است با تولید محصولات نوری یا واسطههای التهابی منحصربهفرد پس از آسیب اشعه ماوراء بنفش که کلیه را برای التهاب آماده میکنند، با تفاوت در حذف نوتروفیلها پس از اشعه ماوراء بنفش در مقایسه با حذف نوار یا عوامل دیگر توضیح داده شود. مشاهده کردیم که نور ماوراء بنفش باعث القای سریع و قوی il{0}}یک RNA پیام رسان (mRNA) در پوست همراه با سطح پروتئین IL{1}}A در گردش بالا (~~برابر افزایش) ، که برای جذب نوتروفیل پس از قرار گرفتن در معرض نور UV مورد نیاز بود. القای همزمان 100- تا 1000-در بیان g-csf پوست نشان میدهد که محور IL-17A/G-CSF مکانیسم احتمالی مسئول نوتروفیلی و بافت نوتروفیل است. در پاسخ به نور UV نقش IL{9}}A در تنظیم گرانولپوئز و جذب نوتروفیل از طریق القای G-CSF در شرایط هموستاتیک به خوبی شناخته شده است و مطالعات اندکی IL{11}}A را برای جذب نوتروفیل در مکانهای مهم شناسایی کردهاند. التهاب استریل (41، 42). در لوپوس، افزایش IL{14}}یک بیان در ضایعات جلدی (43) یافت میشود، و افزایش سطح IL{16}}A در گردش با تظاهرات بدتر بیماری همراه است (44)، اگرچه رابطه خاص با نوتروفیلها، یک جمعیت بیماری زا در این بیماری (13، 17، 18)، ناشناخته باقی مانده است. علاوه بر اثرات مستقیم آن بر حرکت نوتروفیلها از مغز استخوان به واسطه G-CSF، IL{22}}A همچنین ممکن است به انتقال نوتروفیل به مغز کمک کند.کلیهبا تحریک بیان مولکول های چسبنده (مانند VCAM{0}} و E-Selectin) رویکلیهاندوتلیوم (45، 46).
با استفاده از همان مدل قرار گرفتن در معرض اشعه ماوراء بنفش حاد، اخیراً گزارش دادیم که یک دوز واحد نور UV باعث ایجاد یک پاسخ موضعی و سیستمیک IFN-I می شود که برای جذب کارآمد نوتروفیل به پوست مورد نیاز است (6). از آنجایی که نشان داده شده است که IFN-I تولید IL{3}A (47) را القا می کند، قابل قبول است که این مسیرها به طور مستقل یا هماهنگ منجر به جذب نوتروفیل و مهاجرت با واسطه نور UV شود که در اینجا گزارش می کنیم. در حالی که یافتههای ما نقش التهابی IL را نشان میدهد، اثرات سرکوبکننده نور UVB روی IL-17پیش از این در پسوریازیس یک سیگنالدهی گزارش شده بود، جایی که قرار گرفتن پوست پسوریازیس در معرض نور UVB باعث حذف سلولهای T بیماریزا و سلول های دندریک التهابی میلوئید (48، 49). از آنجایی که پوست پسوریاتیک، برخلاف پوست سالم، سرشار از سلولهای T تولیدکننده و پاسخدهنده IL است، تفاوت در ترکیب سلولی احتمالاً پاسخ به نور UVB، از جمله میزان سرکوب IL به واسطه نور UVB را تعیین میکند. -17یک بیان گیرنده (50). دوز UV همچنین ممکن است تعیین کند که آیا اثر التهابی یا درمانی رخ می دهد: دوزهای پایین با پیامدهای ضد التهابی و سرکوب کننده سیستم ایمنی همراه است (51)، احتمالاً با مهار پاسخ سلول های CD8 T (52).
نوتروفیل ها نقش های متعددی را در طول التهاب بافت ایفا می کنند. هنگامی که نوتروفیل ها توسط الگوهای مولکولی مرتبط با پاتوژن و الگوهای مولکولی مرتبط با آسیب (DAMPS) یا با درگیری گیرنده فعال می شوند، نوتروفیل ها مستقیماً با آزاد کردن پروتئازها، ROS و اکستروژن تله های خارج سلولی نوتروفیل (NETs) به آسیب بافت کمک می کنند (53، 54). نوتروفیل ها همچنین می توانند با فاگوسیتوز بقایای سلولی و با فعال کردن عروق مجدد بافت، ترمیم بافت را افزایش دهند (8). در SLE، امضای ژن نوتروفیل یک پیش بینی کننده قوی بیماری فعال از جمله LN و لوپوس جلدی است (17، 18). نوتروفیل ها در ضایعات جلدی (13، 14) و همچنین یافت می شوندکلیهنمونه های بیوپسی (15، 16) از بیماران SLE و خواص التهابی آنها تا حدی به تشکیل NET نسبت داده شده است (16). این فرآیند شامل افزایش تولید ROS (55)، آزادسازی DNA میتوکندریایی (55)، و آزادسازی و القای پروتئین های التهابی، مانند s100A9 (56)، IL{8}}b (57)، و اینترفرون های نوع I (55) است. ، 58). یافته های ما مبنی بر اینکه مهار مهاجرت نوتروفیل به کلیه، s100A9 را لغو کرد و به طور قابل توجهی بیان IL{14}}b وکلیهامتیاز IFN نشان می دهد که عملکردهای التهابی مشابهی ممکن است در بازی وجود داشته باشد. مربوط به بیماری کلیوی در SLE، نوتروفیل ها عمدتاً در اندوتلیوم TI، محل افزایش بیانآسیب کلیهنشانگرهای کیم-1 و لیپوکالین-2 در بافت کلیه LN (59،60). پروتئینوری می تواند به دلیل نفوذپذیری بیش از حد سد گلومرولی به پروتئین ها به دلیل اختلال در جذب مجدد پروتئین توسط لوله ها یا ترکیبی از این مکانیسم ها ایجاد شود (61). آسیب TI در بیماران SLE یک یافته پاتولوژیک مکرر در کلیه های LN است، از جمله آنهایی که آسیب گلومرولی خفیف دارند (61، 62). نشان داده شده است که آسیب TI شدت LN را پیش بینی می کند (63، 64)، اما مکانیسم های ایجاد کننده آن ناشناخته است. از آنجایی که افزایش کیم-1 و لیپوکالین-2 نشانگرهای شناخته شده آسیب TI در SLE هستند (26، 65) و مانع مهاجرت نوتروفیل بهکلیهبا مهار بیان آنها، ما پیشنهاد می کنیم که پروتئینوری گذرا مشاهده شده پس از قرار گرفتن در معرض اشعه ماوراء بنفش نتیجه التهاب TI تحت بالینی با واسطه نوتروفیل است (65). افزایش بیان vcam{2}} کلیه، نشانگر دیگری از آسیب TI در SLE (66)، بیشتر از این مدل پشتیبانی می کند.
علاوه بر انتشار التهاب در محلهای آسیب استریل یا عفونی، نوتروفیلها در محل ارگانهای دوردست هستند (8-10)، جایی که بسته به زمینه، از طریق تولید ROS (11) به آسیب بافت کمک میکنند یا فعال میشوند. سیستم ایمنی سازگار در غدد لنفاوی و مغز استخوان (9، 12). ماهیت التهابی این نوتروفیل ها به توانایی آنها برای خروج از محل اولیه آسیب و مهاجرت به مکان های ثانویه، یعنی تحت rTEM نسبت داده شده است (9-11، 31-34). یافته های ما مبنی بر اینکه PA سلول های حاوی GFP در پوست به دنبال قرار گرفتن در معرض اشعه ماوراء بنفش منجر به شناسایی GFP به علاوه نوتروفیل ها در پوست شد.کلیهبا فنوتیپ rTEM نشان می دهد که یک زیرجمعیت ازکلیهنوتروفیل ها معکوس از پوست در معرض اشعه ماوراء بنفش مهاجرت می کنند (GFP به علاوه نوتروفیل ها 20 درصد از پوست را تشکیل می دهند.کلیهنوتروفیل ها و 20 تا 35 درصد از آنها rTEM هستند. بنابراین، rTEM 4 تا 7 درصد از کل را تشکیل می دهدکلیهنوتروفیل ها). این نسبت rTEM با نسبت گزارش شده پس از آسیب استریل کبد (9 درصد) (36) و آسیب ایسکمی-پرفیوژن مجدد (تقریباً 8 درصد) قابل مقایسه است (11). rTEM در شرایط دیگر نشان داده است که پیش التهابی است (10، 11) و آپوپتوز را مختل می کند (35) که منجر به این احتمال می شود که آنها در ایجاد UV نقش داشته باشند.آسیب کلیهبیان CXCR4 بالا در این نوتروفیل ها به طور خاص مرتبط است، به عنوان یک تصادفکلیهبیان cxcl12، یک لیگاند CXCR4 که توسط پودوسیتها و توبولها بیان میشود (24)، مشاهده شد که احتمالاً یک سیگنال کموتاکتیک برای این جمعیت نوتروفیل ارائه میکند. افزایش بیان CXCR4 در سلول های ایمنی همراه با سطوح بالایکلیهCXCL12 در بیماران SLE مبتلا به LN شناسایی شده است (67)، و این مسیر در لوپوس و همچنین ایسکمی-پرفیوژن مجدد نقش دارد.آسیب کلیهدر موش ها (24، 68). علاوه بر اینکه نشانگر rTEM است، افزایش بیان CXCR4 همچنین نشانگر نوتروفیلهای "پیر" است که میتواند واکنشهای التهابی آسیبرسان به بافت را واسطه کند (38). نقش دقیق CXCR4 در جذب نوتروفیل بهکلیهرا می توان با تضاد CXCR4 همانطور که قبلا در مدل های دیگر آسیب استریل انجام شده بود بررسی کرد (38).

مهاجرت نوتروفیل های بافت خاص و مکانیسم های مسئول بیان متفاوت مولکول های چسبندگی در اندام های مختلف به خوبی شناخته نشده است (69). سطوح بالاتر بیان کموکاین cxcl12 درکلیهاما نه ریه می تواند حضور ترجیحی نوتروفیل های CXCR4hi در کلیه را توضیح دهد. علاوه بر این، القای بیان vcam-1 و e-selectin در کلیه، در مقایسه با عدم تغییر در بیان در ریه، احتمالاً به جذب و حفظ نوتروفیل ترجیحی در کلیه کمک میکند. افزایش 5- تا 6- برابری بیان s100A9 در ریه در مقایسه با افزایش 30- تا 60- برابری در کلیه و همچنین افزایش 6- برابری بیان il{10}}b در ریه در مقایسه با 16-برابر افزایش در کلیه بیشتر نشان دهنده تفاوت بافتی در پاسخ التهابی است. کاهش انفیلتراسیون نوتروفیل کلیه به دنبال خنثی سازی G-CSF را می توان به کاهش تعداد گردش خون و فعال شدن نوتروفیل ها و همچنین کاهش بیان موضعی vcam{13}} و e-selectin نسبت داد. با این حال، نمیتوانیم مطمئن باشیم که آیا تنظیم اولیه این مولکولهای چسبندگی به دنبال قرار گرفتن در معرض اشعه ماوراء بنفش پوست به سیتوکینها/DAMPS مشتق از پوست نسبت داده میشود یا اینکه نوتروفیلها، از طریق انتشار پروتئازهای سرین، مستقیماً به بیان آنها کمک میکنند، همانطور که در موارد دیگر نشان داده شده است. زمینه ها (70). صرفنظر از مکانیسمها، و با توجه به اینکه ما تجزیه و تحلیل جامعی از همه بافتها انجام ندادهایم، مطالعات ما شواهدی برای انتخاب برخی ارگانها در اثرات سیستمیک ناشی از نور UV ارائه میدهد. مطالعات آتی به پیامدهای عملکردی بافتی انتشار سیستمیک نوتروفیل توسط، به عنوان مثال، نشت آلبومین عروقی و تشکیل ادم در ریه می پردازد (11، 36).
در بیماران مبتلا به SLE، ارتباط صریح قرار گرفتن در معرض اشعه ماوراء بنفش پوست با تشدید بیماری سیستمیک دشوار است، زیرا تغییرات قابل توجهی (1 تا 3 هفته) در پاسخ های حساس به نور قابل مشاهده در افراد مختلف وجود دارد (21). علاوه بر این، تحت بالینیآسیب کلیهممکن است تا زمانی که قرار گرفتن در معرض متوالی در معرض اشعه ماوراء بنفش اثرات را تشدید کند، به راحتی از دست می رود. در حالی که ما متوجه شدیم که نوتروفیل واسطه استالتهاب کلیهدر پاسخ به نور UV باعث بیماری بالینی در موشهای سالم نمیشود، چنین مکانیسمی ممکن است به طرق مختلف در شرارههای LN در بیماران لوپوس حساس به نور نقش داشته باشد. درگیر شدن گیرنده Fc توسط کمپلکس های ایمنی می تواند جذب نوتروفیل را افزایش دهد و منجر به آزادسازی ROS و پروتئاز شود (71). افزایش ظرفیت نوتروفیل های لوپوس و LDG ها برای تولید NET ها، که در بیماران SLE به طور موثر پاک نمی شوند (72)، می تواند منجر به آزاد شدن پروتئازهای آسیب رسان به بافت شود (73)، انتشار پاسخ IFN-I (58). ، یا آسیب مستقیم بهکلیهاندوتلیوم با ایجاد آسیب عروقی و نشت (16). علاوه بر این، تفاوتهای اساسی در پوست لوپوس، مانند افزایش سیگنالدهی IFN-I (5، 74) و نقص در جمعیت سلولهای محافظ لانگرهانس (75)، میتواند میزان و ماهیت پاسخهای سیستمیک با واسطه نوتروفیل را نشان دهد. ردیابی مهاجرت نوتروفیل همراه با بازجویی از اتوآنتی بادی ها، تجمع سلول های آپوپتوز و سطوح کم کمپلمان را می توان با استفاده از مدل های جدید لوپوس، مانند جهش یافته های سه گانه (Sle1.Mfge8-/- C1q-/- و Sle1.Mfge8-) بررسی کرد. /−C3−/−) (76) یا سایر سویههای لوپوس به دنبال قرار گرفتن در معرض نور UV.
مکانیسمهای دقیقی که نوتروفیلها را به التهاب در SLE مرتبط میکند، ممکن است تحت تأثیر فنوتیپ نوتروفیل/LDG باشد، زیرا ناهمگنی در این جمعیتها آشکارتر شده است (77). یافته های ما در مورد افزایش جمعیت CXCR4 و ICAM1hiCXCR1lo (rTEM) در گردش، به ویژه در SLE LDG، به این ناهمگنی بیشتر می افزاید و نشان می دهد که برخی از گرانولوسیت های پیش التهابی در خون ممکن است "تجربه بافتی" قبلی داشته باشند، یعنی اقامت در قبل از انتشار سیستمیک، بافت های اندام آسیب دیده، مانند پوست. فنوتیپهای rTEM قبلاً در مایع سینوویال و نوتروفیلهای در گردش بیماران آرتریت روماتوئید (35، 78) و در آسیب ریه مرتبط با پانکراتیت حاد (79) گزارش شدهاند. نقش آنها در SLE مستلزم بررسی بیشتر است.

سیستانچ درد کلیه/کلیه را بهبود می بخشد
مواد و روش ها
موش.تمام آزمایشهای حیوانی توسط کمیته مراقبت و استفاده از حیوانات در دانشگاه واشنگتن، سیاتل تأیید شد. آزمایشهای اولیه با استفاده از موشهای C57BL/6J نر و ماده (آزمایشگاه جکسون، 3 تا 4 ماهه، شکلهای 1 و 2) انجام شد. برای تمام آزمایشات بعدی از موش های ماده استفاده شد. مطالعات PA روی B6 انجام شد. موش ماده Cg-Ptprc Tg(UBC-PA-GFP)1Mnz/J (آزمایشگاه جکسون، 3 تا 4 ماهه). این موش ها با تزریق یک وکتور تراریخته حامل PAGFP (نوعی T203H) تحت کنترل رونویسی پروموتر یوبیکوئیتین C انسانی به جنین C57BL/6 تولید شدند. حیوانات در شرایط عاری از بیماریزا قرار گرفتند و در چرخههای نور تا تاریکی 12 ساعته با دسترسی آزادانه به غذا و آب نگهداری شدند. آزمایشها بر روی همه حیوانات در زمان مشخصی از روز انجام شد تا از تأثیر ریتم شبانهروزی بر مهاجرت نوتروفیل جلوگیری شود (38).
قرار گرفتن در معرض نور UVB و نوار چسب.جنبه پشتی موشهای نر و ماده C57BL/6 حداقل 24 ساعت قبل از تابش با نور UVB تراشیده شد و فقط موشهایی با پوست غیر رنگدانهدار در آزمایشها استفاده شدند. موشها با ایزوفلوران بیهوش شدند و با استفاده از لامپهای FS40T12/UVB (شرکت ملی بیولوژیکی) در معرض یک دوز نور UVB (500 میلیژول بر سانتیمتر مربع) با حداکثر انتشار بین 300 تا 315 نانومتر قرار گرفتند. انرژی نور UVB در سطح پشتی با رادیومتر Photo light IL1400A مجهز به آشکارساز SEL240/UVB (تکنولوژی های نور بین المللی) اندازه گیری شد. موشها 1، 2 یا 6 روز پس از قرار گرفتن در معرض نور UVB معدوم شدند و از موشهای بدون تابش بهعنوان کنترل (D{14}}) استفاده شد (شکل 2A). برداشتن نوار اپیدرمی همانطور که قبلا توضیح داده شد (7) انجام شد و پوست وکلیه24 ساعت پس از آسیب مورد بررسی قرار گرفتند
مهار IL-17A و G-CSF.موش ها 3 ساعت قبل از قرار گرفتن در معرض اشعه ماوراء بنفش (1 × 500 mJ/cm2) با 100 میکروگرم IL ضد موش خالص شده IL{2}}A IgG (BioLegend) یا کنترل ایزوتیپ به صورت داخل وریدی تحت درمان قرار گرفتند (شکل 3I). وجود نوتروفیل در خون، پوست و پرفیوژن با نمککلیهبافت با فلوسیتومتری 24 ساعت پس از قرار گرفتن در معرض اشعه ماوراء بنفش همانطور که در زیر توضیح داده شده است ارزیابی شد. مهاجرت نوتروفیل ها در پاسخ به اشعه ماوراء بنفش با درمان داخل صفاقی موش با 50 میکروگرم آنتی بادی مونوکلونال G-CSF ضد موش یا کنترل ایزوتیپ IgG موش (R&D Systems) 24 ساعت و 3 ساعت قبل از قرار گرفتن در معرض پوست در برابر نور UVB (1 × 500 mJ) مهار شد. /cm2) (شکل 4A). به دنبال پرفیوژن قلبی، تعداد نوتروفیل ها و مونوسیت ها درکلیهبا فلوسیتومتری و بیان ژن توسط qPCR، همانطور که در زیر توضیح داده شده است، ارزیابی شدند. موش هایی که در معرض نور UVB قرار نگرفتند به عنوان یک گروه کنترل اضافی استفاده شدند.
جداسازی سلول ها از اندام های مختلفپس از اتانازی با استنشاق CO2، یک تکه از پوست پشتی برداشته شد و تا زمان پردازش در محلول RPMI (موسسه یادبود پارک رازول) روی یخ نگهداری شد. خون با سوراخ قلبی در سرنگ های پوشش داده شده با اسید اتیلن دی آمین تتراستیک جمع آوری شد. پرفیوژن قلبی متعاقبا با استفاده از سالین بافر فسفات (PBS) (~60 میلی لیتر) از طریق بطن چپ پس از بریدن دهلیز راست انجام شد. پرفیوژن موفق با مشاهده کامل تعیین شدکلیهو رنگ پریدگی ریه ریه ها، کلیه ها، طحال و هر دو استخوان ران با دقت برداشته شدند و تا زمان پردازش نمونه در محلول RPMI روی یخ قرار گرفتند. سلول ها از نواحی معادل بافت پوست (~3{2}} mm2) با خرد کردن و هضم بافت با 0}.28 واحد در میلی لیتر لیبراز TM (روش) و 0.1 میلی گرم در میلی لیتر دئوکسی ریبونوکلئاز I جدا شدند. Worthington) در PBS با Ca + 2 و Mg + 2 به مدت 60 دقیقه در دمای 37 درجه همراه با تکان دادن. سلول ها از یکی جدا شدندکلیهبه ازای هر حیوان؛کلیهطبق پروتکل منتشر شده، بافتها در 2 میلیگرم بر میلیلیتر کلاژناز نوع I (ورثینگتون) به مدت 30 دقیقه در دمای 37 درجه خرد و هضم شدند. سلول های ریه با هضم بافت در PBS (Ca به علاوه 2 و منیزیم به علاوه 2) با 1 میلی گرم در میلی لیتر کلاژناز نوع 1 و 60 U دئوکسی ریبونوکلئاز I جمع آوری شدند. طحال های کامل روی یک صافی سلول 40 میکرومتر خرد شده و با محلول RPMI شسته شدند. خون کامل و سلولهای طحال، مغز استخوان، کلیهها و ریهها با 1X سلولهای قرمز خون (RBC) Lysis Buffer (BD Biosciences) تحت درمان قرار گرفتند. پس از جداسازی/هضم، سلولهای تمام بافتها (40 میکرومتر) فیلتر شدند، با PBS شسته شدند و قبل از شمارش در محلول RPMI معلق شدند.
رنگ آمیزی و آنالیز فلوسایتومتری.سلول ها با Fc Block TruStain FcX (Biolegend) و رنگ آمیزی با رنگ Zombie Aqua Viability (Biolegend) بر اساس توصیه های فروشنده انجام شدند. سلولها شسته شدند و رنگآمیزی سطحی با استفاده از آنتیبادیهای فلورسنت اختصاصی موش خریداری شده از Biolegend انجام شد. جمعیت های مختلف سلول های میلوئیدی در دروازه سلول های ایمنی زنده (Zombie Aqua-CD45 plus) مورد بررسی قرار گرفت. درصد و تعداد نوتروفیل ها (Ly6CintLy6Ghi) و مونوسیت ها (Ly6C به علاوه Ly6G-) اندازه گیری شد. نمایانگر گیتینگ فلوسیتومتری در پیوست SI، شکل S10 ارائه شده است. درصد بیان و میانگین شدت فلورسانس نشانگرهای سطحی در مدل PA (CXCR4، ICAM1، و CXCR1) با استفاده از کنترلهای رنگآمیزی فلورسانس منهای یک (FMO) در دروازه نوتروفیل (Ly6Ghi) تعیین شد. تمامی نمونه ها با استفاده از فلوسایتومتر CytoFLEX (Beckman Coulter) پردازش و داده ها با نرم افزار FlowJo نسخه 10 (Tree Star) تجزیه و تحلیل شدند.
مطالعات فعالسازی نوری (PA).موشهای UBC-PA-GFP تراشیده شدند و قسمتی از پشت با یک دوز نور UVB (5{9}}0 mJ/cm2) مانند بالا تابش شد. فقط ناحیه پوستی که تبدیل به نور می شود در معرض نور UVB قرار گرفت، در حالی که پوست باقی مانده با فویل آلومینیومی پوشانده شد. پس از 24 ساعت از آسیب استریل ناشی از UVB، کل ناحیه پوست تحت تابش UVB با استفاده از یک لامپ دیود ساطع نور 50 وات با فیبر دیافراگم عددی (NA) 0.37 (Mightex) در معرض نور بنفش (405 نانومتر) قرار گرفت. 100 میلی وات (15 دقیقه نوردهی در هر منطقه). این روش بر اساس یک پروتکل منتشر شده از تبدیل نوری خاص پوست (80) بهینه شده است.کلیه هاو ریه ها برای آنالیز فلوسیتومتری 24 ساعت پس از PA جمع آوری و پردازش شدند، همانطور که در بالا توضیح داده شد. رویکرد و جدول زمانی در نمودار در شکل 5A مشخص شده است. درصد GFP به اضافه نوتروفیل ها درکلیهبا آنچه در موش ها تحت سه شرایط کنترل یافت شد: 1) بدون UV و بدون PA، 2) UV اما بدون PA، و 3) بدون UV اما PA مقایسه شد. سطح بیان CXCR4 و فنوتیپ ICAM1hiCXCR1lo در نوتروفیل های GFP plus و GFP- در پوست وکلیهتوسط فلوسیتومتری با استفاده از آنتی بادی های برچسب دار فلورسنت خاص موش خریداری شده از Biolegend مورد ارزیابی قرار گرفتند. برای تعیین اینکه آیا GFP به علاوه نوتروفیل درکلیهمنشا آن از پوست بود و نه خون، پوست یک گروه از موش ها در معرض نور UV و PA همانطور که در بالا توضیح داده شد (گروه I) قرار گرفت، در حالی که در گروه دیگر، پوست در معرض نور UV بود اما PA در ناحیه پوست مجاور انجام شد. در معرض نور UV قرار نگرفته است (گروه II) (نمودار در پیوست SI، شکل S7A).کلیه هاهمانطور که در بالا توضیح داده شد برای آنالیز فلوسیتومتری جمع آوری و پردازش شدند.
بیان ژن و آنالیز پروتئومی.پوست،کلیه،و نمونه های ریه در محلول RNAlater (QIAGEN) ذخیره شدند. RNA توسط کیت RNeasy از QIAGEN استخراج شد و DNA مکمل (cDNA) با استفاده از کیت سنتز cDNA با ظرفیت بالا (Applied Biosystems) سنتز شد. رونوشتهای کموکاینهای التهابی، سیتوکینها و مولکولهای چسبنده توسط qPCR بلادرنگ با استفاده از پرایمرهای فهرستشده در ضمیمه SI، جدول S1 اندازهگیری شد و به میانگین سطوح رونوشت 18S نرمال شد. دوز استفاده شده از نور UVB بر بیان 18S در هیچ یک از اندام ها تأثیری نداشت. بیان نسبی اهداف mRNA با استفاده از فرمول استاندارد 2^ (-Ct) × ضریب تعیین شد. امتیازات IFN از بیان 10 ژن نماینده تحریک شده با اینترفرون (ISG؛ Mx1، Irf7، Isg15، Isg20، Ifi44، ifit1، ifit3، oasl1، usp18، و ifi27l2a) به دست آمد که قبلاً توضیح داده شد (6). ميانگين و انحراف معيار بيان نسبي هر ISG در اندازه گيري تعيين شدکلیه هاموش هایی که در معرض نور UV قرار نگرفته اند (meannoUV و SDnoUV). سپس برای استاندارد کردن سطح بیان هر ISG در کلیه موشهای تحت درمان (ایزوتیپ IgG به اضافه UVB یا a-GCSF به علاوه UVB) استفاده شد. سپس سطوح بیان استاندارد شده برای هر موش خلاصه شد تا نمره بیان IFN بدست آید. i=بیان هر ISG; ژن درمانی=سطح بیان ژن نسبی پس از درمان. و سطح بیان نسبی ژن inoUV=در موش هایی که در معرض نور UVB قرار نگرفته اند. ∑ 10 i=1=Geneitreatment−meanGeneinoUV SD(GeneinoUV ) . سطوح پروتئین در پلاسما و عصاره پروتئین بافت پوست با استفاده از پانل های آنالیت تعریف شده LEGENDplex Mouse Inflammation Panel و Inflammatory Chemokine Panel (Biolegend) اندازه گیری شد.
در صورت رنگ آمیزی بافت های منجمد کلیه.پرفیوژن سالینکلیه هادر پارافورمالدئید 4 درصد به مدت 1 ساعت در دمای اتاق تثبیت شدند و پس از غوطه وری در 3{4}} درصد ساکارز، در محیط برش بهینه (ساکورا فینتک) منجمد شدند. مقاطع بافتی 5- میکرومتر در PBS قبل از رنگآمیزی IF هیدراته شدند. بافت ها با 0.1 درصد تریتون ایکس-100 در PBS نفوذپذیر شدند و متعاقباً در PBS به اضافه 0.1 درصد Triton X{9}}/5 درصد BSA (آلبومین سرم گاوی)/5 درصد سرم خرگوش مسدود شدند. . سلولهای NE و اندوتلیال با رنگآمیزی با NE Cy5 ضد موش (1:100، Bioss) و ضد موش PECAM-1/CD31 Al488 (1:100، Biolegend) به ترتیب در دمای 4 درجه در طول شب شناسایی شدند. حضور نوتروفیل درکلیهبا رنگآمیزی با Anti-Mouse Ly6G Al647 (1:100، Biolegend) تأیید شد. بافت ها با استفاده از ProLong Gold با محیط نصب 4'،6-دیامیدینو-2-فنیلندول (DAPI) (Invitrogen) سوار شدند و با میکروسکوپ فلورسنت Nikon Eclipse 90i (هسته شناسی و تصویربرداری، دانشگاه واشنگتن) تصویربرداری شدند.

ارزیابی بافت شناسی پوستمقاطع بافت پوستی تثبیت شده با پارافین (4 تا 5 میکرومتر) با هماتوکسیلین و ائوزین در دانشگاه واشنگتن بافت شناسی و هسته تصویربرداری قبل از UV، روز 1، روز 2، و روز 6 پس از تابش UVB رنگ آمیزی شدند (n{{{ 7}} زن). پوست به روش کور برای پارامترهای زیر امتیازدهی شد: التهاب درم / زیر پوست، مرگ سلول های اپیدرمی، آکانتوز، هیپرکراتوز، تشکیل پوسته سروسلولار، و فرسایش / زخم. این پارامترها بسته به شدت و وسعت در مقیاس 0 تا 4 به استثنای فرسایش/زخم که به صورت وجود (1) یا غایب (0) نمرهگذاری شد. تصاویر معرف با استفاده از NIS-Elements BR 3.{14}}بیت گرفته شده و در Adobe Photoshop با تنظیمات نور اعمال شده روی کل تصویر قرار داده شده است. بزرگنمایی اصلی بیان شده است.
اندازه گیری ادرارسطح پروتئین ادرار با روش پروتئین برادفورد (Thermo Fisher Scientific) ارزیابی شد. نمونه های ادرار در رقت 1:40 در PBS مورد آزمایش قرار گرفتند و غلظت پروتئین در ادرار بر اساس رقت های سریال غلظت های شناخته شده BSA تعیین شد. نسبت آلبومین/کراتینین ادرار با استفاده از سنجش آلبومین Albuwell و کیت کراتینین Companion (Exocell) طبق دستورالعمل سازنده ارزیابی شد.
جمع آوری نمونه انسانی و آنالیز فلوسیتومتری.این مطالعه توسط هیئت بازبینی موسسه دانشگاه واشنگتن (STUDY00001145) تایید شده است. خون کامل در لوله های هپارینه شده از داوطلبان سالم و بیماران SLE پس از رضایت آگاهانه جمع آوری شد. نوتروفیل ها (PMNs) و PBMCs با جداسازی گرادیان ناپیوسته Ficoll-Paque (GE Healthcare) جدا شدند. PMN ها از گلوله گلبول قرمز با 5 درصد رسوب دکستران خالص شدند. پس از لیز RBC، سلولها با آنتیبادیهای برچسبدار فلورسنت خریداریشده از Biolegend رنگآمیزی شدند و بیان CXCR4 و درصد سلولهای ICAM1hiCXCR1lo در PMNs (CD66b plus) و LDGs (CD15 plus، CD14lo، و CD10 plus در PBMCs) ارزیابی شدند. استراتژی دروازه ای برای رنگ آمیزی LDG و ICAM1hiCXCR1lo بر اساس FMO در پیوست SI، شکل S11 نشان داده شده است. نمونه ها با استفاده از فلوسایتومتر CytoFLEX (Beckman Coulter) پردازش و داده ها با نرم افزار FlowJo نسخه 10 (Tree Star) تجزیه و تحلیل شدند.
تحلیل های آماریداده ها با استفاده از نرم افزار GraphPad Prism 7 (GraphPad Software Inc.) تجزیه و تحلیل و به صورت میانگین ± SEM ارائه شد. تفاوت آماری بین دو گروه داده نسبت به گروه شاهد بدون تابش (D{1}}) با استفاده از آزمون Student مشخص شد. برای تعیین معنیداری آماری بین سه گروه از آنالیز واریانس یکطرفه با مقایسههای چندگانه و Tukey post hoc استفاده شد.
