فلاونوئیدها - هدایای طبیعی برای ارتقای سلامت و طول عمر
Sep 22, 2022
لطفا تماس بگیریدoscar.xiao@wecistanche.comبرای اطلاعات بیشتر
خلاصه:پیری پستانداران با آتروفی پیشرونده بافت ها و اندام ها و تجمع آسیب تصادفی به DNA ماکرومولکولی، پروتئین و لیپیدها همراه است. فلاونوئیدها دارای اثرات آنتی اکسیدانی، ضد التهابی و محافظت کننده عصبی عالی هستند. مطالعات اخیر نشان دادهاند که فلاونوئیدها میتوانند با حذف سلولهای پیر، مهار فنوتیپهای ترشح مرتبط با پیری (SASP) و حفظ هموستاز متابولیک، پیری را به تاخیر بیندازند و طول عمر سالم را طولانیتر کنند. با این حال، تنها چند مطالعه سیستماتیک فلاونوئیدها را در درمان بالینی ضد پیری توصیف کردهاند که نیاز به بررسی بیشتر دارد. این بررسی ابتدا ارتباط بین پیری و آسیب ماکرومولکولی را برجسته می کند. سپس، پیشرفتها در نقش مولکولهای فلاونوئید در افزایش طول عمر و طول عمر موجودات را مورد بحث قرار میدهیم. این مطالعه ممکن است اطلاعات مهمی را برای طراحی دارو و کاربردهای توسعه و بالینی بر اساس فلاونوئیدها ارائه دهد.
کلید واژه ها:فلاونوئیدها؛ آسیب ماکرومولکولی؛ دوره سلامت؛ سالخورده
1. مقدمه
تصور میشود که سالمندی یکی از عوامل خطر بیماریهای مزمن است که بیشترین عوارض، مرگ و میر و مصرف مراقبتهای بهداشتی را در سراسر جهان دارد [1،2]. این گونه بیماری های مزمن عبارتند از تصلب شرایین، بیماری های قلبی عروقی، سکته مغزی، اکثر سرطان ها، دیابت، نارسایی کلیه، بیماری مزمن ریه، پوکی استخوان، آرتریت، نابینایی، زوال عقل و بیماری های عصبی. افزایش سن همچنین افراد را مستعد ابتلا به سندرم سالمندی و کاهش ایمنی و بهبودی فیزیکی میکند. این بیماری های مزمن اغلب در افراد مسن رخ می دهد. با درک اینکه چگونه پیری آسیبشناسی را ممکن میسازد، درمانهای جدیدی برای چندین بیماری مزمن پدید میآیند و فرصتی را برای افزایش طول سلامت انسان با هدف قرار دادن مستقیم پیری فراهم میکنند [3]. بنابراین، یافتن داروهای ضد پیری که ایمنی و اثربخشی استفاده طولانی مدت را برآورده می کنند، همیشه یک استراتژی مهم برای مداخله در زمینه پیری بوده است.
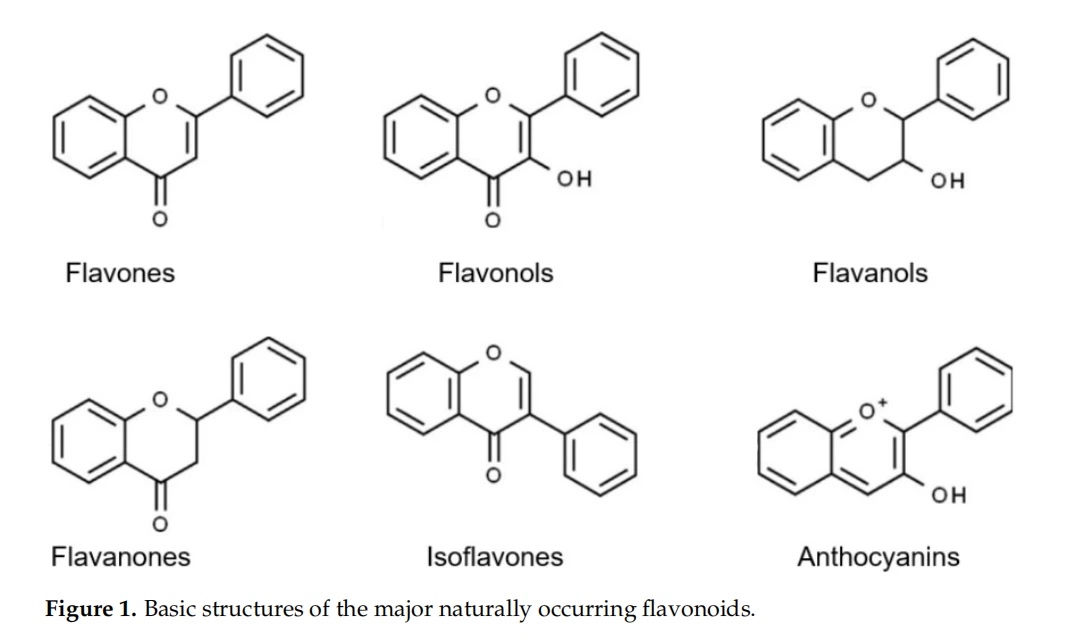
فلاونوئیدها خانواده متنوعی از ترکیبات فنلی طبیعی هستند که معمولاً در میوهها، سبزیجات، چای، شراب و داروهای گیاهی چینی یافت میشوند. فلاونوئیدها دارای اسکلت کربنی C6-C{3}C6 15 هستند که از دو حلقه معطر و یک حلقه پیران تشکیل شده است. اکسیداسیون، که فلاون ها، فلاونول ها، فلاونون ها، ایزوفلاون ها، فلاوانول ها و آنتوسیانین ها هستند (شکل 1) [5]. علاوه بر فعالیت آنتی اکسیدانی شناخته شده، فلاونوئیدها همچنین دارای فعالیت های ضد التهابی، گشادکننده عروق، ضد انعقاد، محافظت کننده قلبی، ضد دیابت، محافظت شیمیایی، محافظت کننده عصبی و ضد چاقی هستند [5]. مطالعات اخیر نشان داده است که فلاونوئیدها نیز فعالیت ضد پیری مناسبی دارند. ترکیب کورستین و داساتینیب برای از بین بردن سلولهای پیر در شرایط آزمایشگاهی، بهبود عملکرد فیزیکی و افزایش طول عمر invivo موشها مشاهده شده است [6]. جالبتر اینکه در آزمایشهای بالینی فاز I در بیماران مبتلا به بیماری کلیوی دیابتی [7] و ایدیوپاتیک مشاهده شده است. بیماری ریوی [8]، نشان داده شده است که تجویز داساتینیب همراه با کورستین به طور موثر بیانگرهای پیری pl6 و SA{16}}gal را کاهش می دهد. فلاونوئیدهای بیشتری مانند فیستین و لوتئولین نیز یافت شده اند که سلول های پیر را از بین می برند و اثرات ضد پیری دارند [9،10]. با این حال، مکانیسم ضد پیری فلاونوئیدها هنوز به طور کامل شناخته نشده است و تحقیقات بیشتری برای ارائه مبنایی برای کاربردهای بالینی آنها در انسان مورد نیاز است.
در اینجا، آخرین پیشرفت های تحقیقاتی در مورد فلاونوئیدها با مزایای ضد پیری را خلاصه می کنیم. توجه ویژه ای به تأثیر آنها در به تاخیر انداختن تجمع آسیب های ترمیم نشده در سلول از طریق کاهش آسیب ناشی از ماکرومولکول ها یا افزایش قابلیت ترمیم سلول داده می شود.فلاونوئیدهانقش فلاونوئیدها در جنبه های بالینی و بالینی نیز مورد بحث قرار گرفته است. این پتانسیل ارائه اطلاعات لازم برای طراحی و توسعه داروهای مبتنی بر این ترکیبات و استفاده بالینی از عوامل ضد پیری را دارد.

لطفا برای دانستن بیشتر اینجا را کلیک کنید
2. پیری سلولی توسط آسیب تعمیر نشده هدایت می شود
اگرچه درک فعلی از پیری هنوز در مراحل اولیه کشف ژنتیکی است، شواهد موجود نشان می دهد که پیری انسان توسط تعادل آسیب و فرآیندهای ترمیم هدایت می شود و تحت تأثیر قرار گرفتن در معرض محیط و ژنتیک قرار می گیرد (شکل 2). یکی از ویژگی های پیری، ارتباط آن با آسیب ماکرومولکولی است. هنگامی که ارگانیسم نتواند سلول ها را به میل خود جایگزین کند یا آسیب را رقیق کند، آسیب درون سلولی تجمع می یابد، به سلول میزبان و سایر سلول ها آسیب می رساند، عملکرد آن را مختل می کند و در نهایت منجر به بیماری های مرتبط با افزایش سن و پیری خود می شود. 9 نشانه پیری خلاصه شده است [2] و به طور گسترده توسط دانشمندان پژوهشگر پیری شناخته شده است. ناپایداری ژنومی ساییدگی تلومر، تغییرات اپی ژنتیکی و از دست دادن پروتئوستاز علل اصلی آسیب هستند. شایع ترین انواع آسیب ماکرومولکولی، آسیب پروتئین DNA و چربی است.
2.1. آسیب و ترمیم DNA
تصور میشود که آسیب DNA یک کاندیدای قوی به عنوان علت اصلی پیری است [11]. آسیب DNA شامل تغییرات اکسیداتیو، شکستگی های یک و دو رشته ای (DSBs) و جهش، هم در شرایط آزمایشگاهی و هم در داخل بدن است [12،13]. بسیاری از مطالعات نشان داده اند که تجمع آسیب DNA با پیری مرتبط است [14،15].هسپریدین استفاده می کندیک سیستم کامل ترمیم DNA نیز برای ترمیم آسیب DNA در سلول ها ایجاد شده است. مسیرهای برجسته ترمیم DNA در سلول های پستانداران عبارتند از: ترمیم برش پایه (BER)، ترمیم عدم تطابق (MR)، ترمیم برش نوکلئوتیدی (NER) و ترمیم شکست دو رشته ای (DSBR). مشاهده شده است که توانایی ترمیم آسیب DNA کاهش می یابد. با پیری[16]. بنابراین، آسیب DNA ترمیم نشده در طول پیری بیشتر تجمع می یابد. آسیب DNA ترمیم نشده می تواند باعث بی ثباتی ژنوم و القای یک آبشار سیگنال شود که منجر به پیری یا مرگ سلولی و فنوتیپ های پیری سلولی مرتبط می شود [17،18]. بیش از 50 اختلال ترمیم DNA بهعنوان درجات مختلفی از همپوشانی فنوتیپها با افزایش سن، مانند تخریب عصبی، سرطان و بیماریهای قلبی عروقی توصیف شدهاند [19].

شکل 2. نمودار تأثیرات و مکانیسم های اصلی که توسط آن آسیب ماکرومولکولی باعث پیری می شود. توهینهای آسیب (استرس ژنوتوکسیک، استرس اکسیداتیو و غیره) در عوامل ژنتیکی یا محیطی به ماکرومولکولها (عمدتاً شامل DNA، پروتئینها و لیپیدها) در طول فرآیند پیری آسیب میرسانند و باعث تجمع آسیب درون سلولی میشوند. در عین حال، قابلیت ترمیم در سلول با افزایش سن کاهش می یابد که باعث تجمع آسیب های ترمیم نشده در سلول می شود. آسیب انباشته نشده ترمیم نشده می تواند منجر به جهش یا انحرافات کروموزومی شود که منجر به بی ثباتی ژنوم می شود. تلومرهای کوتاه شده شدید، پاسخ ترمیم و آسیب DNA (DDR) را فعال می کنند و باعث پیری سلول می شوند. آسیب ترمیم نشده انباشته شده بر اتوفاژی و ER-UPR تأثیر می گذارد و منجر به از بین رفتن استوکیومتری کمپلکس پروتئین می شود. اختلال عملکرد میتوکندری ناشی از NAD به علاوه محرومیت ناشی از تعمیر DNA هسته ای، نقص اتوفاژی میتوکندری ناشی از آسیب DNA، و تغییرات در بیان mtDNA پلیمراز است که بر تکثیر mtDNA تأثیر می گذارد.سیستانچ امپراتوری از دست رفتهآسیبهای انباشتهشده ترمیمنشده مسیر سنجش مواد مغذی را خراب میکند و بر تعمیر و انتقال سیگنال تأثیر میگذارد. آسیب ترمیم نشده انباشته شده باعث پیری سلولی می شود و منجر به فرسودگی مخزن سلول های بنیادی از طریق آپوپتوز ناشی از DDR، پیری، تمایز زودرس و تغییرات در طاقچه سلول های بنیادی می شود. پیری سلول از طریق سیتوکین های التهابی و سیگنال های رشد بازدارنده بر ارتباط سلول به سلول تأثیر می گذارد.

سیستانچ می تواند ضد پیری باشد
2.2. آسیب پروتئین
عوامل مختلف داخلی و خارجی به طور مداوم به پروتئین های داخل سلولی آسیب می رسانند. آسیب رساندن به پروتئین ها به نوبه خود ممکن است بر تعداد بیشماری مسیرهای درون سلولی با توجه به فراوانی آنها تأثیر بگذارد. کنترل کیفیت پروتئین (PQC) برای حفظ عملکرد پروتئوم حیاتی است. کیفیت پروتئین توسط مکانیسم ترجمه و فعالیت پروتئین های کمکی (از جمله چپرون های مولکولی) تضمین می شود، در حالی که تخریب توسط عملکردهای اتوفاژی و پروتئازوم کنترل می شود. تجمع آسیب پروتئین در فرآیند پیری عمدتاً به دلیل (1) کاهش وفاداری ترجمه [20،21]، (ii) تنظیم پایین چپرون های پروتئینی [22،23]، و (iii) کاهش فعالیت پروتئازوم [24] و موارد دیگر است. عوامل در سنتز پروتئین و کنترل کیفیت. پروتئینهای آسیبدیده به استرس پروتئوستاتیک، تجمع پروتئینهای تاخورده/تجمیع شده و سمیت پروتئین کمک میکنند که پیری سلولها را تشدید میکند.
2.3. آسیب چربی
آسیب چربی عمدتاً به دلیل لیپوفوسسین، یک پروتئین غیرقابل تجزیه و محصول اکسیداسیون لیپید است که در سلول های پیر تجمع می یابد [25]. لیپوفوسین یک لیپوپیگمنت اتوفلورسنت است که توسط لیپیدها، فلزات و پروتئینهای نادرست تا شده تشکیل میشود که بهخصوص در سلولهای عصبی، سلولهای عضلانی قلب و پوست فراوان است [26]. ، 28]. نتایج تحقیقات اخیر نشان می دهد که لیپوفوسین می تواند به طور فعال متابولیسم سلولی، مرگ سلولی و آپوپتوز را در سطوح مختلف با مهار پروتئازوم ها، تضعیف اتوفاژی و تخریب لیزوزومی، و عمل به عنوان یک مخزن یون فلزی برای ایجاد ROS تغییر دهد [29]. علاوه بر این، پراکندگی ماهیت رسوبات توزیع شده در سراسر بافت ممکن است از مکانیسم انتشار لیپوفوسین و کاشت دانه های جدید لیپوفوسین حمایت کند [30]. لازم به ذکر است که تجمع آسیب حتی زمانی که تقسیم سلولی متوقف شود ادامه می یابد و می تواند ماه ها یا حتی سال ها ادامه یابد.
2.4. پیامدهای مولکولی، سلولی، و سیستمیک تجمع آسیب تعمیر نشده
هنگامی که آسیب انباشته می شود، تصمیمات سرنوشت سلولی و رویدادهای مرتبط با پیری را هدایت می کند. آسیب ترمیم نشده ارتباط نزدیکی با پیامدهای مولکولی مانند ثبات ژنوم، تلومرهای ناکارآمد، تغییرات اپی ژنتیکی، هموستاز پروتئین و اختلال عملکرد میتوکندری درون سلولی در طول پیری دارد. شواهد انباشته نشان می دهد که آسیب DNA عامل مهمی در تغییرات اپی ژنتیکی مرتبط با سن است [31،32]. آسیب DNA ممکن است با افزایش توقف رونویسی (فشار رونویسی) یا صدای رونویسی به واسطه جهش یا epimutation باعث استرس هموستاز پروتئین شود. این ممکن است روی مونتاژ، استوکیومتری، تاخوردگی صحیح و عملکرد پروتئین ها و کمپلکس های پروتئینی تأثیر بگذارد و منجر به استرس و تجمع پروتئین در حالت پایدار شود. اختلال عملکرد حرکتی مرتبط با سن و آسیبشناسی میتوکندری آسیبدیده در موشهای دارای کمبود پارکین E3 یوبیکوئیتین لیگاز یافت شد، که نشان میدهد اختلال در پاکسازی میتوکندری ناشی از کمبود پارکین ممکن است مبنای پاتولوژی بیماری پارکینسون باشد [33].کسری فلاونوئید خالص میکرونیزه 1000 میلی گرم استفاده می کندترمیم آسیب DINA خود می تواند مکانیسم هموستاز پروتئین را تحت فشار قرار دهد [34]. غذای گیاهی حاوی لیپوفوسین عملکرد ورزشی مگسهای میوه جوان را کاهش میدهد و تجمع پروتئین اصلاحشده با AGE و پروتئین کربونیلاسیون در بافتهای بدنی و همولنف تسریع میشود و به طور قابل توجهی طول عمر مگسهای میوه را کاهش میدهد [35].
آسیب در سطح سلولی منجر به پیری سلول و تخلیه سلول های بنیادی می شود (شکل 2). ترکیباتی مانند بلئومایسین، دوکسوروبیسین یا سیس پلاتین اغلب باعث آسیب غیرقابل جبران DNA و پیری سلولی می شوند [36]. خطای ترجمه به طور قابل توجهی در مگس های پیر افزایش یافت، در حالی که افزایش وفاداری سنتز پروتئین باعث افزایش طول عمر در بین گونه ها شد [21] لیپوفوسین به عنوان یک مشخصه سلول های پیر گزارش شده است [37]. تجمع آسیب در بافت ها همچنین می تواند بر ریزمحیط موجود در طاقچه سلول های بنیادی یا گردش سیستمیک عوامل موثر بر پیری سلول های بنیادی و اندام ها تأثیر بگذارد. گزارش هایی از تجمع آسیب DNA مرتبط با سن در سلول های بنیادی روده مگس سرکه مسن [38] و کریپت های روده موش ها [39] وجود دارد. بنابراین آسیب به سلول ها پیری سلول ها و سلول های بنیادی را تسریع می کند.

تجمع آسیب همچنین بر ریزمحیط ایمنی و حس مواد مغذی در پیری تأثیر می گذارد. در C.elegans، آسیب DNA می تواند یک پاسخ ایمنی ذاتی را تحریک کند، پروتئوستاز و مقاومت در برابر استرس سیستمیک را تقویت کند [40]. پروتئین چپرون HSP70 به عنوان پلی بین یوبیکوئیتین E3 لیگاز PDLIM2 و پروتئازوم عمل می کند تا سیگنال NF-kB را مهار کند[41]. سیستم های آسیب و ترمیم مسیرهای سنجش مواد مغذی را تنظیم می کنند، از جمله ILS، سیرتوئین ها و مسیرهای mTOR تنظیم شده با پروتئین کیناز فعال شده با AMP (AMPK) [42،43]. ATM حسگر آسیب DNA می تواند مسیر AMPK را در پاسخ به تغییرات انرژی فعال کند. خود mTOR به صورت گذرا به دنبال آسیب DNA به روشی وابسته به ATR (حسگر آسیب) فسفریله می شود[4]. مجتمع یوبیکوئیتین لیگاز GID فعالیت AMPK و طول عمر ارگانیسم را تنظیم می کند [45].
به طور خلاصه، تجمع آسیب یکی از علل اصلی پیری سلولی، عدم تعادل سیستمیک بین سلولها و علائم اولیه پیری است.
3. ترکیبات فلاونوئیدی به عنوان عوامل ضد پیری عمل می کنند
در طول دو دهه گذشته، فلاونوئیدها به عنوان مولکولهای غذایی طبیعی امیدوارکننده برای جلوگیری از پیری و بیماریهای مرتبط با پیری مورد توجه قرار گرفتهاند. فلاونوئیدهای ضد پیری با توجه به روشهای مختلف تداخل با پیری، به فلاونوئیدهای سنولیتیک، فلاونوئیدهای سنومورفیک و فعالیت ضد پیری تقسیم میشوند (جدول 1).
3.1. فلاونوئیدهای سنولیتیک
سلولهای پیر و فنوتیپهای ترشح مرتبط با پیری (SASPs) که توسط آنها ترشح میشود، عواملی ضروری هستند که منجر به پیری بافتها و اندامها میشوند [6]. بنابراین، رویکردهای درمانی برای کشتن خاص سلولهای پیر میتوانند طول عمر و طول عمر را افزایش دهند. ترکیبات سنولیتیک میتوانند سلولهای پیر را از بین ببرند [75].اوتفلاوونوئیدکوئرستین در ترکیب با داساتینیب بر روی سلولهای اندوتلیال انسان کهنسال موثر است، که در از بین بردن MEFهای پیر[46]، کاهش بیان فاکتورهای SASP[47] مؤثرتر است. موشهای پیر[6] و بیماریهای مرتبط با افزایش سن مانند بیماریهای قلبی عروقی و دژنراسیون مفصل گیجگاهی فکی را بهبود میبخشند [76]. علاوه بر این، در یک کارآزمایی بالینی برچسب باز، ظرف سه هفته، کورستین خوراکی و داساتینیب 6-دقیقه راه رفتن، سرعت راه رفتن، و توانایی ایستادن از روی صندلی را بهبود بخشید و باتری عملکرد بدن را پنج روز پس از درمان کوتاه کرد. آخرین دوز [5،77].
در یک پانل از 10 پلی فنول مورد بررسی، فیستین در فیبروبلاستهای موش و انسان کهنسال کشتشده بهشدت سنولیتیک بود، در حالی که لوتئولین تأثیر ضعیفی بر پاکسازی سلولهای پیر داشت. فیستین طول عمر متوسط و حداکثری موش های مسن را افزایش داد [9]. قابل توجه است که درمان فیستین به طور قابل توجهی مرگ و میر، پیری سلولی و نشانگرهای التهابی را کاهش داد و آنتی بادی های ضد ویروسی را هنگامی که ویروس کرونای موش مربوط به SARS-CoV در معرض پاتوژن های پیر موش قرار گرفت، افزایش داد [78]. از آنجایی که فیستین اثر خوبی در برابر عوامل التهابی دارد، در تحقیقات بالینی برای کاهش اختلال عملکرد کووید{7}} و پاسخ التهابی بیش از حد در افراد مسن استفاده شده است (NCT0453729). برتون و همکاران نشان داد که لوتئولین به طور قابل توجهی نسبت میکروگلیاهای رنگآمیزی شده برای IL{9}} و IL-6 را در موشهای بالغ تحت درمان با LPS کاهش میدهد [10]. 3.2. فلاونوئیدهای سنومورفیک
Senomorphics به ترکیبات و مکمل های غذایی اشاره دارد که می توانند فنوتیپ های مرتبط با پیری را با سرکوب صریح SASP یا ترشحات پیش التهابی مهار کنند. نتایج تحقیقات اخیر همچنین نشان می دهد که فلاونوئیدهای آپیژنین، کامفرول و 4،4 دی متوکسی کالکون نیز چنین اثرات "بیگانه شکل" دارند (جدول 1). آپیژنین به زیرگروه فلاون ها از فلاونوئیدها تعلق دارد و خودرو با فعال کردن مسیر Nrf2 روند پیری را به تاخیر می اندازد [79]. آپیژنین تا حدی SASP را با مهار سیگنال دهی IL در رده های سلولی فیبروبلاست انسانی از طریق IRAK1 و IRAK4، p{10}MAPK و NF-kB[49] تا حدی مهار می کند. کامفرول یک فلاونول است و به طور قابل توجهی بیان IL-6، IL-8 و IL{15}}b را مهار میکند، اما تأثیر قابلتوجهی بر پیری خود در سلولهای پیر BJ ناشی از بلئومایسین ندارد. یک مطالعه مکانیسم سلولی نشان داد که کامفرول در سلولهای پیر BJ ممکن است، حداقل تا حدی، با تداخل در سیگنالدهی IRAK1/IkBa/NF-kB p65 واسطه شود [50،80].
3.3. یکی دیگر از فعالیت های ضد پیری فلاونوئیدها
علاوه بر این، ثابت شده است که افزایش تعداد فلاونوئیدها روند پیری را به تاخیر می اندازد. همانطور که در جدول 1 نشان داده شده است، این ترکیبات شامل زیر مجموعه های مختلفی از فلاونوئیدها هستند. فلاونوئید 4،4'-dimethoxychalcone (DMC) از گیاه گلپر کایسکی کویزومی (Angelica keiskei Koizumi) مشتق شده است، گیاهی با اثرات افزایش طول عمر و سلامت در طب سنتی چینی. DMC طول عمر مخمرها، کرمها و مگسها را افزایش میدهد و پیری کشتهای سلولی انسانی را از طریق فاکتورهای رونویسی GATA برای القای اتوفاژی کاهش میدهد [51].

Naringenin و nobiletin به طور گسترده در میوه های گیاهان Citrus L. از خانواده Rutaceae یافت می شوند. هر دوی آنها اثرات آنتی اکسیدانی دارند و می توانند ROS را در سلول های پیر کاهش دهند. علاوه بر این، نارینژنین تأثیر قابل توجهی در کاهش نشانگرهای قلبی عروقی آسیب ناشی از افزایش سن دارد [52]. آزمایش تجزیه و تحلیل طول عمر در مگس سرکه نشان داد که درمان با 400 um/L naringenin می تواند طول عمر را تا 22.62 درصد افزایش دهد [53] با این حال، نقش نوبیلتین عمدتاً در تنظیم متابولیسم انرژی غیرطبیعی است. نوبیلتین گیرنده های یتیم مربوط به گیرنده اسید رتینوئید (RORs) را برای بازسازی بیان ژن شبانه روزی و متابولیک، افزایش ریتم شبانه روزی و جلوگیری از سندرم متابولیک هدف قرار می دهد [66]. علاوه بر این، Nobiletin-RORs برای بهینه سازی تنفس میتوکندریایی ماهیچه های اسکلتی و ترویج پیری سالم در موش های رژیم غذایی پرچرب گزارش شده است [67].
جنستئین یک ایزوفلاون است که از محصولات سویا به دست می آید. جنستئین باعث ایجاد اتوفاژی برای کاهش پیری سلولی در سلول های ماهیچه صاف عروق می شود[55]. جنستئین افزایش وابسته به سن در فعالیت NF-kB و بیان ژن پیش التهابی وابسته به NF-KB را در داخل بدن در موش کاهش داد. بنابراین، می توان از آن به عنوان یک ترکیب ضد التهابی استفاده کرد [56]. اثرات ضد پیری نیز برای اپی کاتچین گزارش شده است. اپی کاتچین باعث وارونگی پیری سلول های اندوتلیال می شود و عملکرد عروقی را در موش ها بهبود می بخشد [63]. مشاهده شده است که مکمل اپی کاتچین باعث بهبود میزان بقای موش های مسن و فنوتیپ های مرتبط با سن مانند تحلیل ماهیچه های اسکلتی [64] و اختلال عملکرد مغز [65] می شود.
Myricetin و Dihydromyricetin در چندین گیاه، به ویژه در برخی از میوه ها و سبزیجات معمولی (توت فرنگی، انگور) تولید می شوند. آنها به عنوان مکمل های غذایی در اروپا و ایالات متحده تایید شده اند. آزمایش های بقا نشان می دهد که هر دو ترکیب طول عمر را طولانی می کنند [58،60]. جالب توجه است که میریستین و دی هیدرومیریستین دارای اثرات ضد AD هستند [81].
روتین، یک ترکیب گلیکوزید فلاونوئید طبیعی، اثر ضد پیری گسترده ای را نشان داده است. روتین می تواند اتوفاژی را برای افزایش طول عمر مگس سرکه تحت درمان با HDF [68] القا کند و همچنین می تواند به طور موثری اختلال متابولیک مرتبط با پیری را با تنظیم مسیر سیگنال دهی IIS بهبود بخشد [69]. علاوه بر این، تجویز روتین بیان ROS و سیتوکینهای پیش التهابی (TNF- و IL{4}}) را در سلولهای عصبی کاهش میدهد، که میتواند از پیشرفت AD جلوگیری کند و از مغز پیر محافظت کند یا روند تخریب عصبی را کند کند[70].
هسپریدین یک گلیکوزید فلاوانون مشتق شده از مرکبات است که دارای خواص دارویی مختلفی از جمله آنتی اکسیدان، کاهش دهنده کلسترول و ضد التهاب است. کاربرد موضعی هسپریدین می تواند ناهنجاری های عملکردی اپیدرم پیری از جمله عملکرد غیر طبیعی سد نفوذپذیری اپیدرم، تمایز اپیدرمی، تولید چربی و اسیدی شدن لایه شاخی را بهبود بخشد [82]. هسپریدین Nrf2 را افزایش داد و ROS را کاهش داد و به طور قابل توجهی طول عمر تکثیر مخمر را افزایش داد [71]. درمان با هسپریدین همچنین به طور موثری از قلب موش های مسن با افزایش سطح پروتئین Nrf2 و افزایش فعالیت آنتی اکسیدان های آنزیمی محافظت کرد [72]. علاوه بر این، برخی دیگر از فلاونوئیدهای مرکبات مانند نارینگین، هسپرتین و نئوهسپریدین نیز مهار ROS و فعالیت های بالقوه ضد پیری در مخمر را حفظ کرده اند [83].
تیافلاوین ها از تبدیل کاتچین ها توسط پلی فنل اکسیداز و پراکسیداز درون زا در طی تولید چای سیاه به دست می آیند [84]. مطالعات نشان داده اند که تافلاوین می تواند تکثیر بیش از حد سلول های بنیادی روده را به تاخیر بیندازد، از دیس بیوز روده جلوگیری کند و از فعال شدن مسیر سیگنالینگ Imd جلوگیری کند و در نتیجه طول عمر مگس سرکه را طولانی تر کند. در عین حال، تافلاوین در پیشگیری از کولیت ناشی از DSS در موش ها موثر است [73]. علاوه بر این، تافلاوین می تواند با فعال کردن Nrf2 در مدل استئوآرتریت موش، در برابر پیری سلولی ناشی از استرس اکسیداتیو محافظت کند [85]. علاوه بر این، درمان موش های میانسال با تافلاوین 3-گالات پیری را در سلول های بنیادی عصبی هیپوتالاموس کاهش داد و در عین حال آسیب شناسی مرتبط با پیری را بهبود بخشید [74].
به طور خلاصه، فلاونوئیدهای دارای اثرات ضد پیری هم از نظر نوع و هم از نظر نحوه عملکرد متفاوت هستند. مولکولهای همان زیر کلاس نیز دارای اهداف ضد پیری هستند که نشان میدهد برای آشکار کردن مکانیسمهای تنظیمی مربوطه به تحقیقات دقیقتری نیاز است.
4. فواید فلاونوئیدها در کاهش آسیب پیری
با توجه به تأثیر مهم آسیب بر پیری سلولی و سیستمیک، حذف یا ترمیم آسیب به برقراری مجدد وضعیت تعادلی ترمیم آسیب کمک می کند و در نتیجه سرعت پیری را کاهش می دهد. بسیاری از یافته ها نشان می دهد که فلاونوئیدها نقش اساسی در کاهش آسیب و بازسازی هموستاز بافت ایفا می کنند، همانطور که در شکل 3 نشان داده شده است.
فلاونوئیدها می توانند آسیب های سلولی ناشی از انواع آسیب ها را کاهش دهند. کوئرستین از گلبول های قرمز خون در برابر استرس اکسیداتیو و سمیت ژنتیکی در شرایط آزمایشگاهی محافظت می کند [86]. کوئرستین همچنین میتواند از سلولها در برابر استرس پروتئینهای تاخورده نادرست در شبکه آندوپلاسمی محافظت کند [87] جنیستئین ممکن است با مهار اتصال انتخابی N-CoR و PML- وابسته به فسفوریلاسیون، تاخوردگی اشتباه پروتئین N-CoR ناشی از PML-RAR را به طور قابل توجهی معکوس کند. RAR [88]. Kaempferol [89] و apigenin [90] ممکن است پروتئین مرتبط با محل ورودی ریبوزوم داخلی (IRES) را تغییر دهند تا عفونت ویروسی را محدود کرده و فعالیتهای ترجمه مبتنی بر IRES ویروسی را مهار کنند. به این ترتیب، فلاونوئیدها می توانند آسیب سلولی از منبع را کاهش دهند. بسیاری از فلاونوئیدها می توانند به روش های مختلفی روی آسیب DNA اثر بگذارند. فلاونوئیدهای لوتئولین، نارینژنین و روتین به طور موثر آسیب DNA ناشی از UVB را در شرایط آزمایشگاهی [91] و in vivo [92] کاهش می دهند. گزارش شده است که کورستین با هدف قرار دادن مسیر سیگنالینگ NRF2/Keapl در موش صحرایی، 1،{15}}استرس اکسیداتیو با واسطه دی متیل هیدرازین و آسیب DNA را معکوس می کند [93]. اخیراً گزارش شده است که نانوکپسول های حاوی دی هیدرومیریستین دارای 50 درصد فاکتور محافظت از نور خورشید (SPF-DNA) در برابر آسیب DNA ناشی از UVB هستند.
تابش و محافظت 99.9 درصدی در برابر القای آسیب DNA [94]. همچنین مشخص شد که اپی کاتچین در برابر آسیب DNA ناشی از N-nitrosodibutylamine (NDBA) و N-nitrosopiperidine (NPIP) در سلول های هپاتوکارسینومای انسانی محافظت می کند [95]. اپی کاتچین میریستین ترمیم شکستگی دو رشته ای DNA با اتصال انتهایی غیر همولوگ را در سلول های روده کوچک انسان فعال می کند [96]. بنابراین، فلاونوئیدها می توانند آسیب DNA را کاهش دهند و توانایی ترمیم DNA سلول ها را افزایش دهند و در نتیجه تجمع آسیب های ترمیم نشده را کاهش دهند.
اعتقاد بر این است که آسیب اکسیداتیو نقش کلیدی در فرآیندهای پاتولوژیک مربوط به پیری و بیماریهای مرتبط با افزایش سن دارد و مکانیسمهای بیوشیمیایی زیربنایی آن با جزئیات توضیح داده شده است [2،97]. ظرفیت آنتی اکسیدانی یکی از فعالیت های مهم فلاونوئیدها است. در سلولهای APRE{3}}، پراکندگی جامد آپیژنین بیان آنزیمهای آنتی اکسیدانی را تنظیم میکند و اتوفاژی را از طریق مسیر Nrf2 تنظیم میکند و در نتیجه مهار میکند.آسیب اکسیداتیو شبکیه [98]. در یک مدل پیری طبیعی موش صحرایی، فیستین به طور قابل توجهی پرو اکسیدان ها را کاهش می دهد و سطح آنتی اکسیدان ها را برای مبارزه با استرس اکسیداتیو ناشی از پیری افزایش می دهد [99]. دی هیدرومیریستین می تواند آسیب اکسیداتیو سلول های اندوتلیال ورید ناف انسانی ناشی از نیتروپروساید سدیم را با فعال کردن مسیر سیگنالینگ PI3K/Akt/FoxO3a کاهش دهد [100]. نوبیلتین ROS و اختلال عملکرد میتوکندری ناشی از پالمیتات را در سلولهای 12 کبد آلفا موش کشت شده کاهش میدهد[101]. علاوه بر این، نارینژنین [102]، لوتئولین [103]، جنیستئین [104]، کامفرول [10.5] و کوئرستین [106] همگی برای مهار آسیب اکسیداتیو به طرق مختلف مشاهده شده اند. بنابراین، فلاونوئیدها ممکن است آسیب اکسیداتیو در سلول های پیر را از بین ببرند و به سلول ها کمک کنند تا بر پیری و بیماری های مرتبط با پیری غلبه کنند.
فلاونوئیدها همچنین در روند کاهش و از بین بردن آسیب پروتئین نقش دارند. اپیکاتچین از طریق گیرنده لامینین 67 کیلو دالتون، فاکتور 1A طولانی شدن ترجمه یوکاریوتی (eEF1A) را تنظیم مثبت می کند [107]. درمان فیستین پره آدیپوسیت ها فسفوریلاسیون پروتئین ریبوزومی S6 کیناز 1 (S6K1) 70 کیلو دالتون را کاهش داد. Nobiletin به طور قابل توجهی فعال شدن سیگنالینگ Akt/mTOR را مسدود کرد و به طور قابل توجهی فسفوریلاسیون S6K1 و فاکتور شروع ترجمه یوکاریوتی پروتئین اتصال دهنده 4E 1 (4EBP1) را مهار کرد[108]. S6K دارای فسفر elF4B و پروتئین ریبوزومی S6 (RPS6) را هدف قرار می دهد. در همان زمان، 4EBP به فاکتور شروع یوکاریوتی 4E(eIF4E) در رابط تعامل eIF4E-eIF4G متصل می شود تا از تشکیل مجموعه آغاز ترجمه [109] جلوگیری کند و در نتیجه بر وفاداری ترجمه تأثیر بگذارد.
کوئرستین به طور خاص می تواند سطح بیان HSP70 را خاموش کند. مطالعات قبلی نشان داده اند که مهارکننده های HSP90 دارای فعالیت سنولیتیک هستند [10]. لوتئولین می تواند تغییرات و علائم پاتولوژیک پسوریازیس را با معکوس کردن اثرات بیان IFN-y و HSP90 و ترشح اگزوزومی، تنظیم نسبت سلول های ایمنی و مهار پسوریازیس کاهش دهد. Myricetin با اتصال HSP90 و گیرنده TGF Ⅱ تداخل می کند و در نتیجه از فعال شدن فیبروبلاست جلوگیری می کند. این نشان می دهد که فلاونوئیدها همچنین می توانند فعالیت مولکول های چپرون را تنظیم کنند. فعالیت پروتئازوم و اتوفاژی بخش مهمی از کنترل کیفیت پروتئین و راهی معنادار برای از بین بردن پروتئین های آسیب دیده است. گزارش شده است که Myricetin تجمع پروتئین نورودژنراتیو را با تنظیم مثبت مکانیسم تخریب پروتئازوم از بین می برد [111]. کوئرستین و روتین تنظیم کننده های مثبت فاکتور رونویسی Nrf2 هستند که بیان زیرواحدهای کاتالیزوری پروتئازوم را در نورون ها افزایش می دهد[112]. فیستین بقای سلول های عصبی را با افزایش فعالیت پروتئازوم در هنگام حذف عوامل تغذیه ای تقویت می کند [113]. گزارشهای مرتبط نشان میدهند که تمام فلاونوئیدهای فهرست شده در جدول 2 در تنظیم سطح اتوفاژی نقش دارند[{12}}]. به طور خلاصه، فلاونوئیدها می توانند کنترل کیفیت پروتئین را به روش های مختلف افزایش دهند و در نتیجه آسیب پروتئین را کاهش دهند.
حذف لیپوفوسین در سلول ها منجر به کاهش آسیب چربی می شود که اغلب با بهبود آسیب شناسی مرتبط با افزایش سن همراه است. مطالعات ضد پیری روی فلاونوئیدها نشان داده است که آنها همچنین می توانند لیپوفوسسین را در سلول ها به حداقل برسانند. چندین مطالعه نشان داده اند که کامفرول، میریستین، نارینگین و کورستین می توانند به طور قابل توجهی تجمع لیپوفوسسین را در C. elegans، نشانگر پیری، کاهش دهند [58,122,123]. با این حال، روتین و فیستین، که طول عمر نماتدها را نیز افزایش می دهند، نمی توانند تجمع لیپوفوسسین را در سلول ها به تاخیر بیندازند [122,123]. کوئرستین همچنین میتواند از توسعه اتوفلورسنس مرتبط با لیپوفوسسین در سلولهای پیر جلوگیری کند[124]. علاوه بر این، تجمع لیپوفوسین ارتباط نزدیکی با عملکرد میتوکندری و متابولیسم لیپید دارد [30]. فلاونوئیدها عملکرد میتوکندری را تنظیم می کنند. به عنوان مثال، لوتئولین تنفس میتوکندریایی را در نورون های اولیه افزایش می دهد [125]. فلاونوئیدها می توانند لیپوفوسین را در سلول ها کاهش دهند و بر فرآیندهای مربوط به تولید لیپوفوسسین تأثیر بگذارند.
در مجموع، فلاونوئیدها به طور موثری آسیب DNA، پروتئین و ماکرومولکول های لیپیدی را با کاهش توهین های آسیب کاهش می دهند. در عین حال، آنها می توانند توانایی ترمیم یا پاکسازی آسیب را بهبود بخشند و در نتیجه سرعت تجمع آسیب ترمیم نشده در سلول ها را به میزان قابل توجهی کاهش دهند. با توجه به نقش مهم آسیب ترمیم نشده در القای پیری سلولی، سلول ها یا بافت ها می توانند از اثرات ضد آسیب فلاونوئیدها بهره مند شوند.
5. کاربردهای بالینی فلاونوئیدها در پیری
همانطور که در بالا ذکر شد، نتایج بالینی نشان داده است که فلاونوئیدها اثرات مفیدی در کاهش پیری سلولی دارند. این اثرات مفید فلاونوئیدها می تواند برای انسان ها اعمال شود و در حال حاضر در آزمایش های بالینی در حال آزمایش هستند (جدول 2). کوئرستین سنولیتیک به همراه داساتینیب و فیستین در درمان بالینی پوکی استخوان، بیماری کلیوی دیابتی، بیماری آلزایمر و سایر بیماری های مرتبط با افزایش سن استفاده شده است. شایان ذکر است که فیستین در چندین مطالعه بالینی برای بهبود سلامت جمعیت سالمند مبتلا به کووید-19 گنجانده شده است. علاوه بر این، دو مطالعه بالینی در مورد اثربخشی فیستین در کاهش نشانگرهای شکنندگی و التهاب، مقاومت به انسولین، و تحلیل استخوان در افراد مسن نیز برای این کار در نظر گرفته شده است. سایر تحقیقات بالینی مرتبط با فلاونوئید و پیری به ندرت انجام می شود و فقط جنیستئین کارآزمایی های بالینی را در بیماری آلزایمر و سندرم متابولیک انجام داده است. روتین و ویتامین C نیز در مطالعات بالینی دیابت نوع 2 گنجانده شده است.
به طور خلاصه، اگرچه سنتراپی متشکل از فلاونوئیدها در تحقیقات بالینی در مورد وضعیتهای پیری و بیماریهای مرتبط با پیری گنجانده شده است، هنوز نتایج تجربی قطعی وجود ندارد. ایمنی و اثرات جانبی احتمالی استفاده طولانی مدت از فلاونوئیدها به عنوان داروهای ضد پیری نیز باید در تحقیقات بالینی آینده مورد توجه قرار گیرد.
6. نکات پایانی
فلاونوئیدها را میتوان به عنوان داروهای سنولیتیک برای حذف سلولهای پیر در بافتها، بهبود فنوتیپهای فیزیولوژیکی مرتبط با پیری و برای مهار التهاب و پیری ایمنی ناشی از SASPها بهعنوان «کسونومورفیک» استفاده کرد. در سال های اخیر، بسیاری از فلاونوئیدها نیز به عنوان عوامل ضد پیری ظاهر شده اند. به عنوان مثال، نوبیلتین می تواند با مهار پروتئین ROR در تنظیم چرخه ریتم شبانه روزی، اثر ضد پیری داشته باشد. در عین حال، بسیاری از مطالعات نشان دادهاند که فلاونوئیدها میتوانند آسیب ماکرومولکولها را در سلولها از بین ببرند، توانایی ترمیم DNA را بهبود بخشند و سطح کنترل کیفیت پروتئین را بهبود بخشند، در نتیجه پیری سلولی را کاهش داده و پیری سیستمیک را بهبود میبخشند. با توجه به نقش اصلی آسیب ماکرومولکولی در پیری، فلاونوئید درمانی یک استراتژی موثر ضد پیری خواهد بود. علاوه بر این، فلاونوئیدهای کورستین و فیستین در انواع مطالعات بالینی در مورد وضعیت های مرتبط با افزایش سن گنجانده شده اند. این مطالعات پیش بالینی و بالینی بر روی فلاونوئیدها برای به تاخیر انداختن پیری، مبنای داده مهمی را برای استفاده از فلاونوئیدها در درمان پیری و بیماریهای مرتبط با پیری فراهم میکند.
اگرچه بسیاری از مطالعات اثرات مفید ضد پیری فلاونوئیدها را نشان داده اند، باید به این واقعیت توجه شود که فلاونوئیدهایی که در حال حاضر استفاده می شوند دارای سمیت نامشخص و عوارض جانبی استفاده مداوم طولانی مدت، حلالیت کم، متابولیسم سریع و جذب ضعیف رژیم غذایی هستند. فلاونوئیدها در دستگاه گوارش که مانع پتانسیل دارویی آنها می شود. خوشبختانه، استفاده از فرمولهای مبتنی بر نانوذرات فلاونوئیدها میتواند به طور قابل توجهی فارماکولوژی فلاونوئیدها را بهبود بخشد[126]. ما دلایلی داریم که باور کنیم با اکتشافات تحقیقاتی بیشتر، فلاونوئیدهای محصول طبیعی به ناچار کتابخانه ابزار ضد پیری ما را قویتر غنی میکنند و گزینههای جایگزین برای توسعه و کاربرد داروهای ضد پیری بالینی ارائه میکنند.
این مقاله از Int استخراج شده است. جی. مول. علمی 2022، 23، 2176. https://doi.org/10.3390/ijms23042176 https://www.mdpi.com/journal/ijms






