شناسایی ژن های هاب مرتبط با ایجاد آسیب حاد کلیه
Mar 29, 2022
مخاطب:joanna.jia@wecistanche.com/ واتساپ: 008618081934791
شیائو لین جیانچون لی رویجی تان شیا ژونگ جیکه یانگ لی وانگ
آزمایشگاه پیشگیری و درمان فیبروز اندام با ترکیب طب سنتی چینی و غربی، مرکز تحقیقات طب سنتی چینی و غربی یکپارچه، بیمارستان طب سنتی وابسته، دانشگاه پزشکی جنوب غربی، لوژو، چین

بررسی فله سیستانچ:بسیار خوب برایعملکرد کلیه
کلید واژه ها
تجزیه و تحلیل شبکه هم بیان ژن وزن دار · حادکلیهآسیب·Rplp1.Lgals1
خلاصه
زمینه: حادکلیهصدمه(AKI) یک سندرم بالینی شدید است که باعث بار سنگین پزشکی و اجتماعی و اقتصادی در سراسر جهان می شود. این مطالعه با هدف کشف اهداف مولکولی مرتبط با پیشرفت AKl انجام شد. روشها: یک پایگاه داده عمومی از پایگاهداده NCBI GEO (شماره سریال: GSE121190) نشات گرفته و یک روش ثابت و بیطرفانه تحلیل شبکه هماظهاری ژن وزنی (WGCNA) برای شناسایی ژنهای هاب و مسیرهای بالقوه استفاده شد. علاوه بر این، ژنهای unbiasedhub در 2 مدل کلاسیک AKl در یک مدل جونده تأیید شدند: AKI شیمیایی ایجاد شده توسط AKI ناشی از سیس پلاتین و ایسکمی-پرفیوژن مجدد. نتایج: در نهایت 17 ماژول با روش بی طرفانه WGCNA به دست آمد، که در آن ژنهای ماژول فیروزه همبستگی قوی با توسعه AKl نشان دادند. علاوه بر این، نتایج هستی شناسی ژن نشان داد که ژن های موجود در ماژول فیروزه در کلیه ها نقش دارند.صدمهو فیبروز کلیه بنابراین، ژنهای هاب بیشتر با روشهای تجربی تأیید شدند و در درجه اول Rplp1 و Lgals1 را بهعنوان ژنهای کاندید کلیدی مرتبط با پیشرفت AKI با استفاده از PCR کمی، وسترن بلات، و فلورسانس بافت درجا بهدست آوردند. نکته مهم، بیان Rplp1 و Lgals1 در سطح پروتئین، همبستگی مثبتی با عملکرد کلیه، از جمله کروم سرم و BUN نشان داد. نتیجهگیری: با استفاده از روش بیوانفورماتیک بیطرفانه و تأیید تجربی در نتیجه، این مطالعه پایه و اساس پاتوژنز و توسعه عامل درمانی AKI را ایجاد میکند.
مقدمه
حادکلیهصدمه(AKI) یک سندرم بالینی رایج، شامل انواع فرآیندهای پاتوفیزیولوژیک است [1، 2]. در واقع، بازیابی عملکرد کلیه در AKI اغلب ناقص است و به تدریج به CKD تبدیل می شود که در نهایت به ESRD تبدیل می شود [3]. AKI یک عامل اساسی در CKD و در نتیجه ESRD است [4]. در پیشرفت انتقال AKI به CKD، ناهنجاریهای ساختاری به صورت رسوبگذاری انبساط ماتریکس در مزانژیوم و توبولواینترستیتیوم آشکار میشوند. هدف گذاری
در مورد فیبروز کلیه پس از AKI به عنوان یک رویکرد درمانی برای به حداقل رساندن انتقال در نظر گرفته شده است [5-7].
افزایش کروم پلاسما به عنوان یک معیار کلاسیک برای تشخیص AKI در دهه های گذشته در نظر گرفته شده است. اما ممکن است نشانگر زیستی مناسبی نباشد زیرا اغلب تعادل تولید و دفع کروم را پیشنهاد می کند [8]. اگرچه حذف پیامدهای کوتاهمدت و بلندمدت AKI ضروری است، اما درمانهای درمانی و نشانگرهای زیستی تشخیص زودهنگام هنوز محدود هستند. علاوه بر این، در حال حاضر هیچ بیومارکر معتبر بالینی برای تشخیص فیبروز کلیه پس از AKI وجود ندارد. از این رو، توسعه درمان های درمانی بیشتر و کشف نشانگرهای زیستی بالقوه برای درمان فیبروز و به تاخیر انداختن پیشرفت آن سودمند است [1، 8].
به دلیل روششناسی معیوب زیستشناسی مولکولی، هنوز محدودیتهای خاصی در کاوش جامع کل سیستم بیولوژیکی در بیماریها وجود دارد [9]. به عنوان یک روش بیولوژیکی سیستماتیک برای توصیف الگوهای ارتباط ژنتیکی بین نمونههای مختلف، تجزیه و تحلیل شبکه همبیان ژن وزنی (WGC-NA) عمدتاً برای غربالگری و شناسایی ماژولهای بسیار مشارکتی استفاده میشود. با توجه به درونی ماژول و رابطه بین ماژول ها و فنوتیپ ها، به طور گسترده ای در مطالعه تحلیل omics برای استخراج نشانگرهای زیستی بالقوه یا اهداف درمانی استفاده شده است [10-12]. در مقایسه با دادههایی که فقط بر بیان تفاضلی تمرکز دارند، WGCNA دارای مزایای زیر است: میتواند از اطلاعات کامل استفاده کند، تغییرات جالب فنوتیپها را به هم مرتبط کند، و از نقصهای تحلیل بیان دیفرانسیل که بهطور مصنوعی آستانهها را تنظیم میکند، اجتناب کند. علاوه بر این، WGCNA نه تنها میتواند سطح mRNA نمونهها را تجزیه و تحلیل کند، بلکه برای تحقیقات میکرو RNA و پروتئومیکس نیز استفاده میشود، که کمک بزرگی در یافتن نشانگرهای بیولوژیکی بالقوه و اهداف درمانی است [13، 14].
در مطالعه حاضر، ما یک روش بیوانفورماتیک به خوبی تثبیت شده - WGCNA - برای تجزیه و تحلیل نمایه بیان (شماره سریال NCBI GEO: GSE121190) انجام دادیم و هدف آن شناسایی مسیرهای بالقوه و ژنهای مرتبط با پیشرفت AKI بود. مهمتر از همه، ما از روشهای تجربی برای تأیید بیشتر ژنهای هاب استفاده کردیم تا بینش جدیدی برای وقوع، توسعه و درمان AKI ارائه کنیم.

روش درمان کلیه سیستانچ ردیت
مواد و روش ها
پیش پردازش داده ها
مجموعه داده ها از پایگاه داده GEO به دست آمده است. در این مطالعه، 12 نمونه از مجموعه داده های GSE121190 برای تجزیه و تحلیل WGCNA استفاده شد. دوازده نمونه شامل گروه کنترل و گروه AKI روز 3-/7-/14- القا شده با اسید فولیک (هر گروه 3 نمونه). بسته R "limma" برای تصحیح پس زمینه و پردازش عادی سازی با داده های اصلی استفاده می شود. اگر پروب های متعدد با 1 ژن مطابقت داشته باشند، مقدار متوسط به عنوان مقدار بیان ژن محاسبه می شود [9، 15].
ساخت و تحلیل عملکردی شبکه Co-Expression
سپس، آستانه نرم توسط الگوریتم WGCNA محاسبه می شود. مقدار مستقل از مقیاس و میانگین اتصال ماژول ها تحت آستانه های نرم مختلف با روش گرادیان به منظور تعیین آستانه نرم مناسب مورد آزمایش قرار گرفت [13، 16، 17]. با انتخاب مقادیر آستانه نرم مناسب، شبکه هم بیانی برای اطمینان از صحت نتایج ساخته شد و حداقل تعداد ژن در هر ماژول وجود نداشت.<30. then,="" use="" the="" r="" package="" "clusterprofiler"="" toolkit="" to="" perform="" go="" analysis="">
تایید ژن هاب
در مرحله بعد، ژن های هاب را با توجه به مقدار آستانه در هر ماژول تجزیه و تحلیل کردیم و با استفاده از نرم افزار Cytoscape آنها را به تصویر کشیدیم. ژن هاب به عنوان معیار زیر در نظر گرفته شد: (الف) قدر مطلق اهمیت ژن (GS)، FA 3/7/14 روز بزرگتر یا برابر با 0.2، و (ب) ژن در ماژول اصلی توسط پایگاه داده STRING برای تولید شبکه تعامل پروتئین-پروتئین (PPI) تجزیه و تحلیل شد و 5 ژن برتر با بالاترین اتصال به عنوان ژن هاب برای تأیید بیشتر مورد بررسی قرار گرفتند [20].
مدل های حیوانی ناشی از سیس پلاتین و هیپوکسی-ایسکمی
موش های نر C57BL/6 (سطح SPF، 6~8-هفته ای، 20~25 گرم) از شرکت حیوانات آزمایشی Chengdu Dashuo، Ltd. (SCXK [Sichuan] 2015-030) خریداری و در خانه نگهداری شدند. و تحت شرایط استاندارد مراقبت در مرکز حیوانات تجربی دانشگاه پزشکی جنوب غربی (SYXK [Sichuan] 2018-065) پرورش داده شد. موش ها

شکل 1. ساخت ماژول بیان مشارکتی. دندروگرام خوشه ای 12 نمونه. B تجزیه و تحلیل توپولوژی شبکه برای آستانه های مختلف نرم (قدرت). C ماژول Co-expression ساخته شده توسط الگوریتم هیبریدی پویا. هر گره برگ نشان دهنده یک ژن است و رنگ های مختلف نشان دهنده ماژول های مختلف در نمودار درختی است.
به 3 گروه (n=6 در هر گروه) طبقه بندی شدند: کنترل، Cis-AKI، و IRI-AKI. به موش های گروه Cis-AKI سیس پلاتین (سیگما آلدریچ، ایالات متحده آمریکا) (15 میلی گرم بر کیلوگرم) با تزریق داخل صفاقی تزریق شد [21]. موش های گروه IRI با 1 درصد سدیم پنتوباربیتال بیهوش شدند و روی یک پتوی الکتریکی ترموستاتیک کوچک قرار گرفتند تا دمای بدن در 36 درجه حفظ شود. پس از بیهوشی، برش های جانبی دو طرفه گرفته شد و شریان های شریانی وریدی بسته شدند.
با گیره شریانی به مدت 35 دقیقه. نمک به صورت قطره ای برای حفظ آن اضافه شدکلیه هامرطوب هر 5 دقیقه پس از برداشتن گیره شریانی، برش ها بخیه شد و موش ها در محیط 37 درجه قرار گرفتند [22، 23]. در پایان دوره آزمایشی، موش ها به ترتیب در روزهای 3 و 7 کشته شدند. نمونه خون موش بود

قبل از دررفتگی دهانه رحم به دست آمده است. تمام مراحل آزمایشی توسط کمیته اخلاق دانشگاه پزشکی جنوب غربی (شماره تأیید: 201812-55) تأیید شد.
تجزیه و تحلیل بافت شناسی و تشخیص عملکرد کلیه
اینکلیهطبق روشهای مرسوم به بخشهای پارافینی تبدیل شد. به طور خلاصه،کلیهبافت ها با فرمالدئید 10 درصد تثبیت شدند، آبگیری شدند و در پارافین جاسازی شدند [24]. مقاطع آبگیری شده و با هماتوکسیلین و ائوزین رنگ آمیزی شدند (بیوتیم، چین). در نهایت، بخشها با میکروسکوپ اسلاید مجازی (VS{2}}S6-W، Olympus، ژاپن) عکسبرداری شدند. در همان زمان، کروم سرم و BUN طبق دستورالعملهای کیت اندازهگیری شدند (Nanjing JianCheng، چین).
جداسازی RNA و PCR کمی
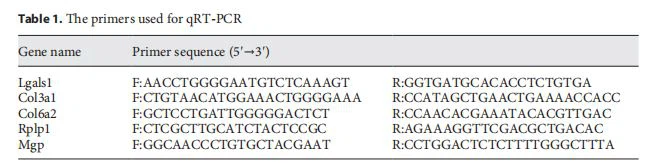
RNA کل با استفاده از کیت استخراج RNA (Tian-gen، Beijing) و DNA مکمل با استفاده از کیت رونویسی معکوس (Promega، شانگهای، چین) مطابق دستورالعمل سازنده به دست آمد. سپس، PCR کمی در سیستم LightCycler® 480 II Real-Time PCR (روش، آلمان) انجام شد. پرایمرها توسط Sangon Biotech (شانگهای، چین) سنتز شدند و توالی ها در جدول 1 موجود است.
وسترن بلات
پروتئین کل جدا و در بافر RIPA حل شد. سپس، غلظت پروتئین با استفاده از کیت سنجش پروتئین BCA (بیوتیم بیوتکنولوژی، چین) شناسایی شد. نمونه های پروتئین بر روی ژل سدیم دودسیل سولفات-پلی آکریل آمید 12 درصد اجرا و به غشاهای PVDF (Millipore, Danvers, MA, USA) منتقل شدند. غشاها با 5 درصد آلبومین سرم گاوی در دمای اتاق به مدت 1 ساعت مسدود شدند و در 4 درجه یک شبه با آنتی بادیهای اولیه نشان داده شده انکوبه شدند: anti-Lgals1 (Cell Signaling Technology, Danvers, MA, USA, 1:1,{10 }}) و آنتی بادی های ضد Rplp1 (Invitrogen, Waltham, MA, USA, 1:500). پس از آن، غشاهای PVDF با تریس بافر سالین توئین شسته و در انکوبه شدند.

دمای اتاق به مدت 1 ساعت با آنتی بادی ثانویه (Invitrogen, Waltham, MA, USA; 1:10,000). نوارها با استفاده از کیت Chemiluminescence ECL (Thermo, Waltham, MA, USA) مشاهده و با استفاده از نرم افزار ImageJ تجزیه و تحلیل شدند.
ایمونوفلورسانس درجا
برای ایمونوفلورسانس بافتی،کلیهبافت ها با محلول فرمالدئید 10 درصد تثبیت شدند و به ترتیب با 10، 20 و 30 درصد ساکارز خشک شدند و سپس در OCT جاسازی شدند. سپس نمونهها به بخشهای 4- میکرومتر تبدیل شدند و 3 بار با PBS به مدت 5 دقیقه شسته شدند. بافت ها با 5 درصد BSA به مدت 1 ساعت در دمای اتاق مسدود شدند و سپس در 4 درجه یک شبه با آنتی بادی های اولیه نشان داده شده انکوبه شدند: anti-Lgals1 (Cell Signaling Technology, Danvers, MA, USA; 1:200) و آنتی بادی های anti-Rplp1. (اینویتروژن، والتهام، MA، ایالات متحده آمریکا؛ 1:100). روز بعد، بافتها با PBS به مدت 5 دقیقه و 3 بار شسته شدند و سپس با آنتیبادیهای ثانویه کونژوگه الکسا فلور® 488- (Cell Signaling Technology، Danvers، MA، USA؛ 1:200) و در دمای اتاق انکوبه شدند. 1 ساعت تصاویر توسط یک میکروسکوپ اسلاید مجازی (VS{24}}S6-W، Olympus، ژاپن) گرفته شد.
تحلیل آماری
آنالیزهای آماری PCR بلادرنگ و وسترن بلات توسط GraphPad Prism 7 انجام شد. در صورت وجود بیش از 2 گروه مقایسه از آنالیز واریانس یک طرفه استفاده شد. p < 0.05="" به="" عنوان="" یک="" تفاوت="" آماری="" در="" نظر="" گرفته="">

شکل 3. تحلیل عملکردی ماژول فیروزه ای. نتایج تجزیه و تحلیل غنیسازی تابع ژن از ماژول فیروزهای. شبکه B PPI از ژن های هاب در ماژول فیروزه ای، و نتایج توسط Cytoscape مشاهده شد. PPI، تعامل پروتئین-پروتئین؛ ECM، ماتریکس خارج سلولی.
نتایج
پیش پردازش داده ها
12 نمونه از داده های آرایه در مجموعه داده های دانلود شده GSE121190 با استفاده از بسته limma زبان R پیش پردازش شدند. برای به دست آوردن ژن های مرتبط با AKI، لازم است تغییرات بیان ژن بین نمونه های طبیعی و AKI مقایسه شود و 25 درصد از ژن ها قبل از واریانس غربال شوند. در نتیجه، در مجموع 5418 ژن برای تجزیه و تحلیل WGCNA دوم به دست آمد.
ساخت ماژول بیان مشارکتی
اول از همه، ابتدا نمونهها برای حذف موارد بیرونی توسط ابزار زبان R hclust خوشهبندی شدند. نتایج در شکل 1A ارائه شده است. سپس، استقلال و میانگین اتصال ماژولها را در آستانههای مختلف اندازهگیری کردیم. همانطور که در شکل 1B نشان داده شده است، می توان از شکل قضاوت کرد که زمانی که مقدار آستانه برابر با 8 باشد، که نه تنها باعث می شود میانگین درجه اتصال شبکه خیلی پایین نباشد، بلکه اطمینان می دهد که شبکه ساخته شده به شبکه بدون مقیاس نزدیک است. شبکه.
در مرحله بعد، ماتریس مجاورت را به یک ماتریس همپوشانی توپولوژیکی تبدیل کردیم تا نویز و همبستگی های کاذب را کاهش دهیم. درخت خوشه بندی سیستم از طریق یک ماتریس همپوشانی توپولوژیکی ایجاد شد، همانطور که در شکل 1C نشان داده شده است. و تعداد ژن ها در هر ماژول توسط الگوریتم برشی هیبریدی پویا کمتر از 30 ژن تعیین شد. در نهایت، 17 ماژول از درخت خوشه سیستم به دست آمد و تعداد ژن های موجود در هر ماژول هم بیانی در جدول 2 نشان داده شده است.
ماژول های کلیدی و غربالگری ژن هاب
پس از آن، ما 3 ماژول برتر (ماژول های قهوه ای، آبی و فیروزه ای) را تجزیه و تحلیل کردیم و به دنبال یافتن ژن های هاب بودیم. الگوهای بیان ژن ها در 3 ماژول مورد تجزیه و تحلیل قرار گرفت. همانطور که در شکل 2 ارائه شد، نتیجه نشان داد که ماژول های آبی و قهوه ای با پیشرفت AKI همبستگی منفی دارند، در حالی که ماژول فیروزه ای با پیشرفت AKI همبستگی مثبت دارد. سپس آنالیز عملکردی را در هر ماژول انجام دادیم و دریافتیم که ژنهای موجود در ماژولهای قهوهای، آبی و فیروزهای کاملاً بهکلیه، توسعه سیستم ادراری تناسلی، برخی از فرآیندهای متابولیک ضروری، و رسوب ماتریکس خارج سلولی (ECM) که به شدت با فیبروز کلیه مرتبط است. به طور خاص، تصور می شود که ماژول فیروزه نقش اساسی در ایجاد فیبروز کلیه پس از AKI ایفا می کند (جزئیات ارائه شده در شکل 3A و مشاهده منبع آنلاین شکل 1A, 2A؛ مراجعه کنید به www.karger.com/doi/ 10.1159/000511661 برای همه مواد تامین آنلاین). سپس به دنبال یافتن ژن های هاب در هر ماژول بودیم و پس از فیلتر اولیه، 5 ژن برتر - Lgals1، Rplp1، Col3a1، Col6a2، و Mgp - در ماژول فیروزه به عنوان ژن هاب در نظر گرفته شدند (همانطور که در شکل 3B نشان داده شده است). ما همچنین تجزیه و تحلیل مشابهی را در ماژولهای آبی و قهوهای انجام دادیم، اما نتوانستیم ژنهای هاب را با توجه به الگوهای بیان و GS آنها پیدا کنیم (همانطور که در منبع آنلاین شکل 1B, 2B ارائه شده است).
بررسی آسیب شناسی بافت شناسی و کلیه
عملکرد
سپس، مدلهای حیوانات Cis-AKI و IRI-AKI را ساختیم. همانطور که در منبع آنلاین نشان داده شده است. شکل 3a، نتایج رنگآمیزی HE نشان میدهد که نکروز لولهای در مدلهای Cis- AKI/IRI-AKI وجود دارد وصدمهبه مرور زمان برجسته شد در همین حال، ما همچنین میتوانیم مشاهده کنیم که در مقایسه با گروه کنترل، افزایش سریع Cr و BUN سرم به روشی وابسته به زمان وجود دارد. در مجموع، همه این نتایج نشاندهنده ساخت موفق مدلهای حیوانی AKI بود.
تایید ژن هاب
برای تأیید بیشتر قابلیت اطمینان روش WGCNA و ژنهای هاب غربالگری که ارتباط نزدیکی با پیشرفت فیبروز کلیوی دارند، بر اساس فوق، هدف ما اعتبارسنجی بیان 5 ژن توپی برتر در مدلهای حیوانی Cis-AKI و IRI-AKI بود. PCR بلادرنگ، وسترن بلات، و ایمونوفلورسانس درجا. سطوح بیان mRNA Lgals1، Rplp1، Col3a1، Col6a2 و Mgp درکلیهموش ها توسط PCR زمان واقعی شناسایی شدند. گزارشهای تحقیقاتی زیادی وجود دارد که نشان میدهد Col3a1، Col6a2 و Mgp با فرآیند فیبروز کلیه مرتبط هستند [23، 25، 26]. با این حال، برای Lgals1 و Rplp1، هیچ مطالعه ای در مورد فیبروز کلیه پس از AKI انجام نشده است، بنابراین وسترن بلات و ایمونوفلورسانس درجا برای تأیید بیشتر بیان Lgals1 و Rplp1 استفاده شد. همانطور که در شکل 4B نشان داده شده است، در مقایسه با گروه عادی، سطح بیان Lgals1 و Rplp1 در موش های Cis-AKI و IRI-AKI نیز به طور قابل توجهی افزایش یافته است. علاوه بر این، ما محل Lgals1 و Rplp1 را با ایمونوفلورسانس درجا ارزیابی کردیم. همانطور که در شکل 5 نشان داده شده است، Rplp1 عمدتا در گلومرول ها و لوله های کلیوی قرار دارد و Lgals1 در لوله های بینابینی و کلیوی توزیع می شود. مهمتر از همه، ما همچنین همبستگی بین Rplp1/Lgals1 و BUN/Cr را تأیید کردیم، و نتایج نشان داد که Rplp1/Lgals1 در سطح پروتئین با BUN/Cr همبستگی مثبت داشت (همه R > 0.5، p < 0.05)="" (شکل="">
بحث
شواهد فزاینده نشان میدهد که AKI در نهایت به CKD/ESRD تبدیل میشود، با بروز بالاتر [4، 27]. تاکنون، درمانهای محدودی برای انتقال از AKI به CKD وجود دارد [28-30]. از این رو، درک بهتر مکانیسم پاتوفیزیولوژیک و شناسایی بیومارکرهای بالقوه برای جلوگیری از این انتقال و بهبود پیش آگهی آن بسیار مفید است. در این مطالعه، ما WGCNA را برای تجزیه و تحلیل دادههای ریزآرایه مربوط به انتقال از AKI به CKD انجام دادیم. در مجموع 17 ماژول به دست آمد، و 3 ماژول اصلی ژن برای تجزیه و تحلیل بیشتر استفاده شد. نتایج حاصل از این مطالعه نشان داد که 3 ماژول ژن ارتباط نزدیکی با یکدیگر دارند
شکل 4. اعتبارسنجی ژن هاب در ماژول فیروزه. کمی سازی بیان mRNA Lgals1، Col3a1، Rplp1، Mgp، و Col6a2 توسط Q-PCR. برای بررسی بیان پروتئین مشخص شده از B وسترن بلات استفاده شد. C تعیین کمیت بیان پروتئین با اسکن چگالی سنجی. ***p < 0.001="" در="" مقایسه="" با="" گروه="" کنترل.="" d،="" e="" همبستگی="" بین="" rplp1/lgals1="" و="" bun/cr="" (همه="" r=""> 0.5، p <>




شکل 5. اعتبارسنجی محل ژن هاب در ماژول فیروزه. A، B محل و بیان Lgals1 و Rplp1 به ترتیب توسط ایمونوفلورسانس درجا.
توسعه فیبروز کلیه پس از AKI در طبقه بندی GO، به عنوان مثال، توسعه سیستم کلیوی، توسعه عروقی کلیه [31، 32]، برخی از فرآیندهای متابولیک [33، 34]، غشای داخلی میتوکندری، غشای داخلی اندامک، و ECM [35-37] ]. عدم تعادل ECM یکی از دلایل اصلی فیبروز کلیه است. پس از AKI، فیبروز تحت تأثیر عوامل متعددی مانند سلول های التهابی انباشته شده، میوفیبروبلاست های فعال شده و غیره قرار می گیرد [30، 33]. بنابراین، مطالعه حاضر بر روی ماژول فیروزه متمرکز شده است زیرا ماژول به شدت با ECM مرتبط است.
سپس، با محاسبه GS، ژنها را در ماژول فیروزه فیلتر کردیم و سپس شبکه PPI را تولید کردیم. از شبکه PPI در ماژول فیروزه می توان نتیجه گرفت که 6 ژن S100a6، Col3a1، Col6a2، Mgp، Rplp1 و Lgals1 بیشترین ارتباط را با سایر ژن های همسایه نشان می دهند و در مرکز شبکه PPI قرار دارند. S100a6 با عضوی از خانواده پروتئین S100 کدگذاری می شود. در ادبیات گزارش شده است که S100a6 ممکن است تکثیر سلولی را تنظیم کند و در فرآیندهای پاتولوژیک با واسطه ایمنی انتقال اپیتلیال- مزانشیمی کلیه و فیبروز شرکت کند [38، 39]. Col3a1 و Col6a2 به ترتیب کلاژن نوع III آلفا-1 و کلاژن نوع VI آلفا-2 زنجیره هستند. آنها کلاژن را کد می کنند، به پروتئین های ماشین خارج سلولی متصل می شوند و در اجزای ماتریکس سلولی بسیار مهم هستند. هنگامی که فیبروز در اندام هایی مانند کبد و کلیه رخ می دهد، بیان این کلاژن ها افزایش می یابد که یک شاخص اساسی برای قضاوت در مورد پیشرفت بیماری و مشاهده اثر درمانی است [23، 25]. Mgp، ماتریکس پروتئین Gla، عضوی از خانواده استئوکلسین/Mgp است که پس از CKD بیان می شود و با پیش آگهی کلیوی مرتبط است [26، 40]. مطابق با مطالعات قبلی، تحقیقات ما همچنین نشان داد که S100a6، Col3a1، Col6a2 و Mgp نشانگرهای بالقوه تشخیصی اولیه فیبروز کلیه پس از AKI هستند.
Rplp1، یک ژن کد کننده پروتئین ریبوزومی که بخشی از زیرواحد 60S است، نقش مهمی در مرحله افزایش طول سنتز پروتئین ایفا می کند. Rplp1 در چندین سلول سرطانی انسان به شدت بیان می شود و فقدان آن بر سنتز پروتئین تأثیر می گذارد و منجر به آپوپتوز می شود [41، 42]. Lgals1 که با نام گالکتین{6}} نیز شناخته میشود، عضوی از خانواده پروتئین -گالاکتو- پیوند جانبی است و در تنظیم آپوپتوز، تکثیر سلولی و تمایز سلولی نقش دارد. Lgals1 یک نقطه داغ تحقیقاتی در زمینه تومورها است و بسیاری از مطالعات اخیر گزارش داده اند که نقش حیاتی در روند فیبروز اندام ایفا می کند. نشان داده شده است که Lgals1 در کلیه های دیابت نوع I و II به شدت بیان می شود و یک نشانگر جدید فیبروز کلیه است [43-45]. با این حال، شایان ذکر است که Rplp1 و Lgals1 در فیبروز کلیه پس از AKI گزارش نشده است. در مطالعه حاضر، ما به طور اولیه ثابت کردیم که Rplp1 و Lgals1 ممکن است به عنوان نشانگرهای زیستی بالقوه در فیبروز کلیه پس از AKI توسط بیوانفورماتیک و روش تجربی مورد استفاده قرار گیرند. تجزیه و تحلیل های تجربی متعدد ما نشان داد که نمایش Lgals1 و Rplp1 به طور چشمگیری در کلیه های IRI-AKI و Cis-AKI افزایش یافته است و بیان 2 ژن پس از 3 روز افزایش یافته و پس از 7 روز کاهش می یابد، که با نتایج تجزیه و تحلیل شده مطابقت دارد. روش بیوانفورماتیک WGCNA
لازم به ذکر است که مطالعه دارای چندین محدودیت است: اول اینکه تعداد نمونه های مورد استفاده برای تجزیه و تحلیل نسبتاً ناکافی است که ممکن است دقت آنالیز را حذف یا کاهش دهد. دوم، ژنهای هاب فقط در مدل جوندگان AKI به جای نمونههای انسانی مورد بررسی قرار گرفتند که ممکن است ترجمه یافتهها را از موش به انسان نیز مختل کند. مطالعات زیادی در مورد LGALS1 در سرطان انسان وجود دارد و بیان آن در سرطان کلیه افزایش یافته است. هدف قرار دادن LGALS1 می تواند از توسعه تومورهای آن جلوگیری کند. اگرچه RPLP1 در اندومتریوز، تومورهای زنان و سایر بیماری ها یافت شده است، اما در کلیه های انسان مطالعه نشده است. تحقیقات بیشتر در مورد ژن های هاب بر روی نمونه های انسانی مانند دفع ادرار ممکن است نقش بیولوژیکی آنها را از نظر بالینی بهتر روشن کند. در نتیجه، مطالعه حاضر پایه و اساس مطالعه بیشتر نقش Rplp1 و Lgals1 در AKI را ایجاد کرد.

cistanche شگفت انگیزبرایبهبودی کلیه
نتیجه گیری
به طور خلاصه، این مطالعه ژن های کلیدی مرتبط با AKI را از طریق تجزیه و تحلیل WGCNA شناسایی کرد و به طور تجربی 2 ژن هاب را با پتانسیل برای تحقیقات بیشتر پیدا کرد، Rplp1 و Lgals1. با این حال، مکانیسم خاص در پاتوژنز AKI تحقیقات بیشتر باقی مانده است. ژنهای کاندید حیاتی انتخاب شده جهتهای تحقیقاتی جدیدی را برای پیشگیری، تشخیص، درمان و پیشآگهی فیبروز کلیه ارائه میکنند.
بیانیه اخلاق
همه حیوانات مطابق با دستورالعمل های مؤسسه ملی بهداشت برای استفاده و مراقبت از حیوانات تحقیقاتی تحت درمان قرار گرفتند.
بیانیه تعارض منافع
نویسندگان اعلام کردند که تضاد منافع وجود ندارد.
منابع تامین مالی
این کار توسط Luzhou - پروژه پلت فرم مشترک پزشکی جنوب غربی (2017LZXNYD-P01 و 2018LZXNYD-PT03)، پروژه ساخت و ساز آزمایشگاه کلیدی پزشکی استان سیچوان (2018#53)، پروژه علم و فناوری سیچوان (2020YJ04) پشتیبانی شد. کمک مالی مشترک شهرداری لوژو - دانشگاه پزشکی جنوب غربی برای معرفی استعدادهای سطح بالا (تیم لان هوی-یائو). and the Southwest Medical University and Affiliated Traditional Medicine Hospital Hospital (2018XYLH-029).
مشارکت های نویسنده
لی وانگ و جیانچون لی این مطالعه را تصور و هماهنگ کردند. شیائو لین مقاله را نوشت. جیانچون لی مقاله را اصلاح کرد. جیانچون لی تجزیه و تحلیل بیوانفورماتیک را انجام داد. شیائو لین آزمایش حیوانی را انجام داد و PCR، IHC و IF را در زمان واقعی انجام داد. Xia Zhong و Jieke Yang WB را انجام دادند و نمونه های کلیوی موش را جمع آوری کردند. رویزی تان تجزیه و تحلیل آماری را انجام داد. همه نویسندگان نتایج را بررسی کردند و نسخه نهایی نسخه خطی را تایید کردند.

تجربه مکملهای سیستانچ در تنظیم عملکرد کلیه
