روزه داری متناوب در سرطان پستان: مروری سیستماتیک و به روز رسانی انتقادی مطالعات موجود قسمت 2
Aug 14, 2023
3.1.4. پیامدهای مرتبط با غدد درون ریز
ما چهار مطالعه را شناسایی کردیم که دادههای مربوط به غلظت انسولین، گلوکز، کتونها، فاکتور رشد شبه انسولین-1 (IGF-1) و پروتئین متصل شونده به IGF (IGFBP) را گزارش کردند.
سیستانچ می تواند به عنوان یک ضد خستگی و تقویت کننده استقامت عمل کند و مطالعات تجربی نشان داده اند که جوشانده سیستانچ توبولوزا می تواند به طور موثری از سلول های کبدی و سلول های اندوتلیال آسیب دیده در موش های شناگر محافظت کند، بیان NOS3 را افزایش دهد و گلیکوژن کبدی را تقویت کند. سنتز، در نتیجه اعمال اثر ضد خستگی. عصاره Cistanche tubulosa غنی از گلیکوزید فنیل اتانوئید می تواند به طور قابل توجهی سطح کراتین کیناز، لاکتات دهیدروژناز و لاکتات سرم را کاهش دهد و سطح هموگلوبین (HB) و گلوکز را در موش ICR افزایش دهد و این می تواند با کاهش آسیب عضلانی نقش ضد خستگی ایفا کند. و به تاخیر انداختن غنی سازی اسید لاکتیک برای ذخیره انرژی در موش. قرص Cistanche Tubulosa به طور قابل توجهی زمان شنای تحمل وزن را طولانی کرد، ذخیره گلیکوژن کبدی را افزایش داد و سطح اوره سرم را پس از ورزش در موش کاهش داد و اثر ضد خستگی آن را نشان داد. جوشانده سیستانچی می تواند استقامت را بهبود بخشد و خستگی را در موش های ورزشکار تسریع کند و همچنین می تواند افزایش کراتین کیناز سرم را بعد از تمرین بارگذاری کاهش دهد و فراساختار ماهیچه های اسکلتی موش ها را پس از ورزش نرمال نگه دارد که نشان دهنده تأثیر آن است. افزایش قدرت بدنی و ضد خستگی Cistanchis همچنین به طور قابل توجهی زمان بقای موش های مسموم با نیتریت را طولانی کرد و تحمل در برابر هیپوکسی و خستگی را افزایش داد.

همیشه روی خسته کلیک کنید
【برای اطلاعات بیشتر:george.deng@wecistanche.com / WhatApp:8613632399501】
زورن و همکاران [25] اثرات IF را بر پارامترهای متابولیک سرم قبل از هر چرخه شیمی درمانی مطالعه کردند. پارامترهای متابولیک شامل غلظت سرمی انسولین، IGF-1، هورمون محرک تیروئید (TSH)، تری یدوتیرونین آزاد (fT3) و تیروکسین آزاد (fT4) بود. نویسندگان کاهش قابل توجهی در غلظت میانگین fT3 در گروه STF گزارش کردند (-0.47 ± 0.09؛ 95% فاصله اطمینان (CI)، 0.64–( −0.30؛ p < {{20}}.001)، در حالی که میانگین fT4 به طور قابل توجهی در طول چرخه های STF افزایش یافت در مقایسه با چرخه کالری نرمال (0.37 ± 0.82؛ 95% فاصله اطمینان (CI)، 0.09-1.55؛ p=0.028). در نهایت، هر دو میانگین غلظت انسولین (44.1±169.4-؛ 95% فاصله اطمینان (CI)، 257.1-(-81.8)؛ p <0.001) و IGF{40}} (5.4 ± 33.3؛ 95% CI، 44.1-(22-) ؛ p <0.001) به طور قابل توجهی در طول چرخه STF کاهش یافت [25].
دی گروت و همکاران (2015) [27] غلظت سرمی گلوکز، انسولین، IGF-1، هورمون محرک تیروئید (TSH) و پروتئین اتصال دهنده فاکتور رشد انسولین 3 (IGF-BP3) را در هر دو گروه IF و غیر IF (شاهد شاهد) مورد مطالعه قرار دادند. ). نمونه خون وریدی قبل از تصادفی سازی، حداکثر 2 هفته قبل از درمان (پایه) و مستقیماً قبل از تجویز شیمی درمانی گرفته شد. مقادیر متوسط گلوکز خون در هر دو گروه، بین دو نقطه زمانی افزایش یافت (به ترتیب 0.042.0=0 و p=0.043).
در گروه STF، تفاوت معنی داری در غلظت انسولین میانه بین نقاط دو زمانی گزارش نشد، اما در گروه غیر STF، انسولین ناشتا افزایش یافت (0.043.p=0). میانگین غلظت IGF{4}} در گروه STF (که 24 ساعت قبل و بعد از شروع شیمی درمانی ناشتا بودند) افزایش یافت (012/0=0) اما در گروه غیر STF تغییری گزارش نشد، در حالی که هیچ تغییری مشاهده نشد. در هر گروهی برای غلظت IGF-BP3 مشاهده شد. در نهایت، TSH به طور قابل توجهی در گروه غیر STF کاهش یافت (p=0.034) اما در گروه STF کاهش یافت [27].
دورف و همکاران [28] سه گروهی را که قبل از شیمی درمانی به مدت 24، 48 و 72 ساعت (به 48 قبل از شیمی درمانی و 24 بعد از شیمی درمانی تقسیم شده بودند) در بیماران قبل از میلاد که قبلاً با TCH (دوستاکسل، کربوپلاتین، تراستوزوماب) درمان شده بودند، مورد مطالعه قرار دادند. از مهمترین موارد، غلظت IGF{8}} به طور میانگین 3-0٪ (-44٪، -12٪) در گروه 24 ساعته، -33٪ در گروه 48 ساعته و - کاهش یافت. 8% در گروه 72 ساعته 1-روز پس از شیمی درمانی (p=0.32 در مقایسه با هر 3 گروه کوهورت)، در حالی که غلظت سرمی هیدروکسی بوتیرات در گروههای 48 و 72 ساعت پس از شیمیدرمانی افزایش یافت. 28]. ماریناک و همکاران همچنین گزارش داد که هر 2 ساعت افزایش در مدت زمان ناشتا بودن شبانه با سطح هموگلوبین A1C (HbA1c) 0}}.37 mmol/mol ({32}} -0}.37؛ 95% CI) مرتبط است. ، −0.72 تا -0.01) [23].
3.1.5. اثرات نامطلوب IF
اثرات نامطلوب مرتبط با روزه در چهار مطالعه گزارش شده است. در اکثریت قریب به اتفاق، عوارض جانبی پس از شروع شیمی درمانی [19] رخ می دهد، از جمله سردرد، تب، بی خوابی، خستگی، سرگیجه، سبکی سر، کاهش وزن، هیپوگلیسمی، هیپوناترمی و افت فشار خون، گرسنگی، حالت تهوع خفیف پس از مصرف آبگوشت یا آب میوه، و واکنش های ارتواستاتیک، در حالی که در برخی موارد، سوء تغذیه و سوء تغذیه گزارش شده است [19،20،28]. هیچ عارضه جانبی شدید مرتبط با روزه گزارش نشد و کاهش وزن ناشی از روزه به سرعت توسط اکثر بیماران به دست آمد.
4. بحث
طبق دانش ما، این اولین بررسی سیستماتیک از اثرات زیرگروه های IF بر بیماران BC است.

ما داده های موجود را به علائم گزارش شده توسط بیمار از طریق نمرات کیفیت زندگی، و همچنین نشانگرهای سرمی بالینی و عینی سمیت ناشی از شیمی درمانی و پیامدهای مرتبط با غدد درون ریز تقسیم کردیم تا هرگونه مزیت بالینی بالقوه IF را در محیط بالینی روزانه شناسایی کنیم. نتایج موجود با درجه بالایی از ناهمگونی در رابطه با رژیمهای IF، مدت زمان و پیامدهای سلامت از پیش تعیینشده در ارتباط با زمان اجرای IF، و همچنین عدم گنجاندن گروههای کنترل در بیشتر مطالعات مشخص شد (n=7). با این حال، ما فرض میکنیم که بهبود نشانگرهای آزمایشگاهی سمیت ناشی از شیمیدرمانی شناساییشده در سه مطالعه میتواند ابزار مفیدی برای آزمایشهای کنترلشده به خوبی طراحیشده آینده در این زمینه باشد.
اکثر مطالعات (n=4) که بر روی اثرات بالقوه IF بر کیفیت زندگی بیماران قبل از میلاد تحت شیمیدرمانی متمرکز شدهاند، بهبودی را در مقیاسهای FACT-G و FACIT-F و همچنین معیارهای اصطلاحات رایج مبتنی بر امتیاز گزارش کردند. برای رویدادهای نامطلوب موسسه ملی سرطان [16-19]. با این حال، هیچ معیار تایید شده اضافی از کیفیت زندگی، و همچنین هرگونه تنظیم برای عوامل اضافی که می تواند با علائم گزارش شده توسط بیمار تداخل داشته باشد، گنجانده نشد. اگرچه بیماران قبل از میلاد تحمل بیشتری نسبت به شیمی درمانی نشان دادند و در عوارض جانبی ناشی از شیمی درمانی (مانند خستگی، تهوع، استفراغ، کاهش اشتها و اضطراب) بهبود یافتند، ما داده های موجود را کمیاب و با کیفیت پایین برای بهبود کیفیت زندگی قبل از میلاد در نظر می گیریم. بیماران.
در تجزیه و تحلیل خود، بهبودی را در نشانگرهای آسیب DNA پس از شیمی درمانی شناسایی کردیم، و یک رویکرد عملی برای شناسایی مزایای واضح از طریق کارآزماییهای خوب طراحی شده آینده را ترسیم کردیم.
بهبود استرس اکسیداتیو لکوسیتی و -H2AX (تشکیل شده توسط فسفوریلاسیون باقیمانده سر{2}} نوع هیستونی H2AX) [24]، و همچنین گشتاور دم زیتون به عنوان نشانگرهای شکستگی DNA دو رشته ای ناشی از شیمی درمانی. این نشانگرها به طور گسترده برای اندازه گیری آسیب DNA پس از تابش استفاده می شوند، جایی که ثابت شده است که بیان با آسیب بافت سالم مرتبط است [27]. فسفوریلاسیون H2AX نشان دهنده وجود شکستگی های DNA دو رشته ای است و بنابراین می تواند به عنوان نشانگری برای سمیت ناشی از شیمی درمانی در سلول های سالم استفاده شود، همانطور که در کارآزمایی فاز I/II با بیماران تحت درمان با ترکیبی از شیمی درمانی و بلینوستات مشاهده شد [27] ]. با این وجود، استفاده از -H2AX به عنوان یک نشانگر برای سمیت ناشی از شیمی درمانی برای سلول های طبیعی نسبتاً بررسی نشده است [27].
ما نتوانستیم اثرات قابل توجه IF را بر پاسخ شیمی درمانی یا رادیولوژیکی و عود تومور شناسایی کنیم. نتایج موجود محدود بود و معیارهای تأیید شده عود بیماری را در بر نگرفته است، همچنین در یک مورد بر اساس دادههای خود گزارششده و تماسهای تلفنی نیمهسالانه.
این نتایج نمیتواند نتایج قبلی را در مدلهای موش تأیید کند، جایی که دو چرخه ناشتا در ترکیب با سیکلوفسفامید برای کاهش رشد تومور در دوره کوتاهمدت کافی است [29].
می توان فرض کرد که در انسان، تعداد بیشتری از چرخه های FMD ممکن است برای مشاهده برخی مزایای بالینی مهم تر باشد. در آن زمینه، بهبود پایبندی بیمار، برای دوره های طولانی تر، می تواند برای مشاهده هرگونه فعالیت ضد توموری مرتبط با FMD مفید باشد [29]. یافته جالب دیگر کاهش گزارش شده غلظت انسولین و IGF-1 در گروه های ناشتا در دو مطالعه و همچنین افزایش غلظت سرمی هیدروکسی بوتیرات پس از 48 و 72 ساعت پس از شیمی درمانی بود. با این حال، این یافته ها با وزن بدن، سن و توده عضلانی تنظیم نشدند. مدل های حیوانی قبلی نشان می دهد که سرم-هیدروکسی بوتیرات یک مهارکننده قوی هیستون داستیلاز درون زا است که از سلول ها در برابر استرس اکسیداتیو محافظت می کند. از سوی دیگر، افزایش غلظت IGF{8}} آپوپتوز را مهار میکند، تکثیر سلولی را تقویت میکند و باعث بیثباتی ژنتیکی میشود و تومورزایی را افزایش میدهد [30]. مطالعات آینده برای ایجاد ارتباط علت و معلولی بین کتوژنز ناشی از IF و اثرات روی محور IGF{13}} و پیامدهای خاص مربوط به BC در انسان مورد نیاز است.
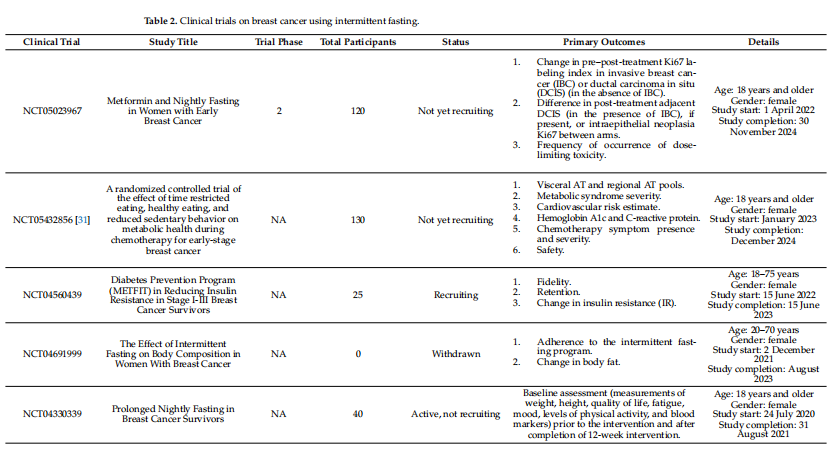
به طور کلی، IF در جمعیت های موجود در این تجزیه و تحلیل به خوبی تحمل شد، و نشان می دهد که می تواند یک رویکرد عملی و ایمن برای بهبود نتایج سلامت در ارتباط با رژیم های شیمی درمانی معتبر یا سایر روش های درمانی باشد. یکی از مطالعات وارد شده [23] گزارش داد که بیمارانی که بیشتر از یا مساوی 13- ساعت روزه میگیرند، خطر عود قبل از میلاد را کاهش میدهند، اما این یافتهها در سایر مطالعات موجود تأیید نشد. لازم به تاکید است که کاهش وزن ناشی از روزه پس از قطع دوره های IF لغو شد، یافته ای که می تواند برای بیماران مبتلا به کاشکسی مهم تلقی شود، اما چالش بازیابی وزن در زنان چاق مبتلا به این بیماری را نیز به همراه دارد. در حال حاضر، چهار کارآزمایی بالینی در حال انجام است (یکی از آنها خارج شد) (جدول 2) که اثرات IF را در بیماران BC مطالعه میکنند، که طیف متغیر در این زمینه و نیاز به کارآزماییهای مداخلهای کنترلشده به خوبی طراحی شده را برجسته میکند.
این بررسی سیستماتیک دارای چندین محدودیت است. اول، ما فقط مطالعات منتشر شده به زبان انگلیسی را شامل میشویم. دوم، به دلیل ناهمگونی انواع سرطان، مداخلات و نقاط پایانی مطالعات وارد شده، ما نتوانستیم یک متاآنالیز انجام دهیم. در نهایت، اگرچه ما با نویسندگانی تماس گرفتیم که دادههای بیشتری را برای پیامدهای اضافی درخواست میکردند، پاسخها فقط محدود به موارد ارائهشده در تجزیه و تحلیل فعلی بود، بنابراین پیامدهای بهداشتی اضافی لحاظ نشدند.
تا آنجا که به نقاط قوت مرور سیستماتیک ما مربوط می شود، مطالعات شامل چندین نوع روزه داری است که بینشی کامل از طیف گسترده ای از زیرگروه های IF ارائه می دهد. علاوه بر این، موضوع این بررسی تحت یک زمینه کاملاً ناشناخته و مورد علاقه قرار می گیرد، بنابراین مطالعه ما را از دیدگاه ما، مبتکرانه می کند.
در نتیجه، ما نتوانستیم اثرات مفید مرتبط با IF را بر کیفیت زندگی، پاسخ پس از شیمی درمانی، یا علائم مرتبط و همچنین معیارهای عود تومور در بیماران BC شناسایی کنیم. ما یک اثر بالقوه سودمند IF را بر سمیت ناشی از شیمی درمانی، بر اساس نشانگرهای DNA و آسیب لکوسیت شناسایی کردیم. با این حال، این نتایج از سه مطالعه به دست آمده و نیاز به اعتبار بیشتر دارد.
مشارکت نویسنده:جستجوی ادبیات، غربالگری عنوان/چکیده، ارزیابی کامل مقاله، ارزیابی کیفیت مقالات، و استخراج داده ها به طور مستقل توسط MA، AV، و VK انجام شد. وضوح و/یا تایید MA، AV، و SNK پیش نویس دستنوشته را تهیه کردند. SNK نسخه نهایی نسخه خطی را نوشت. همه نویسندگان نسخه منتشر شده نسخه خطی را خوانده و با آن موافقت کرده اند.

منابع مالی: این تحقیق هیچگونه بودجه خارجی دریافت نکرده است.
بیانیه هیئت بررسی نهادی:قابل اجرا نیست.
بیانیه رضایت آگاهانه:قابل اجرا نیست.
بیانیه در دسترس بودن داده ها:داده های ارائه شده در مطالعه در صورت درخواست نویسنده مسئول در دسترس است.
تضاد علاقه:نویسندگان هیچ تضاد منافع را اعلام نمی کنند.
منابع
1. کمیته مشورتی آمار سرطان کانادا. انجمن سرطان کانادا 2021.
2. دوسوس، ال. خیمنز-کرونا، ای. رومیو، آی. Boutron-Ruault، MC; بوتن، آ. دوپره، تی. فاغرازی، جی. کلاول-چاپلون، اف. Mesrine، پروتئین واکنشی S. C و خطر سرطان پستان پس از یائسگی: نتایج حاصل از مطالعه کوهورت E3N. کنترل علل سرطان 2014، 25، 533-539. [CrossRef]
3. Longo، VD; فونتانا، L. محدودیت کالری و پیشگیری از سرطان: مکانیسم های متابولیک و مولکولی. Trends Pharmacol. علمی 2010، 31، 89-98. [CrossRef]
4. Rynders، CA; توماس، EA; زمان، ع. پان، ز. کاتناچی، VA; ملانسون، EL اثربخشی روزهداری متناوب و تغذیه محدود با زمان در مقایسه با محدودیت انرژی مداوم برای کاهش وزن. Nutrients 2019, 11, 2442. [CrossRef] [PubMed]
5. دونالدسون، ام اس تغذیه و سرطان: مروری بر شواهد رژیم غذایی ضد سرطان. Nutr. J. 2004, 3,
19. [CrossRef] [PubMed]
6. دانلی، LS; Shaw, RL; پگینگتون، ام. آرمیتاژ، سی جی; ایوانز، دی جی؛ هاول، آ. هاروی، MN "برای من این است که احساس نکنم در حال رژیم هستم": تجزیه و تحلیل موضوعی از تجربیات زنان از یک رژیم غذایی متناوب با محدودیت انرژی برای کاهش خطر سرطان سینه. جی. هوم. Nutr. رژیم غذایی 2018، 31، 773-780. [CrossRef]
7. مالینوفسکی، بی. زالوسکا، ک. W˛esierska، A.; Sokołowska، MM; سوشا، م. لیزنر، جی. پاولاک اوسی نسکا، ک. Wici ´nski، M. روزه متناوب در اختلالات قلبی عروقی - مروری. مواد مغذی 2019، 11، 673. [CrossRef]
8. کلیفتون، KK; ما، CX; فونتانا، ال. پترسون، LL روزه متناوب در پیشگیری و درمان سرطان. CA Cancer J. Clin. 2021، 71، 527-546. [CrossRef] [PubMed]
9. Lv، M. زو، ایکس. وانگ، اچ. وانگ، اف. Guan، W. نقش محدودیت کالری، رژیم غذایی کتوژنیک و روزه متناوب در طول شروع، پیشرفت و متاستاز سرطان در مدل های حیوانی: یک بررسی سیستماتیک و متاآنالیز. PLoS ONE 2014, 9, e115147. [CrossRef] [PubMed]
10. لوین، من; سوارز، جی. برندهورست، اس. بالاسوبرامانیان، پ. چنگ، سی.-و. مادیا، اف. فونتانا، ال. میریسولا، ام جی؛ گوارا آگیره، جی. وان، جی. و همکاران مصرف کم پروتئین با کاهش عمده IGF-1، سرطان و مرگ و میر کلی در جمعیت 65 ساله و جوانتر اما نه مسنتر همراه است. سلول متاب. 2014، 19، 407-417. [CrossRef]
11. کیم، ای جی; چوی، م.-ر. پارک، اچ. کیم، ام. هنگ، جی. لی، جی.-ای. چون، اچ اس. لی، KW; پارک، JHY چربی رژیم غذایی رشد تومور جامد و متاستاز سلول های سرطان پستان موش 4T1 و مرگ و میر را در موش های BALB/c مقاوم به چاقی افزایش می دهد. سرطان سینه Res. 2011، 13، R78. [CrossRef]
12. Lamming، DW; کامینگز، NE; راستلی، آل. گائو، اف. کاوا، ای. برتوزی، بی. اسپلتا، اف. پیلی، ر. فونتانا، L. محدودیت پروتئین رژیم غذایی، mTORC1 را در تومورها و بافت های بدنی مدل زنوگرافت موش حامل تومور کاهش می دهد. Oncotarget 2015, 6, 31233–31240. [CrossRef] [PubMed]
13. ساندارام، س. Yan, L. تغذیه با محدودیت زمانی باعث کاهش تومورزایی پستان با رژیم غذایی پرچرب در موشهای MMTV-PyMT میشود. Nutr. Res. 2018، 59، 72-79. [CrossRef] [PubMed]
14. لی، سی. صفدی، اف.ام. رافاقلو، ال. وی، ام. مادیا، اف. پارلا، ای. هوانگ، دی. کوهن، پی. بیانچی، جی. Longo، VD سطوح کاهش یافته IGF-I حفاظت افتراقی از سلول های طبیعی و سرطانی را در پاسخ به روزه داری و بهبود شاخص شیمی درمانی واسطه می کند. سرطان Res. 2010، 70، 1564-1572. [CrossRef]
15. هنگ، QN; Pluye، P. فابرگس، اس. بارتلت، جی. بردمن، اف. باربری، م. داگنایس، پ. گانیون، M.-P. گریفیث، اف. نیکلائو، بی. و همکاران ابزار ارزیابی ترکیبی (MMAT)، نسخه 2018؛ ثبت حق چاپ (#1148552); دفتر مالکیت معنوی کانادا: Gatineau، QC، کانادا، 2018.
16. Cella, D. The Functional Assessment of Cancer Therapy-Anemia (FACT-An): ابزاری جدید برای ارزیابی نتایج در کم خونی و خستگی سرطان. سمین. هماتول. 1997، 34، 13-19. [PubMed]
17. کلکنر، ا. Reschke، JE; آلتمن، بیجی؛ بلچر، ای. دان، RF؛ فلمینگ، اف جی; گیلمور، ن. جنسن-باتالیا، م. کلکنر، آی. لین، پی. و همکاران یک مداخله غذایی با محدودیت زمانی 10-ساعته برای رفع خستگی مرتبط با سرطان در میان بازماندگان سرطان. جی. کلین. اونکول. 2021، 39، 12109. [CrossRef]
18. مندوزا، TR; وانگ، XS; کلیلند، CS; موریسی، ام. جانسون، کارشناسی; Wendt، JK; Huber، SL ارزیابی سریع شدت خستگی در بیماران سرطانی: استفاده از فهرست خستگی مختصر. سرطان 1999، 85، 1186-1196. [CrossRef]
19. Bauersfeld, SP; Kessler، CS; ویشنیوسکی، م. یانش، آ. استکهان، ن. استنج، آر. کونز، بی. بروکنر، بی. سهولی، ج. Michalsen، A. اثرات روزه داری کوتاه مدت بر کیفیت زندگی و تحمل به شیمی درمانی در بیماران مبتلا به سرطان پستان و تخمدان: یک مطالعه آزمایشی متقاطع تصادفی. BMC Cancer 2018, 18, 476. [CrossRef]
20. بدار، ت. اسماعیل، ع. الشانقیتی، الف. ایمنی و امکان سنجی روزه داری مسلمانان هنگام دریافت شیمی درمانی. IOSR J. Pharm. 2014، 4، 15-20. [CrossRef]
21. ماس، س. Le Bonniec، A. Cousson-Gélie, F. چرا زنان در طول شیمی درمانی سرطان سینه روزه می گیرند؟ مطالعه کیفی تجربه بیمار. برادر J. روانی سلامت. 2019، 24، 381-395. [CrossRef]
22. صفدی، اف.ام. دورف، تی. کوین، دی. فونتانا، ال. وی، ام. لی، سی. کوهن، پی. Longo، VD Fasting و درمان سرطان در انسان: گزارش سری مورد. پیری 2009، 1، 988-1007. [CrossRef]
23. Marinac، CR; نلسون، SH; برین، CI; هارتمن، اس جی. ناتاراجان، ال. پیرس، جی پی؛ Flatt، SW; سیرز، دی دی. پترسون، RE روزهداری طولانیمدت شبانه و پیشآگهی سرطان سینه. جاما اونکول. 2016، 2، 1049-1055. [CrossRef]
24. ماه، LJ; ال اوستا، ا. Karagiannis، T. H2AX: نشانگر مولکولی حساس آسیب و ترمیم DNA. لوسمی 2010، 24، 679-686. [CrossRef]

25. زورن، اس. اهرت، ج. شوبله، آر. راوتنبرگ، بی. آیهورست، جی. برتز، اچ. اوربان، پ. راینور، الف. تأثیر روزهداری کوتاهمدت اصلاحشده و ترکیب آن با رژیم غذایی حمایتی روزهدار در طول شیمیدرمانی بر بروز و شدت سمیتهای ناشی از شیمیدرمانی در بیماران سرطانی - یک مطالعه آزمایشی متقاطع کنترلشده. BMC Cancer 2020, 20, 578. [CrossRef]
26. دی گروت، اس. لوگتنبرگ، RT; کوهن، دی. Welters، MJP; احسان، من. Vreeswijk، MPG; اسمیت، VTHBM؛ د گراف، اچ. Heijns، JB; Portielje، JEA; و همکاران گروه تحقیقات سرطان پستان هلندی (BOOG). رژیم غذایی تقلید ناشتا به عنوان مکمل شیمی درمانی نئوادجوانت برای سرطان سینه در کارآزمایی تصادفی فاز 2 DIRECT چند مرکزی. نات. اشتراک. 2020، 11، 3083. [CrossRef] [PubMed]
27. دی گروت، اس. Vreeswijk، نماینده مجلس؛ Welters, MJ; گریوستاین، جی. بوئی، جی جی. یوچمز، ا. هوتسما، دی. پوتر، اچ. ون در هوون، جی جی; نورتیه، جی دبلیو. و همکاران اثرات روزه داری کوتاه مدت بر تحمل شیمی درمانی کمکی (نئو) در بیماران مبتلا به سرطان پستان منفی HER: یک مطالعه آزمایشی تصادفی شده. BMC Cancer 2015, 15, 652. [CrossRef]
28. دورف، سل; گروشن، اس. گارسیا، آ. شاه، م. تسائو وی، دی. فام، اچ. چنگ، CW; برندهورست، اس. کوهن، پی. وی، ام. و همکاران ایمنی و امکان سنجی روزه داری در ترکیب با شیمی درمانی مبتنی بر پلاتین. BMC Cancer 2016, 16, 360. [CrossRef]
29. ورنیری، سی. لیگوریو، اف. زاترین، ای. ریولتینی، ال. de Braud، F. رژیم غذایی تقلید کننده روزه به همراه شیمی درمانی در درمان سرطان سینه. نات. اشتراک. 2020, 11, 4274. [CrossRef]
30. تیواری، س. ساپکوتا، ن. Han, Z. اثر روزه بر سرطان: مروری روایی شواهد علمی. Cancer Sci. 2022، 113، 3291-3302. [CrossRef] [PubMed]
31. کریستنسن، RA; هایکوکسی، ام جی. نادلر، م. پرادو، سی ام؛ کوچک، SD؛ ریکارد، JN; پیتوسکین، ای. پاترسون، دی. مکی، جی آر. تامپسون، RB; و همکاران منطق و طراحی IMPACT-women: یک کارآزمایی تصادفیسازی و کنترلشده در مورد تأثیر خوردن محدود به زمان، تغذیه سالم، و کاهش رفتار بیتحرکی بر سلامت متابولیک در طول شیمیدرمانی برای سرطان پستان در مراحل اولیه. برادر J. Nutr. 2022، 1-20، پیش از چاپ. [CrossRef]
سلب مسئولیت/یادداشت ناشر:اظهارات، نظرات، و داده های موجود در همه نشریات صرفاً متعلق به نویسنده(ها) و مشارکت کننده(ها) است و نه MDPI و/یا ویرایشگر(ها). MDPI و/یا ویرایشگر(های) مسئولیت هرگونه آسیب به افراد یا دارایی ناشی از هر ایده، روش، دستورالعمل، یا محصولاتی را که در محتوا ذکر شده است، سلب میکنند.
【برای اطلاعات بیشتر:george.deng@wecistanche.com / WhatApp:8613632399501】






