Lipidomics تغییرات لیپید کلیه ناشی از سیس پلاتین را در طی آسیب حاد کلیه و کاهش آنها توسط سیلاستاتین آشکار می کند.
Feb 21, 2022
خلاصه: سمیت کلیوی یکی از عوارض عمده شیمی درمانی مبتنی بر سیس پلاتین است که منجر به حاد می شودآسیب کلیهدر حدود 30 درصد از بیماران، بدون مداخله پیشگیرانه یا درمان برای استفاده بالینی در دسترس هستند. ثابت شده است که سیلاستاتین در مدلهای in vitro و in vivo اثر محافظتی نفرو برای درمانهای سیس پلاتین دارد، که اخیراً وارد آزمایشهای بالینی شده است. درک عمیق تر در سطح مولکولی ناشی از سیس پلاتینآسیب کلیویو اثر عوامل محافظتی بالقوه می تواند کلیدی برای توسعه درمان های محافظت کننده نفروی موفق و ایجاد نشانگرهای زیستی جدید باشد.آسیب کلیویومحافظت از نفرو. یک رویکرد لیپیدومی هدفمند، با استفاده از LC-MS/MS، برای تعیین کمیت 108 گونه لیپیدی (شامل فسفولیپیدها، اسفنگولیپیدها و کلسترول آزاد و استریف شده) درکلیهعصاره قشر و مدولا از موش های تحت درمان با سیس پلاتین و/یا سیالاستاتین. تا 56 و 63 گونه چربی به ترتیب در قشر و مدولا پس از درمان سیس پلاتین تغییر یافتند. درمان همزمان با سیالاستاتین بسیاری از این تغییرات چربی را به طور کامل یا جزئی با توجه به سطوح کنترل کاهش داد. تجزیه و تحلیل چند متغیره نشان داد که گونه های چربی را می توان برای تمایز استفاده کردآسیب کلیویومحافظت از نفرو، با استرهای کلسترول متمایزترین گونه همراه با سولفاتیدها و فسفولیپیدها هستند. بیومارکرهای تشخیصی بالقوه ناشی از سیس پلاتین آسیب کلیویو سیاستاتینمحافظت از نفرونیز یافت شدند.
کلید واژه ها:لیپیدومیک؛ سیس پلاتین؛ آسیب حاد کلیه؛ سیلاستاتین محافظت از نفرو؛ نشانگرهای زیستی؛ استرهای کلسترول؛ اسفنگولیپیدها؛ فسفولیپیدها؛ شیمی درمانی
مقدمه سمیت کلیوی یک عارضه جانبی جدی شیمی درمانی سیس پلاتین [1] با حاد استآسیب کلیه(AKI) در حدود. 30 درصد از بیماران تحت درمان [2]. این همچنین عامل اصلی محدود کننده دوز و یک اشکال مهم درمان های مبتنی بر سیس پلاتین، یکی از مرتبط ترین درمان ها برای تومورهای جامد است [2]. سیس پلاتین تجمع می یابد و باعث آسیب می شودکلیهسلول های اپیتلیال توبول پروگزیمال (RPTECs) و آسیب به ویژه در بخش S3 لوله پروگزیمال قرار دارد که ازکلیهقشر به سمت اتصال کورتیکومدولاری و مدولای بیرونی [3]. با این حال، آسیب مستقیم به حلقه هنل مدولاری نیز پیشنهاد شده است [4،5]. یک سری رویدادهای سلولی در رابطه باکلیهآسیب سلولی توبولی، به دنبال جذب سیس پلاتین، از جمله استرس اکسیداتیو، استرس نیتروزاتیو، آسیب عروقی، التهاب، آسیب میتوکندری یا مهار Na plus، K + ATPase در غشای سلولی، و استرس شبکه آندوپلاسمی، و به دنبال آن مرگ سلولی توبول پروگزیمال عمدتاً توسط آپوپتوز (هر دو شامل مسیرهای درونی و بیرونی) یا نکروز که منجر به از دست دادنعملکرد کلیه[2،6،7]. این در کاهش نرخ فیفیلتراسیون گلومرولی (GFR) و سطوح سرمی منیزیم و پتاسیم، با افزایش نیتروژن اوره خون (BUN) و کراتینین سرم آشکار می شود [2].

رویکردهای مختلفی برای آن بررسی شده استمحافظت از نفرودر طول درمانهای سیس پلاتین هم در شرایط آزمایشگاهی و هم در داخل بدن، بر اساس تعدادی از اهداف مولکولی [7-9]. با این حال، اختلال احتمالی اثر سیتوتوکسیک سیس پلاتین بر سلولهای تومور و یک اثر محافظتی اغلب ناقص، توسعه محافظهای مجدد را محدود کرده است [9]. در نتیجه، هیچ مداخله ای برای استفاده بالینی وجود ندارد که با موفقیت از AKI ناشی از سیس پلاتین پیشگیری یا درمان کند [7]. درک عمیق تر از مسیرهای مولکولی مربوط به AKI ناشی از سیس پلاتین و اهداف بالقوه برایمحافظت از نفرودر این زمینه حیاتی به نظر می رسد.
ثابت شده است که سیلاستاتین به طور موثر محافظت می کندکلیهاز آسیب ناشی از چندین عامل، از جمله سیس پلاتین [10،11]، جنتامایسین [12]، ونکومایسین [13]، سیکلوسپورین A و تاکرولیموس [14]، در هر دو مدل in vitro و in vivo. سیلاستاتین با مهار انتخابی اثر محافظتی خود را اعمال می کندکلیهدهیدروپپتیداز I (DHP-I) واقع در قایق های لیپیدی در مرز براش RPTECs [11]. در نتیجه، فرآیندهای شامل بیرونیسازی غشاء مانند آپوپتوز بیرونی با واسطه Fas توسط سیاستاتین مختل میشوند و پیشرفت آنآسیب کلیویپس از بازداشت یک توهین سمی [11]. جدای از اختلال آپوپتوز بیرونی توسط سیستاتین، استرس اکسیداتیو، التهاب و تجمع ترکیبات نفروتوکسیک همگی کاهش یافته است [10-13،15،16]. بدین ترتیب،عملکرد کلیهتحت درمان همزمان با سیس پلاتین و سیالاستاتین حفظ می شود [11]. اخیراً، سیالاستاتین آزمایشات بالینی فاز I را برای استفاده از آن به عنوان محافظ نفرو با موفقیت به پایان رسانده است و در شرف ورود به فاز دوم آزمایشات است. یک مطالعه امیدوارکننده اخیر همچنین نشان داد که سیستاتین (که به صورت ایمی پنم به همراه سیستاتین تجویز می شود) ممکن است در بیماران مبتلا به کارسینوماتوز صفاقی در طول درمان هیپرترمیک سیس پلاتین داخل صفاقی به یک اثر محافظت کننده بازدارنده دست یابد [17].
در سالهای اخیر، فناوریهای omics، بهویژه پروتئومیکس [18،19] و متابولومیکس [20-23]، برای کشف نشانگرهای زیستی تشخیص اولیه جدید AKI، به غیر از BUN یا کراتینین در سرم مفید ثابت شدهاند [18،20]. علاوه بر این، تجزیه و تحلیل متابولومیک می تواند اطلاعات ارزشمندی را برای درک مکانیسم های سیس پلاتین در سمیت کلیوی [5،24] و اثر درمانی نفروپروتکتورهای بالقوه [25-27] ارائه دهد.
به طور خاص، لیپیدومیکس نیز می تواند اطلاعات مربوطه را در موردبیماری کلیوی[28]، با توجه به اینکه لیپیدها نقشهای کلیدی ساختاری، سیگنالدهی سلولی و متابولیسم را ایفا میکنند و میتوانند در سلولها، بافتها و سیالات زیستی تحت تغییر قرار گیرند.کلیهشرایط پاتولوژیک [29،30]. در این راستا، افزایش سطح تری گلیسیرید و اسیدهای چرب غیر استریفیه شده در آن مشاهده شدکلیهدر طول درمان با سیس پلاتین [31]، علاوه بر لیپیدهای خنثی تال [32]. سطوح بالای اسفنگولیپیدها - سرامیدها (Cer) و هگزوسیل سرامیدها (HexCer) - نیز درکلیهقشر در طول AKI ناشی از سیس پلاتین [33]. از سوی دیگر، گونه های فسفولیپید، از جمله فسفاتیدیل کولین (PC)، فسفاتیدیل اتانول آمین (PE) و لیزوفسفاتیدیل کولین (LPC) نیز یافت شد که دربافت کلیهیا سلول ها در طول درمان سیس پلاتین [26]. سطوح گونه های مختلف LPC نیز در سرم موش پس از تجویز سیس پلاتین تغییر یافت [23]. علاوه بر این، یک روش نیمه کمی غیر هدفمند تصویربرداری با طیف سنجی جرمی امکان مقایسه توزیع لیپید در موش صحرایی را فراهم کرد.کلیهبخشها و پیشنهاد کردند که سیس پلاتین منجر به تغییرات در فسفولیپیدهای مختلف (PC، PE، فسفاتیدیل گلیسرولها (PG)، فسفاتیدیللینوزیتولها (PI)، فسفاتیدیل سرینها (PS)، اسیدهای فسفاتیدیک (PA))، سولفاتیدها (Sulf)، یا کاردیولیپینها) شد. (نشان دادن رفتارهای متفاوت در قشر و مدولا)، در حالی که درمان مشترک با سیستاتین تمایل به کاهش برخی از این تغییرات داشت [4].
در این کار، ما یک گام فراتر رفتهایم و نگاهی دقیقتر به لیپیدهای ساختاری مهم در آن انداختهایمکلیهمانند فسفولیپیدها (PC، LPC و PE)، اسفنگولیپیدها (Sulf، اسفنگومیلین ها (SM)، دی هیدروسفنگومیلین ها (dhSM)، Cer، دی هیدروسرامیدها (dhCer)، HexCer، دی هیدروهگزوزیل سرامیدها (dhHexCer)) و کلسترول آزاد (FC) و کلسترول آزاد شده (FC) اشکال (استرهای کلسترول (CE))، پوشش طبقات و گونه های جدید لیپید و با استفاده از یک رویکرد کمی هدفمند قابل اعتمادتر مبتنی بر کروماتوگرافی مایع همراه با تجزیه و تحلیل طیف سنجی جرمی پشت سر هم (LC-MS/MS). در مجموع 108 گونه چربی در هر دو مورد اندازه گیری قرار گرفتندکلیهعصارههای قشر و مدولا از موشهای تحت درمان، به منظور درک بهتر اثر نفروتوکسیک سیس پلاتین و اثر محافظتی نفروپروکتین سیلاساتین. اطلاعات جدید در مورد تأثیر سیس پلاتین مرتبط با AKI برکلیهگونه های چربی به دست آمد و بینش های بیشتری در مورد اثر محافظتی سیستاتین به دست آمد، که منجر به کاهش برخی از تغییرات چربی خاص ناشی از سیس پلاتین درکلیهقشر یا مدولا بیومارکرهای بالقوه متنوع ناشی از سیس پلاتینآسیب کلیویومحافظت از نفروبا سیاستاتین نیز یافت شد.
نتایج
اثر محافظتی سیلاستاتین در برابر آسیب کلیوی ناشی از سیس پلاتین
ارزیابیعملکرد کلیهدر موشهای تحت درمان با سیس پلاتین و/یا سیستاتین برای اولین بار با استفاده از چندین شاخص بیوشیمیایی در سرم و ادرار انجام شد. همانطور که در جدول 1 نشان داده شده است، کراتینین سرم، BUN، پروتئین های ادرار، حجم ادرار و دفع کسری سدیم و پتاسیم به دلیل درمان سیس پلاتین در مقایسه با گروه کنترل به طور قابل توجهی افزایش یافت، در حالی که درمان همزمان با سیستاتین و سیس پلاتین منجر به کاهش آنها در مقایسه شد. با سطوح کنترل از سوی دیگر، GFR در موش های تحت درمان با سیس پلاتین نسبت به نمونه های کنترل کاهش یافت، در حالی که تجویز همزمان سیالاستاتین این اثر را کاهش داد. این نتایج تایید می کندآسیب کلیویناشی از سیس پلاتین و محافظت توسط سیستاتین. سیلاستاتین به تنهایی هیچ تاثیری بر روی آن نشان ندادعملکرد کلیهمولفه های.

آنالیز هیستوپاتولوژیک نیز در مقاطع رنگ آمیزی شده با هماتوکسیلین/ائوزین برای بررسی تغییرات مورفولوژیکی مربوط بهآسیب کلیوی. شکل 1 علائم آسیب ناشی از سیس پلاتین را در ناحیه پروگزیمال نشان می دهدکلیهلوله ها، از جمله تورم لوله، جدا شدن بقایای سلولی، یا از دست دادن غشای مرزی برس (شکل 1C,G,I). تجمع گچ های پروتئینی نیز در لوله های قشر و مدولا مشاهده شد (به ترتیب شکل 1C، G). این برخلاف مورفولوژی طبیعی است که در گروههای کنترل یا سیاستاتین در قشر مغز (به ترتیب شکل 1A،B) و مدولا (به ترتیب شکل 1E،F) مشاهده میشود. درمان همزمان سیلاستاتین با سیس پلاتین منجر به کاهش واضح تمام این تغییرات ناشی از سیس پلاتین در قشر و بصل النخاع شد (شکل 1D,H,J).
سیس پلاتین تغییر طبقات کلی لیپیدهای کلیوی در قشر و مدولا. اثر محافظتی سیلاستاتین
سطح کل کلاس های مختلف چربی، از جمله استرول ها (CE، FC)، فسفولیپیدها (LPC، PC، PE) و اسفنگولیپیدها (Cer، dhCer، HexCer، dhHexCer، Sulf، SM، dhSM) درکلیهکورتکس و مدولا، به منظور ارزیابی اثر کلی سیس پلاتین بر روی لیپیدها در طول AKI. نتایج کامل آنالیز لیپید در جدول S1 آمده است. همانطور که در شکل 2A,B مشاهده می شود، روندهای کاملا مشابهی در قشر و مدولا برای همه گروه ها مشاهده شد. CE و Cer به طور قابل توجهی افزایش یافتند، در حالی که SM، dhSM، و PE، هر دو در قشر و مدولا در طول درمان سیس پلاتین، با توجه به گروه های کنترل کاهش یافت. در این میان، Cer و CE از برجسته ترین تغییرات مشاهده شده ناشی از سیس پلاتین رنج می برند. علاوه بر این، dhCer و HexCer به طور قابل توجهی در مدولا افزایش یافت، در حالی که در قشر، dhHexCer افزایش یافت و LPC و سولف در طی درمان با سیس پلاتین کاهش یافت.

شکل 1. آنالیز هیستوپاتولوژیک رنگ آمیزی هماتوکسیلین/ائوزینکلیهبخش محافظت سیس پلاتین در برابر آسیب ناشی از سیس پلاتین را نشان می دهد. تصاویر با بزرگنمایی 20× برای قشر کنترل (A) نشان داده می شوند. (ب) قشر سیالاستاتین؛ (C) قشر سیس پلاتین؛ (د) سیس پلاتین به علاوه قشر سیالاستاتین. (E) کنترل مدولا. (F) سیالاستاتین مدولا. (G) سیس پلاتین مدولا. و (H) سیس پلاتین به اضافه سیالاستاتین مدولا. نوار مقیاس از A تا H نشان دهنده 100 میکرومتر است. تصاویر دقیق ازکلیهلوله هایی با بزرگنمایی 60 × برای (I) سیس پلاتین و (J) سیس پلاتین به اضافه سیلاستاتین نمایش داده می شوند. نوار مقیاس برای I و J نشان دهنده 25 میکرومتر است.کلیویشاخص های آسیب نشان داده شده است: →: تجمع پروتئین درکلیهلوله ها & منطقه: تورم لوله. *: از بین رفتن غشای مرزی برس. #: جدا شدن بقایای سلولی.
مصرف همزمان سیستاتین و سیس پلاتین تمایل به کاهش برخی از این تغییرات لیپیدی ناشی از سیس پلاتین داشت که در نتیجه هیچ تفاوتی با گروه های کنترل در مورد سطوح Cer و dhHexCer در قشر مغز یا dhCer، HexCer، SM، dhSM و PE ایجاد نمی کند. سطوح در مدولا علاوه بر این، در مورد افزایش CE ناشی از سیس پلاتین در قشر مغز، سیس پلاتین تجویز همزمان با سیس پلاتین منجر به کاهش قابل توجهی در سطح سطوح در مقایسه با گروه سیس پلاتین شد، اگرچه بهبود با توجه به گروه های کوآترول جزئی بود. بقیه طبقات چربی تغییر یافته توسط سیس پلاتین در درمان شرکتی درمان نشده باقی ماندند. از سوی دیگر، خود سیالاستاتین هیچ تاثیری بر چربیهای قشر و مدولا نداشت، به جز LPC و dhCer در قشر مغز که به نظر میرسید به ترتیب نسبت به گروه کنترل کاهش یافته و افزایش یافته است. سطوح کل FC، PC، و dhHexCer هیچ تغییر قابل توجهی در قشر و مدولا پس از درمان سیس پلاتین نشان نداد.
شکل 2C،D نقشه های حرارتی همبستگی را برای طبقات چربی در قشر و مدولا به ترتیب نشان می دهد که روندهای مشابهی را ارائه می دهد.

جداسازی گونه های لیپید کلیوی فردی توسط درمان سیس پلاتین. سیلاستاتین تضعیف کننده اگکت
استرهای کلسترولتجزیه و تحلیل پنج گونه منفرد CE (CE 18:1، CE 18:2، CE 18:0، CE 20:4، و CE 22:6) انجام شده درکلیهکورتکس و مدولا نشان داد که سیس پلاتین به طور قابل توجهی هر یک از آنها را در مقایسه با سطوح کنترل افزایش داد (شکل 3). از سوی دیگر، مصرف همزمان سیستاتین و سیس پلاتین منجر به کاهش کلی در سطوح تک تک گونه های CE با توجه به تیمار سیس پلاتین شد که از نظر آماری برای همه گونه های CE در قشر و CE 18:2 در مدولا معنی دار بود. در شکل 3 مشاهده می شود. این بهبود در گونه های کورتکس CE ناشی از هم نشینی سیالاستاتین در مقایسه با سطوح گروه کنترل جزئی بود، در حالی که هیچ بهبود آماری معنی داری در اکثر گونه های مدلا CE (به جز CE 18:2) برای تجویز همزمان سیالاستاتین مشاهده نشد. در مقایسه با سیس پلاتین نتایج تجزیه و تحلیل آماری کامل بر روی گونه های چربی قشر مغز و مدولا به ترتیب در جداول S2 و S3 نشان داده شده است.

اسفنگولیپیدها: Cer، dhCer، HexCer، dhHexCer، SM، dhSM و Sulfدر مجموع 43 گونه اسفنگولیپید در منطقه اندازه گیری شدکلیهقشر و بصل النخاع برای ارزیابی تأثیر تیمار سیس پلاتین و سیالاستاتین بر سطوح آنها، همانطور که در شکل 4 نشان داده شده است. می توان مشاهده کرد، تیمار سیس پلاتین منجر به افزایش قابل توجهی در 19 گونه از شما در چهار کلاس درکلیهقشر و مدولا. مجدداً، درمان همزمان با سیس پلاتین و سیس پلاتین تمایل به کاهش اثر سیس پلاتین را نشان می دهد، با کاهش کلی سطوح لیپیدهای تغییر یافته توسط سیس پلاتین در قشر و مدولا. در واقع، برای گونههای dhCer (شکل 4B) و dhHexCer (شکل 4D)، هیچ تفاوتی بین گروههای تیمار شده با سیس پلاتین بهعلاوه سیسپلاتین و گروههای کنترل برای گونههای تغییر یافته با سیسپلاتین مشاهده نشد که نشاندهنده بهبودی کامل است. در مورد Cer (شکل 4A) و HexCer (شکل 4C)، این بازیابی برای برخی از گونه های تغییر یافته نیز وجود داشت، مانند HexCer 34:1 (قشر و مدولا) و HexCer 38:1 و HexCer 42:1 (مدولا). ) Cer 36:1، Cer 38:1، Cer 40:1، Cer 42:1، و Cer 42:2 در قشر مغز. و Cer 34:1 و Cer 42:2 در مدولا، که به طور کامل یا تا حدی بهبود یافته است. برعکس، تیمار سیس پلاتین به همراه سیالاستاتین همچنان تفاوت معنیداری را با توجه به گروههای کنترل برای Cer 36:1، Cer 38:1، Cer 40:1، Cer 42:1 و HexCer 36:1 در مدولا نشان داد، بدون اینکه بهبودی داشته باشد. اثر بازیابی بسیار بهتری که سیاستاتین در قشر مغز اعمال می کند نسبت به مدولا برای Cer و HexCer.
در مورد گونه های SM (شکل 4E) و dhSMt (شکل 4F)، سیس پلاتین منجر به کاهش قشر و مدولا برای گونه های کوتاه ترین و طولانی ترین زنجیره شد که از نظر آماری برای SM 34:1، dhSM 34 معنی دار بود:{{{ 5}}، SM 42:2، SM 42:1 و dhSM 42:1. در مقابل، اثر مشاهده شده برای تیمار سیس پلاتین بر روی گونههای زنجیره میانی SM و dhSM در قشر و بصل النخاع افزایش داشت که از نظر آماری برای dhSM 36 معنیدار بود:0 (هم در قشر و هم در مدولا) و dhSM 4{{{{ 15}}:0، SM 36:1، SM 38:1، و SM 40}:1 در مدولا. تجویز همزمان سیس پلاتین و سیالاستاتین در بسیاری از موارد سطوح گونه های SM و dhSM را عادی می کند، با SM 34:1، SM 36:1، SM 38:1، SM 40:1، SM 42:2، SM 42:1، dhSM 36:0، dhSM 40:0 و dhSM 42:1 تفاوتی با گروه های کنترل در مدولا نشان نمی دهد. در نهایت، برخی از گونه های سولف نیز با تیمار سیس پلاتین در منطقه تغییر یافتندکلیهقشر و مدولا، همانطور که در شکل 4G نشان داده شده است. در حالی که سولف 4{14}}:1 به طور قابل توجهی در قشر و مدولا پس از درمان سیس پلاتین افزایش یافته است، گونه های دیگر مانند Sulf-OH 40:1 یا زنجیره بلند Sulf-OH 42:2، Sulf-OH. 42:2 در قشر مغز کاهش یافت، با Sulf 42:0 و Sulf-OH 42:1 نیز در هر دو قشر و مدولا کاهش یافت. سیلاستاتین تجویز همزمان با سیس پلاتین مجدداً منجر به یک اثر بهبودی خفیف شد، به ویژه برای سولف 40:1 (قشر و مدولا) و سولف 40:2 و سولف-OH 42:1 (بصل النخاع)، که تفاوتی در مقایسه با گروه کنترل نشان نداد.

فسفولیپیدها: PC، PE و LPCکمی سازی 60 گونه فسفولیپید (28 PC، 20 PE، و 12 LPC) درکلیهقشر و مدولا برای ارزیابی تغییرات بالقوه ناشی از سیس پلاتین و اثر محافظتی مجدد سیالاستاتین نتایج برای گونه های PC به ترتیب در شکل 5A,B نشان داده شده است. همانطور که مشاهده می شود، سیس پلاتین به طور قابل توجهی تا 19 گونه PC را در قشر یا مدولا تغییر داد. اکثر این گونه های PC توسط سیس پلاتین کاهش یافتند، به استثنای PC 40:2، PC 40:4 و PC 34:2 که در قشر مغز افزایش یافتند. همانطور که در شکل 5C،D مشاهده می شود، کسر گونه های PC بسیار اشباع نشده در هر دو قسمت بصل النخاع و قشر به طور قابل توجهی کاهش یافت، در حالی که کسر گونه های حاوی دو پیوند دوگانه به طور قابل توجهی افزایش یافت. درمان با هر دو سیس پلاتین و کیلاست آتین اثرات مشابهی با آنچه قبلا مشاهده شده بود نشان داد، با برخی از اثرات تضعیف کننده مشاهده شد، در برخی موارد منجر به بازیابی کامل سطوح PC، بدون تفاوت قابل توجه با گروه کنترل، یا به بهبود نسبی شد. این بازیابی عمدتاً در نتایج مربوط به تعیین گونه های پلی اتیلن در قشر و بصل النخاع به ترتیب در شکل 6A،B نشان داده شده است. در مجموع 16 گونه پلی اتیلن به طور قابل توجهی توسط سیس پلاتین در قشر یا مدولا تغییر یافتند که بیشترین تعداد گونه های تغییر یافته در مدولا یافت شد. در بیشتر موارد، گونه های پلی اتیلن با تیمار سیس پلاتین کاهش یافت، به جز PE 38:2، PE 40:6 و PE 40:4 که در قشر، مدولا یا هر دو قشر و بصل الخلقه افزایش یافتند. به ترتیب. بر این اساس، با توجه به طول کل زنجیره های اسید چرب در گونه های پلی اتیلن در بصل النخاع، مقدار کل پلی اتیلن با 34، 36 و 38 درجه سانتی گراد با سیس پلاتین به طور قابل توجهی کاهش یافت، در حالی که گونه های 40 درجه سانتی گراد، همانطور که در شکل 6C نشان داده شده است، افزایش یافت. . درمان توام با سیس پلاتین با سیس پلاتین باعث کاهش بیشتر تغییرات ناشی از سیس پلاتین در گونه های پلی اتیلن منفرد یافت شده در بصل النخاع شد، و سطوح بدون تفاوت معنی داری را در مقایسه با گروه های کنترل در 11 گونه از 15 گونه تغییر یافته با سیس پلاتین در مدولا، با 2 گونه PE بیشتر ارائه داد. تا حدی بهبود یافت. با این حال، در قشر، تنها 2 گونه از 11 گونه تغییر یافته با سیس پلاتین با سیستاتین برای کنترل سطوح، با 2 گونه PE اضافی که تا حدی بهبود یافتند، بازیابی شدند. مشابه مشاهدات برای گونه های PC، کسر گونه های پلی اتیلن غیر اشباع به طور قابل توجهی در بصل النخاع کاهش یافت، در حالی که کسر گونه های حاوی پیوندهای دوگانه 1-3 به طور قابل توجهی افزایش یافت، همانطور که در شکل 6D نشان داده شده است.


با توجه به تجزیه و تحلیل گونه های LPC، بسیاری از تغییرات ناشی از سیس پلاتین مشاهده شده درکلیهکورتکس، که در آن LPC 16:1، LPC 16:0، LPC 18:1، LPC 18:0، LPC 20:3، LPC 22:6 و LPC 22:5 به طور قابل توجهی کاهش یافتند. با توجه به نمونه های کنترل، همانطور که در شکل 7 الف مشاهده می شود. از سوی دیگر، LPC 17:1 و LPC 18:2 در طول درمان سیس پلاتین در بصل النخاع افزایش یافته است (شکل 7B). درمان همزمان با سیس پلاتین و سیالاستاتین هیچ اثر بازیابی بر روی گونه های LPC قشر نداشت. برعکس LPC 17:1 و LPC 18:2 در بصل النخاع بازیابی شد، بدون تفاوت معنی داری در مقایسه با نمونه های شاهد.

لیپیدهای کلیه به عنوان متغیرهای طبقه بندی برایآسیب کلیهو حفاظت
تجزیه و تحلیل چند متغیره با استفاده از همه متغیرهای چربی اندازهگیری شده در قشر و بصل النخاع انجام شد تا ارزیابی شود که آیا این گونهها میتوانند برای طبقهبندی گروهی و تشخیص ناشی از سیس پلاتین استفاده کنند یا خیر.آسیب کلیویومحافظت از نفروتوسط سیلاستاتین تجزیه و تحلیل اجزای اصلی (PCA) و پیش بینی های متعامد به تجزیه و تحلیل تمایز ساختارهای نهفته (OPLS-DA) با استفاده از لیپیدهای قشر یا مدولا به طور جداگانه انجام شد، همانطور که در شکل 8 نشان داده شده است. تجزیه و تحلیل PCA قشر (شکل 8A) و مدولا (شکل 8B) لیپیدها به مدلها توانایی نشان دادن جدایی واضح از گروه سیس پلاتین را با توجه به گروههای کنترل و سیالاستاتین ارائه میدهند که دو گروه آخر از نزدیک خوشهبندی میشوند. از سوی دیگر، گروه تحت درمان با سیس پلاتین به همراه سیس پلاتین تمایل به جدا شدن از گروه سیس پلاتین و قرار گرفتن در بین گروه کنترل و سیس پلاتین داشتند که نشان دهنده تفاوت بین گروه ها است. همه مدلهای PCA، R2 را بالاتر از 0.7 و Q2 را بالاتر از 0.5 نشان دادند.

تجزیه و تحلیل OPLS-DA چند گروهی همچنین خوشه بندی جدا شده از گروه های مختلف را با استفاده از متغیرهای چربی قشر (شکل 8C) یا مدولا (شکل 8D) نشان داد. مدلهای OPLS-DA مقادیر Q2 قابل قبول و مقادیر R2 بالاتر از 0.7 ارائه کردند و در طول آزمایش جایگشت برای 100 تکرار معتبر هستند، همانطور که در شکل 8E,F نشان داده شده است. ویژگی هایی با اهمیت متغیر در نمرات طرح ریزی (VIP) بالاتر از 1 را می توان در شکل 8G,H یافت که به ترتیب نشان دهنده چربی های قشر یا مدولا است که تأثیر بیشتری بر جداسازی گروه ها دارند. این شامل گونه های چربی متنوع از کلاس های CE، اسفنگولیپید و فسفولیپید بود. برای تعیین تفاوت های لیپیدی خاص بین گروه های فردی مربوط به درمان سیس پلاتین ومحافظت از نفروآنالیز بیشتر OPLS-DA به طور جداگانه با لیپیدهای قشر و مدولا انجام شد، همانطور که به ترتیب در شکل های 9 و 10 مشاهده می شود. مدلهای OPLS-DA برای سیس پلاتین در مقایسه با گروه کنترل، سیس پلاتین به علاوه سیس پلاتین در مقایسه با سیس پلاتین، و همچنین سیس پلاتین به علاوه سیلاساتین در مقایسه با گروه کنترل ساخته شد. متمایزترین مدل های OPLS-DA بین گروه های کنترل و گروه های تحت درمان با سیس پلاتین یا سیس پلاتین به علاوه سیس پلاتین، با در نظر گرفتن بالاترین مقادیر R2 و Q2 آنها، با اعتبارسنجی مناسب بر اساس نتایج آزمایش جایگشت با 100 چرخه بود (شکل 9A,B,D, E و شکل 10A,B,D,E).

از سوی دیگر، مدلهای OPLS-DA برای گروههای سیسپلاتین بهعلاوه سیسپلاتین و سیسپلاتین، هر دو با استفاده از لیپیدهای قشر (شکل 9C) یا مدولا (شکل 1{12}}C)، همچنین تمایز گروهی را با مقادیر مناسب R2 و Q2 مجاز میدانند. و نتایج اعتبارسنجی مناسب از 100-تستهای جایگشت چرخه (شکلهای 9F و 10F)، با لیپیدهای مدولا آنهایی هستند که قابلیت پیشبینی بهتری دارند. نمودارهای S برای مدلهای مختلف OPLS-DA در شکل 9G,H,I و شکل 10G,H,I برای ویژگیهای چربی قشر یا مدولا گنجانده شده است. گونه هایی با |p(corr)| بالاتر از 0.5 و نمرات VIP بالاتر از 1 در نمودارهای S به عنوان مرتبط ترین ویژگی برای تبعیض گروه ها مشخص شده اند. داده های کامل شامل مقادیر p(corr) و VIP از مدل های OPLS-DA به همراه آمار تک متغیره برای هر گونه لیپید را می توان در جداول تکمیلی S2 (لیپیدهای قشر بدن) و S3 (لیپیدهای مدولا) یافت. به نظر واضح است کهکلیهلیپیدهای قشر و مدولا می توانند به عنوان معیارهای متمایز کننده برای القا شده توسط سیس پلاتین عمل کنندآسیب کلیویو برای سیستاتینمحافظت از نفرودر طول درمان سیس پلاتین

لیپیدهای کلیوی به عنوان نشانگرهای زیستی بالقوه آسیب کلیوی ناشی از سیس پلاتین به منظور انتخاب بیومارکرهای چربی بالقوه آسیب کلیوی
ناشی از سیس پلاتین، یک ترکیب معیار چندگانه از مقادیر p آماری معنیدار از تجزیه و تحلیل تک متغیره سیسپلاتین در مقابل گروههای کنترل، و همچنین مقادیر p(corr) و VIP موجود در مدل OPLS-DA مرتبط، استفاده شد. لیپیدهای انتخاب شده با مقادیر p < 0.05;="" fdr="">< 0.1;="" |p(corr)|=""> 0.5 و VIP > 1 را می توان در جدول 2 (لیپیدهای قشر بدن) و جدول 3 (لیپیدهای مدولا) یافت که در آن تغییر چین (FC) و نواحی زیر منحنی (AUC) برای منحنی های مشخصه عملکرد گیرنده (ROC) نیز گنجانده شده است.
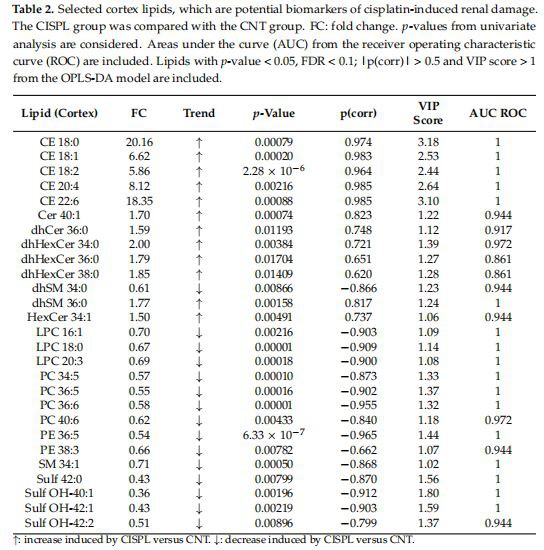
همانطور که مشاهده می شود، حداکثر 4{4}} لیپید از بصل النخاع و 27 لیپید از قشر مغز، شامل گونه های CE، اسفنگولیپیدها و فسفولیپیدها، به ترتیب در جداول 2 و 3 انتخاب شده اند. مقادیر AUC برای منحنیهای ROC بهدستآمده برای هر لیپید بالاتر از 0.85 بود و در بیشتر موارد نزدیک به 1 بود که نشاندهنده قابلیتهای خوب تمایز گونهها بین سیسپلاتین و گروههای کنترل است. بهطور قابلتوجهی، گونههای CE افزایشیافته با سیس پلاتین (CE 18:1، CE 18:2، CE 18:0، CE 20:4، و CE 22:6) متمایزترین به نظر میرسند. ویژگی های هر دو در بصل النخاع و قشر، نشان دادن بالاترین مقادیر FC، VIP، p(corr)، و AUC. dhHexCer 34:0 یکی دیگر از چربی های افزایش یافته در قشر مغز با FC بالا و نمرات مرتبط است. از سوی دیگر، سولفاتیدهایی مانند Sulf 42:0، Sulf-OH 40:1، یا Sulf-OH 42:1 نیز در قشر مغز کاملاً مرتبط هستند، در حالی که PE 36:5، PE 38:6، PE 38:5. PC 36:5 یا PC 36:6 نیز در بصل النخاع بسیار مهم هستند، همه آنها در طول درمان سیس پلاتین کاهش می یابد.

لیپیدهای کلیوی به عنوان نشانگرهای زیستی بالقوه محافظت از نفرو سیلاستاتین
برای انتخاب بیومارکرهای لیپیدی بالقوه حفاظت سیس پلاتین در برابر سمیت نفرو سیس پلاتین، همان رویکرد معیارهای چندگانه مشابه در بخش 2.5، با استفاده از تجزیه و تحلیل تک متغیره سیس پلاتین به علاوه سیالاستاتین در مقابل گروه های سیس پلاتین، و مقادیر p(corr) و VIP موجود در OPLS- مربوطه استفاده شد. مدل DA لیپیدهای انتخاب شده با مقادیر p < 0.05;="" fdr="">< 0.1;="" |p(corr)|=""> 0.5 و VIP > 1 را می توان در جدول 4 (لیپیدهای قشر بدن) و جدول 5 (لیپیدهای مدولا) یافت، که در آن FC و AUC برای منحنی های ROC نیز محاسبه شده است.

همانطور که در جدول 4 مشاهده می شود، تمام گونه های CE (CE 18:1، CE 18:2، CE 18:0، CE 20:4، و CE 22:6) در کورتکس را می توان به عنوان قوی ترین شاخص محافظت اعمال شده توسط سیلاستاتین در نظر گرفت که در عین حال تغییرات ناشی از سیس پلاتین را به طور قابل توجهی کاهش می دهد. PE 36:5 و dhHexCer 34:0 در قشر نیز نشانگرهای زیستی بالقوه مهمی برای محافظت از سیستاتین هستند، به ویژه دومی، که به دلیل استفاده از سیلاستاتین به سمت سطوح کنترل، بهبود کامل مییابد. در مورد لیپیدهای بصل النخاع، همانطور که در جدول 5 نشان داده شده است، مقدار بیشتری از نشانگرهای زیستی بالقوه محافظت سیالاستاتین نسبت به قشر پیدا شد. قابل توجه است که به نظر می رسد سولف 4{37}}:2 با در نظر گرفتن بالاترین امتیازات FC و VIP، متمایزترین گونه در مدولا باشد. گونههای مختلف PC و PE نیز یافت شد، از جمله PE 36:5، PE 38:5، PE 38:6، PE 36:4، PE 34:3، و PC 36:6، به غیر از Cer. 42:2، dhHexCer 36:0، و HexCer 34:1، به عنوان نشانگرهای زیستی مهم حفاظت سیالاستاتین در مدولا. در تمام موارد، این لیپیدها با بازیابی جزئی یا کلی ناشی از سیستاتین در سطوح کنترل در مقایسه با سطوح تغییر یافته آنها توسط سیس پلاتین همراه بودند. برای همه گونهها، مقادیر AUC برای منحنیهای ROC بهدستآمده بالاتر از 0.85 بود که قابلیت تشخیص خوب آنها را ثابت میکند.
بحثدر این کار، ما در مجموع 108 گونه چربی شامل لیپیدهای ساختاری مهم مانند فسفولیپیدها، اسفنگولیپیدها و کلسترول را به همراه اشکال استری شده آن درکلیهقشر و مدولا از موش های تحت درمان با سیس پلاتین و/یا سیالاستاتین. این به منظور درک بهتر اثر نفروتوکسیک سیس پلاتین و اثر محافظتی سیستاتین انجام شد. بیش از 63 گونه چربی به طور قابل توجهی در مدولا توسط تیمار سیس پلاتین تغییر یافتند، در حالی که 56 گونه چربی در قشر مغز تحت تأثیر قرار گرفتند، که بازتاب آن است.آسیب کلیویدر هر دو منطقه اگرچه، به طور سنتی، اکثر مطالعات AKI ناشی از سیس پلاتین بر روی سلول های توبول پروگزیمال وکلیهآسیب قشر مغز، جایی که تجمع دارو عمدتاً متمرکز است، مطالعات اخیر به این واقعیت اشاره دارد که آسیب در بصل النخاع حتی ممکن است به همان شدتی باشد که در قشر، بر اساس سنجش آپوپتوز TUNEL [5]. این ممکن است مربوط به تجمع سیس پلاتین در بخش S3 لوله های پروگزیمال [3،5] باشد که به سمت بصل النخاع خارجی نزول می کند، جدای از آسیب احتمالی مستقیم و ثانویه حلقه هنله [4]. علاوه بر این، بصل النخاع به عنوان حساس ترین مورد اشاره شدکلیهمنطقه ای برای مشاهده تغییرات متابولیت جهانی مرتبط با سیس پلاتین در مقایسه با قشر [5]. نتایج قبلی ما همچنین به آسیب مستقیم سلول های مدولا (به غیر از آسیب ثانویه) توسط سیس پلاتین اشاره کرد که در تغییرات مختلف فسفولیپید و کاردیولیپین منعکس شده است [4]. این نتایج جدید مشاهدات را با گونهها و کلاسهای چربی اضافی که توسط سیس پلاتین تغییر مییابند گسترش میدهند و ارتباط آسیب مدولا را در AKI ناشی از سیس پلاتین تقویت میکنند.
اگرچه FC درکلیهبه طور قابل توجهی با درمان سیس پلاتین تغییر نکرد، هم کل CE و هم تمام گونه های CE اندازه گیری شده به طور قابل ملاحظه ای در هر دو قشر (8 برابر افزایش برای کل CE) و مدولا (افزایش چهار برابر برای CE کل) در ارتباط با سیس پلاتین القا شده افزایش یافتند.آسیب کلیویکلسترول جزء کلیدی غشای پلاسما است که در بین فسفولیپیدها قرار می گیرد و بر سیالیت، بار سطحی و برهمکنش گروه های سر قطبی تأثیر می گذارد [35،36]. حضور آن در قایقهای لیپیدی نیز اساسی است و برهمکنشهای آبگریز با SM برقرار میکند و برای جداسازی مولکولها و کنترل برهمکنش آنها با سایر اجزای غشا ضروری است [37]. سلول ها تعادل کلسترول را بین سنتز نو در شبکه آندوپلاسمی (ER) و جذب با واسطه LDL حفظ می کنند. بیشتر کلسترول در غشای پلاسمایی قرار دارد، اما همچنین می تواند به ER بازگردد، جایی که FC می تواند (از طریق استریفیکاسیون با واسطه ACAT) به CE تبدیل شود، که به عنوان یک شکل ذخیره سیتوزولی کلسترول در نظر گرفته می شود [36]. CE همچنین می تواند به FC هیدرولیز شود و چرخه استر کلسترول را تشکیل دهد [36]. این واقعیت که FC در طول درمان با سیس پلاتین تغییر نکرده است، اما CE در هر دو قشر و مدولا افزایش یافته است، نشان دهنده تغییر است.کلیهمتابولیسم کلسترول مرتبط با AKI ناشی از سیس پلاتین مطالعات قبلی مشاهدات کاملاً مشابهی را در سلولهای لوله پروگزیمال انسان HK و در قشر کلیوی موشها در طول ایسکمی حاد نشان داد.آسیب کلیه، با FC بدون تغییر و افزایش سطح CE [36]. در آن مورد، آسیب غشای پلاسمایی، که باعث افزایش قاچاق FC از غشاء به ER میشود، قابل قبولترین توضیح به نظر میرسد که منجر به افزایش نسل CE میشود. در این رابطه، آسیب به قایقهای لیپیدی غنی از کلسترول به جای غشای پلاسمایی در افزایش قاچاق کلسترول به ER مؤثرتر به نظر میرسد [36]. نقش محافظت کننده سلولی CE نیز در چنین مطالعات قبلی ذکر شده است. افزایش سطح CE نیز در موش گزارش شدکلیهکورتکس در مرحله اولیه نفروپاتی دیابتی [29]. نتایج همچنین با افزایش جهانی لیپیدهای خنثی در همخوانی داردکلیهتوبول های پروگزیمال گزارش شده در طول درمان سیس پلاتین [32]. نتایج ما برای اولین بار به افزایش جهانی در کل CE علاوه بر گونه های CE منفرد، هر دو درکلیهقشر و مدولا، در طول AKI ناشی از سیس پلاتین. از سوی دیگر، به نظر میرسید که خود سیلاستاتین CE 18:0 و CE 22:6 را فقط در قشر مغز کمی افزایش میدهد، اگرچه سطح کل FC یا CE بدون تغییر بود. این اثر خفیف می تواند به دلیل این واقعیت باشد که هدف آن، DHP-I، در قایق های لیپیدی در لوله پروگزیمال (عمدتا در قشر) قرار دارد و ممکن است برخی اختلالات کوچک در غشاء در طول تعامل آن به وجود آید. از طرف دیگر، مصرف همزمان سیس پلاتین و سیس پلاتین منجر به کاهش تمام گونه های CE افزایش یافته توسط سیس پلاتین در قشر مغز شد، در حالی که در بصل النخاع، تقریباً هیچ اثر بهبودی مشاهده نشد و تنها بهبود نسبی CE18:2 بود. . این به عملکرد خاص سیستاتین در سلول های توبول پروگزیمال اشاره می کند، که محافظت قابل توجهی از گسترش مرگ سلولی مربوط به آسیب مستقیم سیس پلاتین بر غشای پلاسمایی و رافت های لیپیدی در قشر مغز دارد، در حالی که به نظر می رسد آسیب سلولی مربوط به عدم تعادل کلسترول در کل مدولا باشد. تا حد زیادی بدون محافظت باقی بماند.
اسفنگولیپیدها لیپیدهای فعالی هستند که عمدتاً در غشای سلولی یافت می شوند و از نظر قایق لیپیدی کاملاً غنی هستند [37]. سرامیدها متابولیتهای مرکزی متابولیسم اسفنگولیپید هستند که شامل مولکولها و آنزیمهای مختلف با نقشهای مهم در فرآیندهای سلولی، در جلوگیری از رشد سلولی، آپوپتوز، تمایز، مقاومت دارویی و پیری میشوند [38،39]. علاوه بر این، اسفنگولیپیدها در مسیرهای مربوط به مرگ سلولی سرطان سیس پلاتین و AKI شرکت می کنند [33]. سرامیدها می توانند از طریق چندین مسیر تولید شوند، از جمله سنتز de novo، هیدرولیز اسفنگومیلین، یا بازیافت اسفنگولیپیدهای پیچیده [38]. سنتز de novo مسیر اصلی است، و در ER، از پالمیتویل-CoA و سرین، از طریق یک سری مسیرهای آنزیمی برای تولید اسفنگانین، که از طریق دی هیدروسرامید سنتاز (CerS) به دی هیدروسرامیدها منتهی می شود، انجام می شود. در نهایت، اشباع نشدن dhCer سر را تولید می کند [40]. SM همچنین می تواند توسط اسفنگومیلینازها هیدرولیز شده و Cer را تولید کند. Cer میتواند به اسفنگولیپیدهای پیچیدهتری در دستگاه گلژی تبدیل شود: فسفریله شده برای تولید Cer-1-، یک مولکول سیگنالدهنده. با عمل SM سنتاز به SM تبدیل می شود. یا گلیکوزیله برای تولید هزوکسیل سرامیدها (گلوکوزیل یا گالاکتوزیل سرامیدها)، پیش سازهای سولفاتیدها [38]. Cer همچنین می تواند به اسفنگوزین، پیش ساز اسفنگوزین{11}فسفات (S1P)، با نقش مهمی در بقای سلولی و تکثیر، التهاب، و مقاومت دارویی [39] تجزیه شود. در نهایت، تخریب S1P به اتانول آمین و هگزادسنال مسیر خروجی این مسیر است [38].

در طول کمیسازی گونههای اسفنگولیپید، افزایش جهانی در سطوح کل Cer، dhCer، HexCer، و dhHexCer در طول درمان سیسپلاتین مشاهده شد که مخصوصاً برای Cer مرتبط بود. تفاوت در مورد کنترلکلیهزمانی که زیرگونههای منفرد کمی مشخص شدند، 19 گونه از 22 گونه در قشر مغز (11 گونه) و/یا مدولا (18 گونه) با تیمار سیس پلاتین افزایش یافتند، آشکارتر بودند. این مطابق با مشاهدات قبلی است که به افزایش Cer و HexCer در ماوس اشاره می کندکلیهقشر مرتبط با درمان سیس پلاتین [33]، اما در اینجا، ما دریافتیم که مدولا نیز تحت تأثیر این اثر قرار می گیرد.
این مشاهدات می تواند منعکس کننده افزایش تولید متابولیک Cer/dhCer و HexCer/dhHexCer باشد. از یک سو، این امر می تواند از طریق افزایش فعالیت CerS، با توجه به مشاهدات قبلی در این زمینه، انجام شودکلیهقشر مغز، که در آن فعالیت زنجیره بلند CerS در طول درمان سیس پلاتین اندازه گیری شد و مهار CerS منجر به کاهش تجمع مشاهده شده Cer/HexCer شد [33]. علاوه بر این، کاهش ناشی از سیس پلاتین در سطوح SM/dhSM که در قشر و بصل النخاع یافت می شود، نشان دهنده افزایش تولید Cer/dhCer توسط هیدرولیز SM/dhSM از طریق مسیر اسفنگومیلیناز (SMase) است [38]، با تأثیر ویژه بر روی زنجیره بلند Cer/dhCer که همه در مدل های AKI مضر هستند [40]. این همچنین با این واقعیت مطابقت دارد که گونههای با زنجیره بلند Cer در طول AKI [40] و با مشاهدات قبلی افزایش فعالیت SMase درکلیهقشر در طول درمان سیس پلاتین [33]. Cer در آپوپتوز ناشی از سیس پلاتین از طریق سیگنال دهی در مسیرهای درونی و بیرونی نقش دارد [39]. در مسیر ذاتی میتوکندری، سیس پلاتین باعث نفوذپذیری غشای خارجی میتوکندری می شود. افزایش Cer، همراه با متابولیتهای پاییندست آن، میتواند به این نفوذپذیری کمک کند، و تشکیل کانالها توسط Cer، آپوپتوز را در غشای میتوکندری تسهیل میکند، و اجازه میدهد Bax به غشای خارجی میتوکندری وارد شود و همچنین جریان خروجی سیتوکروم C [39]. علاوه بر این، آپوپتوز بیرونی با واسطه Fas از گیرنده Fas واقع در قایقهای لیپیدی استفاده میکند که خوشهبندی آن توسط فعالسازی SMase ناشی از سیس پلاتین و افزایش سر انجام میشود [39]. بنابراین، Cer آپوپتوز را در AKI ناشی از سیس پلاتین تعیین می کند، در حالی که به نظر می رسد سطح بندی آنها از طریق تبدیل آنها به HexCer محافظت کننده باشد [33] و با مقاومت به سیس پلاتین [39] همراه است. سر تولید شده در مقادیر زیاد نیز می تواند بر خواص فیزیکی غشاها تأثیر بگذارد و می تواند کلسترول را جابجا کرده و استریفیکاسیون آن را تحریک کند [35]. از سوی دیگر، SM عمدتاً در غشاهای پلاسمایی وجود دارد و ارتباط مستقیمی با مولکول های کلسترول دارد، به ویژه در قایق های لیپیدی [41]. فقدان بازسازی SM می تواند برای عملکرد مناسب غشاء منفی باشد [41].
سولف به وفور درکلیه،به ویژه در غشای آپیکال توبول های دیستال [42]. اگرچه آنها برای عادی ضروری نیستندعملکرد کلیهمشخص شده است که کمبود سولف با افزایش تولید گلیکولیپیدهای سولفاته و کول ترول جبران می شود [42]. سولفاتید یک لیگاند کلیدی ال سلکتین استکلیه،با نقش حیاتی در نفوذ مونوسیت به داخلکلیهبینابینی [42]. از سوی دیگر، میلین و پروتئین لنفوسیتی مرتبط با لیپید رافت (MAL) با سولفاتیدها و گلیکوسفنگولیپیدها درکلیهغشاها، به تثبیت و مرتبسازی میکرو دامنههای غنیشده با گلیکوسفنگولیپید کمک میکنند [42]. نتایج ما در مورد تغییرات سولف در قشر و مدولا مطالعات قبلی را تأیید می کند که در آن گونه های مختلف سولفاتید نیز توسط سیس پلاتین در کلیه تغییر می کند [34].
تمام گونههای Cer، dhCer، HexCer و dhHexCer که در قشر مغز توسط سیسپلاتین تغییر یافته بودند، به طور جزئی یا کامل با تجویز همزمان سیستاتین بازیابی شدند، در حالی که در مدولا، مقدار زیادی از گونههای Cer بازیابی نشدند، با بازیابی تقریباً کامل dhCer. ، HexCer و dhHexCer. با توجه به دخالت گونه های Cer در آپوپتوز بیرونی واسطه Fas و انسداد آن با اتصال سیستاتین به DHP-I در قایق های لیپیدی در لوله پروگزیمال، این می تواند اثر محافظتی و بازیابی Cer را که عمدتاً در سلول های قشر رخ می دهد توضیح دهد. در مورد SM، dhSM و سولف، به نظر می رسد که بازیابی سیاستاتین در بصل النخاع مرتبط تر از قشر مغز باشد، و این نشان می دهد که آسیب ثانویه توسط عمل سیاستاتین در لوله های پروگزیمال که به بصل النخاع خارجی می رسند، مختل می شود.آسیب کلیویمتمرکز شده است [4].
فسفولیپیدها فراوان ترین گونه ها در غشای سلولی هستند، جایی که PC و تا حدی PE غالب است، با حضور بیشتر PC در سمت مجرا و PE در برگچه سیتوزولی فراوانتر است [35،43]. از سوی دیگر، لیزوفسفولیپیدها گونه های سیگنال دهی هستند که می توانند از هیدرولیز گلیسروفسفولیپیدها از جمله LPC تولید شوند [35]. اکثر 60 گونه PC، PE، و LPC تعیین شده توسط تیمار سیس پلاتین، چه در قشر یا مدولا، با PC و LPC تغییرات بیشتری در قشر مغز ایجاد کردند، در حالی که تغییرات مرتبط با PE متعددتر بود. و در مدولا برجسته است. تغییرات ازکلیهگونه های PC، PE، یا LPC در نتیجه تیمار سیس پلاتین مطابق با مشاهدات گزارش شده قبلی درکلیهدر طول AKI [4،5،26،34،44]. نتایج ما نشان می دهد که بیشتر گونه های PE، PC و LPC تغییر یافته توسط سیس پلاتین در هر دو قشر و مدولا کاهش یافت. با توجه به اثر محافظ نفروپروتکتی سیالاستاتین، به طور قابل توجهی، درجه بالاتری از اثر بازیابی جزئی یا کلی در مدولا برای لیپیدهای تغییر یافته توسط سیس پلاتین نسبت به قشر مغز مشاهده شد. واقعیت جالب دیگر این است که تمام گونههای PC، PE و LPC افزایشیافته با سیس پلاتین در قشر و بصل النخاع توسط سیستاتین بازیابی شدند، در حالی که بیشتر گونههای کاهشیافته سیسپلاتین در قشر مغز همچنان در طول درمان مشترک با سیستاتین تغییر میکردند. این ممکن است نشان دهنده درجه بالاتری از آسیب مستقیم ناشی از تجمع سیس پلاتین در قشر مغز باشد، بدون محافظت توسط سیستاتین باقی بماند و منجر به مرگ سلولی و PC، PE (اجزای اصلی غشای سلولی) و انتشار LPC در اجسام آپوپتوز شود. بنابراین، کاهش سطح آنها. در مقابل، آسیب ثانویه مرتبط با آپوپتوز بیرونی و متعاقب آن تجمع پروتئین در لوله های پروگزیمال می تواند توسط سیاستاتین محافظت شود. این نشان می دهد که گونه های PC، PE، و LPC در بصل النخاع کاهش یافته و بیشتر به آسیب سلولی ثانویه ناشی از سیس پلاتین مربوط می شود. از سوی دیگر، افزایش گونههای PC، PE و LPC ممکن است با بازسازی غشای سلولی یا فرآیندهای سیگنالدهی مرتبط باشد، که با توجه به این نتایج، ممکن است بیشتر مربوط به آسیب ناشی از سیسپلاتین آپوپتوز بیرونی ثانویه باشد که توسط سیستاتین محافظت میشود.
علاوه بر این، کاهش ناشی از سیسپلاتین در درصد گونههای PC و PE با زنجیرههای چرب بسیار غیراشباع نیز مشاهده شد که میتواند با فرآیندهای پراکسیداسیون لیپیدی مرتبط باشد و با سیستاتین کاهش مییابد [4،10،11].
در سطح جهانی، در گونههای لیپیدی که در اینجا کمیسازی شده است، اثر بازیابی سیستاتین در 26 مورد از 56 لیپید تغییر یافته با سیسپلاتین در قشر مغز و در 50 مورد از 63 لیپید تغییر یافته با سیسپلاتین در مدولا مشاهده شد. شاید، این منعکس کننده درجه بالایی از تغییرات چربی مرتبط با آسیب مستقیم میتوکندری محافظت نشده اعمال شده توسط سیس پلاتین به طور عمده در قشر مغز در مقایسه با مدولا باشد، با تغییرات چربی بیشتر مرتبط با محافظت از آسیب ثانویه که در کل مدولا شناسایی شده است. علاوه بر این، تجزیه و تحلیل چند متغیره امکان شناسایی بیومارکرهای جدید لیپیدی را برای AKI و سیس پلاتین ناشی از سیس پلاتین فراهم کرد.محافظت از نفرواز جمله گونه های CE، Sulf، PE، PC، Cer، یا HexCer، همانطور که در بخش های 2.5 و 2.6 توضیح داده شده است. از یافتههای ما، CE 18:2 و PE 36:5 نشانگرهای زیستی کاندید احتمالی هستند که میتوانند همزمان آسیب سیس پلاتین و سیلاستاتین را تشخیص دهند.محافظت از نفرودر هر دو قشر و مدولا. با این حال، از آنجایی که بازیابی این دو گونه با سیالاستاتین جزئی است، گونه های مناسب تر به عنوان نشانگرهای زیستی dhHexCer 34:{1}} در قشر مغز و سولف 42:0 در بصل النخاع هستند که قادر به تشخیص هر دو هستند.آسیب کلیویو محافظت، با سیستاتین که به طور کامل سطوح تغییر یافته توسط سیس پلاتین خود را نسبت به گروه کنترل بازیابی می کند. این را می توان به هر آسیب کلیوی با واسطه لیگاند Fas/Fas تعمیم داد، اما باید در مطالعات آینده تأیید شود. چندین بیومارکر جدید برای AKI در سالهای اخیر پیشنهاد شدهاند که عمدتاً پروتئینها هستند (مانند KIM{2}} [45] یا NGAL [46]). این واقعیت که ما نشانگرهای زیستی بالقوه جدیدی از AKI ناشی از سیس پلاتین و محافظت سیس پلاتین مرتبط با ماهیت چربی درکلیهبافت، دانش موجود را گسترش می دهد و گزینه های تکمیلی را برای تشخیص، پیش آگهی و پیگیری بهتر ارائه می دهد. در واقع، ترکیبی از شناسایی نشانگرهای زیستی ممکن است حتی بهطور بالقوه به عنوان نشانهای از یک AKI خاص ناشی از یک نفروتوکسین خاص (مانند سیس پلاتین) یا علت دیگری استفاده شود و حتی وضعیت/پیشرفت بیماری را متمایز کند. گام دیگر این است که تعیین کنیم آیا نتایج ما تغییر کند یا خیرکلیهالگوهای چربی نیز در چربی های در گردش خون یا ادرار منعکس می شود. این باعث تشخیص بیومارکر برای AKI و سیس پلاتین ناشی از سیس پلاتین می شودمحافظت از نفرودر بیماران امکان پذیرتر است.
تغییرات مرتبط با AKI ناشی از سیس پلاتین در سطوح لیپید متعدد و متنوع است و شامل لیپیدهای ساختاری مهم در سطح کامل می شود.کلیهساختار: قشر و مدولا. تضعیف بسیاری از این تغییرات توسط سیاستاتین پتانسیل عالی آن را برای بهبود نشان می دهدعملکرد کلیهو کاهش تغییرات ساختاری مرتبط با چربی، در ارتباط با نرمال شدهکلیهمرفولوژی. باز هم، سیستاتین برای تشخیص آسیب مستقیم سلولی محافظت نشده ناشی از سیس پلاتین و تغییرات ثانویه مربوط به آسیب اولیه مفید است، که می تواند در لوله های پروگزیمال با انسداد سیالاستاتین مسیر آپوپتوز با واسطه Fas مختل شود.
مواد و روش ها
معرف هاCilastatin (با مهربانی توسط Merck Sharp و Dohme SA، مادرید، اسپانیا ارائه شد) و سیس پلاتین (Pharmacia Nostrum (مادرید، اسپانیا) استفاده شد. محلول NaCl {{{0}}.9 درصد (Braun Medical SA، بارسلونا، اسپانیا) برای تهیه محلولهای دارویی برای تجویز استفاده شد. ß-1،10-N-dodecanoyl-D-erythro-sphingosine [HexCer 30:1 (d18:1/12:0)]، N-dodecanoyl D -اریترو اسفنگانیل فسفوریل کولین [dhSM 3{{5{72}}}}:0 (d18:0/12:0)]، 1،2-دیمیریستولئویل-sn گلیسررو-3- فسفوکولین [PC 28:2 (14:1/14:1)]، 1-هپتادکانوئیل-2-هیدروکسی-sn-گلیسررو{48}} فسفوکولین [LPC (17:0)]، و 1، 2- dipalmitoleoil-sn-glycero-3-phosphoethanolamine [PE 32:2 (16:1/16:1)] از Avanti Polar Lipids (آلاباستر، آلاباما، ایالات متحده آمریکا) خریداری شد. N-tetracosanoyl- Deuterated D-erythro-sphingosine [Cer 42:1-d7 (d18:1/24:0)]، N-stearoyl D-erythro-dihydrosphingosine [dhCer (36:0-d3)] و C{79}}sulfogalactosylceramide [Sulf 34:1(d18:1/16:0)] از Matreya LLC (کالج ایالتی، PA، ایالات متحده آمریکا) خریداری شد. کلسترول-d7 (FC-d7) و کلسترول-d7 پالمیتات [CE (16:{93}}d7)] از سیگما آلدریچ بودند.
حلالها و معرفهای درجه HPLC یا LC-MS به طور انحصاری شامل متانول (MeOH)، استونیتریل (ACN) و ایزوپروپانول (iPrOH) (VWR International Eurolab، بارسلونا، اسپانیا)، و همچنین کلروفرم، دی کلرومتان و آمونیوم برای مات استفاده شدند. (NH4COOH) (Sigma-Aldrich, Merck Life Science SL, مادرید, اسپانیا). آب فوق خالص از یک سیستم تصفیه Milli-Q (Millipore، Merck Life Science SL، مادرید، اسپانیا) به دست آمد.
مدل حیوانیموش های صحرایی نر بالغ ویستار (WKY، کریفا، بارسلونا، اسپانیا) در Instituto de Investigación Sanitaria Gregorio Marañón (IiSGM، مادرید، اسپانیا) پرورش داده شدند. اینها تحت شرایط دما، نور و رطوبت کنترل شده با دسترسی آزاد به غذا و آب نگهداری می شدند. درمانها به صورت داخل صفاقی همانطور که قبلاً توضیح داده شد [4،11] به چهار گروه از موشها (n=6 حیوان در هر گروه) انجام شد: گروه 1: کنترل (CNT) - 0. 9 درصد NaCl به موشها تزریق شد. موشهای صحرایی به روشی مشابه درمانهای گروههای 3 و 4. گروه 2: سیلاستاتین (CIL) - تزریقی (15{16}} میلی گرم در کیلوگرم وزن بدن (وزن بدن) در روز). گروه 3: سیس پلاتین (CISPL) تزریقی (دوز منحصر به فرد 5 میلی گرم در کیلوگرم وزن بدن در روز 0). و گروه 4: سیس پلاتین به علاوه سیستاتین (CISCIL) - تزریق 5 میلی گرم در کیلوگرم وزن بدن در روز 0 و تزریق سیلاساتین (150 میلی گرم در کیلوگرم وزن بدن در روز). حیوانات پنج روز پس از شروع درمان قربانی شدند. قبل از این، ادرار 24 ساعته در قفس های متابولیک از هر موش جمع آوری شد. سرم خون نیز با سانتریفیوژ جدا شد. کلیه ها پس از پرفیوژن با محلول سالین 0.9 درصد در دمای 4 درجه سانتیگراد خارج شدند و سپس کپسولاسیون انجام شد. قشر و مدولای سمت چپکلیهو نیمی از سمت راست با برش عرضیکلیهبریده شدند، در مایع N2 منجمد شدند و در نهایت در دمای 80 درجه سانتیگراد نگهداری شدند. نیمه دیگر سمت راستکلیهبرای مطالعات بافت شناسی در 4 درصد پارافورمالدئید و پارافین جاسازی شده تثبیت شد.
مطالعات بافت شناسیرنگآمیزی هماتوکسیلین/ائوزین (Sigma-Aldrich, Steinhem, Germany) روی موش صحرایی ساژیتال 5 میکرومتری انجام شد.کلیهبخش ها یک میکروسکوپ معکوس IX70 (المپوس، هامبورگ، آلمان) برای گرفتن میکروعکس با بزرگنمایی 20× و 60×، برای بررسی بافت شناسی استفاده شد.
شاخص های عملکرد کلیهAutoAnalyzer Cobas 711 (روش، بازل، سوئیس) برای تعیین BUN، کراتینین، سدیم و پتاسیم در نمونههای سرم استفاده شد. نرخ کلیرانس کراتینین برای محاسبه GFR استفاده شد. پروتئین کل در ادرار با استفاده از روش اسید سولفوسالیسیلیک [47] تعیین شد.
همگن سازی بافت کلیهبافتهای قشر و مدولا (هر کدام تقریباً 50 میلیگرم) به لولههای پلاستیکی 1.5 میلیلیتری حاوی 800 میکرولیتر محلول بافر لیز اضافه شدند: 50 میلیمولار Tris-HCl pH 7.5، 125 میلیمولار NaCl، 5 میلیمولار NaF، 1.4 میلیمولار Na4O4، mM23، Na4O7P. و مهارکننده پروتئاز (Pierce Biotechnology, Inc., Rockford, IL, USA) و دانه های زیرکونیوم 1.5 میلی متری. بافت ها در یک هموژنایزر BeadBug (Benchmark D{20}}E, Bechmark Scientifific, Sayreville, NY, USA) در 4500 دور در دقیقه در سه چرخه 90 ثانیه ای جدا شدند. هموژن بیشتر به مدت 40 ثانیه در 10 درصد دامنه فراصوت شد و در 600× گرم به مدت 1 دقیقه در دمای 4 درجه سانتیگراد سانتریفیوژ شد. مقدار کمی از مایع رویی حاصل 1:10 برای تعیین پروتئین کل توسط سنجش پروتئین اسید بیسینکونیک (BCA) (Pierce Biotechnology Inc., Rockford, IL, USA) رقیق شد. بقیه عصاره پروتئینی در دمای 80 درجه سانتیگراد تا آنالیز لیپیدومی نگهداری شد.

آنالیز لیپیدومی توسط LC-MS/MSلیپیدها از بافت ها (معادل 25{15}} میکروگرم پروتئین کل) به روش Folch [48] استخراج شدند. 10 میکرولیتر از مخلوط استاندارد داخلی (IS) قبل از استخراج لیپید برای بدست آوردن کمیت مولی نسبی گونه های چربی، همانطور که قبلاً توضیح داده شد، اضافه شد [49]. مخلوط IS شامل موارد زیر بود: CE (16:0-d7)، FC-d7، Cer (42:{{{0}}} d7)، HexCer (30 :1)، LPC (17:0)، PC (28:2)، PE (32:2)، SM (30:1)، dhSM (30:0)، dhCer (35:0) و Sulf (34) :1)، در غلظت های ارائه شده در جدول S4. عصاره های لیپیدی تحت یک جریان نیتروژن خشک شده و در 250 میکرولیتر استونیتریل/ایزوپروپانول (1:1، حجم: حجم) بازسازی شدند، به مدت 10 دقیقه تحت فراصوت قرار گرفتند و سپس به ویال تزریق منتقل شدند.
پنج میکرولیتر از عصاره لیپیدی روی یک سیستم LC Eksigent UltraLC{{{0}} (AB-Sciex LLP، Framingham، MA، USA) تزریق شد. گونه ها بر روی یک ستون Kinetex C18 (100 × 2.1 میلی متر، 1.7 میکرومتر؛ Phenomenex، Macclesfifield، UK) که در دمای 55 درجه سانتی گراد کار می کرد، جدا شدند. شستشو با استفاده از مخلوط دوتایی از حلال A (60 درصد استونیتریل در آب، 10 میلی مولار NH4COOH) و حلال B (90 درصد ایزوپروپیل الکل در استونیتریل، 10 میلی مولار NH4COOH) و گرادیان خطی از 60 درصد A تا 100 درصد B در 12 استفاده شد. دقیقه و 100 درصد B تا 60 درصد A در 8 دقیقه، با سرعت جریان 0.4 میلی لیتر در دقیقه. ابزار QTrap 4000 (AB-Sciex LLP, Framingham, MA, USA) برای تشخیص لیپید با نرم افزار Analyst 1.6.2 استفاده شد. نیتروژن هم به عنوان گاز خشک کردن (T: 500 ◦C، فشار: 30 psi) و هم به عنوان گاز نبولیزاسیون (50 psi) استفاده شد. تشخیص در الکترواسپری (ESI) حالت مثبت برای تمام کلاس های لیپید به استثنای سولف، که در حالت منفی ESI تجزیه و تحلیل شد تنظیم شد. CE و FC با استفاده از منبع یونیزاسیون شیمیایی فشار اتمسفر (APCI) در حالت یون مثبت آنالیز شدند. یک رویکرد هدفمند برای تشخیص چربی تنظیم انتقال نظارت بر واکنش چندگانه (MRM) برای هر گونه لیپید در زمانهای ماند آنها استفاده شد (جدول S5). کروماتوگرام های پیک LC-MS/MS با استفاده از نرم افزار Skyline نسخه 4.1 (آزمایشگاه MacCoss، سیاتل، WA، ایالات متحده آمریکا) پردازش شدند [50]. گونه های چربی با مقایسه مستقیم مساحت هر گونه با مساحت IS برای کلاس لیپیدی آنها، همانطور که قبلاً توضیح داده شد، کمی سازی شدند [49]. نتایج به صورت nmol/mg پروتئین بیان شد. سطح کل کلاس لیپید به عنوان مجموع گونه های کلاس لیپید فردی تعیین شد. گونه های لیپید بر اساس نماد توصیه شده [51] تعیین شدند.
تحلیل آماریمقادیر به صورت میانگین ± انحراف معیار بیان شد. SPSS 11.5 (SPSS، شیکاگو، IL، ایالات متحده آمریکا) برای آمار توصیفی و ارزیابی تفاوت های آماری در متغیرها بین گروه ها با استفاده از تجزیه و تحلیل واریانس استفاده شد. برای مقایسه دو گروهی غیرجفتی متغیرهای لیپیدی، آزمونهای پارامتریک (t Student's un جفت نشده دو دنباله) یا آزمونهای ناپارامتریک (Mann-Whitney) پس از تست نرمال (Shapiro-Wilk) انجام شد. روش بنجامینی-هوچبرگ برای تصحیح نرخ کشف کاذب (FDR) مقادیر p هنگام مقایسه گونههای مختلف لیپیدی مورد استفاده قرار گرفت. یک مقدار p دو طرفه < 0.05="" و="" fdr="">< 0.1="" برای="" شناسایی="" تفاوتهای="" آماری="" معنیدار="" برای="" جلوگیری="" از="" گم="" شدن="" نامزدهای="" نشانگر="" زیستی="" بالقوه="" در="" نظر="" گرفته="" شد.="" تغییر="" برابری="" گروه="" x="" در="" مقابل="" گروه="" y="" به="" عنوان="" نسبت="" مقادیر="" میانگین="" برای="" متغیرهای="" گروه="" مربوطه="" x:y="" محاسبه="">
تجزیه و تحلیل دادههای چند متغیره (MVDA) با استفاده از SIMCA نسخه 14.1 (MKS Umetrics, Uppsala, Sweden) و MetaboAnalyst 5 انجام شد. {{20}}21)) [52]، از جمله PCA بدون نظارت و OPLSDA تحت نظارت. مقادیر گمشده با استفاده از روش k-نزدیکترین همسایه جایگزین شدند. متغیرها قبل از MVDA تغییر شکل داده و مقیاس پارتو شدند. مدل ها با توجه به مقادیر R2 و Q2 آنها ارزیابی شدند. OPLS-DA با آزمون جایگشت (100 چرخه) اعتبارسنجی شد. نمرات VIP و نمودارهای S از مدلهای OPLS-DA برای شناسایی متغیرهای مرتبط در CISPL در مقابل CNT، CISCIL در مقابل CNT، و CISCIL در مقابل CISPL استفاده شد. انطباق همزمان با VIP > 1، بارگذاری به صورت ضریب همبستگی |p(corr)| > 0.5، و p-value دو طرفه <0.05 و="" fdr=""><0.1 برای="" مقایسه="" دو="" گروهی="" معیارهای="" مورد="" استفاده="" برای="" انتخاب="" نشانگر="" زیستی="" بالقوه="" بودند.="" مقادیر="" auc="" از="" نمودارهای="" منحنی="" roc="" به="" دست="">
ثبت اختراعاتپتنتهای زیر تا حدی به کار ارائهشده در این دستنوشته مربوط میشوند: "استفاده از سیلاستاتین برای کاهش سمیت کلیوی ترکیبات مختلف" (شماره ثبت اختراع EP2,143,429 B1؛ US 9,216,185 B2؛ US 9,522,128 B2؛ و US9,757,349 B). اینها به بیمارستان بنیادی تحقیقاتی بیومدیکا گرگوریو مارانیون (FIBHGM) اختصاص داده شده و توسط FIBHGM به Telara Pharma SL مجوز داده شده است Telara Pharma SL در حال حاضر یک قرارداد مجوز با Arch Biopartners منعقد کرده است.
