سلول های بنیادی مزانشیمی و وزیکول های خارج سلولی در درمان بیماری های کلیوی
Mar 06, 2023
یولینگ هوانگ و لینا یانگ*
خلاصه
بیماری های کلیوی به دلیل افزایش میزان بروز و مرگ و میر، سلامت انسان را تهدید می کند. در مطالعات پیش بالینی و بالینی، تایید شده است که سلول های بنیادی مزانشیمی (MSCs) هنگامی که برای درمان بیماری های کلیوی استفاده می شوند، موثر و ایمن هستند. سلول های بنیادی مزانشیمی نقش خود را عمدتاً با ترشح فاکتورهای تغذیه ای و تحویل وزیکول های خارج سلولی (EVs) ایفا می کنند. مواد ژنتیکی و پروتئین های موجود در EVs مشتق از MSC (MSC-EVs)، به عنوان یک وسیله مهم ارتباط سلولی، به کانون تحقیقاتی برای درمان هدفمند بیماری های کلیوی تبدیل شده است. در حال حاضر، MSC-EVs اثرات درمانی مشهودی بر آسیب حاد کلیه (AKI)، بیماری مزمن کلیوی (CKD)، نفروپاتی دیابتی (DN) و بیماری آترواسکلروتیک رنواسکولار (ARVD) نشان داده اند. با این حال، نقش آنها در کلیه پیوندی بحث برانگیز است. این بررسی مکانیسمهایی را که توسط آن MSC-EVs این بیماریها را در مدلهای حیوانی درمان میکنند، خلاصه میکند و مشکلات خاصی را پیشنهاد میکند و انتظار دارد که عملکرد بالینی مربوطه را در آینده تسهیل کند.
کلید واژه ها: بیماری های کلیویسلول های بنیادی مزانشیمی، وزیکول های خارج سلولی
معرفی
بیماری های کلیوی با افزایش میزان بروز و مرگ و میر آنها به یک موضوع مهم بهداشت جهانی تبدیل شده اند [1]. بیماری های شایع کلیوی شامل آسیب حاد کلیه (AKI)، بیماری مزمن کلیه (CKD)، نفروپاتی دیابتی (DN)، نفریت لوپوس و نفروپاتی فشار خون بالا، ناشی از علل مختلف است. روشهای اصلی درمانی علیه این بیماریهای کلیوی شامل دارودرمانی، دیالیز و پیوند کلیه است [2، 3]. با این حال، درمان های جدید به دلیل محدودیت های درمان دارویی، ناراحتی دیالیز و کمبود اهداکنندگان برای پیوند کلیه پدیدار می شوند [4]. در سال های اخیر، سلول های بنیادی به عنوان یک درمان ترمیمی جدید، برای درمان بسیاری از بیماری ها از جمله بیماری های کلیوی مورد استفاده قرار گرفته اند. بنابراین، سلول های بنیادی مزانشیمی به وسیله ای جدید برای درمان بیماری های کلیوی تبدیل شده اند. در مقایسه با سلول های بنیادی مزانشیمی، درمان بیماری های کلیوی با وزیکول های خارج سلولی مشتق از MSC (MSCEVs) با مزایایی مانند ایمنی زایی کمتر و تومورزایی مشخص می شود [6]. با این حال، مسیر و مکانیسم عمل MSC-EVs در درمان بیماری های کلیوی مشخص نشده است، و استفاده بالینی از MSC-EVs هنوز در حال بررسی است. با توجه به این موضوع، در این بررسی، وضعیت تحقیقات مربوط به MSC-EVs در درمان را خلاصه میکنیم.بیماری های کلیوی.

Cمزایای مردانه استانچه
MSC-EVs
ویژگی های بیولوژیکی سلول های بنیادی مزانشیمی
سلول های بنیادی را می توان با توجه به مرحله رشد به دو دسته سلول های بنیادی جنینی و بالغ تقسیم کرد. سلول های بنیادی بالغ به سلول های تمایز نیافته در بافت های تمایز یافته گفته می شود و در بافت ها و اندام های مختلف بدن وجود دارند. سلول های بنیادی مزانشیمی به عنوان نوعی از سلول های بنیادی بالغ چند توان خود تجدید شونده، می توانند به انواع مختلفی از سلول ها تمایز یابند. سلول های بنیادی مزانشیمی را می توان از بافت های متعددی مانند سلول های بنیادی مزانشیمی مشتق از مغز استخوان (BMMSCs) [7]، سلول های بنیادی مزانشیمی مشتق از چربی (ADMSCs) [8]، سلول های بنیادی مزانشیمی مشتق از بند ناف انسانی (huMSCs) [9]، سلول های بنیادی مزانشیمی مشتق از جفت انسانی جدا کرد. [10] و آنهایی که از پالپ، پوست، خون و ادرار دندان گرفته می شوند [5، 11]. در تحقیقات موجود عمدتاً از BMMSCها، ADMSCها و HuMSCها استفاده می شود. تحقیقات نشان داده است که سلول های بنیادی مزانشیمی مناطق آسیب دیده را از طریق تعامل مستقیم و اثر پاراکرین [12، 13] مکان یابی می کنند در حالی که کمتر به عملکرد تمایز وابسته هستند [14]. از طریق علامت گذاری، مشخص شد که، پس از تزریق به بدن، MSCها می توانند به طور خاص در مناطق آسیب دیده کلیه قرار گیرند [15-17]. مکانیسمهای مولکولی خانهسازی سلولهای بنیادی مزانشیمی مبتنی بر یک مدل چند مرحلهای است، از جمله اتصال اولیه توسط سلکتینها، فعالسازی توسط سیتوکینها، توقف توسط اینتگرینها، دیاپدیز یا انتقال، و مهاجرت به سمت کموکاینها [18]. لازم به ذکر است که کموکاین ها و گیرنده های آنها به عنوان واسطه های مهم خانه سازی MSC شناخته می شوند. با این حال، سطوح بیان پایین مولکول های خانگی کارایی درمان MSC را محدود می کند [19]. د ویت و همکاران و شرپفر و همکاران. توضیح داده اند که مشکل اصلی پس از تجویز MSC این است که آنها بافت هدف را هدف قرار نمی دهند و اثر درمانی آنها را محدود می کند [20، 21]. سپس، تجویز هدف، هدایت مغناطیسی، اصلاح ژنتیکی، و مهندسی سطح سلول، در میان دیگران، برای تسهیل خانهسازی MSC مورد مطالعه قرار میگیرند [18]. سلولهای بنیادی مزانشیمی عمدتاً از طریق تحویل سیستمیک و زایمان موضعی برای بافتهای هدف تجویز میشوند، اولی شامل داخل شریانی و داخل وریدی و دومی شامل تزریق موضعی، داخل عضلانی، تزریق مستقیم بافت و کاشت مستقیم مبتنی بر کاتتر است. با این حال، هیچ اتفاق نظری در مورد روش بهینه برای تزریق MSC وجود ندارد [12]. همچنین، سلولهای بنیادی مزانشیمی میتوانند با ترشح فاکتورهای تغذیهای مانند فاکتورهای رشد، کموکاینها و سیتوکینها بر روی سلولهای محیطی عمل کنند یا با تشکیل نانولولههای تونلی، ترشح وزیکولهای خارج سلولی (EVs) و ترکیب شدن با سلولها، ساختارهای درون سلولی و حتی میتوکندری را تحویل دهند [22]. در آن زمان، سنتز و آزادسازی EV های حاوی پروتئین، اسید نوکلئیک ریبوز پیام رسان (mRNA)، و اسید نوکلئیک میکرو ریبوز (miRNA) از طریق پاراکرین به کانون تحقیقات فعلی تبدیل شده است. به طور خلاصه، MSCs/MSC-EV ها می توانند به روش های مختلفی عمل کنند، همانطور که در شکل 1 نشان داده شده است.
ویژگی های بیولوژیکی EVs
EVs، نوعی وزیکول در مقیاس نانو که توسط سیتوممبران محصور شدهاند، میتوانند به اگزوزومها (Exos)، میکرووزیکولها (MVs) و اجسام آپوپتوز (شکل 1) تقسیم شوند که قطر آنها 30-150 نانومتر، 200-1000 نانومتر و 800- است. به ترتیب 5000 نانومتر [23]. EV ها به عنوان یک وسیله مهم ارتباط بین سلولی، به طور گسترده در مایعات بدن از جمله خون، ادرار و مایع آمنیوتیک وجود دارند. EV ها از طریق جوانه زدن وارد اندوزوم ها می شوند تا اجسام چند وزیکولی (MVBs) را تشکیل دهند، سپس MVB ها با سیتوممبران ترکیب می شوند تا EV ها را آزاد کنند [24]. EV ها حاوی DNA، RNA، پروتئین ها و لیپید هستند و مواد موجود در EV ها به طور خاص توسط متروسیت ها تعیین می شوند [25]. این پایه و اساس استفاده از EV ها را به عنوان نشانگر تشخیصی بیماری می گذارد. به عنوان یک نشانگر تشخیصی غیر تهاجمی، EVs توجه زیادی را به خود جلب کرده است.

شکل 1 عملکرد MSCs/MSC-EVs. سلول های بنیادی مزانشیمی می توانند به طور خاص در نواحی آسیب دیده کلیه قرار گیرند. سپس، سلولهای بنیادی مزانشیمی با ترشح فاکتورهای تغذیهای مانند فاکتورهای رشد، کموکاینها و سیتوکینها بر روی سلولهای محیطی عمل میکنند یا با تشکیل نانولولههای تونلی، ترشح EVs و ترکیب شدن با سلولها، ساختارهای درون سلولی و حتی میتوکندری را تحویل میدهند. EV ها از طریق جوانه زدن وارد اندوزوم ها می شوند تا MVB ها را تشکیل دهند، سپس MVB ها با سیتوممبران ترکیب می شوند تا EV ها را آزاد کنند. EV ها را می توان به اگزوزوم، MVs و اجسام آپوپتوز تقسیم کرد. EV ها، به ویژه Exos، حاوی DNA، RNA، پروتئین و لیپید هستند. سلول های بنیادی مزانشیمی، سلول های بنیادی مزانشیمی؛ EVs، وزیکول های خارج سلولی؛ MVB ها، اجسام چند وزیکولی؛ MVs، میکرووزیکول ها
به عنوان مثال، miRNA های Exos ادراری به طور قابل اعتمادی پیشرفت AKI را منعکس می کنند [26]. EVs برای مشخص کردن رد در پیوند قلب آلوژنیک استفاده می شود [27]. MSC-EV ها می توانند پیشرفت بیماری های کلیوی را از طریق مکانیسم های ضد آپوپتوز، ضد التهاب، ضد فیبروز، آنتی اکسیدان و غیره به تاخیر بیندازند. تحقیقات دیگر همچنین نشان داد که EV های مشتق شده از منابع دیگر نیز می توانند عملکرد کلیوی از جمله سلول های توبولار کلیوی را بهبود بخشند. 28، 29]، سلول های بنیادی مزانشیمی گلومرولی [30]، سلول های بنیادی مزانشیمی جدا شده از بیضه [31] و حتی ادرار [32]. این خودروهای الکتریکی راه جدیدی را برای درمان بیماری های کلیوی آغاز کردند.

گیاه چینی سیستانچ
علاوه بر این، خودروهای الکتریکی می توانند طیف وسیع تری از نقش ها را تحت طراحی و کنترل مهندسی زیستی ایفا کنند. وسایل نقلیه الکتریکی می توانند انواع مختلفی از داروها را از طریق اصلاح قبل و بعد از انتشار [33] حمل کنند و نقش درمانی خود را با بارگذاری مواد روی آن و هدف قرار دادن بعدی [34] مانند میکرو مولکول ها، پروتئین ها و اسیدهای نوکلئیک ایفا کنند [35]. وسایل نقلیه الکتریکی به عنوان یک حامل دارویی برای بیماریهای مختلف، مانند حمل داروهای ضد نئوپلاستیک [36] و ضد التهاب [37] به کانون تحقیقاتی تبدیل شدهاند. ویژگی جذب EVs به شدت به سطح EVs و سلولهای پذیرنده، از جمله اینتگرینها، پروتئوگلیکانها، لکتینها، گلیکولیپید و غیره بستگی دارد که میتوانند به هدفگیری کمک کنند [38]. با این حال، احتباس کم و پایداری ضعیف EVs پس از پیوند، کاربرد بیشتر در عمل کلینیک را محدود میکند. برای تقویت اثر درمانی MSC-EVs برای بیماریهای کلیوی، EVs در یک ماتریکس کلاژن [39]، ماتریکس متالوپروتئیناز{13}}هیدروژل پپتید خود مونتاژ شونده حساس [40] و هیدروژل آرژنین-گلیسیناسپارتات (RGD) محصور میشوند [41] ماندگاری آنها طولانی شود و در نتیجه باعث آزادسازی پایدار شود. به طور واضح، هیدروژلهای RGD با واسطهگری زیرواحدهای اینتگرین v، 3 و 8 با EVs تعامل دارند [41]. علاوه بر کند کردن روند حذف EVs، کپسولاسیون میتواند به کلیه EVs کمک کند تا آسیب کلیوی را با کاهش آسیب پاتولوژیک، ترویج تکثیر سلولی، مهار آپوپتوز سلولهای کلیوی، تقویت فعالسازی اتوفاژیک، و افزایش رگزایی و همچنین بهبود فیبروز کاهش دهد [39- 41]. همچنین مشخص شده است که بیان بیش از حد اکتبر{22}} میتواند اثر درمانی MSC-EVs [42] را بهبود بخشد، و هیپوکسی سلولهای بنیادی مزانشیمی را تحریک میکند تا EVs بیشتری ترشح کنند [43]. MSC-EV های پردازش شده با اریتروپویتین می توانند محتوای miRNA را در EV ها افزایش دهند و بنابراین ممکن است به افزایش اثر محافظتی بر کلیه کمک کنند [44].
MSC-EVs و بیماری های کلیوی
MSC-EV و AKI
AKI در بیماران بدحال شایع است، حتی مرگ و میر آن دسته از بیماران AKI که در بخش مراقبت های ویژه نیستند به 10-20 درصد می رسد [45]. هنوز کمبود درمان های خاص و موثر برای AKI وجود دارد، در حالی که پیوند سلول های بنیادی امیدوارکننده است. آزمایشهای متعدد مزایای MSCها را در درمان AKI تأیید کردهاند و روشهای زیادی برای افزایش تأثیر MSCها در سالهای اخیر پدیدار شدهاند. برای مثال، IL{3}}A میتواند درصد Treg را از طریق مسیر COX-2/PGE2 افزایش دهد و عملکرد سرکوبکننده ایمنی سلولهای بنیادی مزانشیمی را شبیهسازی کند [46]. با پوشاندن سلول های بنیادی مزانشیمی با آنتی بادی های معطوف به مولکول آسیب کلیوی{7}}، ماندگاری سلول های بنیادی مزانشیمی در کلیه ایسکمیک طولانی تر می شود [47]. در مدل موش AKI القا شده با سیس پلاتین، سلول های بنیادی مزانشیمی به طور مستقیم با استفاده از یک تکنیک کم تهاجمی به آئورت تزریق می شوند که سرعت موثر استفاده از سلول های بنیادی مزانشیمی را بهبود می بخشد [48]. با پیشرفت تحقیقات، شواهد نشان می دهد که MSCEV ها نقش مهمی در درمان AKI دارند. MSC-EV ها می توانند AKI را با مهار اکسیداسیون، آپوپتوز و التهاب و تنظیم رگ زایی، چرخه سلولی، بازسازی، اتوفاژی و تکثیر [49-54] تسکین دهند (شکل 2). با این حال، برای AKI با پاتوژنزهای مختلف، مواد سیگنالی که از MSC-EVs به سلول های هدف منتقل می شوند، ویژگی های منحصر به فرد خود را نشان می دهند. پاتوژنزهای اصلی AKI شامل سمیت کلیوی داروها، آسیب ایسکمی خونرسانی مجدد (IRI) ناشی از پیوند و سپسیس است. به همین ترتیب، مدلهای آزمایشی AKI عمدتاً توسط سیس پلاتین، جنتامایسین، پاراکوات، ایسکمی-پرفیوژن مجدد (I/R) با انسداد شریانهای کلیوی یکطرفه یا دو طرفه و سپسیس ناشی از بستن و سوراخ شدن روده (CLP) القا میشوند. مکانیسم های MSC-EV در مدل های مختلف AKI در این بررسی در جدول 1 خلاصه شده است.

Cistanche tubulosa beneficios-کلیه
(Cistanche deserticola یک داروی سنتی چینی است که معمولاً در عمل بالینی استفاده می شود، که دارای اثرات گرم کردن و تقویت کننده یانگ کلیه، مرطوب کردن روده ها و اجابت مزاج، و تقویت کننده جوهر خون است. این دارو اثر قوی گرم کننده و تقویت کننده یانگ کلیه دارد. می توان از آن برای درمان سردرد در ناحیه کمر و زانو ناشی از کمبود یانگ کلیه، تکرر ادرار، ناتوانی جنسی، انزال زودرس، اسپرماتوره و سایر بیماری ها استفاده کرد.)
آسیب کلیه ناشی از I/R
I/R یک پاتوژنز شایع AKI است. در آزمایشهای حیوانی، مدلهای I/R عموماً با مسدود کردن شریانها و سیاهرگهای کلیوی یکطرفه یا دوطرفه و سپس تأمین اکسیژن ایجاد میشوند. تحقیقات قبلی نشان داد که huMSC-EV ها می توانند IRI کلیه را در موش صحرایی تسکین دهند، مستقل از اثر ترویج رگزایی ناشی از فاکتور القاکننده هیپوکسی-1 [49]. MSC-EVها همچنین می توانند ماکروفاژها را در مدل I/R از طریق مسیرهای مختلف برای تسکین AKI مهار کنند. در آزمایشات انجام شده توسط Zou و همکاران، MVهای مشتق شده از سلول های بنیادی مزانشیمی ژله وارتون انسانی (hWJMSCs) بیان کموکاین کلیوی CX3CL1 را با miR{7}}a/15b/16 سرکوب می کنند و تعداد CD68 به علاوه ماکروفاژها را کاهش می دهند [55] ]. شن و همکاران دریافت که گیرنده کموکاین CC{13}} بیان شده در BMMSC-Exos با عمل به عنوان یک طعمه برای اتصال لیگاند CCL2، جذب و فعال سازی CCL2 را برای ماکروفاژها مهار می کند [56].
آپوپتوز ارتباط نزدیکی با IRI دارد. گو و همکاران از طریق آزمایشهای in vivo و in vitro تأیید کرد که EVهای مشتق شده از hWJMSCs (hWJMSC-EVs) با مهار شکافت میتوکندری با استفاده از miR، آپوپتوز سلولهای اپیتلیال لولهای کلیوی (TECs) را کاهش میدهند [57]. علاوه بر این، لی و همکاران. بیان کرد که MSC-Exo با مهار بیان عوامل التهابی (IL{4}}، TNF-، NF-kappa B و IFN-) و عوامل مرتبط با آپوپتوز (کاسپاز{9}}، شکاف، پیشرفت IRI را کند کرد. کاسپاز{10}}، Bax، و Bcl-2) [50].

شکل 2 مسیرهای عملکردی MSC-EVs در مدل های مختلف AKI. MSC-EV ها می توانند AKI را با مهار اکسیداسیون، آپوپتوز و التهاب و تنظیم رگ زایی، چرخه سلولی، بازسازی، اتوفاژی و تکثیر تسکین دهند. سلول های بنیادی مزانشیمی، سلول های بنیادی مزانشیمی؛ EVs، وزیکول های خارج سلولی؛ AKI، آسیب حاد کلیه؛ I/R، ایسکمی خونرسانی مجدد. CLP، بستن سکوم و سوراخ کردن
آنتی اکسیدان یک اقدام موثر برای کاهش I/R است. ژانگ و همکاران نشان داد که hWJMSC-EVs اثر آنتی اکسیدانی خود را با فعال کردن فاکتور هستهای-اریتروئید 2- Nrf2/ARE [57] مرتبط میکنند. پس از آن، آزمایش های Cao و همکاران. نشان داد که BMMSC-EV مسیر سیگنالینگ Keap{6}}Nrf2 را در TECs با انتقال miRNA-200a{9}} فعال میکند، بنابراین میتوکندری را تعدیل میکند تا نقش آنتیاکسیدانی ایفا کند [51].
مدل AKI ناشی از سیس پلاتین
مدل های AKI ناشی از داروها عموماً از طریق القای سیس پلاتین ایجاد می شوند. با استفاده از مدل AKI ناشی از سیس پلاتین، برونو و همکاران. دریافتند که BMMSC-MVs با القای بیان ژنهای ضد آپوپتوز (Bcl-XL، Bcl2، و BIRC8) در TECs و مهار بیان ژنهای pro-apoptotic (Casp1، Casp8 و LTA) از کلیه محافظت میکنند [58]. ژو و همکاران به این نتیجه رسیدند که huMSC-Exos میتواند تکثیر نفروسیتها را در شرایط in vivo و in vitro با القای فسفوریلاسیون و فعالسازی مسیر 1/2 کیناز تنظیمشده خارج سلولی (ERK) تحریک کند [52]. د آلمیدا و همکاران عملکرد ADMSC-MVs را در تنظیم سلول های آسیب دیده و شبکه miRNA-mRNA خاص برجسته کرد. برای مثال، miR{16}} Ulk2 را برای تنظیم اتوفاژی و miR{18}} Cul1 را برای تعدیل چرخه سلولی هدف قرار میدهد [53]. وانگ و همکاران کشف کردند که پیش پردازش huMSC-Exo می تواند از سمیت کلیوی ناشی از سیس پلاتین در داخل بدن و در شرایط آزمایشگاهی با فعال کردن اتوفاژی جلوگیری کند [59]. جیا و همکاران دو مطالعه انجام داد و 14-3-3ζ را به عنوان یک مکانیسم جدید اتوفاژی فعال شده توسط huMSC-Exos شناسایی کرد:14-3-3ζ روی ATG16L عمل میکند، که اتوفاژی را فعال میکند و بنابراین از AKI ناشی از سیس پلاتین جلوگیری میکند [60، 61]. الله و همکاران اخیرا پیشنهاد شده است که BMMSC-EVs و سونوگرافی متمرکز پالسی هر دو آسیب سلولی ناشی از سیس پلاتین را با مهار التهاب NLRP3 با واسطه hsp کاهش میدهند [62].
مدل AKI به دلیل میولیز ناشی از گلیسیرین
در سال های اخیر، مدل AKI به دلیل میولیز ناشی از گلیسیرین نیز بسیار مورد توجه قرار گرفته است. در چنین مدلی، برونو و همکاران. دریافتند که BMMSC-EVs (عمدتا Exos) در mRNA خاصی (CCNB1، CDK8، و CDC6) غنی شدهاند، که بر شروع و پیشرفت چرخههای سلولی تأثیر میگذارد. miRNA های غنی شده باعث افزایش تکثیر توسط فاکتورهای رشد (HGF و IGF{4}}) می شوند و بنابراین AKI را تسکین می دهند [63]. از طریق مهندسی زیستی، تاپارو و همکاران. افزایش miRNA های خاص (has-miR-10a-5p، هم-miR{10}}}a{11}}p، هم has-miR-127-3p، و هم has-miR -486-5p) در BMMSCEVها برای شبیهسازی اثر پیشسازنده آن و کاهش آسیب کلیه ناشی از گلیسیرین [54].
CLP
مدل AKI تهیه شده توسط CLP AKI مربوط به سپسیس در بیماران بدحال را شبیه سازی می کند. در موش های مبتلا به سپسیس، ژانگ و همکاران. نشان داد که huMSC-Exos با افزایش سطح miR{3}}b در حالی که بیان کیناز مرتبط با گیرنده اینترلوکین را کاهش میدهد، فعالیت NF-kB را مهار میکند [64]. به طور مشابه، گائو و همکاران. بیان کرد که ADMSC-Exo می تواند NF-kB را از طریق مسیر سیگنالینگ SIRT1 تنظیم کند، بنابراین التهاب AKI مربوط به سپسیس را مهار می کند [65].

MSC-EV و CKD
شواهد جدیدی وجود دارد که ثابت می کند، در بسیاری از موارد، AKI ممکن است به CKD تبدیل شود [66]. پس از ایجاد AKI، خطرات اضافی ابتلا به بیماریهای کلیوی مرحله نهایی و CKD به ترتیب به میزان 0.4 و 10 مورد سالانه در هر 100 بیمار AKI افزایش مییابد [67]. CKD با فیبروز برگشت ناپذیر پیشرونده پارانشیم کلیه مشخص می شود. بسیاری از بیماری ها می توانند به CKD تبدیل شوند، از جمله AKI، دیابت، آترواسکلروز و سندرم های نفروتیک. شواهد متعددی در مورد درمان CKD با سلول های بنیادی مزانشیمی در کارآزمایی های پیش و پس از بالینی به دست آمده است. در تحقیقات اخیر مشخص شده است که پیش شرطی سازی ملاتونین توانایی درمانی سلول های بنیادی مزانشیمی را در پیوند اتولوگ و آلوژنیک افزایش می دهد [68، 69]. در یک کارآزمایی بالینی که شامل یک 18-ماه پیگیری هفت بیمار واجد شرایط CKD بود، ثابت شده است که MSCهای اتولوگ تک دوز در بیماران CKD ایمن و قابل تحمل هستند [70]. سپس محققان دریافتند که محیط شرطی شده سلول های بنیادی مزانشیمی فیبروز ناشی از انسداد یک طرفه حالب (UUO) توسط پرولیفراسیون و ضد آپوپتوز را تسکین می دهد [71]. تا به امروز، بسیاری از مطالعات پیش بالینی ثابت کرده اند که MSC-EVs در درمان CKD موثر هستند.
در مدل موش سمیت مزمن کلیوی ناشی از سیکلوسپورین، محیط شرطی شده فاقد EVs، MSC-EVs و EVs می تواند پیش آگهی بیماری های کلیوی را بهبود بخشد [72]. در مدل نفروپاتی اسید آریستولوکیک، MSC-EV ها به طور قابل توجهی بیان ژن های پروفیبروژنیک مانند -SMA، TGF 1 و Col1a1 را کاهش می دهند [73]. در مدل UUO، وانگ و همکاران. دریافتند که BMMSC-Exos فیبروز بینابینی کلیه را با مهار TGF{10}} با miRNA-let7c کاهش میدهد [74]. اخیراً، برخی از محققان (در مدل موش) دریافتند که huMSCExos فیبروز بینابینی کلیه را با سرکوب مسیر P38MAPK/ERK با واسطه ROS تسکین میدهد [75]. چن و همکاران پیشنهاد کرد که ADMSC-Exos اصلاح شده با فاکتور نوروتروفیک مشتق از گلیال با فعال کردن مسیر SIRT1/eNOS، مویرگ های اطراف عروقی در فیبروز توبولو بینابینی را تحریک می کند [76]. علاوه بر این، تحقیقات قبلی همچنین پیشنهاد کرد که ADMSC-Exos بیان فاکتور رونویسی Sox9 TECs را تنظیم میکند و فرزندان سلولهای Sox9 پلاس بازسازی توبولهای کلیوی را به جای تبدیل فیبروتیک تسهیل میکنند، بنابراین انتقال AKI-CKD را کند میکنند [17. 77].
【Contact】 Email: xue122522@foxmail.com / Whats App: 0086 18599088692 / Wechat: 18599088692
MSC-EV و DN
DN پاتوژنز اصلی برای ESRD است. تحقیقات متعدد نشان می دهد که پیوند MSC می تواند پیشرفت DN را کند کند. یک کارآزمایی تصادفی کنترل شده گزارش داد که استفاده از سلول های پیش ساز مزانشیمی در افراد مبتلا به دیابت نوع 2 ایمن و امکان پذیر است [78]. با این حال، مشکلات رد ایمنی در پیوند آلوژنیک و آسیب ناشی از هیپرگلیسمی به سلول های بنیادی مزانشیمی اتولوگ وجود دارد. برای حل این مشکلات، ناگایشی و همکاران. به طور ابتکاری از مایع رویی عصاره ژله وارتون برای بهبود مورفولوژی، ظرفیت تکثیر و ظرفیت تحرک سلولی BMMSCهای مشتق شده از دیابت استفاده کرد که پیوند اتولوگ مؤثر را ممکن می سازد [79]. اخیراً، برخی از محققان همچنین تلاش کردند تا سلول های بنیادی مزانشیمی را با ماکروفاژهای صفاقی [80] کشت داده و سلول های بنیادی مزانشیمی را با آنزیم مبدل آنژیوتانسین 2 [81] اصلاح کنند تا ظرفیت درمانی سلول های بنیادی مزانشیمی برای DN را بهبود بخشند.
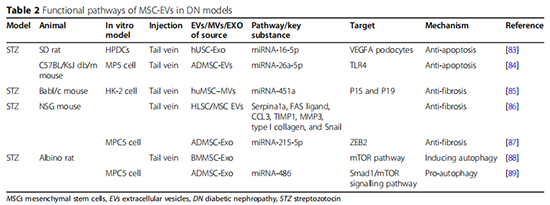
مکانیسم MSC-EVs، به عنوان یک وسیله جدید برای درمان DN، تحت کاوش مداوم است. گالو و همکاران دریافتند که سلولهای بنیادی سلولهای بنیادی کبد انسان (HLSC) میتوانند سلولهای مزانژیال را از آسیب ناشی از هیپرگلیسمی از طریق انتقال miR محافظت کنند [82]. همچنین، هیپرگلیسمی می تواند مستقیماً باعث آسیب سلول های پادوسیت شود. تغییرات پاتولوژیک پودوسیت ها ارتباط نزدیکی با پیشرفت DN دارد. MSC-EVs میتوانند از سلولهای پادوسیت و سایر سلولهای کلیوی با روشهای مختلف، از جمله اثرات ضد آپوپتوز، ضد فیبروز، و پیشآتوفاژیک محافظت کنند، بنابراین DN را درمان میکنند (شکل 3). دوان و همکاران نشان داد که Exo جدا شده از محیط شرطی شده سلول های بنیادی مشتق شده از ادرار انسان، بیان VEGFA و آپوپتوز پودوسیت ها را توسط miRNA{10}p مهار می کند و در نتیجه DN را تسکین می دهد [83]. توسط Duan و همکاران ثابت شده است. که ADSCEV miRNA{12}}a{13}}p آپوپتوز ناشی از هیپرگلیسمی پودوسیتها را در موش با کاهش مسیرهای سیگنالینگ TLR4 و NF-kB/VEGFA سرکوب میکند [84]. ضد فیبروز همچنین یک مکانیسم اصلی است که در درمان DN با MSC-EVs مورد استفاده قرار می گیرد. ژونگ و همکاران گزارش داد که MSC-MVها قادر به سرکوب مهارکنندههای چرخه سلولی P15 و P19 در داخل بدن و در شرایط آزمایشگاهی از طریق miRNA{23}}a هستند، چرخه سلولی را مجدداً شروع میکنند و در نتیجه EMT و فیبروز بینابینی را معکوس میکنند [85]. گرانج و همکاران در نظر گرفته شده است که EVs HLSCها و MSCها می توانند پیشرفت فیبروز گلومرولی و بینابینی توبولی را در مدل های موش DN با مهار کردن ژن مرتبط با فیبروز Serpia1a، لیگاند FAS، CCL3، TIMP1، MMP3، کلاژن نوع I [و Snail] مهار و معکوس کنند. 86]. جین و همکاران تأیید کرد که ADMS C-Exo با سرکوب رونویسی ژنتیکی ZEB2 توسط miRNA، EMT پودوسیت ها را ضعیف می کند{34}}p [87]. اتوفاژی نیز اخیراً به عنوان مکانیزمی برای به تاخیر انداختن DN در نظر گرفته شده است. ابراهیم و همکاران تایید کرد که MSC-Exos اتوفاژی را افزایش می دهد و سپس پیشرفت DN را از طریق مسیر سیگنالینگ mTOR کند می کند [88]. جین و همکاران همچنین نشان داد که ADMSC-Exo میتواند مسیر سیگنالینگ Smad1/mTOR را توسط miRNA{40}} مهار کند، که اتوفاژی را ترویج میکند و آپوپتوز را در پودوسیتها مهار میکند، بنابراین علائم DN را بهبود میبخشد [89]. جزئیات کارآزمایی های فوق در جدول 2 خلاصه شده است.
MSC-EVs و بیماریهای رنواسکولار آترواسکلروتیک

شکل 3 مسیرهای عملکردی MSC-EVs در DN. MSC-EVs میتوانند از سلولهای پادوسیت و سایر سلولها با روشهای مختلف، از جمله اثرات ضد آپوپتوز، ضد فیبروز، و اثرات پیشآتوفاژیک محافظت کنند، بنابراین DN را درمان میکنند. سلول های بنیادی مزانشیمی، سلول های بنیادی مزانشیمی؛ EVs، وزیکول های خارج سلولی؛ DN، نفروپاتی دیابتی
آترواسکلروز علت اصلی تنگی شریان کلیوی است. بیماری رنواسکولار آترواسکلروتیک (ARVD) می تواند ایسکمی مزمن کلیه را القا کند و بیشتر منجر به فیبروز شود که به ESRD تبدیل می شود. آنژیوپلاستی کلیه ترانس لومینال از راه پوست یک جراحی رایج برای درمان ARVD است. با این حال، بازیابی عملکرد کلیه آتروفیک دشوار است. آزمایشهای حیوانی تأیید کردهاند که ترکیب سلولهای بنیادی مزانشیمی با ARVD برای درمان تنگی شریان کلیوی آترواسکلروتیک به بازیابی عملکرد کلیه کمک میکند [90]. پس از آن، چندین آزمایش بالینی ایمنی تزریق ADMSCهای اتولوگ را در درمان ARVD نشان دادند [91-93]. به دنبال این، ADMSC-EVs نیز در کانون تحقیقات اخیر قرار گرفته است. در مدل بیماری رنواسکولار یک طرفه پیچیده کننده سندرم متابولیک (MetS)، Eirin و همکاران. ثابت کرد که ADMSC-EV های اتولوگ سیستم میکروواسکولار کلیه را در خوک های مبتلا به بیماری های متابولیک عروق کلیوی بهبود می بخشد [94]. علاوه بر این، سیمونی و همکاران. همچنین miRNA را در MSC-EVs به عنوان یک هدف مهم برای ARVD شناسایی کرد [95]. علاوه بر این، MSC-EVها همچنین مزایای Treg را توسط TGF- در آن افزایش میدهند و بنابراین عملکرد کلیه را با تنگی شریان کلیوی در مدل MetS پلاس RAS بهبود میبخشند [96]. ADMSC-EV های اتولوگ همچنین می توانند تبدیل فنوتیپ های ماکروفاژها را از M1 به M2 از طریق IL{14}} تحریک کنند تا تنگی شریان کلیوی را تسکین دهد [97].
در همان زمان، برخی از محققان پیشنهاد کردند که MSC-Exos تنها می تواند تا حدودی پیری کلیه های ناشی از تنگی شریان کلیوی را تسکین دهد [98]. متدها قادر به تغییر میزان بارگذاری miRNA بر روی EV ها، تنظیم مثبت miRNA مربوط به پیری در EVs، و حتی محدود کردن استفاده از EVs در درمان ترمیمی اگزوژن از طریق رونویسی غیرطبیعی هستند [99-101]. ژائو و همکاران دریافتند که ADMSCهای اتولوگ می توانند از طریق مطالعات مقایسه ای میکروسیرکولاسیون را بهتر حفظ کنند، در حالی که ADMSC-EV ها در حفظ دست نخوردگی نفروسیت ها و کاهش نکروز عملکرد بهتری دارند [102]. به طور خلاصه، ارزش کاربرد MSC-EVs در درمان ARVD همچنان مورد مناقشه است و تحقیقات بیشتر برای آشکار کردن اثربخشی آنها ضروری است.
MSC-EVs و پیوند کلیه
پیوند کلیه روش درمانی ارجح برای بیماران در مرحله پایانی نارسایی کلیه است. کمبود اندام های اهدا کننده و نیمه عمر پیوند، درمان را محدود می کند [4]. علاوه بر این، AKI ناشی از ایسکمی به طور گسترده در پیوند کلیه به دلیل زمان در دسترس برای ایجاد ایسکمی با توجه به تاخیر بین الحاق کلیه از اهداکننده به خونرسانی مجدد ایسکمی کلیه در گیرنده ها دیده می شود [103].
این نیز یکی از دلایل اصلی تاخیر در عملکرد پیوند است. برای حل این مشکلات، ذخیره سازی سرد استاتیک، پرفیوژن ماشین هیپوترمیک (HMP) و چندین داروی جدید که ایسکمی و خونرسانی مجدد را هدف قرار می دهند تحت مطالعه هستند [104]. کار دل ریو و همکاران. تایید کرد که HMP و پرفیوژن منطقه ای نرموترمیک نسبت به انبار سرد استاتیک ارجحیت دارند [105]. همچنین، محققان به یافتن راههای مؤثر دیگری برای تکمیل تکنیکهای کنونی اختصاص یافتهاند.
یک کارآزمایی شامل 105 فرد پیوند کلیه چینی که MSCهای اتولوگ را در جریان خون مجدد کلیه پیوندی دریافت کردند، نشان می دهد که استفاده از MSCها در پیوند کلیه امکان پذیر و بی خطر است [106]. با این حال، کارآزمایی مشابهی که اخیرا توسط تیم تحقیقاتی دیگری انجام شد، نشان داد که عوارض بعد از عمل پیوند کلیه، عوارض عفونی، عملکرد کلیه، دفعات پس زدن و زمان بقا، همگی تفاوتهای آماری را با کنترل در 1- نشان نمیدهند. پیگیری سال [107]. بنابراین، اثر محافظتی MSC-EVs در کلیه های پیوندی مورد بحث است. گرگورینی و همکاران ثابت کرد که افزودن MSCs/EVs به محلول بلزر در دوره HMP می تواند با حفظ مکانیسم آنزیمی ضروری برای زنده ماندن سلول، کلیه را از آسیب ایسکمیک محافظت کند [108]. آزمایشات کوچ و همکاران. نشان داد که MSC-EV ها واکنش ایمنی به پیوند کلیه آلوژنیک را تا حدی تنظیم می کنند [109]. Jose Ramirez-Bajo و همکاران، با ایجاد یک مدل موش پیوند کلیه هتروتوپیک به طور قابل توجهی متفاوت از این هستند. دریافتند که سلولهای بنیادی مزانشیمی اتولوگ زمان بقای پیوندها و افراد را در مدل رد کلیه موش طولانیتر میکنند، در حالی که EVs این کار را نمیکنند [110]. این موضوع به ندرت مورد مطالعه قرار می گیرد و قبل از نتیجه گیری به تحقیقات بیشتری نیاز است.
بدن سازی سیستانچ
مشکلات و چشم اندازها
در تحقیقات قبلی، سلول های بنیادی مزانشیمی نقش مثبتی در درمان بیماری های مختلف کلیوی ایفا می کنند. به عنوان مثال، MSC-CM گلومرولونفریت غشای پایه ضد گلومرولی آزمایشی را به واسطه عملکرد ضد التهابی ماکروفاژ M2 تسکین می دهد [111]. در لوپوس اریتماتوز سیستمیک (SLE)، پیوند MSC آلوژنیک آسیب کلیه را کاهش می دهد [112]. آزمایشات بالینی همچنین نشان می دهد که درمان بیماران SLE با سلول های بنیادی مزانشیمی آلوژنیک از اهداکنندگان سالم هم ایمن و هم امکان پذیر است [113]. در مدل سندرم نفروتیک ناشی از آدریامایسین، سلول های بنیادی مزانشیمی عمدتاً با تنظیم التهاب نقش خود را در ترمیم کلیه ایفا می کنند [114]. علاوه بر این، اهداکنندگان سالم و بیماران مبتلا به سندرم نفروتیک ایدیوپاتیک (INS) تفاوتهای آشکاری در عملکرد و مورفولوژی سلولهای بنیادی مزانشیمی نشان نمیدهند، که نشان میدهد سلولهای بنیادی مزانشیمی میتوانند برای درمان INS با سلولهای اتولوگ استفاده شوند [115]. درمان MSC با مکانیسم پاراکرین که تعادل سیتوکین Th1/Th2 را تعدیل می کند، اثرات مفیدی بر IgAN اعمال می کند [116]. در مدل موش گلومرولونفریت ناشی از ضد Thy1، سلول های بنیادی مزانشیمی پیش شرطی هیپوکسیک آپوپتوز گلومرولی، اتوفاژی و التهاب را از طریق انتقال سیگنال HIF1/VEGF/Nrf2 کاهش می دهند [117]. MSCها فشار خون کلیوی را تسکین می دهند و عملکرد کلیه را در مدل کلیپ 2-کلیه، 1- [118] بهبود می بخشند. هیچ عارضه جانبی و عوارض جانبی شدیدی از نظر بالینی هنگام درمان آنتی بادی در برابر واسکولیت مرتبط با آنتی بادی سیتوپلاسمی آنتی نوتروفیل [119] و بیماری کلیه پلی کیستیک اتوزومال غالب [120] با سلول های استرومایی مزانشیمی اتولوگ مشاهده نشد. تحقیقات موجود همچنین پیشنهاد میکند که سلولهای بنیادی مزانشیمی احتمالاً گلومرولوسکلروزیس سگمنتال کانونی را از طریق IL تسکین میدهند{26}} [121].
در نتیجه، هم مدلهای حیوانی و هم آزمایشهای بالینی شواهد زیادی از پتانسیل سلولهای بنیادی مزانشیمی در درمان بیماریهای کلیوی ارائه کردند. با این حال، تحقیقات کمی در مورد درمان بیماری های ذکر شده با MSC-EVs وجود دارد، که باید مورد بررسی قرار گیرد. این امکان پذیر است زیرا جداسازی، خالص سازی و تولید انبوه خودروهای برقی همچنان یک چالش است. علاوه بر این، مکانیسمی که توسط آن MSC-EVs بیماری های کلیوی را درمان می کنند، روشن نشده است. علاوه بر این، با در نظر گرفتن منبع بهینه، دوز مناسب، و مسیر مناسب تجویز EVs، تحقیقات بیشتری برای ارزیابی اثربخشی کاربرد MSC-EVs در درمان بالینی بیماریهای کلیوی باید انجام شود.
نتیجه
در این بررسی، ما پیشرفتهای اخیر در اثرات پیچیده و حیاتی MSC-EVs در بیماریهای کلیوی، از جمله AKI، CKD، DN، ARVD و پیوند کلیه را خلاصه کردیم. تعداد زیادی از مقالات تأیید میکنند که اکثر بیماریهای کلیوی میتوانند از MSC-EV بهره ببرند. با این حال، اثرات پیوند کلیه هنوز بحث برانگیز است. اگرچه MSC-EV های جدا شده از منابع مختلف به عنوان عوامل درمانی برای بیماری های کلیوی در مطالعات حیوانی و آزمایشات بالینی امیدوارکننده است، اما مطالعات بیشتری ضروری است زیرا در حال حاضر تنها چند کار بالینی شرح داده شده است.
اختصارات
سلول های بنیادی مزانشیمی: سلول های بنیادی مزانشیمی.
EVs: وزیکول های خارج سلولی.
MSC-EVs: EVs مشتق شده از MSC;
CKD: بیماری مزمن کلیه؛
DN: نفروپاتی دیابتی.
ARVD: بیماری رنواسکولار آترواسکلروتیک.
AKI: آسیب حاد کلیه.
BMMSCs: سلول های بنیادی مزانشیمی مشتق از مغز استخوان.
ADMSCs: مشتق از چربی
MSCs; HuMSCs: سلول های بنیادی مزانشیمی مشتق از بند ناف انسان.
mRNA: پیام رسان ریبوز نوکلئیک اسید.
miRNA: میکرو ریبوز نوکلئیک اسید.
MVs: میکرووزیکول ها.
Exos: Exosomes;
MVBs: اجسام چند وزیکولی.
RGD: آرژنین-گلیسین-آسپارتات؛
IRI: آسیب خونرسانی مجدد ایسکمیک.
I/R: ایسکمی خونرسانی مجدد.
CLP: بستن و سوراخ کردن سکوم.
hWJMSCs: سلول های بنیادی مزانشیمی ژله ای وارتون انسانی.
hWJMSCEVs: EV های مشتق شده از hWJMSCs.
TECs: سلول های اپیتلیال لوله ای.
ERK: کیناز تنظیم شده خارج سلولی.
UUO: انسداد یک طرفه حالب.
HLSC: سلول های بنیادی کبد انسان.
ARVD: بیماری رنواسکولار آترواسکلروتیک.
MetS: سندرم متابولیک. HMP:
پرفیوژن دستگاه هیپوترمیک؛
SLE: لوپوس اریتماتوز سیستمیک.
INS: سندرم نفروتیک ایدیوپاتیک
قدردانی
ما از بنیاد ملی علوم طبیعی چین (Grant No. 81970663) و بنیاد علوم طبیعی استان لیائونینگ (Grant No. 2019-BS-277) سپاسگزاریم.
مشارکت نویسندگان
لینا یانگ در طراحی مطالعه مشارکت داشت. Yuling Huang و Lina Yang جمع آوری داده ها را انجام دادند، داده ها را تجزیه و تحلیل کردند و مقاله را نوشتند. همه نویسندگان نسخه نهایی را خوانده و تایید کردند.
منابع مالی
این تحقیق توسط بنیاد ملی علوم طبیعی چین (Grant No. 81970663) و بنیاد علوم طبیعی استان لیائونینگ (Grant No. 2019-BS-277) پشتیبانی شد.
در دسترس بودن داده ها و مواد
مجموعه داده های مورد استفاده و تجزیه و تحلیل در تحقیق حاضر در صورت درخواست معقول از نویسنده مسئول در دسترس است.
اعلامیه ها
تایید اخلاق و رضایت برای شرکت
قابل اجرا نیست.
رضایت برای انتشار
قابل اجرا نیست.
منافع رقابتی
نویسندگان اعلام می کنند که هیچ منافع رقابتی ندارند.
دریافت: 4 ژانویه 2021 پذیرش: 15 مارس 2021
منابع
1. Fraser SDS، Roderick PJ. بیماری کلیوی در مطالعه بار جهانی بیماری 2017. Nat Rev Nephrol. 2019؛ 15 (4): 193-4. https://doi.org/10.1038/s41 581-019-0120-0.
2. Chade AR. عروق کوچک، نقش بزرگ: میکروسیرکولاسیون کلیه و پیشرفت آسیب کلیوی. فشار خون. 2017؛ 69 (4): 551-63. https://doi.org/10.1161/ HYPERTENSIONAHA.116.08319.
3. Kramer A, Pippias M, Noordzij M, Stel VS, Afentakis N, Ambuhl PM, et al. گزارش سالانه ثبت انجمن کلیه اروپا - انجمن دیالیز و پیوند اروپا (ERA-EDTA) 2015: خلاصه. Clin Kidney J. 2018; 11 (1): 108-22. https://doi.org/10.1093/ckj/sfx149.
4. باستانی ب. حال و آینده کمبود عضو پیوندی: برخی درمان های بالقوه. جی نفرول. 2020؛ 33 (2): 277-88. https://doi.org/10.1007/s4 0620-019-00634-x.
5. Squillaro T، Peluso G، Galderisi U. آزمایشات بالینی با سلول های بنیادی مزانشیمی: به روز رسانی. پیوند سلولی 2016؛ 25 (5): 829-48. https://doi.org/10.3727/0963 68915X689622.
6. عباس زاده حمید، قربانی ف. درخشانی محمد، موثق پور علی، یوسفی محمد. J Cell Physiol. 2020؛ 235 (2): 706-17. https://doi. org/10.1002/jcp.29004.
7. da Silva ML، Chagastelles PC، Nardi NB. سلول های بنیادی مزانشیمی تقریباً در تمام اندام ها و بافت های پس از زایمان قرار دارند. J Cell Sci. 2006؛ 119 (11): 2204-13.
8. Zuk PA، Zhu M، Mizuno H، Huang J، Futrell JW، Katz AJ، Benhaim P، Lorenz HP، Hedrick MH. سلول های چند خطی از بافت چربی انسان: پیامدهایی برای درمان های مبتنی بر سلول مهندس بافت 2001؛ 7 (2): 211-28. https://doi.org/10.1 089/107632701300062859.
9. Erices A، Conget P، Minguell JJ. سلول های پیش ساز مزانشیمی در خون بند ناف انسان برادر جی هماتول. 2000؛ 109 (1): 235-42. https://doi.org/10.1 046/j.1365-2141.2000.01986.x.
10. in't Anker PS، Scherjon SA، Kleijburg-van der Keur C، de Groot-Swings G، Claas FHJ، Fibbe WE، و همکاران. جداسازی سلول های بنیادی مزانشیمی با منشاء جنینی یا مادری از جفت انسان. سلولهای بنیادی. 2004؛ 22 (7): 1338-45.
11. Bharadwaj S، Liu G، Shi Y، Wu R، Yang B، He T، Fan Y، Lu X، Zhou X، Liu H، Atala A، Rohozinski J، Zhang Y. تمایز چند پتانسیل سلول های بنیادی مشتق شده از ادرار انسان پتانسیل برای کاربردهای درمانی در اورولوژی سلولهای بنیادی. 2013؛ 31 (9): 1840-56. https://doi.org/10.1002/stem.1424.
12. Caplan H، Olson SD، Kumar A، George M، Prabhakara KS، Wenzel P، Bedi S، Toledano-Furman NE، Triolo F، Kamhieh-Milz J، Moll G، Cox CS Jr. تحویل درمانی سلول های استرومایی مزانشیمی: انتقالی چالش های کاربرد بالینی جلو ایمونول. 2019؛ 10 https://doi.org/10.3389/fimmu.2 019.01645.
13. Sierra-Parraga JM، Merino A، Eijken M، Leuvenink H، Ploeg R، Moller BK، و همکاران. اثر ترمیمی سلول های استرومایی مزانشیمی بر سلول های اندوتلیال پس از آسیب هایپوکسیک و التهابی. سلول های بنیادی Res Ther. 2020؛ 11 (1): 352.
14. Rangel EB، Gomes SA، Kanashiro-Takeuchi R، Saltzman RG، Wei C، Ruiz P، Reiser J، Hare JM. سلول های پیش ساز/بنیادی c-kit(+) مشتق شده از کلیه به بازیابی پودوسیت در مدل پروتئینوری حاد کمک می کنند. Sci Rep. 2018; 8 (1): 14723. https://doi.org/10.1038/s{10}}x.
15. Hauger O، Frost EE، van Heeswijk R، Deminiere C، Xue R، Delmas Y، و همکاران. ارزیابی MR خانهسازی گلومرولی سلولهای بنیادی مزانشیمی نشاندار مغناطیسی در یک مدل موش نفروپاتی. رادیولوژی. 2006؛ 238 (1): 200-10. https://doi.org/10.1148/radiol.2381041668.
16. Ma H، Wu Y، Zhang W، Dai Y، Li F، Xu Y، Wang Y، Tu H، Li W، Zhang X. اثر سلول های استرومایی مزانشیمی بر نفروپاتی ناشی از دوکسوروبیسین در موش صحرایی. سیتوتراپی 2013؛ 15 (6): 703-11. https://doi.org/10.1016/j.jcyt.2013.02. 002.
17. Zhang K، Chen S، Sun H، Wang L، Li H، Zhao J، Zhang C، Li N، Guo Z، Han Z، Han ZC، Zheng G، Chen X، Li Z. میکروسکوپ دو فوتونی in vivo نقش سلول Sox9 پلاس را در بازسازی کلیه در مدل موش با درمان وزیکول خارج سلولی نشان می دهد. جی بیول شیمی. 2020؛ 295 (34): 12203-13. https://doi.org/10.1074/jbc.RA120.012732.
18. Ullah M, Liu DD, Thakor AS. خانه سازی سلول های استرومایی مزانشیمی: مکانیسم ها و استراتژی هایی برای بهبود علم. 2019؛ 15:421-38. https://doi.org/1 0.1016/j.isci.2019.05.004.
19. Hocking AM. نقش کموکاین ها در سلول های بنیادی مزانشیمی که به زخم ها منتقل می شوند. Adv مراقبت از زخم. 2015؛ 4 (11): 623-30. https://doi.org/10.1089/ زخم.2014.0579.
20. de Witte SFH، Luk F، Parraga JMS، Gargesha M، Merino A، Korevaar SS، و همکاران. تعدیل ایمنی توسط سلول های استرومایی مزانشیمی درمانی (MSC) از طریق فاگوسیتوز MSC توسط سلول های مونوسیتی تحریک می شود. سلولهای بنیادی. 2018؛ 36 (4): 602-15. https://doi.org/10.1002/stem.2779.
21. Schrepfer S، Deuse T، Reichenspurner H، Fischbein MP، Robbins RC، Pelletier MP. پیوند سلول های بنیادی: سد ریه پروسه پیوند 2007؛ 39 (2): 573-6. https://doi.org/10.1016/j.transproceed.2006.12.019.
22. Zhao L, Hu C, Han F, Wang J, Chen J. توانایی های بازسازی سلول های بنیادی مزانشیمی از طریق عمل به عنوان وسیله ای ایده آل برای تحویل اجزای درون سلولی در آسیب حاد کلیه. J Cell Mol Med. 2020؛ 24 (9): 4882-91. https://doi.org/1 0.1111/jcmm.15184.
23. He CJ، Zheng S، Luo Y، Wang B. ترانوستیک اگزوزوم: زیست شناسی و پزشکی ترجمه. ترانوستیک ها 2018؛ 8 (1): 237-55. https://doi.org/10.71 50/thno.21945.
24. Colombo M، Raposo G، Thery C. بیوژنز، ترشح، و تعاملات بین سلولی اگزوزوم ها و سایر وزیکول های خارج سلولی. Annu Rev Cell Dev Biol. 2014؛ 30 (1): 255-89. https://doi.org/10.1146/annurev-cellbio-101 512-122326.
25. Kalluri R، LeBleu VS. زیست شناسی، عملکرد و کاربردهای زیست پزشکی اگزوزوم ها. علوم پایه. 2020;367(6478):640.
26. Sonoda H، Lee BR، Park KH، Nihalani D، Yoon JH، Ikeda M، و همکاران. پروفایل miRNA اگزوزوم های ادراری برای ارزیابی پیشرفت آسیب حاد کلیه. Sci Rep. 2019; 9
27. Castellani C، Burrello J، Fedrigo M، Burrello A، Bolis S، Di Silvestre D، و همکاران. وزیکول های خارج سلولی در گردش به عنوان بیومارکر غیر تهاجمی رد در پیوند قلب J پیوند ریه قلب. 2020؛ 39 (10): 1136-48. https://doi. org/10.1016/j.healun.2020.06.011.
28. Zou X، Kwon SH، Jiang K، Ferguson CM، Puranik AS، Zhu X، Lerman LO. سلول های لوله مانند پراکنده کلیوی اثرات محافظتی در کلیه موش تنگی ایجاد می کنند که با انتشار وزیکول های خارج سلولی انجام می شود. Sci Rep. 2018; 8 (1): 1263. https://doi.org/10.1038/s41598-018-19750-y.
29. Dominguez JM II، Dominguez JH، Xie D، Kelly KJ. میکرووزیکول های خارج سلولی انسان از لوله های کلیوی آسیب ایسکمی-پرفیوژن مجدد کلیه را در موش ها معکوس می کند. PLoS One. 2018؛ 13 (8)
30. Ranghino A، Bruno S، Bussolati B، Moggio A، Dimuccio V، Tapparo M، Biancone L، Gontero P، Frea B، Camussi G. اثرات پیش سازهای کلیوی گلومرولی و لوله ای و وزیکول های خارج سلولی مشتق شده بر بهبودی از آسیب حاد کلیه . سلول های بنیادی Res Ther. 2017؛ 8 (1): 24. https://doi.org/10.1186/ s13287-017-0478-5. 31. De Chiara L، Famulari ES، Fagoonee S، van Daalen SKM، Buttiglieri S، Revelli A، و همکاران. خصوصیات سلول های بنیادی مزانشیم انسانی جدا شده از بیضه سلول های بنیادی بین المللی 2018؛ 2018: 1-9. https://doi.org/10.1155/2018/{16}}.
32. Grange C، Papadimitriou E، Dimuccio V، Pastorino C، Molina J، O'Kelly R، و همکاران. وزیکول های خارج سلولی ادراری حامل Klotho بهبود عملکرد کلیه را در مدل آسیب حاد لوله ای بهبود می بخشد. Mol Ther. 2020؛ 28 (2): 490- 502. https://doi.org/10.1016/j.ymthe.2019.11.013.
33. گارسیا-مانریکه پی، ماتوس ام، گوتیرز جی، پازوس سی، کارمن بی-ال.ام. بیومواد درمانی بر اساس وزیکول های خارج سلولی: طبقه بندی مهندسی زیستی و مسیرهای آماده سازی تقلیدی J وزیکول های خارج سلولی. 2018; 7 (1)
34. Baek G، Choi H، Kim Y، Lee HC، Choi C. وزیکول های خارج سلولی مشتق از سلول های بنیادی مزانشیمی به عنوان درمان و به عنوان یک پلت فرم تحویل دارو. سلول های بنیادی Transl Med. 2019؛ 8 (9): 880-6. https://doi.org/10.1002/sctm.{10}}.
35. Ha D، Yang N، Nadithe V. اگزوزوم ها به عنوان حامل های دارویی درمانی و وسایل انتقال در سراسر غشاهای بیولوژیکی: دیدگاه های فعلی و چالش های آینده. Acta Pharm Sin B. 2016؛ 6 (4): 287-96. https://doi.org/10.101 6/j.apsb.2016.02.001.
36. Melzer C, Rehn V, Yang Y, Bahre H, von der Ohe J, Hass R. اگزوزوم های مشتق شده از MSC با تاکسول یک وسیله درمانی برای هدف قرار دادن سرطان سینه متاستاتیک و سایر سلول های سرطانی فراهم می کنند. سرطان ها 2019؛ 11 (6)
37. Tang TT، Wang B، Lv LL، Liu BC. نانودرمانهای مبتنی بر وزیکول خارج سلولی: مرزهای نوظهور در درمان ضد التهابی ترانوستیک ها 2020؛ 10 (18): 8111-29. https://doi.org/10.7150/thno.47865.
38. Mathieu M, Martin-Jaular L, Lavieu G, Thery C. ویژگی های ترشح و جذب اگزوزوم ها و سایر وزیکول های خارج سلولی برای ارتباط سلول به سلول. Nat Cell Biol. 2019؛ 21 (1): 9–17. https://doi.org/10.1038/s{11}}.
39. Liu Y، Cui J، Wang H، Hezam K، Zhao X، Huang H، و همکاران. بهبود اثرات درمانی وزیکول های خارج سلولی مشتق از MSC با ماتریکس کلاژن تزریقی برای درمان تجربی آسیب حاد کلیه. سلول های بنیادی Res Ther. 2020؛ 11 (1)
40. Zhou Y، Liu S، Zhao M، Wang C، Li L، Yuan Y، Li L، Liao G، Bresette W، Zhang J، Chen Y، Cheng J، Lu Y، Liu J. خود آزاد شده از وزیکول خارج سلولی تزریقی مونتاژ هیدروژل نانوفیبر پپتیدی به عنوان یک درمان بدون سلول پیشرفته برای بازسازی بافت J کنترل انتشار. 2019؛ 316:93-104. https://doi.org/10.1 016/j.jconrel.2019.11.003.
41. ژانگ سی، شانگ ای، چن ایکس، میدگلی ای سی، وانگ زی، ژو دی، وو جی، چن پی، وو ال، وانگ ایکس، ژانگ ک، وانگ اچ، کونگ دی، یانگ زی، لی زی، چن ایکس. نانوالیاف فوق مولکولی حاوی پپتیدهای آرژنین-گلیسین-آسپارتات (RGD) کارایی درمانی وزیکول های خارج سلولی را در ترمیم کلیه افزایش می دهد. نانو ACS. 2{10}}20;14(9):12133-47. https://doi.org/10.1021/acsnano.0c05681.
42. Zhang ZY، Hou YP، Zou XY، Xing XY، Ju GQ، Zhong L، Sun J. Oct{6}} اثرات درمانی وزیکول های خارج سلولی مشتق از سلول های بنیادی مزانشیمی را در آسیب حاد کلیه افزایش دادند. کليه پرس خون Res. 2020; 45 (1): 95-108. https://doi.org/10.1159/000504368.
43. Collino F، Lopes JA، Correa S، Abdelhay E، Takiya CM، Wendt CHC، و همکاران. سلول های استرومایی مزانشیمی مشتق از چربی تحت هیپوکسی: تغییرات در ترشح وزیکول های خارج سلولی و بهبود بهبود کلیه پس از آسیب ایسکمیک. سلول فیزیول بیوشیمی. 2019؛ 52 (6): 1463-83.
44. Wang Y, Lu X, He J, Zhao W. تأثیر اریتروپویتین بر میکرووزیکول های مشتق شده از سلول های بنیادی مزانشیمی که از عملکرد کلیوی بیماری مزمن کلیه محافظت می کند. سلول های بنیادی Res Ther. 2015؛ 6 (1): 100. https://doi.org/10.1186/ s13287-015-0095-0.
45. Hoste EAJ، Kellum JA، Selby NM، Zarbock A، Palevsky PM، Bagshaw SM، Goldstein SL، Cerdá J، Chawla LS. اپیدمیولوژی جهانی و پیامدهای آسیب حاد کلیه نات ریو نفرول. 2018؛ 14 (10): 607-25. https://doi.org/10.1038/s41 581-018-0052-0.
46. Bai M، Zhang L، Fu B، Bai J، Zhang Y، Cai G، Bai X، Feng Z، Sun S، Chen X. IL{1}}A کارایی سلول های بنیادی مزانشیمی را در خونرسانی مجدد ایسکمیک بهبود می بخشد. آسیب کلیوی با افزایش درصد Treg توسط مسیر COX-2/PGE2. کلیه های داخلی 2018؛ 93 (4): 814-25. https://doi.org/10.1016/j.kint.2017.08.030.
47. زو ایکس، جیانگ کی، پورانیک AS، جردن کی ال، تانگ اچ، ژو ایکس، لرمان لو. هدف قرار دادن سلول های بنیادی مزانشیمی موش به مولکول آسیب کلیه{1}} کارایی درمانی آنها را در آسیب مزمن ایسکمیک کلیه بهبود می بخشد. سلول های بنیادی Transl Med. 2018؛ 7 (5): 394-403. https://doi.org/10.1002/sctm.17-0186.
48. Ullah M, Liu DD, Rai S, Razavi M, Choi J, Wang J, et al. یک رویکرد جدید برای رساندن وزیکول های خارج سلولی درمانی به طور مستقیم به کلیه موش از طریق خون شریانی آن. سلول ها. 9 (4) 2020
49. Zou X، Gu D، Xing X، Cheng Z، Gong D، Zhang G، Zhu Y. وزیکول های خارج سلولی مشتق از سلول های استرومایی مزانشیمی انسان آسیب خونرسانی مجدد ایسکمیک کلیوی را کاهش می دهند و رگزایی را در موش ها افزایش می دهند. Am J Transl Res. 2016؛ 8 (10): 4289-99.
50. Li L، Wang R، Jia Y، Rong R، Xu M، Zhu T. اگزوزوم های مشتق شده از سلول های بنیادی مزانشیمی از طریق مهار التهاب و آپوپتوز سلولی، آسیب ایسکمیک-پرفیوژن مجدد کلیه را بهبود می بخشد. فرانت مد. 2019؛ 6 https://doi.org/10.3389/fmed.2019.00269.
51. Cao H، Cheng Y، Gao H، Zhuang J، Zhang W، Bian Q، Wang F، du Y، Li Z، Kong D، Ding D، Wang Y. ردیابی in vivo وزیکول های خارج سلولی مشتق از سلول های بنیادی مزانشیمی در حال بهبود میتوکندری! عملکرد در آسیب خونرسانی مجدد ایسکمی کلیوی. نانو ACS. 2020؛ 14 (4): 4014-26. https://doi.org/10.1021/a csnano.9b08207.
52. Zhou Y، Xu H، Xu W، Wang B، Wu H، Tao Y، Zhang B، Wang M، Mao F، Yan Y، Gao S، Gu H، Zhu W، Qian H. اگزوزوم های آزاد شده توسط بند ناف انسان سلول های بنیادی مزانشیمی در برابر استرس اکسیداتیو کلیه ناشی از سیس پلاتین و آپوپتوز در داخل بدن و در شرایط آزمایشگاهی محافظت می کنند. سلول های بنیادی Res Ther. 2013؛ 4 (2): 34. https://doi.org/10.1186/scrt194.
53. de Almeida DC، Bassi EJ، Azevedo H، Anderson L، Taemi Origassa CS، Cenedeze MA، و همکاران. یک شبکه تنظیمکننده miRNA-mRNA با ترمیم بافت ناشی از سلولهای استرومایی مزانشیمی در آسیب حاد کلیه مرتبط است. جلو ایمونول. 2017؛ 7 https://doi.org/10.3389/fimmu.2016. 00645.
54. Tapparo M، Bruno S، Collino F، Togliatto G، Deregibus MC، Provero P، و همکاران. پتانسیل بازسازی کلیوی وزیکول های خارج سلولی مشتق شده از سلول های استرومایی مزانشیمی مهندسی شده miRNA. Int J Mol Sci. 2019; 20 (10)
55. Zou X، Zhang G، Cheng Z، Yin D، Du T، Ju G، و همکاران. میکرووزیکولهای مشتقشده از سلولهای استرومایی مزانشیمی ژله وارتون انسانی با سرکوب CX3CL1 آسیب ایسکمی-پرفیوژن مجدد کلیه را در موشها بهبود میبخشند. سلول های بنیادی Res Ther. 2014؛ 5 (2): 40. https://doi.org/10.1186/scrt428.
56. Shen B, Liu J, Zhang F, Wang Y, Qin Y, Zhou Z, Qiu J, Fan Y. اگزوزوم CCR2 مثبت منتشر شده توسط سلول های بنیادی مزانشیمی عملکرد ماکروفاژها را سرکوب می کند و آسیب کلیوی ناشی از ایسکمی/پرفیوژن مجدد را کاهش می دهد. سلول های بنیادی بین المللی 2016؛ 2016: 1-9. https://doi.org/10.1155/2016/1240301.
57. Gu D, Zou X, Ju G, Zhang G, Bao E, Zhu Y. سلولهای استرومایی مزانشیمی مشتق از وزیکولهای خارج سلولی آسیب خونرسانی مجدد ایسکمی کلیوی حاد را با مهار شکافت میتوکندری از طریق miR بهبود میدهند-30. سلول های بنیادی بین المللی 2016؛ 2016: 1-12. https://doi.org/10.1155/2016/2093940.
58. Bruno S، Grange C، Collino F، Deregibus MC، Cantaluppi V، Biancone L، و همکاران. میکرووزیکول های مشتق شده از سلول های بنیادی مزانشیمی بقا را در مدل کشنده آسیب حاد کلیه افزایش می دهد. PLoS One. 2012؛ 7 (3)
59. Wang B، Jia H، Zhang B، Wang J، Ji C، Zhu X، Yan Y، Yin L، Yu J، Qian H، Xu W. قبل از جوجه کشی با اگزوزوم hucMSC از سمیت کلیوی ناشی از سیس پلاتین با فعال کردن اتوفاژی جلوگیری می کند. . سلول های بنیادی Res Ther. 2017؛ 8 (1): 75. https://doi.org/10.1186/s{10}}.
60. جیا اچ، لیو دبلیو، ژانگ بی، وانگ جی، وو پی، تاندرا ن، لیانگ زی، جی سی، یین ال، هو ایکس، یان یی، مائو اف، ژانگ ایکس، یو جی، زو دبلیو، کیان اچ. اگزوزوم HucMSC تحویل 14-3-3 زتا اتوفاژی افزایش یافته از طریق مدولاسیون ATG16L در جلوگیری از آسیب حاد کلیه ناشی از سیس پلاتین. Am J Transl Res. 2018؛ 10 (1): 101-13.
61. Wang J، Jia H، Zhang B، Yin L، Mao F، Yu J، Ji C، Xu X، Yan Y، Xu W، Qian H. HucMSC اگزوزوم منتقل شده 14-3-3 زتا از آسیب سیس پلاتین جلوگیری می کند. به سلول های HK-2 با القای اتوفاژی در شرایط آزمایشگاهی. سیتوتراپی 2018؛ 20 (1): 29-44. https://doi.org/10.1016/j.jcyt.2017.08.002.
62. Ullah M, Liu DD, Rai S, Concepcion W, Thakor AS. سرکوب التهابی NLRP3 با واسطه HSP، زمینه ساز برگشت آسیب حاد کلیه به دنبال وزیکول خارج سلولی و درمان ترکیبی اولتراسوند متمرکز است. Int J Mol Sci. 2020; 21 (11)
63. برونو اس، تاپارو ام، کولینو اف، چیابوتو جی، درگیباس MC، لیندوسو RS، و همکاران. پتانسیل بازسازی کلیوی جمعیت های مختلف وزیکول خارج سلولی مشتق شده از سلول های استرومایی مزانشیمی مغز استخوان. Tissue Eng A. 2017; 23 (21-22): 1262-73. https://doi.org/10.1089/ten.tea.2017.0069.
64. Zhang R، Zhu Y، Li Y، Liu W، Yin L، Yin S، Ji C، Hu Y، Wang Q، Zhou X، Chen J، Xu W، Qian H. اگزوزوم های سلول های بنیادی مزانشیمی بند ناف انسان سپسیس را کاهش می دهند. آسیب حاد کلیه مرتبط از طریق تنظیم بیان microRNA-146b. بیوتکنول لت. 2020؛ 42 (4): 669-79. https://doi.org/10.1007/s{10}}.
65. Gao F, Zuo B, Wang Y, Li S, Yang J, Sun D. عملکرد محافظتی اگزوزوم ها از سلول های بنیادی مزانشیمی مشتق از بافت چربی در آسیب حاد کلیه از طریق مسیر SIRT1. زندگی علمی. 2020؛ 255:117719. https://doi.org/10.1016/j. lfs.2020.117719.
66. Bassegoda O، Huelin P، Ariza X، Sole C، Juanola A، Gratacos-Gines J، و همکاران. ایجاد بیماری مزمن کلیه پس از آسیب حاد کلیه در بیماران مبتلا به سیروز شایع است و نتایج بالینی را مختل می کند. جی هپاتول. 2020; 72 (6): 1132-9. https://doi.org/10.1016/j.jhep.2019.12.020.
67. به EJ، Jayasinghe K، Glassford N، Bailey M، Johnson DW، Polkinghorne KR، Toussaint ND، Bellomo R مراجعه کنید. تعاریف قرار گرفتن در معرض کلیه های داخلی 2019؛ 95 (1): 160-72. https://doi. org/10.1016/j.kint.2018.08.036.
68. Yoon YM، Lee JH، Song KH، Noh H، Lee SH. اگزوزومهای تحریکشده با ملاتونین، پتانسیل بازسازی سلولهای بنیادی/ استرومایی مزانشیمی ناشی از بیماری مزمن کلیه را از طریق پروتئینهای پریون سلولی افزایش میدهند. J Pineal Res. 2020; 68 (3)
69. صابری ک، پاسبخش پ، امیدی ع، برهانی حقیقی م، نکونام، امیدی ن، قاسمی س، کاشانی امام رضا. پیش شرطی سازی ملاتونین سلول های بنیادی مزانشیمی مشتق از مغز استخوان، پیوند آنها را تقویت می کند و بازسازی کلیه را در مدل موش بیماری مزمن کلیوی بهبود می بخشد. جی مول هیستول. 2019; 50 (2): 129-40. https://doi.org/10.1007/s{10}}.
70. مخلوف ع، شکرچیان س.، مقدسعلی ر.، عین اللهی ب، دستغیب محمد، جانبابایی گل، حسینی س. مطالعه ایمنی با 18 ماه پیگیری. سیتوتراپی 2018؛ 20 (5): 660-9. https://doi.org/10.1016/j.jcyt.2018.02.368.
71. Liu B، Ding FX، Liu Y، Xiong G، Lin T، He DW، Zhang YY، Zhang DY، Wei GH. سلولهای بنیادی مزانشیمی مشتق از بند ناف انسانی محیطی را که دارای محیطی شرطیشده هستند، فیبروز بینابینی را تضعیف میکنند و ترمیم سلولهای اپیتلیال لولهای را در مدلی غیرقابل برگشت از انسداد یک طرفه حالب تحریک میکنند. نفرولوژی. 2018؛ 23 (8): 728-36. https://doi.org/10.1111/nep.13099.
72. Ramirez-Bajo MJ، Martin-Ramirez J، Bruno S، Pasquino C، Banon-Maneus E، Rovira J، و همکاران. پتانسیل محافظتی نفرو سلول های استرومایی مزانشیمی و وزیکول های خارج سلولی آنها در مدل موشی سمیت مزمن نفروتوکسی سیکلوسپورین. Front Cell Dev Biol. 2020؛ 8
73. Kholia S, Herrera Sanchez MB, Cedrino M, Papadimitriou E, Tapparo M, Deregibus MC, et al. وزیکول های خارج سلولی مشتق از سلول های بنیادی مزانشیمی آسیب کلیه را در نفروپاتی اسید آریستولوکیک بهبود می بخشد. Front Cell Dev Biol. 2020؛ 8:188.
74. Wang B، Yao K، Huuskes BM، Shen HH، Zhuang J، Godson C، Brennan EP، Wilkinson-Berka JL، Wise AF، Ricardo SD. سلول های بنیادی مزانشیمی microRNA-let7c اگزوژن را از طریق اگزوزوم ها برای تضعیف فیبروز کلیه تحویل می دهند. Mol Ther. 2016؛ 24 (7): 1290-301. https://doi.org/10.1038/mt.2016.90.
75. Zhang L، Zhu XY، Zhao Y، Eirin A، Liu L، Ferguson CM، و همکاران. تحویل انتخابی داخل کلیوی وزیکول های خارج سلولی مشتق از سلول های بنیادی مزانشیمی آسیب میوکارد را در بیماری رنواسکولار متابولیک تجربی کاهش می دهد. Basic Res Cardiol. 2020; 115 (2)
76. Chen L, Wang Y, Li S, Zuo B, Zhang X, Wang F, Sun D. اگزوزوم های مشتق شده از سلول های بنیادی مزانشیمی چربی انسانی اصلاح شده با GDNF با فعال کردن مسیر سیگنالینگ SIRT1/eNOS از دست دادن مویرگی اطراف لوله را در فیبروز بینابینی توبولی بهبود می بخشد. ترانوستیک ها 2020؛ 10 (20): 9425-42. https://doi. org/10.7150/thno.43315.
77. Zhu F، Shin OLSCL، Pei G، Hu Z، Yang J، Zhu H، و همکاران. سلول های بنیادی مزانشیمی مشتق از چربی از اگزوزوم ها برای کاهش انتقال AKI-CKD از طریق فعال سازی Sox9 وابسته به سلول های اپیتلیال لوله ای استفاده کردند. انکوتارگت. 2017؛ 8 (41): 70707-26. https://doi.org/10.18632/oncotarget.{11}}.
78. Packham DK، Fraser IR، Kerr PG، Segal KR. سلول های پیش ساز مزانشیمی آلوژنیک (MPC) در نفروپاتی دیابتی: یک مطالعه تصادفی، کنترل شده با دارونما، افزایش دوز. ابی پزشکی. 2016؛ 12:263-9. https://doi. org/10.1016/j.ebiom.2016.09.011.
79. Nagaishi K, Mizue Y, Chikenji T, Otani M, Nakano M, Saijo Y, Tsuchida H, Ishioka S, Nishikawa A, Saito T, Fujimiya M. عصاره های بند ناف ناهنجاری های دیابتی را در سلول های بنیادی مزانشیمی مشتق از مغز استخوان بهبود می بخشد. اثرات درمانی خود را بر نفروپاتی دیابتی افزایش دهند. Sci Rep. 2017; 7 (1): 8484. https://doi.org/10.1038/s41598-017-08921-y.
80. Li Y، Liu J، Liao G، Zhang J، Chen Y، Li L، Li L، Liu F، Chen B، Guo G، Wang C، Yang L، Cheng J، Lu Y. مداخله اولیه با سلول های بنیادی مزانشیمی با بهبود ریزمحیط التهابی از نفروپاتی در موش های دیابتی جلوگیری می کند. Int J Mol Med. 2018؛ 41 (5): 2629-39. https://doi.org/10.3 892/ijmm.2018.3501.
81. Liu Q، Lv S، Liu J، Liu S، Wang Y، Liu G. سلول های بنیادی مزانشیمی اصلاح شده با آنزیم مبدل آنژیوتانسین 2 برای بهبود فیبروز گلومرولی در نفروپاتی دیابتی برتر هستند. Diabetes Res Clin Pract. 2020; 162:108093. https://doi.org/10.1016/j.diabres.2020.108093.
82. Gallo S, Gili M, Lombardo G, Rossetti A, Rosso A, Dentelli P, et al. وزیکولهای خارج سلولی مشتق از سلولهای بنیادی و حامل microRNA: رویکردی جدید برای تداخل با تولید کلاژن سلولهای مزانژیال در یک محیط هیپرگلیسمی. PLoS One. 2016؛ 11 (9)
83. Duan YR، Chen BP، Chen F، Yang SX، Zhu CY، Ma YL، Li Y، Shi J. microRNA اگزوزومی{6}}p از سلولهای بنیادی مشتق شده از ادرار انسان، نفروپاتی دیابتی را از طریق محافظت از پودوسیت بهبود میبخشد. J Cell Mol Med. 2019; https://doi.org/10.1111/jcmm.14558.
84. Duan Y، Luo Q، Wang Y، Ma Y، Chen F، Zhu X، Shi J. وزیکول های خارج سلولی مشتق از سلول های بنیادی مزانشیمی چربی حاوی microRNA-26a-5p هدف TLR4 و محافظت در برابر نفروپاتی دیابتی جی بیول شیمی. 2020؛ 295 (37): 12868-84. https://doi.org/10.1074/jbc.RA120.012522.
85. Zhong L، Liao G، Wang X، Li L، Zhang J، Chen Y، Liu J، Liu S، Wei L، Zhang W، Lu Y. سلول های بنیادی مزانشیمی-میکرووزیکول-miR-451یک بهبود اولیه آسیب کلیه دیابتی با تنظیم منفی P15 و P19. Exp Biol Med. 2018؛ 243 (15–16): 1233–42. https://doi.org/10.1177/1535370218819726.
86. Grange C، Tritta S، Tapparo M، Cedrino M، Tetta C، Camussi G، Brizzi MF. وزیکولهای خارج سلولی مشتق از سلولهای بنیادی پیشرفت فیبروز را در یک مدل موش نفروپاتی دیابتی مهار و برمیگردانند. Sci Rep. 2019; 9 (1): 4468. https://doi.org/10.1038/s41598-019-41100-9.
87. Jin J, Wang Y, Zhao L, Zou W, Tan M, He Q. miRNA Exosomal-215-5p مشتق شده از سلول های بنیادی مشتق از چربی انتقال اپیتلیال-مزانشیمی پودوسیت ها را با مهار ZEB2 تضعیف می کند. Biomed Res Int. 2020؛ 2020: 1-14. https://doi.org/10.1155/2020/2685305.
88. ابراهیم ن، احمد IA، حسین NI، Dessouky AA، فرید ع، Elshazly AM، و همکاران. اگزوزوم های مشتق شده از سلول های بنیادی مزانشیمی نفروپاتی دیابتی را با القای اتوفاژی از طریق مسیر سیگنالینگ mTOR بهبود بخشید. سلول ها. 2018؛ 7 (12)
89. Jin J، Shi Y، Gong J، Zhao L، Li Y، He Q، Huang H. اگزوزوم ترشح شده از سلول های بنیادی مشتق شده از چربی، نفروپاتی دیابتی را با ترویج شار اتوفاژی و مهار آپوپتوز در پودوسیت کاهش می دهد. سلول های بنیادی Res Ther. 2019؛ 10 (1): 95. https://doi.org/10.1186/s13287-019-1177-1.
90. Eirin A، Zhu XY، Ferguson CM، Riester SM، van Wijnen AJ، Lerman A، Lerman LO. تحویل داخل کلیوی سلول های بنیادی مزانشیمی آسیب میوکارد را پس از معکوس کردن فشار خون بالا در بیماری رنواسکولار خوک کاهش می دهد. سلول های بنیادی Res Ther. 2015؛ 6 (1): 7. https://doi.org/10.1186/scrt541.
91. Saad A, Dietz AB, Herrmann SMS, Hickson LJ, Glockner JF, McKusick MA, et al. سلول های بنیادی مزانشیمی اتولوگ باعث افزایش پرفیوژن قشر مغز در بیماری های عروقی می شوند. جی ام سوک نفرول. 2017؛ 28 (9): 2777-85. https://doi. org/10.1681/ASN.2017020151.
92. Abumoawad A, Saad A, Ferguson CM, Eirin A, Herrmann SM, Hickson LJ, et al. در یک کارآزمایی بالینی فزاینده فاز 1a، تزریق سلولهای بنیادی مزانشیمی اتولوگ برای بیماریهای عروقی، جریان خون و نرخ فیلتراسیون گلومرولی را افزایش میدهد و در عین حال نشانگرهای زیستی التهابی و فشار خون را کاهش میدهد. کلیه های داخلی 2020؛ 97 (4): 793-804. https://doi.org/10.1016/j. kint.2019.11.022.
93. Sivanathan KN، Coates PT. بهبود عملکرد کلیه انسان در بیماری های عروقی با سلول های بنیادی مزانشیمی کلیه های داخلی 2020; 97 (4): 655-6. https://doi.org/10.1016/j.kint.2019.12.020.
94. Eirin A، Zhu XY، Jonnada S، Lerman A، van Wijnen AJ، Lerman LO. وزیکولهای خارج سلولی مشتق از سلولهای بنیادی مزانشیمی، ریز عروق کلیوی را در بیماریهای متابولیک رنواسکولار در خوک بهبود میبخشند. پیوند سلولی 2018؛ 27 (7): 1080-95. https://doi.org/10.1177/0963689718780942.
95. Simeoni M، Borrelli S، Garofalo C، Fuiano G، Esposito C، Comi A، و همکاران. آترواسکلروتیک-نفروپاتی: مروری روایی به روز. جی نفرول. 2021; 34(1):125-36.
96. آهنگ T، Eirin A، Zhu X، Zhao Y، Krier JD، Tang H، Jordan KL، Woolard JR، Taner T، Lerman A، Lerman LO. وزیکول های خارج سلولی مشتق از سلول های بنیادی مزانشیمی سلول های T تنظیمی را برای بهبود آسیب مزمن کلیه القا می کنند. فشار خون. 2020؛ 75 (5): 1223-32. https://doi.org/10.1161/HYPERTENSIONA HA.119.14546.
97. Eirin A، Zhu XY، Puranik AS، Tang H، McGurren KA، van Wijnen AJ، و همکاران. وزیکول های خارج سلولی مشتق از سلول های بنیادی مزانشیمی التهاب کلیه را کاهش می دهند. کلیه های داخلی 2017؛ 92 (1): 114-24. https://doi.org/10.1016/j.kint.{10}}.12.023.
98. Kim SR، Zou X، Tang H، Puranik AS، Abumoawad AM، Zhu XY، و همکاران. افزایش پیری سلولی در کلیه تنگی موش و انسان: تأثیر سلولهای بنیادی مزانشیمی J Cell Physiol. 2021؛ 236 (2): 1332-44.
99. Eirin A, Ferguson CM, Zhu XY, Saadiq IM, Tang H, Lerman A, Lerman LO. وزیکول های خارج سلولی آزاد شده توسط سلول های استرومایی/بنیادی مزانشیمی مشتق از بافت چربی از خوک های چاق قادر به ترمیم کلیه آسیب دیده نیستند. سلول های بنیادی Res. 2020؛ 47:101877. https://doi.org/10.1016/j.scr.2020.101877.
100. Pawar AS، Eirin A، Tang H، Zhu XY، Lerman A، Lerman LO. رونوشت و پروتئوم فاکتور نکروز تومور-آلفا در سلولهای بنیادی مزانشیمی مشتق از بافت چربی خوکهای مبتلا به سندرم متابولیک تنظیمشده بالا. سیتوکین. 2020؛ 130:155080. https://doi.org/10.1016/j.cyto.2020.155080.
101. Li Y، Meng Y، Zhu X، Saadiq IM، Jordan KL، Eirin A، و همکاران. سندرم متابولیک میکرو RNA های مرتبط با پیری را در وزیکول های خارج سلولی مشتق شده از سلول های بنیادی/استرومایی مزانشیمی خوکی و انسان افزایش می دهد. سیگنال ارتباط سلولی 2020؛ 18 (1)
102. ژائو وای، ژو ایکس، ژانگ ال، فرگوسن سی ام، سونگ تی، جیانگ کی، کانلی اس ام، کریر جی دی، تانگ اچ، سعدیق آی، جردن کیال، لرمن آ، لرمان لو. سلولهای بنیادی/ استرومایی مزانشیمی و نتاج وزیکول خارج سلولی آنها از طریق مکانیسمهای مختلف باعث کاهش آسیب کلیه خوکی پس از تنگی میشوند. توسعه سلول های بنیادی 2020؛ 29 (18): 1190-200. https://doi.org/10.1089/scd.2020.0030.
103. Jain S، Plenter R، Nydam T، Jani A. مسیرهای آسیبی که منجر به AKI در مدل پیوند کلیه موش می شود. پیوند. 2020؛ 104 (9): 1832-41. https://doi.org/10.1097/TP.0000000000003127.
104. Wekerle T، Segev D، Lechler R، Oberbauer R. استراتژیهایی برای حفظ طولانیمدت عملکرد پیوند کلیه. لانست. 2017؛ 389 (10084): 2152-62. https://doi.org/10.1016/S0140-6736(17){11}}.
105. دل ریو اف، آندرس ا. پیوند کلیه از اهداکنندگان پس از مرگ کنترل نشده گردش خون: تجربه اسپانیایی کلیه های داخلی 2019؛ 95 (2): 420-8. https://doi.org/10.1016/j. kint.2018.09.014.
106. Tan J، Wu W، Xu X، Liao L، Zheng F، Messinger S، Sun X، Chen J، Yang S، Cai J، Gao X، Pileggi A، Ricordi C. درمان القایی با سلول های بنیادی مزانشیمی اتولوگ در زندگی پیوند کلیه مرتبط یک کارآزمایی تصادفی کنترل شده. جاما. 2012؛ 307 (11): 1169-77. https://doi.org/10.1001/jama.2 012.316.
107. Sun Q، Huang Z، Han F، Zhao M، Cao R، Zhao D، Hong L، Na N، Li H، Miao B، Hu J، Meng F، Peng Y، Sun Q. سلول های بنیادی مزانشیمی آلوژنیک به عنوان القا درمان در آلوگرافت کلیه ایمن و امکان پذیر است: نتایج آزمایشی یک کارآزمایی تصادفی کنترل شده چند مرکزی. J Transl Med. 2018؛ 16 (1): 52. https://doi.org/10.1186/s12967-018-1422-x.
108. گرگورینی ام، کورادتی وی، پاتونیری ای اف، روکا سی، میلانسی اس، پلوسو آ، کانواری اس، د سکو ال، دوگو ام، آوانزینی MA، مانتلی ام، ماستری ام، اسپوزیتو پی، برونو اس، لیبتا سی، دال کانتون A، Rampino T. پرفیوژن کلیه جدا شده موش با سلول های استرومایی مزانشیمی/وزیکول های خارج سلولی از آسیب ایسکمیک جلوگیری می کند. J Cell Mol Med. 2017؛ 21 (12): 3381-93. https://doi. org/10.1111/jcmm.13249.
109. Koch M, Lemke A, Lange C. وزیکول های خارج سلولی از MSC پاسخ ایمنی به آلوگرافت های کلیوی را در یک مدل موش متفاوت MHC تعدیل می کنند. سلول های بنیادی بین المللی 2015؛ 2015: 1-7. https://doi.org/10.1155/2015/486141.
110. خوزه رامیرز-باجو ام، روویرا جی، لازو-رودریگز ام، بانون-مانئوس ای، توبیتا وی، مویا-رول دی، و همکاران. تاثیر سلول های استرومایی مزانشیمی و وزیکول های خارج سلولی آنها در مدل رد کلیه موش صحرایی Front Cell Dev Biol. 2020؛ 8
111. Iseri K, Iyoda M, Ohtaki H, Matsumoto K, Wada Y, Suzuki T, Yamamoto Y, Saito T, Hihara K, Tachibana S, Honda K, Shibata T. اثرات درمانی و مکانیسم محیط های شرطی شده از سلول های بنیادی مزانشیمی انسان در مورد گلومرولونفریت ضد GBM در موش WKY Am J Physioly Renal Physiol. 2016; 310(11):F1182–F91. https://doi.org/10.1152/ajprenal.00165.2016.
112. Cheng RJ، Xiong AJ، Li YH، Pan SY، Zhang QP، Zhao Y، Liu Y، Marion TN. سلول های بنیادی مزانشیمی: سلول های بنیادی مزانشیمی آلوژنیک ممکن است سرکوبگر سیستم ایمنی باشند اما MSC های اتولوگ در بیماران لوپوس ناکارآمد هستند. Front Cell Dev Biol. 2019؛ 7 https://doi.org/10.3389/fcell.2019.00285.
113. Barbado J, Tabera S, Sanchez A, Garcia-Sancho J. پتانسیل درمانی پیوند سلولهای استرومایی مزانشیمی آلوژنیک برای نفریت لوپوس. لوپوس. 2018؛ 27 (13): 2161-5. https://doi.org/10.1177/0961203318804922.
114. Kim HS، Lee JS، Lee HK، Park EJ، Jeon HW، Kang YJ، و همکاران. سلول های بنیادی مزانشیمی التهاب کلیه را در نفروپاتی ناشی از آدریامایسین بهبود می بخشد. شبکه ایمنی 2019؛ 19 (5)
115. Starc N, Li M, Algeri M, Conforti A, Tomao L, Pitisci A, Emma F, Montini G, Messa P, Locatelli F, Bernardo ME, Vivarelli M. خصوصیات فنوتیپی و عملکردی سلولهای استرومایی مزانشیمی جدا شده از بیماران اطفال با سندرم نفروتیک ایدیوپاتیک شدید. سیتوتراپی 2018; 20 (3): 322-34. https://doi.org/10.1016/j.jcyt.2017.12.001.
116. Hyun YY، Kim IO، Kim MH، Nam DH، Lee MH، Kim JE، Song HK، Cha JJ، Kang YS، Lee JE، Kim HW، Han JY، Cha DR. سلول های بنیادی مشتق شده از چربی عملکرد کلیه را در مدل موش نفروپاتی IgA بهبود می بخشد. پیوند سلولی 2012; 21 (11): 2425-39. https://doi.org/10.3727/096368912X639008.
117. Chang HH، Hsu SP، Chien CT. پیوند داخل کلیوی سلول های بنیادی مزانشیمی پیش شرطی هیپوکسیک، گلومرولونفریت را از طریق آنتی اکسیداسیون، استرس ضد ER، ضد التهاب، ضد آپوپتوز و ضد اتوفاژی بهبود می بخشد. آنتی اکسیدان ها 2020؛ 9 (1)
118. Varela VA، Oliveira-Sales EB، Maquigussa E، Borges FT، Gattai PP، Novaes ADS، و همکاران. درمان با سلول های بنیادی مزانشیمی باعث بهبود فشار خون عروقی می شود و توانایی کلیه طرف مقابل برای دفع سدیم را حفظ می کند. کليه پرس خون Res. 2019؛ 44 (6): 1404-15. https://doi.org/10.1159/ 000503346.
119. Gregorini M، Maccario R، Avanzini MA، Corradetti V، Moretta A، Libetta C، Esposito P، Bosio F، Dal Canton A، Rampino T. واسکولیت کلیوی مرتبط با آنتی بادی سیتوپلاسمی آنتی نوتروفیل درمان شده با ارزیابی اتولوگ مزانشیمی سلول های استرومایی: سهم مکانیسم های با واسطه ایمنی Mayo Clin Proc. 2013؛ 88 (10): 1174-9. https://doi.org/10.1016/j. mayocp.2013.06.021.
120. مخلوق ع، شکرچیان س.، مقدسعلی ر.، عین اللهی ب، حسینی س.، جروقی ن، بلوریه، بهاروند، حسین، اقدمی ن. ایمنی و تحمل سلول های استرومایی مزانشیمی مغز استخوان اتولوگ در بیماران ADPKD. سلول های بنیادی Res Ther. 2017؛ 8 (1): 116. https://doi.org/10.1186/s13287-017-0557-7.
121. Shi Y, Xie J, Yang M, Ma J, Ren H. پیوند سلول های بنیادی مزانشیمی بند ناف به موش های مبتلا به گلومرولواسکلروز سگمنتال کانونی تظاهرات بیماری را به تاخیر انداخت. Ann Transl Med. 2019؛ 7 (16)


