متیل جاسمونات واکنشهای متمایز تانن، فاونوئید و فیتواکسی لیپین قابل هیدرولیز را در برگ انار (Punica Granatum L.) ایجاد میکند.
Mar 18, 2022
لطفا تماس بگیریدoscar.xiao@wecistanche.comبرای اطلاعات بیشتر
لیپیدها در برگ های انار تیمار شده با MeJA به اسیدهای چرب آزاد و فیتواکسی لیپین تبدیل شدند.
علاوه بر فلاونوئیدها و آنتوسیانینها، تغییرات در مولکولهای لیپید نیز در برگهای انار در 72- ساعت پس از القای MeJA مشهود بود (شکل 5a). از 102 متابولیت متفاوت انباشته شده، 23 لیپید، اسیدهای چرب یا فیتواکسی لیپین بودند (جدول S6). بر خلاف مونوآسیل گلیسرول (MAG) (18:4) ایزومر 1 که تجمع افزایش یافته، هفت گلیسرولیپید، از جمله MAG (18): 1)ایزومر، MAG (18:3)ایزومر4،گالاکتوزیلمونوآسیل گلیسرول (DGMG) (18:2)ایزومر،DGMG(18:2)ایزومر2،DGMG(18:2)ایزومر3،مونوگالاکتوزیلایزومرهای مونوآسیل گلیسرول (MGMG) (18:2) و ایزومر2 MGMG(18:2) با اعمال MeJA به برگها 3-5 برابر کاهش یافتند (شکل 5a؛ جدول S6). فسفولیپیدها LysoPC 18: 0 و 18:1 افزایش بیش از دو برابری در برگهای تیمار شده با MeJA نشان دادند (جدول S6).

لطفا برای دانستن بیشتر اینجا کلیک کنید
کاربرد MeJA اگزوژن سطوح JA و ایزولوسین (JA-Ile) را به ترتیب 4.{2}} برابر و 2.{4}} برابر در برگهای انار افزایش داد (جدول S6). مختلف غیر JAفیتواکسی لیپین هااز جمله هیدروپراکسیدهای اسیدهای چرب، اسیدهای چرب اپوکسی، اسیدهای چرب هیدروکسی، اسیدهای چرب کتو واستیلنیکاسیدهای چرب، به طور قابل توجهی در برگهای تیمار شده با MeJA افزایش یافته است (شکل 5a؛ جدول S6). افزایش تجمع اسید پونیسیک، یک PUFA (18:3) که در روغن هسته انار فراوان است، در برگهای تیمار شده با MeJA نیز مشاهده شد (جدول S6).


شکل 3 سطح فلاونوئید و آنتوسیانین تغییر کردمتیلبرنامه jasmonate (MeJA). متابولیتهایی با افزایش، کاهش و تغییر غیر قابل توجه تجمع (آستانه دو برابری) در برگهای انار تیمار شده با MeJA در مقایسه با گروه شاهد، که در 72- ساعت پس از تیمار برداشت شدند، به رنگهای سبز، قرمز، و آبی به ترتیب واسطههای مسیری که در آنالیز طیفسنجی جرمی یونیزاسیون کروماتوگرافی مایع-الکترواسپری مایع شناسایی نشدند، به رنگ سیاه نشان داده شدهاند. فلش های چین دار چند مرحله واکنش را نشان می دهند.



خصوصیات بیوشیمیایی یک LOX کاندید برای اصلاح اسیدهای چرب در برگ های انار تیمار شده با MeJA
برای کشف ژنهای متابولیکی که در تغییر متابولیسم اسیدهای چرب به سمت فیتواکسیلیپینها دخیل هستند، رونوشتهای برگهای انار تیمار شده با ساختگی و MeJA برای DEGهایی که بهعنوان لیپاز یا LOX مشروح میشوند مورد تجزیه و تحلیل قرار گرفتند. دو ژن لیپاز Pgr004895 و Pgr00112 بیان افزایش یافتهای را نشان دادند. در ترانسکریپتومهای 24-h پس از درمان MeJA و افزایش قابلتوجه بیان با تجزیه و تحلیل qPCR بلادرنگ تأیید شد (شکل 5b). از سوی دیگر، لیپاز Pgr024441 بیان کاهش یافته را در آنالیز رونوشت نشان داد، که توسط نتیجه qPCR بلادرنگ پشتیبانی نشد (شکل 5b). به طور جالب توجه، افزایش بیان Pgr025417، یک LOX فرضی، در رونوشتهای برگهای جمعآوریشده در 2- ساعت، 6- ساعت،24- و 72- ساعت پس از تیمار MeJA مشاهده شد. (شکل S1). تجزیه و تحلیل واقعی qPCR بیشتر نشان داد که بیان Pgr025417 به طور مداوم افزایش یافته است، که از 4- تا 20- برابر، در برگهای جمع آوری شده از 2 تا 72- ساعت پس از تیمار MeJA (شکل 5c) متغیر است.

سیستانچ می تواند ایمنی را بهبود بخشد
برای تعیین اینکه آیا LOX فرضی (Pgr{10}}25417) در افزایش تولید فیتواکسی لیپین در برگهای تیمار شده با MeJA نقش داشته است، توالی و فعالیت آن مورد بررسی قرار گرفت. هنگامی که توالی اسید آمینه Pgr025417 آنالیز شد، بقایای His، Asn، و Ile که مربوط به هماهنگ کننده اتم آهن در محل فعال سویا LOX L-1 (Minor et al.1996) هستند در Pgr025417 (شکل 6a). علاوه بر این، پیش بینی می شود که PgrO25417 در کلروپلاست (احتمال احتمال 0.9096) با پپتید سیگنال شکاف بین 64 و 65 aa (شکل 6a) موضعی شود. در میان 11 LOX فرضی (786 aa تا 970 aa) شناسایی شده در ژنوم مشروح انار، 5 LOX دیگر: Pgr025413، Pgr025418، Pgr009839، Pgr016852، و Pgr013780 نوع Pgr013780، و Pgr013780 با گروههای Pgr013780 و Pgr013780 با گروههای Pgr013780 بستهبندی شده و دارای ویژگیهای دیگری هستند که از نوع Pgr013780 هستند. (شکل 6b). جالب توجه است، در حالی که Pgr008562، Pgr025678، Pgr018982، و PgrO18980 با LOX های دو لپه ای نوع I جمع شده اند. Pgr020032 ارتباط دورتری با نوع دیگر ILOX دارد (شکل 6b). برای تعیین فعالیت آنزیمی PgrO25417، پروتئین نوترکیب (906 aa، ~ 102 کیلو دالتون؛ شکل 6c) با استفاده از اسید لینولئیک به عنوان سوبسترا مورد سنجش قرار گرفت. محصولات اکسید شده اسید لینولئیک توسط Pgr025417 تولید شد، همانطور که با جذب بیشتر در طول موج 598 نانومتر نشان داد زمانی که مقادیر بیشتری از پروتئین نوترکیب در مخلوط واکنش وجود داشت (شکل 6d).
پاسخ رونویسی به کاربرد MeJA اگزوژن در برگهای انار
To understand whether the changes in HTs,flavonoids, lipids, fatty acids, and phyto-oxylipins are regulated transcription-ally, transcriptomes of MeJA-and mock-treated pomegranate leaves collected at2-h,6-h,24-h,and72-h were compared and identified 34 transcription factors(TFs) that showed differen-tial expression (Log,FCl>1، P تنظیم شده<0.05)(table 1);31="" of="" these="" tfs="" also="" exhibited="" significantly="" changed="" expression="" by="" real-time="" qpcr="" analysis="" (fig.7).="" notably,="" a="" zinc-finger="" tf="" pgr009895="" showed="" increased="" expression="" at="" three="" out="" of="" the="" four="" time="" points(2-h,24-h,and="" 72-h)(fig.7a).the="" expression="" of="" pgr002863(pcf5-like),pgr002859(bzip1)and="" pgr006935(auxin="" response="" factor)was="" increased,="" and="" pgro11269="" (myb)="" decreased="" upon="" meja="" elicitation="" at="" two="" time="" points(fig.="" 7a,="" b).both="" pgro09366(anthocyanin="" regu-latory="" c1="" protein/myb)and="" pgro03015(myb)displayed="" increased="" expression="" at="" 6-h,="" but="" decreased="" expression="" at="" 72-h="" (fig.="" 7b).the="" expression="" of="" 12="" tfs="" was="" enhanced="" at="" only="" one="" time="" point,including="" pgr009357(2-h),pgr027831="" (2-h),pgr023581(6-h),pgr009363(6-h),pgr000147="" (6-h),="" pgr021507(6-h),="" pgr021504(6-h),pgr020147(24-h),="" pgr025715(72-h),pgr023629(72-h),pgr015728(72-h),and="" pgr004388(72-h)(table="" 1;fig.7b,c).on="" the="" other="" hand,="" the="" expression="" of="" 12="" tfs="" was="" suppressed="" in="" meja-treated="" pomegranate="" leaves="" at="" one="" time="" point,="" including="" pgr013499="" (2-h),pgr023409="" (2-h),pgr017106(6-h),pgr010911(24-h),pgr017568(72-h),pgr024750(72-h),pgr004878(72-h)pgr002084(72-h),pgr008889(72-h),pgr004532(72-h),="" pgr020131="" (72-h),and="">
برای ارزیابی تنظیم رونویسی ژنهای کاندید که ممکن است در تعدیل مسیرهای فلاونوئیدی و اسید چرب/فیتو-اکسی لیپین پس از القای MeJA عمل کنند، مکانهای اتصال به TF در مناطق پروموتر ژنهای کاندید با استفاده از PlantRegMap (Tian et al.2020) پیشبینی شد. TFها به صورت بیوانفورماتیکی از Eucalyptus Grandis شناسایی شدهاند که ارتباط نزدیکی با انار در Myrtales دارد (جدول S7). برای PgrO25417 (LOX فرضی)، 80 محل اتصال 65 TF شناسایی شد، از جمله مکانهای اتصال فراوان برای MYB (10 مکان TFs.15) و WRKY (11 TFs، 18 محل)، اما بدون مکانهای اتصال برای TFs انگشت روی دوقطبی (جدول) S7). از آنجایی که CHS و CHI در نقطه ورودی مسیرهای بیوسنتزی فلاونوئید و آنتوسیانین قرار دارند و بیان ژن را در ترانسکریپتوم و آنالیزهای qPCR بلادرنگ نشان دادند (شکلهای S1 و 4)، محرکهای احتمالی CHS (Pgr005566) و CHI (Pgr025966) همچنین برای سایتهای اتصال TF فرضی مورد بررسی قرار گرفت. برای CHS، 104 محل اتصال از 76 TF وجود دارد که MYB (20 TFs، 23 سایت) و LH (13 TFs، 23 سایت) فراوانترین TFs هستند (جدول S7). برای CHI، 93 محل اتصال 78 TF وجود دارد که bHLH (16 TFs، 23 سایت) و WRKY (13 TFs، 13 سایت) فراوان ترین TF ها هستند (جدول S7).
بحث
تغییرات متابولیکی منحصربهفرد ناشی از کاربرد MeJA اگزوژن، عملکرد HTs، فلاونها/فلاونولهای متیله و فیتواکسیلیپینها را در پاسخ انار به MeJA نشان میدهد.
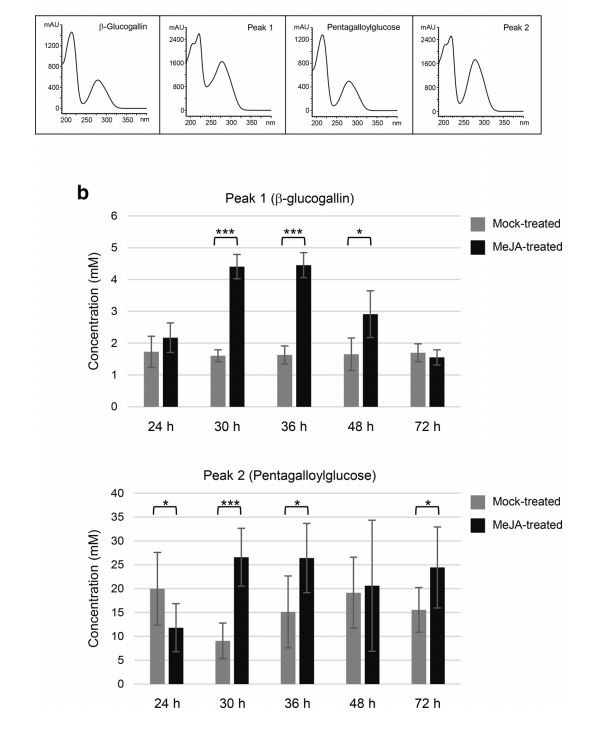
MeJA نقش ثابتی در برانگیختن پاسخ استرس در گیاهان دارد (چئونگ و چوی 2003). تجمع دو واسطه مسیر HT - گلوکوگالین و پنتا-گالوئیل گلوکز در برگ ها در {3}} ساعت پس از کاربرد MeJA القا شد (شکل 2b)، که نشان می دهد آنها در پاسخ به تنش های غیرزیستی و زیستی در محیط عمل می کنند. این نتیجه همچنین عملکرد HT ها را در محافظت از انار از تنش های غیرزیستی در بافت پوست میوه تایید می کند (Schwartz et al.2009; Habashi et al.2019). مربوط به افزایش تجمع متابولیت HT، شیکیمات و ژن های مسیر بیوسنتزی HT نیز افزایش بیان را نشان دادند (شکل 1). خصوصیات بیوشیمیایی قبلی چهار ایزوفرم SDH انگور (Vitis vinifera) نشان داد که فقط VvSDH3 و VySDH4 میتوانند اسید گالیک را از 3-دهیدروشیکیمات تولید کنند (Bontpart et al.2016). با توجه به رونویسی و آنالیزهای qPCR بلادرنگ ما، PgSDH3_1 و PgSDH3_2، همولوگ های WvSDH3، اما نه PgSDH4، همولوگ VSDH4، بیان القا شده توسط MeJA را نشان دادند (شکل های S1 و 1) . این مشاهدات نشان میدهد که PgSDH3_1 و PgSDH3_2 احتمالاً در سنتز HTs در پاسخ به درمان MeJA و تنشهای محیطی نقش دارند. علاوه بر این، بیان افزایش یافته PgUGT8423 و PgUGT84A24، که آنزیم های کاتالیزور مرحله متعهد بیوسنتز HT را رمزگذاری می کنند، توسط برنامه MeJA از نقش HT ها در پاسخ به استرس پشتیبانی می کند.
در 72- ساعت پس از القای MeJA، یک سرکوب کلی فلاونوئیدها و آنتوسیانین ها در برگ های انار مشاهده شد (شکل 3؛ جدول S6)، که برخلاف افزایش تجمع این ترکیبات مشاهده شده در بسیاری از گیاهان دیگر است (Pandey et al. al.2016؛ De Geyter et al.2012؛ Shafiq et al.2011؛ Flores and Ruiz del Castillo 2014؛ Portu et al. 2015). با این حال، سه فلاون و فلاوانول متیله: دی-O-متیل کورستین، فروش 5-O-هگزوسید، و کریزوئه-ریول O-hexosyl-O-hexoside با وجود کاهش پیش سازهای بیوسنتزی غیر متیله، در سطح بیشتری انباشته شدند. (شکل 3؛ جدول S6). کوئرستین تک و دی-O- متیله از تریکوم گونه های سولاناس ترشح می شود و پیشنهاد شده است که در دفاع از گیاهان، احتمالاً به شیوه ای خاص گونه ای عمل کند (Wollenweber and Dörr 1995). رودا و همکاران 2003). همچنین نشان داده شد که گلیکوزیدهای کریزوبریل، لوتئولین و آپیژنین از تغذیه علفخواران آبزی بر روی برگهای Potamogeton lucens (pondweed) در آزمایشات آزمایشگاهی جلوگیری کردند (Erhard et al.2007). تجمع ناشی از متیلهفلاون ها / فلاونول هادر برگ های انار نشان می دهد که آنها ممکن است در پاسخ استرس ناشی از MeJA نقش داشته باشند و پیامدهایی برای دفاع در برابر زخم، عوامل بیماری زا و گیاهخواران در این گونه درختی داشته باشند.

علاوه بر HT ها، فلاونوئیدها و آنتوسیانین ها، تغییرات متابولیکی قابل توجه اضافی شامل بسیج اسیدهای چرب آزاد از لیپیدها و بیوسنتز فیتواکسی لیپین ها در 72- ساعت پس از کاربرد MeJA بود (شکل 5a). افزایش سه برابری اسید پونیسیک (18:3، cis-9، trans-11، cis-13) بر القای MeJA نقش بالقوه این PUFA را با یک سیستم پیوند دوگانه سه مزدوج در سیگنال دهی استرس یا دفاع شیمیایی مستقیم گیاهان انار (جدول S6). کاهش همزمان MAG، MGMG و DGMG همچنین نشان میدهد که اسید پونیسیک معمولاً میتواند به این گلیسرولیپیدها در برگهای انار کونژوگه شود (شکل 5a؛ جدول S6). از میان فیتواکسی لیپینها، افزایش JA و JA-Ile در برگهای انار تیمار شده با MeJA میتواند به دلیل دمتیلاسیون MeJA اعمال شده برونزا برای تشکیل JA باشد، که متعاقباً به JA-Ile تبدیل میشود (جدول S6) (Stuhlfelder et al. .2004). همچنین ممکن است نشان دهد که MeJA می تواند مستقیماً بیوسنتز JA و مشتقات آن را در انار تنظیم کند. ترکیبات فرار مشتق شده از Phyto-oxylipins گزارش شده است که در واکنش سیگنالی به زخمی شدن و حملات پاتوژن نقش دارند (Lim et al.2017). مطالعات اخیر همچنین نقش ضد میکروبی مستقیم فیتواکسی لیپینهای غیر JA را نشان داده است، اگرچه مبنای مکانیکی برای چنین عملکردهایی هنوز مشخص نیست (Deboever et al. 2020). تولید القایی فیتواکسی لیپین در انار مشاهدات قبلی در سایر گیاهان را تأیید می کند. باید مشخص شود که آیا این فیتواکسی لیپین ها بیوسید هستند یا برای تحریک پاسخ ایمنی ذاتی در انار عمل می کنند.
متابولیسم فلاونوئید و آنتوسیانین اصلاح شده، اما نه فیتواکسی لیپین، بر اثر القای MeJA حداقل تا حدی در سطح رونویسی تنظیم می شود.
مطابق با کاهش تجمع فلاونوئیدها و آنتوسیانین ها، ژن های کد کننده CHS و CHI، دو آنزیم که در نقطه ورود بیوسنتز فلاونوئید و آنتوسیانین قرار گرفته اند، بیان کمتری را در برگ های تیمار شده با MeJA نشان دادند (شکل 4). به طرز جالبی، یک همولوگ انار (PgrO09366) از پروتئین تنظیمکننده آنتوسیانین MYB TF ذرت C1 در ابتدا در برگهای تیمار شده با MeJA در 6- ساعت تنظیم مثبت شد، اما سپس در برگهای تیمار شده با MeJA در 72- ساعت کاهش یافت (جدول 1). ؛ شکل 7b). یک همولوگ انار (PgrO10911) از ذرت MYB TF P در برگهای تیمار شده با MeJA در 24- ساعت کاهش یافت (جدول 1؛ شکل 7c). همانطور که در مطالعات در ذرت نشان داده شده است، کلر چندین ژن را در بیوسنتز فلاونوئید و آنتوسیانین فعال می کند، مانند CHS(C2)، دی هیدرو فلاونول ردوکتاز (A1)، آنتوسیانیدین 3-O-گلوکوزیل ترانسفراز (BZ1) و لوکوآنتوسیانی-دین دیوکسی ژناز A2) (Lesnick and Chandler 1998; Sainz et al.1997; Quattrocchio et al.1993). از سوی دیگر، P بیان A1 را کنترل میکند، اما BZ1 را کنترل نمیکند (Grotewold و همکاران 1994). در ذرت، C1 (MYB TF) برای تنظیم بیان ژنهای بیوسنتزی آنتوسیانین در هماهنگی با R(bHLH TF) کار میکند. مول و همکاران 1998؛ گاف و همکاران 1992). Pgr024750، یک bHLH TF، همچنین در برگهای تیمار شده با MeJA در 72- ساعت کاهش یافت و میتواند شریک بالقوه همولوگ C1 انار باشد (جدول 1؛ شکل 7c). علاوه بر این، مکانهای اتصال برای MYB و bHLH TFs در نواحی پروموتر CHS و CHI احتمالی انار از طریق تجزیه و تحلیل بیوانفورماتیک شناسایی شدند (جدول S7). روی هم رفته، این نتایج نشان میدهد که کاهش کلی فلاونوئیدها و آنتوسیانینها حداقل تا حدی از طریق کنترل رونویسی ژنهای بیوسنتزی مرحله اولیه حاصل میشود.
کاهش چندین گلیسرولیپید در برگهای تیمار شده با MeJA مشاهده شد (شکل 5). با این حال، همولوگهای انار (شمارههای دسترسی بانک ژن: XP_031374952 و XP_031374953) از Arabidopsis Wrinkled1 (ArWRI1)، یک TF خانواده APETALA2(AP2) که تنظیمکننده اصلی برای بیوسنتز لیپید گیاهی در نظر گرفته میشود. (سرناک و بنینگ 2004)، به طور مشابه در برگهای تیمار شده با ساختگی و MeJA بیان شد (داده ها نشان داده نشده است). توصیف عملکردی TFهای پاسخگو به القای MeJA (جدول 1؛ شکل 7) به طور بالقوه می تواند نقش تنظیم کننده ای را برای متابولیسم لیپید در برگ های انار نشان دهد.

LOX انار (Pgr025417) با افزایش مداوم بیان پس از کاربرد MeJA اگزوژن، اکسیداسیون اسیدهای چرب را کاتالیز کرد و پیش بینی شد که در کلروپلاست موضعی شود (شکل 5c و 6). بنابراین، Pgr025417 احتمالاً در بیوسنتز JA که در این محفظه درون سلولی انجام میشود، دخیل است (شکل 6). از 11 LOX احتمالی موجود در انار، 5 عدد سیتوزولی (نوع I) و 6 عدد کلروپلاستیک (نوع II) هستند (شکل 6b). از آنجایی که فیتواکسی لیپین های غیر JA در سیتوزول سنتز می شوند (Ponce de Le6n و همکاران 2015)، یک یا چند نوع ILOX ممکن است مسئول تبدیل PUFA به فیتواکسی لیپین های غیر JA بر اساس القای MeJA باشند. با توجه به اینکه LOX (Pgr025417) با افزایش پایدار بیان ژن در برگ های تیمار شده با MeJA در یک محفظه درون سلولی متفاوت از فیتواکسی لیپین های غیر JA قرار دارد، احتمالاً آنزیم های مسئول تولید فیتواکسی لیپین های غیر JA ناشی از MeJA هستند. به صورت رونویسی مدوله نشده است.
کاربرد اگزوژن MeJA باعث ایجاد پاسخ های رونویسی در برگ های انار شد
مطالعه اخیر در Arabidopsis نشان داد که یک شبکه تنظیمی پیچیده غنی شده با MYC(bHLH)، فاکتور پاسخ اتیلن (ERF) و TFهای خانواده MYB در پاسخ رونویسی اولیه ناشی از MeJA دخیل بود (Hickman et al.2017). همولوگ های انار ERF TFها، از جمله Pgr013499(2-h)، PgrO00147(6-h) و PgrO21504 (6-h)، و همولوگهای MYB TF، از جمله PgrO09357 (2-h) )،Pgr009366(6-h)،Pgr003015(6-h)، و Pgr011269 (6-h)، از جمله TFهایی بودند که بیان متفاوتی در برگ های تیمار شده با MeJA در زمان های اولیه جمع آوری شدند. (جدول 1؛ شکل 7). همانطور که در بالا مورد بحث قرار گرفت، همولوگ های انار از فلاونوئید ذرت و پروتئین های تنظیم کننده آنتوسیانین C1 و P (MYB TFs)، و یک bHLH TF کاهش بیان را نشان دادند و به طور بالقوه می توانند کاهش کلی فلاونوئیدها و آنتوسیانین ها را کنترل کنند. علاوه بر این، ناحیه پروموتر LOX (PgrO25417) حاوی محلهای اتصال WRKY، MYB، و bZIP TFs (جدول S7) است، که نشان میدهد میتوان آنها را با TFهای متفاوت بیان شده متعلق به این خانوادههای TF در پاسخ به کاربرد MeJA تنظیم کرد. .
بیان مقایسه ای ژن و تجزیه و تحلیل متابولیت برگ های تیمار شده با MeJA، بررسی مسیرهای مختلف فنلی در میوه ها را تسهیل می کند.
درک پاسخهای متابولیکی و رونویسی برگهای انار به کاربرد MeJA به وضوح برای بهبود سلامت و بهرهوری گیاه (یعنی تولید میوه) مرتبط است. علاوه بر این، بیان مقایسهای ژن و تجزیه و تحلیل متابولیتهای برگهای تیمار شده با MeJA نیز فرصتی را برای روشن کردن تنظیم مسیرهای HT، فلاونوئید و آنتوسیانین که در بافتهای برگ و میوه وجود دارند، فراهم میکند (Bar-Ya'akov et al.2019). ). ترکیبات فنلی HTs، فلاونوئیدها و آنتوسیانین ها به فعالیت های مفید برای سلامتی انسان در میوه های انار کمک زیادی می کنند، اما کنترل تولید و تجمع آنها به طور گسترده در انار (برای فلاونوئیدها و آنتوسیانین ها) یا هیچ گونه گیاهی (برای HTs) مورد بررسی قرار نگرفته است. ). به عنوان مثال، مطالعات قبلی بر روی میوههای انار با استفاده از MeJA، سطوح آنتوسیانینها و فلاونوئیدها را در میوهها پس از برداشت، بدون بررسی بیان ژنهای ساختاری یا تنظیمکننده مربوط به این متابولیتها تعیین کردند (کوشش صبا و زارعی 2019؛ Garcia-Pastor et al.2020). ). از سوی دیگر، مطالعه کنونی TFها (مانند MYB TFs) را نشان داد که بیان متفاوتی را در برگهای تیمار شده با MeJA و ساختگی با الگوهای بیانی مشابه با ژنهای بیوسنتزی HT، فلاونوئید و آنتوسیانین نشان دادند (شکل 7؛ جدول 1). . این TF ها به طور بالقوه در تنظیم مسیرهای HT، فلاونوئید و آنتوسیانین نقش دارند، بنابراین تحقیقات بیشتر در آینده را تضمین می کند.
شایان ذکر است که مطالعه ما افزایش خاصی در فلاونوئیدهای متیله و کاهش عمومی سایر فلاونوئیدها را در برگ های انار تیمار شده با MeJA نشان داد که نشان دهنده نقش بالقوه فلاونوئیدهای متیله در محافظت از برگ های انار در برابر عوامل بیماری زا است (شکل 3؛ جدول S6). گزارش قبلی در مورد میوههای انار تیمار شده با MeJA نشاندهنده افزایش تجمع فلاونوئیدها بود، اگرچه تنها محتوای کل فلاونوئید بدون تعیین کمی مولکولهای فلاونوئید مشخص شد (کوشش صبا و زارعی 2019). به این ترتیب، تجزیه و تحلیل عمیق تری از میوه های انار تیمار شده با MeJA مورد نیاز است تا امکان مقایسه جانبی تغییرات فلاونوئیدی در بافت برگ و میوه فراهم شود. برخلاف افزایش آنتوسیانین ها در میوه های انار پس از کاربرد MeJA (گارسیا پاستور و همکاران 2020)، سطح آنتوسیانین ها در برگ های تیمار شده با MeJA کاهش یافت (شکل 3؛ جدول S6). این نابرابری می تواند به دلیل نقش مشخصی باشد که آنتوسیانین ها در بافت های برگ و میوه بر اثر حملات پاتوژن ایفا می کنند. در واقع، تجمع افتراقی آنتوسیانین ها در برگ ها و میوه ها بر نیاز به بررسی پاسخ های MeJA در بافت های مختلف انار تاکید می کند.
نتایجی که اظهار شده
مطالعه ما تغییرات متابولیکی منحصربهفردی را در HTs، فلاونوئیدها، آنتوسیانینها و فیتواکسی لیپینها در برگهای انار نشان داد که توسط کاربرد اگزوژن MeJA ایجاد شدهاند. رونویسی و تجزیه و تحلیل بیوشیمیایی نشان داد که، در حالی که سرکوب چند فلاونوئیدها و آنتوسیانین ها حداقل تا حدی در سطح رونویسی رخ می دهد، افزایش بیوسنتز فیتواکسی لیپین های غیر JA احتمالاً از طریق رونویسی کنترل نمی شود. این کار تحقیقات بیشتری را در مورد معماری تنظیمی متابولیسم HT، فلاونوئید و آنتوسیانین، هماهنگی پاسخهای متابولیک در برگهای انار به کاربرد MeJA، و همچنین نقشی که متابولیتهای با تجمع القایی در سیگنالدهی و/یا دفاع شیمیایی مستقیم دارند، آغاز میکند.
بیانیه مشارکت نویسنده LC و LT مطالعه را درک کردند. LC و WS آزمایشاتی را انجام دادند. LC، WS، و LT داده ها را تجزیه و تحلیل کردند.LC، WS، و LT دستنوشته را نوشتند. همه نویسندگان نسخه نهایی را خوانده و تایید کردند.
اطلاعات تکمیلی نسخه آنلاین حاوی مطالب تکمیلی است که در https://doi.org/10.1007/s00425-021-03735-9 موجود است.
تشکر و قدردانی ما از همکاران آکادمی علوم کشاورزی و جنگلداری Panzhihua برای ارائه دانه های انار مورد استفاده در این مطالعه تشکر می کنیم. ما همچنین از دکتر Binjie Ge در باغ گیاه شناسی چنشان شانگهای برای کمک در شناسایی و ثبت نمونه کوپن تشکر می کنیم.
بودجه این کار توسط کمیسیون علم و فناوری شهرداری شانگهای تحت کمک مالی 14DZ2260400 و صندوق ویژه تحقیقات علمی دفتر اداری محوطه سازی و ظاهر شهر شانگهای تحت کمک های مالی G172403 و G182403 حمایت شد.
در دسترس بودن داده ها و مواد مجموعه داده های رونوشت تولید شده و تجزیه و تحلیل شده در طول مطالعه حاضر در آرشیو خواندن توالی (SRA) در NCBI با شماره دسترسی PRJNA600139 موجود است. مجموعه داده های پروفایل متابولیت تولید شده و تجزیه و تحلیل شده در طول مطالعه فعلی در این منتشر شده گنجانده شده است. مقاله و فایل های تکمیلی آن
این مقاله از Planta (2021) 254:89 https://doi.org/10.1007/s{5}} استخراج شده است
