مونو سدیم گلوتامات باعث ایجاد تغییراتی در پروفایل های متابولیک کبدی و کلیوی و میکروبیوم روده موش های صحرایی ویستار می شود.
Feb 22, 2022
خلاصه:مصرف کوتاه مدت و بلندمدت مونوسدیم گلوتامات (MSG) pH ادرار را افزایش می دهد اما اثرات آن بر مسیرهای متابولیک در کبد، کلیه و میکروبیوتای روده ناشناخته باقی می ماند. برای پرداختن به این مشکل، ما موشهای نر بالغ نژاد ویستار را بررسی کردیم که برای دریافت آب آشامیدنی با یا بدون 1 گرم درصد MSG به مدت 2 هفته (n=10، هر کدام) اختصاص داده شده بودند. ما یک مطالعه متابولومیک مبتنی بر طیفسنجی رزونانس مغناطیسی هستهای (NMR) روی ژژنوم انجام دادیم.کبد، وکلیه هادر حالی که نمونه های مدفوع برای استخراج DNA باکتریایی برای بررسی میکروبیوتای روده با استفاده از توالی یابی ژن 16S rRNA جمع آوری شد. ما شاهد تغییرات قابل توجهی درکبددر مقایسه با موشهای تحت درمان با MSG در سطوح گلوکز، پیریدوکسین، لوسین، ایزولوسین، والین، آلانین، کینورنات و نیکوتین آمید. در میانکلیهمتابولیت ها، سطح تری متیل آمین (TMA) افزایش یافت و پیریدوکسین پس از درمان MSG کاهش یافت. توالییابی ژن 16S rRNA نشان داد که موشهای تحت درمان با MSG، Firmicutes، باکتریهای روده مرتبط با متابولیسم TMA، همراه با کاهش گونههای Bififidobacterium را افزایش دادهاند. داده های ما از تأثیر مصرف MSG بر روی پشتیبانی می کندکبدوکلیهمتابولیسم بر اساس تغییرات میکروبیوم روده، ما حدس می زنیم که TMA و متابولیت های آن مانند تری متیل آمین-N-اکسید (TMAO) ممکن است واسطه اثرات MSG بر رویسلامت کلیه.
کلید واژه ها:مونوسدیم گلوتامات؛ میکروبیوتای روده؛ مسیر سوخت و ساز؛ متابولومیک؛ میکروبیوم؛ تری متیل آمین؛ کلیه؛ کبد
مقدمهمونوسدیم گلوتامات (MSG) معمولاً به غذاها اضافه می شود تا خوش طعم بودن را افزایش دهد، به ویژه در غذاهای آسیایی و غذاهای فرآوری شده صنعتی [1]. MSG بدون توجه به مقدار آن توسط سازمان غذا و دارو (FDA) [2] یک ماده ایمن برای مصرف انسان در نظر گرفته می شود، علیرغم داده های اخیر که نشان می دهد میانگین مصرف روزانه MSG 3-4 گرم است و هر گرم اضافی MSG خطر را افزایش می دهد. ابتلا به سندرم متابولیک [3]. مقادیر بالای MSG رژیم غذایی با اضافه وزن [4،5] و فشار خون [6] مرتبط است، اما نتایج متناقض است [7،8].

تلاشهایی برای آشکار کردن اثرات MSG بر اندامهای متابولیک حیوانات با مصرف تزریقی [9،10] یا خوراکی [11،12] انجام شده است. در یکی از این تلاش ها برای بررسی اثرات MSG در موش صحراییکلیه هانتایج نشان داد که مصرف کوتاه مدت [13] و بلند مدت [11] MSG باعث قلیایی شدن ادرار در موش ها می شود، اگرچه مکانیسم قلیایی شدن ادرار ثابت نشده است. متابولومیک یک رویکرد رایج برای تعریف تغییرات متابولیت ها از شرایط مختلف است [14،15]. مصرف کوتاه مدت MSG باعث تغییرات خاصی در متابولیت های ادراری از جمله دی متیل آمین (DMA) و متیل آمین (MA) شد که متابولیت های مشتق شده از روده از تری متیل آمین (TMA) هستند. TMA یک آمین آلیفاتیک فرار با زنجیره کوتاه است که بوی مشخصه ماهی را فراهم می کند. در واقع، باکتریهای روده TMA را از ماهیهای رژیمی تولید میکنند یا میتوانند از سایر مواد مغذی از جمله کولین و کارنیتین که در تخممرغ و گوشت قرمز فراوان هستند، تولید شود [16]. بخش عمده ای از TMA به صورت آنزیمی به تری متیل آمین-N-اکسید بی بو (TMAO) تبدیل می شود و سطوح بالای TMAO پلاسما با بیماری قلبی عروقی (CVD) مرتبط است [17]، مزمن.بیماری کلیوی(CKD) [18] و دیابت [19].
ما در اینجا از ابزارهای متابولومیک برای بررسی اثرات مصرف کوتاه مدت MSG بر متابولوم پلاسما استفاده کردیم.کبد،کلیهو روده، و همبستگی بین نتایج متابولومیک و تغییرات میکروبیوتای روده را تجزیه و تحلیل کرد. دادههای ما ممکن است بینشهای مکانیکی جدیدی در مورد اثرات MSG رژیمی ارائه دهد و در عین حال نشانگرهای زیستی آسیب اندام ناشی از MSG را نیز نشان دهد.
مواد و روش ها
حیواناتبیست موش صحرایی نر 6-هفتهای ویستار (وزن حدوداً 200 گرم) از مرکز حیوانات آزمایشگاهی ملی (دانشگاه ماهیدول، سالایا، بانکوک، تایلند) بهدست آمد که به مدت 2 هفته در قفسهای متابولیکی از جنس استنلس استیل سازگار شدند. سپس تحت شرایط استاندارد دما (2 ± 23 درجه سانتیگراد)، رطوبت (30 تا 60 درصد) و روشنایی (350-400 لوکس) 12 ساعت چرخه تاریکی/12 ساعت روشنایی حفظ می شود. در طول مطالعه، موشها با پلت تجاری شماره CP 082 (گروه همراه کامل، بانکوک، تایلند) ارائه شدند. تمام آزمایشها با پیروی از دستورالعملهای مرکز حیوانات آزمایشگاهی شمال شرقی (NELAC)، دانشگاه Khon Kaen، تایلند انجام شد. علاوه بر این، این مطالعه توسط کمیته اخلاق حیوانات دانشگاه Khon Kaen، تایلند (AEKKU-NELAC5/2558) تایید شد.
معرف هابرای تغذیه حیوانات از MSG خالص با درجه غذایی (99 درصد) (آجینوموتو، توکیو، ژاپن) استفاده شد. متانول و کلروفرم با گرید تجاری از RCI LABSCAN LIMITED (بانکوک، تایلند) برای استخراج بافت خریداری شد، آب با گرید LC-MS از Merck (دارمشتات، آلمان)، دی هیدروژن فسفات پتاسیم (KH2PO4) و اکسید دوتریوم (D2) خریداری شد. از Merck (دارمشتات، سوئیس)، آزید سدیم (NaN3) توسط آژانس مواد شیمیایی اروپا (ECHA، هلسینکی، فنلاند)، سدیم تری متیلسیلیل-[2،2،3،{12}}H4]-پروپیونات (TSP) تولید شد. یک استاندارد داخلی برای تجزیه و تحلیل NMR، از بیوتکنولوژی سانتا کروز (سانتا کروز CA، ایالات متحده آمریکا) به دست آمد. برای طیف سنجی جرمی، ایزوپروپانول درجه تجاری (C3H8O) و اسید فرمیک (CH2O2) از RCI LABSCAN LIMITED (بانکوک، تایلند) خریداری شد.
طراحی تجربیموش ها به طور تصادفی برای دریافت آب آشامیدنی با (n=10) یا بدون (n=10) 1 گرم درصد MSG به مدت 2 هفته قرار گرفتند. آب اسمز معکوس (RO) (غلظت کلر 3-4 ppm) برای مطالعه حیوانی زمانی که همه موشها دسترسی آزاد به غذا داشتند استفاده شد. مصرف روزانه آب (ml) و غذا (g) و همچنین وزن بدن هفتگی (g) ثبت شد. 24 دفع ادراری (ml/rat/day) در طول دوره مطالعه ثبت شد. نمونه خون مدفوع و دم (100 میکرولیتر پلاسما) 2 هفته قبل از قربانی کردن حیوانات با استفاده از دی اکسید کربن (CO2) پس از 12- ساعت ناشتا جمع آوری شد. نمونه های بافت، به عنوان مثال، ژژنوم،کبدوکلیه،قبل از نگهداری در دمای 80 درجه سانتیگراد تا زمانی که برای تجزیه و تحلیل استفاده شوند، جمع آوری و در نیتروژن مایع منجمد شدند.
آماده سازی و تجزیه و تحلیل نمونههر بافت (1{8}}0 میلیگرم توده مرطوب) برای استخراج متابولیت طبق پروتکلهای منتشر شده قبلی استفاده شد [20]. قبل از اکتساب NMR، فاز قطبی عصارههای بافتی مجدداً در بافر NMR 580 میکرولیتری (بافر فسفات سدیم 100 میلیمولار، pH 7.4، در D2O، حاوی 0.1 میلیمولار TSP و 0.2 درصد NaN3) معلق شد، بهطور مختصر گردابی شد و 12،000× گرم به مدت 5 دقیقه در دمای 4 ◦C. پس از آن، 550 میکرولیتر از مخلوط قبل از تجزیه و تحلیل NMR به یک لوله شیشهای NMR (گروه دوران، ماینز، آلمان) با قطر خارجی 5 میلیمتر منتقل شد. تقریباً 250 میلی گرم مدفوع با 500 میکرولیتر آب با درجه HPLC (Merck, Darmstadt, آلمان) مخلوط شد و با استفاده از میکسر گردابی با سرعت 2500 دور در دقیقه به مدت 15 دقیقه در دمای اتاق همگن شد. سپس سوسپانسیون مدفوع در 12، × گرم به مدت 15 دقیقه در دمای 4 درجه سانتیگراد سانتریفیوژ شد و 540 میکرولیتر از مایع رویی به میکرولوله های تمیز 1.5 میلی لیتری و 60 میکرولیتر بافر NMR (بافر KH2PO4 1.5 مولار، pH 7) منتقل شد. در D2O حاوی 2 میلی مولار TSP و 1 درصد NaN3) اضافه شد. سپس لولهها برای مدت کوتاهی ورتکس شدند، سانتریفیوژ شدند و در دمای 12×g به مدت 10 دقیقه سانتریفیوژ شدند و در نهایت 580 میکرولیتر از مخلوط برای تجزیه و تحلیل به یک لوله شیشهای NMR با قطر خارجی 5 میلیمتر منتقل شد.
عصارههای بافتی و نمونههای مدفوع با استفاده از یک طیفسنج NMR با فرکانس 4 مگاهرتز (Bruker Biospin, Rheinstetten, USA) در دمای 15/298 کلوین مورد تجزیه و تحلیل قرار گرفتند. طیفها به پیک TSP (δ1H { {14}}.00)، مرحلهای و خط پایه با استفاده از MATLAB (Mathworks، Natrick، MA USA) تصحیح شد. سیگنال پیک TSP (δ1H H1.{8}}–0.005) از تمام بافتها و پیک TSP (δ1H H1.20–0.157) از مدفوع حذف شد. علاوه بر این، پیک آب از ژژنوم حذف شد (δ1H 4.50 و 5.20)،کبد(δ1H 4.68 و 5.{4}})،کلیه(δ1H 4.31 و 5.74) و مدفوع (δ1H 4.18 و 5.23). علاوه بر این، طیفهای خام در معرض همترازی پیک و نرمالسازی قرار گرفتند [21]. دادههای طیفی همه نمونهها با استفاده از آنالیز مؤلفه اصلی بدون نظارت (PCA) و تصحیح سیگنال متعامد نظارت شده به ساختارهای پنهان- تجزیه و تحلیل متمایز (O-PLS-DA) تجزیه و تحلیل شدند. دادهها میانگینمرکز و با واریانس واحد (UV) مقیاسبندی شدند. مدلهای O-PLS-DA با مقادیر R2X، R2Y و Q2Y ارزیابی میشوند که به ترتیب نشاندهنده تناسب، کسری از واریانسهای ماتریس Y و توانایی پیشبینی مدل هستند [22]. برای جلوگیری از برازش بیش از حد، اعتبار سنجی متقاطع برابری برای 500 تکرار انجام شد. جایگشت p-value برای نشان دادن اعتبار مدل استفاده شد. متغیرهای مهم هر مدل معتبر از طریق ضرایب همبستگی O-PLS-DA با تصحیح نرخ کشف کاذب بنجامینی-هوچبرگ انتخاب شدند (05/0 > P). طیفسنجی همبستگی کل آماری (STOCSY) [23]، پایگاههای اطلاعاتی تغییر شیمیایی داخلی و پایگاه داده متابولوم انسانی (HMDB نسخه 4، ایالات متحده آمریکا) [24] برای شناسایی متابولیتها استفاده شد.
تجزیه و تحلیل غنیسازی مسیر نیز با استفاده از MetaboAnalyst (http://www. metaboanalyst.ca/ (دسترسی در 14 ژوئیه 2020)) انجام شد [25]. تصویر مسیر متابولیک توسط Cytoscape [26] ایجاد شد. تغییرات در متابولیتها توسط STOCSY مشخص شد و تجزیه و تحلیل تک متغیره با بررسی غلظت نسبی متابولیتهای با تفاوت قابلتوجه، محاسبه ادغام قلههای طیف انجام شد. با توجه به p-value محاسبه شده توسط آزمون t Student با استفاده از GraphPad Prism 7 (Ver. 7, GraphPad Software, Inc., La Jolla, CA, USA).
آماده سازی نمونه پلاسما برای آنالیز UHPLC-ESI-QTOF-MSپلاسما (50 میکرولیتر) با 150 میکرولیتر ایزوپروپانول (IPA) مخلوط شد و به دنبال آن 24- ساعت انکوباسیون در دمای 20 درجه سانتیگراد برای رسوب دادن پروتئین انجام شد. همه نمونه ها دو بار در دمای 13،{5}}× gat 4◦C به مدت 10 دقیقه سانتریفیوژ شدند. در مجموع 50 میکرولیتر از هر نمونه گرفته شد و در یک لوله میکرو سانتریفیوژ 1.5 میلی لیتری برای ساخت نمونه کنترل کیفیت (QC) جمع شد و 120 میکرولیتر از هر مخلوط نمونه به یک درج شیشه ای HPLC منتقل شد.

تجزیه و تحلیل UHPLC-ESI-QTOF-MSتجزیه و تحلیل UHPLC-ESI-QTOF-MS در آزمایشگاه بین المللی پدیده دانشگاه Khon Kaen (KKUIPL) استفاده شد. عصاره های فاز آبی نمونه ها بر روی پلت فرم فاز معکوس آنالیز شدند. بخش جداسازی با استفاده از یک سیستم UHPLC (بروکر، دارمشتات، آلمان) با شدت بروکر HPLC انفرادی C18 2 انجام شد. دارمشتات، آلمان) استفاده شد. دمای ستون روی 55 درجه سانتیگراد و دمای نمونه برداری خودکار روی 4 درجه سانتیگراد تنظیم شد. فاز متحرک A 10{{2{0}} درصد آب درجه HPLC با 0.1 درصد اسید فرمیک (FA) و فاز متحرک B 1 بود0 {{30}} درصد متانول با 0.1 درصد FA. نرخ جریان در 0. }} دقیقه، 0.25 میلیلیتر/دقیقه)، 99.9-75 درصد A (2.{49}}–10.0 دقیقه، 0. 4 میلیلیتر/دقیقه)، 2{{6{0}} درصد A (1{0}.0-12.0 دقیقه، 0.4 میلیلیتر در دقیقه)، 10 درصد A (12.0-21.0 دقیقه، 0.4 میلیلیتر/ دقیقه)، 0.1 درصد A (21.0-23.0 دقیقه، 0.4 میلی لیتر در دقیقه)، 99.9 درصد A (24.0-26.0 دقیقه، 0.4 میلی لیتر در دقیقه). حجم تزریق نمونه 4 میکرولیتر برای هر دو حالت قطبیت یونیزاسیون مثبت و منفی اعمال شد.
تجزیه و تحلیل طیف سنجی جرمی با استفاده از یک سیستم فشرده ESI-Q-TOF (بروکر، دارمشتات، آلمان) انجام شد. فرمات سدیم (HCOONa) حاوی 2 میلی مولار هیدروکسید سدیم، 0.1 درصد FA و 50 درصد IPA مستقیماً به عنوان کالیبرنت خارجی با سرعت جریان 0.5 میکرولیتر در دقیقه تزریق شد. شرایط در حالت قطبیت یونیزاسیون مثبت - محدوده جرمی 50-1300 m/z، ولتاژ مخروطی 31 V، ولتاژ مویرگی 4500 V، دمای منبع 220 ◦C، دمای desolvation 220 ◦C، جریان گاز تخلیه 8 L/min. شرایط حالت قطبیت یونیزاسیون منفی - محدوده m/z: 50-900 m/z، ولتاژ مخروط 31 V، ولتاژ مویرگی 4500 V، دمای منبع 220 ◦C، دمای desolvation 220 ◦C، جریان گاز تخلیه 8 L/min.
تجزیه و تحلیل میکروبیوم رودهDNA با استفاده از کیت DNA QiAamp® PowerFecal® Pro (Qiagen، Hilden، آلمان) استخراج شد. DNA استخراج شده در OD 260/280 با استفاده از اسپکتروفتومتر Nanodrop2000c (Thermo scientifific, Waltham, MA, USA) اندازه گیری شد. تمام DNA استخراج شده تا زمان انجام آنالیز در دمای 20◦C حفظ شد. ناحیه V{4}V4 ژن RNA ریبوزومی 16S (rRNA) برای هر نمونه با استفاده از پرایمر جهانی رو به جلو V3 (50-CCTACGGGNGG CWGCAG-30) و پرایمر معکوس V4 ({8}) تکثیر شد. {11}}GACTACHVGGGTATCTAATCC-30). واکنش PCR شامل 2x KAPA HiFi HotStart ReadyMix، 12.5 نانوگرم الگوی DNA و 5 میکرومولار از هر پرایمر، با دناتوراسیون اولیه در دمای 95 درجه سانتیگراد به مدت 3 دقیقه و سپس 25 سیکل دناتوراسیون در دمای 95 درجه سانتیگراد به مدت 30 ثانیه در 55 درجه سانتیگراد، بازپخت C برای 30 ثانیه، تمدید در 72 ◦C برای 30 ثانیه، و تمدید نهایی در 72 ◦C به مدت 10 دقیقه. یک چیپ Agilent DNA 1000 و Agilent 2100 Bioanalyzer (Agilent Technologies، Palo Alto، CA، USA) برای تعیین کمیت محصول تقویت شده ترکیب شدند. آمپلیکون های PCR با استفاده از دانه های AMPure XP برای خالص سازی خالص شدند. ژن جزئی rRNA 16S با استفاده از پلتفرم Illumina MiSeq (Illumina Inc., San Diego, CA, USA) توالی یابی شد.
کتابخانه توالییابی 16S rRNA با استفاده از DNA ژنومی (gDNA) تهیه شد و توالیهای جفتی منطبق با استفاده از FLASH ادغام شدند (http://ccb.jhu.edu/software/ FLASH/ (در 29 ژوئن 2020 در دسترس قرار گرفت) [27] . فیلترینگ با کیفیت، توالیهای حاوی خواندنهای با کیفیت پایین را حذف کرد و با استفاده از CD-HIT-OTU (http://weizhong-lab.ucsd.edu/ cd-hit-otu (دسترسی در 29 ژوئن 2020)) [28] و rDnaTools انجام شد. بسته بندی OTU ها (واحدهای طبقه بندی عملیاتی) با 97 درصد هویت آستانه با استفاده از الگوریتم UCLUST بر اساس شباهت 100 درصد طبقه بندی شدند. توالی هایی که بیشتر یا مساوی 97 درصد شباهت داشتند به همان OTU اختصاص داده شدند. توالی های نماینده OTU هم تراز شدند و با استفاده از پروژه پایگاه داده ریبوزومی (RDP) از نظر طبقه بندی طبقه بندی شدند و با پایگاه های داده مرجع NCBI مقایسه شدند. طبقه بندی بر اساس پایگاه داده ژن سبز (http://greegenes.lbl. gov/ (دسترسی در 29 ژوئن 2020) است. خروجی طبقهبندی قرائتها در چندین سطح طبقهبندی - پادشاهی، شاخه، طبقه، نظم، خانواده، جنس، و گونهها با استفاده از بینشهای کمی در اکولوژی میکروبی (QIIME) [29].
تحلیل آماریتجزیه و تحلیل آماری غذا و آب مصرفی، حجم ادرار و وزن بدن بهصورت میانگین ± انحراف معیار در هر گروه از حیوانات گزارش شد و تفاوتهای بین گروهها از نظر معنیداری با آزمون t-student با p-value < {{2} }.05 از نظر آماری معنی دار در نظر گرفته شد.
نتایج
تاثیر MSG بر مصرف غذا و آب، وزن بدن و حجم ادرارموشهای تحت درمان با MSG و موشهای کنترل، مقدار مشابهی از غذا دریافت کردند (به ترتیب 1.94 ± 17.44 و 1.37 ± 18.46 گرم در روز) (شکل 1A) و وزن بدن (به ترتیب 17.23 ± 333.58 و 15±333.80 گرم در موش). (شکل 1B). با این حال، مصرف آب در موشهای تحت درمان با MSG (36/18 ± 38/52 میلیلیتر در روز) در مقایسه با گروه کنترل (39/8 ± 38/38 میلیلیتر در روز) به طور قابلتوجهی بیشتر بود (شکل 1C). در هر دو گروه تحت درمان با MSG و شاهد، خروج ادرار با گذشت زمان افزایش مییابد، اگرچه افزایش قابل توجهی فقط در موشهای تحت درمان با MSG مشاهده شد (92/3 ± 42/15 میلیلیتر در موش در روز قبل از درمان و 78/8 ± 09/29 میلیلیتر در موشهای صحرایی / موش). روز پس از درمان). همچنین، اگرچه از نظر آماری معنیدار نیست، خروجی ادرار موشهای تحت درمان با MSG (78/8 ± 09/29 میلیلیتر در موش در روز) ظاهراً بیشتر از کنترلها (55/10 ± 15/23 میلیلیتر در موش در روز) بود (شکل 1D).

تغییرات متابولیک در اندام های مهم متابولیکطیف NMR نمونههای بافت جمعآوریشده پس از دو هفته درمان MSG مورد بررسی قرار گرفت. PCA داده های طیفی NMR در ابتدا برای مشاهده هر گونه خوشه بندی آشکار و نقاط پرت انجام شد (شکل 2). خوشه بندی واضح و جداسازی کامل در پروفایل های متابولیت کبدی بین گروه کنترل و گروه تحت درمان با MSG با مقدار p جایگشت 0 مشاهده شد.002، R2X 58 درصد، Q2Y 0.84، و R2Y از 0.93 در نمودارهای امتیاز PCA و O-PLS-DA نشان داده شده است (شکل 2A، B). یک نمودار بارگذاری ضریب متناظر با OPLS با تخصیص متابولیت در شکل 3 با معنی دار ارائه شده است.کبدمدل های نشان داده شده در شکل 3A. تمام تغییرات قابل توجه در متابولیت ها در جدول 1 خلاصه شده است. در کبد، سطوح بالاتری از شش متابولیت شامل گلوکز، پیریدوکسین، 2-دئوکسیاوریدین، اینوزین، ناشناخته 1 و 2 در گروه تحت درمان با MSG یافت شد، در حالی که یازده متابولیت از جمله لوسین، ایزولوسین، والین، آلانین، N-استیل گلیکوپروتئین، استون، 1،3 دی متیلورات، هیستامین، گزانتین، کینورنات و نیکوتین آمید در گروه کنترل به طور معنی داری بالاتر بود. نمودار امتیاز PCA بر اساسکلیهمتابولیتها (شکل 2C) هیچ خوشهبندی واضحی را بین دو گروه نشان نمیدهند و مدل O-PLS-DA از نظر آماری با مقدار p جایگشت 0 معنیدار بود.018، R2X 56 درصد، Q2Y از 0.29، و R2Y از 0.74 (شکل 2D). دو متابولیت تغییر یافته در یافت شدبافت های کلیهبا سطح تری متی لامین به طور قابل توجهی بالاتر و پیریدوکسین به طور قابل توجهی کمتر در گروه تحت درمان با MSG در مقایسه با گروه شاهد (شکل 3B). در مقابل، نتایج ژژونوم (شکل 2E، F)، مدفوع و پلاسما (شکل 2 و شکل S1) هیچ خوشهبندی بین گروههای درمان و کنترل نشاندادهشده در نمودارهای امتیازات PCA و O-PLS-DA را نشان نداد.

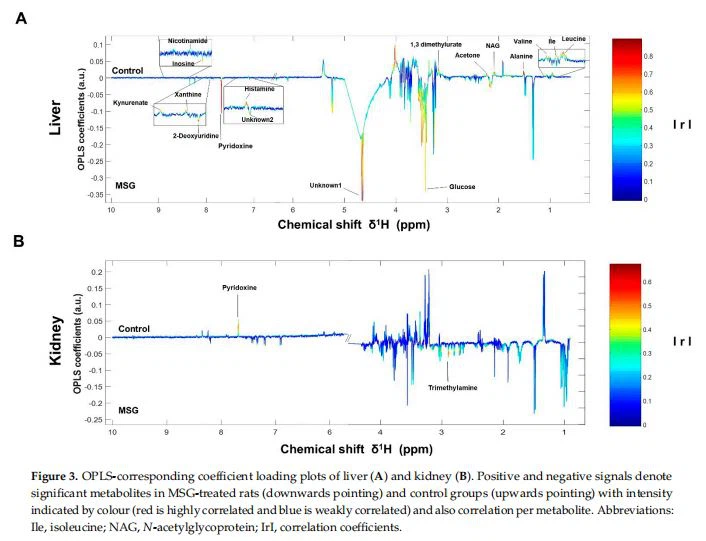
مسیرهای همبستگی متابولیت های مهم درکبدوبافت های کلیهبا استفاده از شناسه های KEGG بررسی و توسط نرم افزار Cytoscape تولید شدند. متابولیت ها به شبکه متابولیک مرتبط می شوند. هنگامی که این نتایج برای ترسیم یک نقشه مسیر متابولیک به منظور نشان دادن یک همبستگی شهودی تر ترکیب شدند، مشخص شد که متابولیت ها عمدتاً با مسیرهای متابولیک، مانند گلوکونئوژنز کبدی، اسیدهای آمینه شاخه دار، ویتامین B6 و متابولیسم های تری متیل آمین مرتبط هستند. شکل S3).

مصرف MSG میکروبیوم روده را تغییر می دهدنتایج تجزیه و تحلیل ترکیب باکتریایی مدفوع نشاندهنده هفت شاخه، 15 طبقه، 19 راسته، 46 خانواده، 127 جنس و 22 گونه از همه گروههای حیوانی بود. 7-10 گونه برتر انتخاب شدند و درصد فراوانی نسبی جوامع باکتریایی در سطح شاخه، طبقه، ردیف، خانواده، جنس و گونه ایجاد شد (شکل 4). در سطح شاخه، چهار فیلای نسبتاً فراوان به ترتیب زیر بودند - Firmicutes > Bacteroidetes > Proteobacteria > Actinobacteria در همه حیوانات (شکل 4A). فراوانی اکتینوباکتریا در موش های تحت درمان با MSG (0.30 درصد) به طور قابل توجهی کمتر از موش های کنترل (1.32 درصد) بود (شکل 5A).
در سطح کلاس، فراوان ترین میکروبیوتا باسیل > کلستریدیا > باکتریویدیا > اریسیپلوتریشیا در همه حیوانات بود (شکل 4B). گروه تحت درمان با MSG به طور قابل توجهی کلستریدیا (31.59 درصد) بالاتر از گروه کنترل (19.25 درصد) داشتند. با این حال، موشهای تحت درمان با MSG نسبت به موشهای کنترل (1.09 درصد) بهطور قابلتوجهی اکتینوباکتری کمتری داشتند (0.15 درصد) (شکل 4B). هنگامی که در سطح مرتبه تفسیر شد، لاکتوباسیل ها، کلستریدیال ها، باکتریوئیدال ها، اریسیپلوتریکال ها در همه حیوانات فراوان بودند (شکل 4C). کلستریدیاها در موشهای تحت درمان با MSG (59/31 درصد) بهطور معنیداری بیشتر از موشهای کنترل (25/19 درصد) بودند، در حالی که بیفیفیدوباکتریالها در موشهای تحت درمان با MSG (06/0 درصد) نسبت به موشهای کنترل (06/1 درصد) بهطور معنیداری کمتر بود.
چهار خانواده فراوان که معمولاً در همه حیوانات آزمایشی مشاهده میشوند به ترتیب زیر بودند - Lactobacillaceae > Erysipelotrichaceae > Clostridiaceae > Prevotellaceae (شکل 4D). در سطح خانواده، Bififidobacteriaceae به طور قابل توجهی پایین تر بود، اما Clostridiales شناسایی نشده در موش های تحت درمان با MSG در مقایسه با موش های کنترل به طور قابل توجهی بالاتر بود. فراوانی نسبی چهار جنس برتر مشاهده شده در همه حیوانات به ترتیب زیر بود - لاکتوباسیلوس > توریسی باکتر > پرووتلا < کلستریدیوم="" (شکل="" 4e).="" یک="" نقشه="" حرارتی="" از="" فراوانی="" نسبی="" در="" سطح="" جنس،="" فراوانی="" کمتر="" لاکتوباسیلوس="" و="" فراوانی="" کلستریدیوم="" بیشتر="" را="" در="" موشهای="" تحت="" درمان="" با="" msg="" نشان="" داد="" (شکل="" 5b).="" علاوه="" بر="" این،="" فراوانی="" کمتر="" بیفیفیدوباکتریوم="" نیز="" در="" موشهای="" تحت="" درمان="" با="" msg="" ({6}}.06="" درصد)="" در="" مقایسه="" با="" موشهای="" کنترل="" (1.06="" درصد)="" مشاهده="">
در سطح گونه، چهار گونه باکتری روده رایج در همه موشها به ترتیب لاکتو باسیلوس اینستینالیس، توریسیباکتر سانگوینیس، کلستریدیوم سائودینسه و موریباکلوم رودهای بودند (شکل 4F). در گروه تحت درمان با MSG، Flintibacter butyricus به طور قابل توجهی بیشتر از گروه کنترل بود، در حالی که Faecalibaculum rodentium و Bififidobacterium pseudolongum به طور قابل توجهی کمتر فراوان بودند.


بحث
چندین خط شواهد به طور مداوم مصرف MSG را با اثرات نامطلوب بر سلامت انسان، مانند بروز بیشتر سندرم متابولیک [3]، اضافه وزن [4،5] و فشار خون شریانی [6] مرتبط میدانند. با این وجود، دادهها در برخی موارد متناقض بودهاند و مکانیسمهای اساسی همچنان نامشخص است. برای مقابله با این موضوع، تغییرات متابولیکی بافت و تغییرات میکروبی روده ناشی از مصرف MSG را بررسی کردیم. همانطور که در نمایش شماتیک در شکل 6 نشان داده شده است، مصرف MSG متابولیت های مرتبط با گلوکونئوژنز کبدی، متابولیسم اسید آمینه شاخه دار (BCAA)، ویتامین B6 و متابولیسم تری متیل آمین را تغییر داد. علاوه بر این، مصرف کوتاه مدت MSG فراوانی نسبی Bififidobacterium را که یک باکتری مفید در نظر گرفته می شود و کلستریدیوم مربوط به تولید TMA و TMAO را سرکوب کرد [30].

در کبد، متابولیتهایی مانند گلوکز، پیریدوکسین (B6)، 2-دئوکسیاوریدین، اینوزین، ناشناخته 1 و 2 در حیوانات تحت درمان با MSG به طور قابلتوجهی بالاتر از گروه کنترل بود، در حالی که یازده متابولیت (یعنی لوسین، ایزولوسین، والین) آلانین، N-استیل گلیکوپروتئین، استون، 1،{7} دی متیلورات، هیستامین، گزانتین، کینورنات و نیکوتین آمید) به طور قابل توجهی کمتر بودند. اولاً، سطوح بالاتر گلوکز ممکن است نشان دهنده افزایش گلوکونئوژنز کبدی مرتبط با MSG باشد که با قند خون بالا پلاسما گزارش شده قبلی در خوک های تازه متولد شده دریافت کننده مکمل MSG (1 گرم بر کیلوگرم وزن بدن) مطابقت دارد [31]. دوم، کاهش سطح آلانین و سه BCAA، از جمله والین، لوسین و ایزولوسین، ممکن است با کاتابولیسم اسید آمینه و متابولیسم انرژی مرتبط باشد که در آن اسکلتهای کربنی آنها میتواند به عنوان پیشساز برای گلوکونئوژنز استفاده شود (آلانین، والین و ایزولوسین به عنوان اسیدهای آمینه گلوکوژنیک). و تولید انرژی از طریق چرخه اسید تری کربوکسیلیک (TCA). در توافق با گزارش قبلی، ما دریافتیم که محصولات تخریب لوسین و لیزین، بتا هیدروکسی ایزووالرات و 5-آمینووالرات به ترتیب در ادرار موشهای تحت درمان با MSG به طور قابلتوجهی بیشتر بود [13]. سوم، افزایش پیریدوکسین درکبدو کاهش پیریدوکسین درکلیهموشهای تحت درمان با MSG تغییر متابولیسم ویتامین B6 را پیشنهاد کردند. ما همچنین کاهش سطح هیستامین، کینورنات، و نیکوتین آمید را در بدن پیدا کردیمکبدموشهای تحت درمان با MSG، که محصولات آنزیمهای وابسته به B6- در متابولیسم هیستیدین و تریپتوفان هستند. ارتباط بین دریافت MSG و متابولیسم ویتامین B6، هیستیدین و تریپتوفان نیاز به بررسی بیشتر دارد. چهارم، موش های تحت درمان با MSG سطوح بالاتری از تری متیل آمین (TMA) درکلیه. TMA از ترکیبات غذایی از جمله کولین، ال-کارنیتین و بتائین توسط عمل آنزیم های میکروبی سنتز می شود [16]. TMA تا حد زیادی به صورت غیرفعال در گردش خون پورتال جذب می شود و عمدتاً توسط مونواکسیژنازهای حاوی فلفلاوین کبدی (FMOs) به تری متیل آمین-N-اکسید (TMAO) اکسید می شود. بخش کوچکی از TMA به دی متیل آمین (DMA) و متیل آمین (MA) اکسید می شود و در نهایت در ادرار دفع می شود [32،33]. سطوح بالاتری از DMA و MA در ادرار موش های تحت درمان با MSG قبلا گزارش شده بود [13]. چندین مطالعه نشان داده اند که افزایش پیش سازهای TMA، کولین، یا متابولیت های آن، TMAO، می تواند منجر به پیشرونده شود.کلیهفیبروز توبولو بینابینی، بیماری قلبی عروقی و مزمنبیماری کلیوی[34-36]. بنابراین، سطح TMA بالا درکلیهممکن است ارتباط بین مصرف MSG وآسیب کلیوی
با حرکت از تغییرات مشاهده شده در TMAها، ما میکروبیوتای روده موشهای تحت درمان با MSG را بررسی کردیم و تغییر دو شاخه اصلی، Firmicutes و Bacteroidetes را نشان دادیم. فراوانی بالاتر Firmicutes، اما فراوانی کمتر از Bacteroidetes، در موش های تحت درمان با MSG مشاهده شد. در سطح جنس، موشهای تحت درمان با MSG دارای رقص فراوان کلستریدیوم و فراوانی کمتری از لاکتوباسیلوس و بیفیدوباکتریوم بودند. جنس Clostridium شامل گروهی از میکروارگانیسم های متعلق به شاخه Firmicutes است. مقداری گونه های کلستریدیوم با تولید آنزیم هایی برای تبدیل کولین یا ترکیبات غذایی به TMA با متابولیسم TMA مرتبط هستند [33،37،38]. افزایش باکتری های روده تولید کننده TMA، به عنوان مثال، گونه های کلستریدیوم، از افزایش متابولیت های TMA در روده پشتیبانی می کند.کلیهو ادرار موش های تحت درمان با MSG. علاوه بر این، مصرف MSG جمعیت Bififidobacterium را کاهش داد، یک باکتری پروبیوتیک که نقش مهمی در هموستاز روده و سلامت دارد [39]. کربوهیدرات های ساده و قابل هضم مانند لاکتوز و ساکارز در دستگاه گوارش فوقانی توسط میزبان و باکتری هایی مانند لاکتوباسیل ها متابولیزه می شوند. با این حال، کربوهیدرات های غیر قابل هضم، به عنوان مثال، فیبر غذایی، در دستگاه گوارش تحتانی توسط اعضای میکروبیوتای روده، از جمله Bififidobacterium متابولیزه می شوند. رژیم غذایی با محتوای بالای چربی های اشباع شده و قندهای ساده اما فاقد فیبر غذایی مانند رژیم غذایی سبک غربی ممکن است به تعداد کمتری از باکتری های مفید کمک کند [40]. کاهش بیفیدوباکتریوم، یک باکتری خوب، در بیماری های التهابی مزمن مانند چاقی [41]، هپاتیت B [42] و دیابت گزارش شده است [43،44]. اثر مصرف MSG بر روی میکروبیوتای روده در انسان، قبلاً بدون تغییر قابل توجهی در ترکیب میکروبی در مقایسه با پایه گزارش شده بود [45]. تأثیر کم MSG بر میکروبیوتای روده در این مطالعه ممکن است به دلیل دوز پایین مکمل MSG (2 گرم در روز) باشد، زیرا میانگین دریافت روزانه MSG در مشاهدات ما 4 گرم در روز است [3]. ما دریافتیم که هر 1 گرم مصرف روزانه MSG خطر ابتلا به سندرم متابولیک را افزایش می دهد. اگرچه مکانیسم مصرف MSG که منجر به بیماریهای متابولیک میشود مشخص نیست، کاهش بیفیفیدوباکتریوم در حیوانات تحت درمان با MSG ممکن است یک سرنخ باشد. به طور تصادفی، کاهش بیفیفیدوباکتریوم در موش های تحت درمان با MSG که در مطالعه حاضر یافت شد، مشابه موش های مبتلا به کمبود ویتامین B6 است [46]. مطالعه فشرده در مورد اینکه چگونه MSG باعث کاهش باکتری های خوب و تغییر وضعیت ویتامین B6 می شود، نیاز به بررسی بیشتر دارد.

ما نشان دادیم که مصرف MSG باعث القای کبدی وکلیهتغییرات متابولیکی دخیل در گلوکونئوژنز و متابولیسم اسید آمینه زنجیرهای شاخهدار، ویتامین B6 و متابولیسم TMA، همراه با تغییرات ترکیبی میکروبیوتای روده. این مشاهدات نشان می دهد که مسیرهای متابولیک تغییر یافته ممکن است با اثرات نامطلوب مصرف طولانی مدت MSG، به ویژه بر رویکبدوکلیه
