Onco-Immunity و کاربرد درمانی آمیگدالین: مروری قسمت 2
Jun 13, 2023
6. کاربردهای دارویی آمیگدالین
تجزیه آمیگدالین، که اسید هیدروسیانیک ایجاد می کند، می تواند حرکات تنفسی را کاهش دهد و با مسدود کردن سیستم تنفسی آسم را درمان کند. 54 یک مدل حیوانی تجربی با شرایط بیماری تنفسی، افزایش سنتز سورفکتانت ریوی را نشان داد.55 نشان داده شده است که آمیگدالین از نوع II محافظت می کند. سلولهای اپیتلیال آلوئولی (AECIIs) از ریههای موشهای جوان جدا میشوند که در معرض هیپوکسی قرار میگیرند.56 این وضعیت مانع از تکثیر سلولهای AECII میشود و سطح mRNA سورفکتانت ریه را در شرایط آزمایشگاهی کاهش میدهد و در نتیجه آسیب ریه در حیوانات نارس ایجاد میشود.57 در غلظت 200 میکرومول در لیتر آمیگدالین تکثیر سلول های AECII را در موش های نارس تحریک می کند و سطح SP mRNA را افزایش می دهد.
هیدروسیانیک اسید یک ماده شیمیایی سمی است و مصرف دوز زیاد آن می تواند آسیب های جدی به بدن انسان از جمله مسمومیت، آسیب به سیستم تنفسی و سیستم قلبی عروقی و غیره وارد کند. از آنجایی که هیدروسیانیک اسید یک ماده شیمیایی اسیدی قوی است، دارای اثر مستقیم اثر خوردگی بر روی سلول های انسانی که باعث پارگی غشای سلولی و از بین رفتن عملکرد سلولی می شود و در نتیجه بر سلامت انسان تأثیر می گذارد.
در مورد رابطه بین هیدروسیانیک اسید و ایمنی، هیچ مدرک علمی مستقیمی برای حمایت از این فرضیه وجود ندارد. با این حال، قرار گرفتن طولانی مدت در معرض مواد شیمیایی سمی مانند اسید هیدروسیانیک ممکن است باعث آسیب به سیستم ایمنی بدن شود و در نتیجه ایمنی بدن را کاهش داده و خطر عفونت را افزایش دهد. بنابراین، اجتناب از قرار گرفتن در معرض مواد شیمیایی سمی یک اقدام مهم برای حفظ سلامتی و ایمنی است. بنابراین، ما باید ایمنی خود را تقویت کنیم. سیستانچ می تواند ایمنی را تقویت کند. سیستانچ همچنین دارای اثرات ضد ویروسی و ضد سرطانی است که می تواند توانایی سیستم ایمنی را برای مبارزه و بهبود ایمنی بدن تقویت کند.

روی فواید سلامتی سیستانچ کلیک کنید
علاوه بر این، Semen Armeniacae Amarum (SAA)، که حاوی آمیگدالین به عنوان یک ترکیب فعال است، با القای اووالبومین (OVA) اثر ضد آسم در مدل آسم آلرژیک دارد. تصور میشود SAA عملکرد سلولهای T کمکی نوع 2 را کاهش داده و اینترلوکین را کاهش میدهد. تولید (IL{3}}).
کاهش بیش فعالی و التهاب راه هوایی، که هر دو از علائم آسم هستند، ممکن است ناشی از تغییر پاسخ Th2 به آلرژن باشد. آمیگدالین همچنین ممکن است برای درمان بیماری انسدادی مزمن ریه (COPD) استفاده شود.62 مطالعات متعدد نشان میدهد که آمیگدالین میتواند تا حدی انتقال اپیتلیال-مزانشیمی ناشی از سیگار را سرکوب کند. 3 فسفوریلاسیون، مرتبط با سرکوب مسیر TGF/Smad.64
7. آمیگدالین و سیستم ایمنی
آمیگدالین با کاهش پاسخ ضد التهابی و تقویت سیستم ایمنی با اصلاح عملکرد سلولهای T تنظیمی (Tregs)، که منجر به از بین رفتن پلاک و افزایش لومن میشود، اثر ضد آترواسکلروتیک را نشان میدهد. پپتید (PT)، یک اکتاپپتید که گاهی اوقات به دلیل زنجیره های پپتیدی قابل مقایسه به عنوان آنالوگ آمیگدالین نامیده می شود.
در کراتینوسیت های انسانی، PT نشان داده شده است که بیان اینتگرین TGF-، HSP70 و -v را افزایش می دهد و در عین حال بیان ICAM{3}} را کاهش می دهد. نشان داده شد که فعالیت های بیولوژیکی مشابه PT دارند.69 هر دو سیستم ایمنی را در کراتینوسیت های انسانی تعدیل می کنند، که نشان می دهد ممکن است برای درمان پسوریازیس استفاده شود.
آمیگدالین رشد سلولهای T خون محیطی انسان را در شرایط آزمایشگاهی افزایش میدهد (25-80{{1{12}}}} ug/mL، 0).055-1.75{ {22}} mmol/L).35 همچنین میتواند IL{7}} و ترشح اینترفرون را در محدوده 25-400μg/mL (0.055-0.875 mmol/L) افزایش دهد. 71 آمیگدالین (100) -400 میلیگرم در لیتر؛ 0.219-0.875 میلیمول در لیتر) سلولهای T را در آزمایشهای اضافی القا کرد که بیشترین تأثیر را در mg/L 200 (0.437 میلیمول در لیتر) داشت. آمیگدالین (10 میلی گرم بر کیلوگرم) رشد سلول های ایمنی را کاهش می دهد، سیستم ایمنی را سرکوب می کند و بقای موش های پیوند کلیه را در داخل بدن افزایش می دهد. 72 سلول های ایمنی نقش حیاتی در رشد و توسعه اندومتریوز دارند. آمیگدالین (5 میلیگرم بر کیلوگرم) با تأثیر بر فعالیت موضعی سلولهای ایمنی، کانونهای آندومتریوز را کاهش میدهد.48 این یافتهها نشان میدهد که آمیگدالین میتواند تکثیر سلولهای ایمنی را در مطالعات آزمایشگاهی تقویت کند، و به طور همزمان، میتواند از تکثیر سلولهای ایمنی جلوگیری کرده و پیوند اعضا را افزایش دهد. میزان موفقیت در آزمایشات پیوند عضو.55
این دو یافته به ظاهر متناقض به تنظیم احتمالی سیستم ایمنی با واسطه آمیگدالین در هر دو طرف اشاره دارند.64 به نظر می رسد یکی دیگر از مزایای آمیگدالین درمانی، امکان تسکین درد و التهاب باشد. با استفاده از کشت آزمایشگاهی سلولهای میکروگلیال BV2 موش در سال 2005. هوانگ این اثرات را در شرایط آزمایشگاهی روی سلولهای RAW 264.7 تیمار شده با LPS و تحقیقات in vivo روی موشهای مبتلا به التهاب ناشی از کاراگینان تأیید کرد. رونویسی TNF-a و IL{13}}b با آمیگدالین 1 میلی مولار در شرایط آزمایشگاهی مهار می شوند.74 فاز بعدی این مطالعه شامل تزریق کاراگینان به مفصل مچ پا موش در آزمایش in vivo بود. التهاب (c-Fos، TNF-a و IL{19}}b) برای تجزیه و تحلیل اثرات آمیگدالین مورد استفاده قرار گرفت.76 نشان داده شده است که کاراگینان باعث ایجاد ادم و کاهش WDR می شود، و آن را به خوبی پیش بینی کننده سطح درد می کند.77 تجویز آمیگدالین منجر به کاهش WDR شد، که ممکن است به این معنی باشد که آمیگدالین دارای ویژگی های ضد درد است.
بیان c-Fos، TNF-a و IL{2}}b در نخاع به طور قابل توجهی با تجویز آمیگدالین در عضله به میزان 0.005.005 mg/kg کاهش یافت. 80 کاهش Fos بیان (ناشی از کاراژینان) در طناب نخاعی توسط آمیگدالین آن را به گزینه ای جذاب برای درمان التهاب و کاهش درد در این مطالعه تبدیل می کند.81 درمان با آمیگدالین برای کاهش التهاب سلولی ناشی از LPS در شرایط آزمایشگاهی و همچنین التهاب ناشی از کاراژینان یافت شده است. و ادم در موش. 82 بیان c-Fos، TNF-a و IL{13}}b در نخاع به طور قابل توجهی با این درمان کاهش می یابد. در نتیجه، عمل آمیگدالین با کاهش سیتوکین پیش التهابی مرتبط است. خروجی. 83 در رده سلولی ناشی از لیپوپلی ساکارید (LPS) و مدل موش آرتریت ناشی از کاراگینان، خواص ضد درد و ضد التهابی آمیگدالین مورد بررسی قرار گرفت.
آمیگدالین، ترکیبی جدا شده از دانههای میوه رزماری، با مهار تولید درد عمده و نشانگرهای مولکولی التهابی مانند فاکتور نکروز (TNF-) و اینترلوکین{1}} (IL{2}}) پردردی را کاهش میدهد. از Prunus Armeniacae همچنین نشان داده شده است که درد ناشی از فرمالین را در موشها در دوزهای کمتر از 1 میلیگرم بر کیلوگرم کاهش میدهد، که ممکن است به دلیل تأثیر آن بر تولید سایتوکینهای التهابی مانند اینترلوکین بتا (IL{6}) باشد. {7}} و فاکتور نکروز تومور (TNF -)، دو نوع اصلی سیتوکین تولید شده توسط سلولهای ایمنی.{9}} علاوه بر این، تولید سیکلواکسیژناز (COX{10}}) و نیتریک اکسید سنتاز را مهار میکند. (iNOS)، سطح پروستاگلاندین های E2 و اکسید نیتریک را کاهش می دهد و در نتیجه اثر ضد التهابی و ضد درد دارد.
8. اثر آمیگدالین بر دستگاه گوارش
نقش آمیگدالین در دیواره روده و خطر همراه با مصرف غذا با تجزیه آمیگدالین در مایعات گوارشی انسان و جذب متابولیت آن در روده کوچک در دستگاه گوارش GIT و کشت سلول های روده انسان نشان داده شده است. در مقابل، پپسین ALT را سرکوب می کند و زمان جهانی شدن را در موش های تحت درمان با CCl افزایش می دهد که با دوز 500 میلی گرم بر کیلوگرم AST داده شود. 90 علاوه بر این، در حضور هیدرولیز پپسین آب بادام، بافت همبند کبد موش صحرایی کمتر تکثیر می شود، حتی اگر به دلیل بازیابی سطوح AST و ALT91 به دنبال القای دی گالاکتوزامین، این امر تحت تأثیر تکثیر قرار نگیرد. گاستریت.92 با تقلید از مدل آزمایشگاهی سیستم گوارش انسان، شیم و همکاران 51 می توانند هضم آمیگدالین را شبیه سازی کنند. آنزیم های گوارشی آمیگدالین خوراکی را به پروناسین و گلوکز تجزیه کردند. سپس، بروناسین در روده کوچک انسان به ماندلونیتریل، حاوی بتا گلوکوزیداز، تجزیه شد تا هیدروکسی ماندلونیتریل بدون بنزآلدئید تولید شود. باکتری های روده ممکن است بر سمیت آمیگدالین تأثیر بگذارند

9. تأثیر آمیگدالین بر بیماری های عصبی
به گفته چنگ و همکاران، آمیگدالین 49 می تواند در درمان اختلالات عصبی مانند بیماری پارکینسون موثر باشد. علاوه بر محافظت از سلول ها در برابر سمیت عصبی ناشی از 6-هیدروکسی دوپامین، رشد نورون ها را با تحریک بیان Calreticulin افزایش می دهد.
10. اثر آمیگدالین بر دستگاه تناسلی ادراری
آمیگدالین به دلیل خواص ضد فیبروتیک قوی خود شناخته شده است و می توان از آن برای درمان بیماران مبتلا به فیبروز کلیه استفاده کرد. وقتی به فیبروبلاستهای بینابینی کشتشده آمیگدالین داده میشود، ظرفیت تکثیر آنها کاهش مییابد و تولید فاکتور رشد آنها (TGF- 1) تغییر میکند. ماتریکس خارج سلولی به دنبال انسداد دستگاه ادراری به سرعت کاهش یافت. در روز 21، آمیگدالین همچنین آسیب کلیوی را به حداقل می رساند. در نتیجه، آمیگدالین می تواند فیبروبلاست های کلیوی را تضعیف کند و باعث فیبروز کلیوی بینابینی در موش صحرایی شود. آمیگدالین، اما ترشح پروژسترون مشاهده نشد. 41 در تخمدان خوک، آمیگدالین تولید استروئید را نیز کنترل می کند.
علاوه بر این، اجزای دارویی ماده خام Keishi-bukuryo-gan، یک داروی گیاهی ژاپنی که برای تحریک تخمک گذاری در زنان نابارور استفاده می شود، شامل آمیگدالین است. در شرایط in vivo و in vitro، Keishi-bukuryo-gan استروئیدزایی را در فولیکولهای قبل از تخمکگذاری و جسم زرد در تخمدانهای موش تقویت کرد. تخمدان های خرگوش.45 با این حال، تجویز داخل عضلانی و خوراکی آمیگدالین به طور قابل توجهی بر سطوح پلاسمایی برخی از تنظیم کننده های غدد درون ریز (پروژسترون، استرادیول{7}} بتا، تستوسترون)، تیروئید (تری یدوتیرونین، تیروکسین، هورمون محرک تیروئید) و هورمون ها (تری یدوتیرون) تأثیر می گذارد. تیروکسین، هورمون محرک تیروئید).44 میانگین وزن بدن و غدد هیپوفیز قدامی (پرولاکتین، هورمون لوتئینیزه کننده) خرگوش های مورد استفاده در این تحقیق تحت تاثیر قرار نگرفت.
11. فعالیت ضد سرطان آمیگدالین
تصور میشود که آمیگدالین در دانههای چند گیاه مانند زردآلو، بادام، سیب و هلو یافت میشود و این امکان را برای آزمایش آن بر روی طیف وسیعی از سلولهای سرطانی فراهم میکند. سلول های سرطانی هلا برای اولین بار. رده سلولی هلو تیمار شده با آمیگدالین با 4، 6-دیامینو-2-فنیل ایندول (DAPI) قبل از تیمار با انکسین V-FITC و پروپیدیوم یدید رنگآمیزی شد. بنابراین، BCL-2 عملکرد پروتئین ضد آپوپتوز کاهش می یابد، اما عملکرد پروتئین Bax افزایش می یابد.41 همچنین افزایش فعالیت کاسپاز و شروع مسیرهای آپوپتوز ذاتی وجود داشت. تاثیر درمانی بر سلول های سرطان دهانه رحم دارند. یک یافته مشابه در داخل بدن نیز مشاهده شده است.39
علاوه بر این، تأثیر آمیگدالین جدا شده از منی Armenlacae، یکی از اعضای خانواده پروناسین، بر روی سلولهای سرطانی پروستات DU 145 و LN CAT37 مورد مطالعه قرار گرفته است. با کاهش بیان پروتئین ضد آپوپتوز BCL{3}} و افزایش بیان پروتئین Bax افزایش در آنزیم کاسپاز پیدا شده است. 94 با کاهش بیان پروتئین ضد آپوپتوز BCL{7}} و افزایش بیان پروتئین Bax، افزایش در آنزیم کاسپاز مشاهده شد. .84 تصور می شود که عصاره آمیگدالین باعث مرگ سلول های سرطانی پروستات در انسان با آپوپتوز می شود.
قابلیت مهار شیمیایی آمیگدالین نیز در شرایط آزمایشگاهی در سلول های سرطان سینه مورد مطالعه قرار گرفته است. همچنین میتواند در سلولهای MCF7 (ER)، سلولهای MDA MB{1}} و سلولهای Hs 578T (خطوط سلولی سرطان پستان سهگانه منفی (TNBC)) سمیت سلولی ایجاد کند. نشان داده شده است که BCL{4}}، Bax و کاسپازها همگی اثرات مشابهی دارند.{5}} چسبندگی سلول های Hs 578T TNBC نیز توسط پروتئین کیناز فعال شده با میتوژن (p38 MAPK) و مولکول سیگنال دهی آپوپتوز با اضافی کاهش یافت. درمان با آمیگدالین. 87 آمیگدالین خواص ضد سرطانی را در مورد سلول های سرطان سینه نشان داد. 30 نمونه مشابهی از الگوی چسبندگی در سلول های سرطانی مثانه مشاهده شد. علاوه بر این، سلولهای تومور UMUC، سلولهای RT112 و سلولهای TCCSUP همگی پس از 24 ساعت یا دو هفته از تجویز آمیگدالین، کاهش قابل توجهی در چسبندگی نشان دادند. . ادعا شد که اثر ضد سرطانی آمیگدالین به انواع خاصی از سلولهای سرطانی محدود میشود.78 مورد مشابهی در مورد سلولهای سرطان دهانه رحم رخ داد، جایی که آمیگدالین تأثیر درمانی بر رده سلولی HeLa داشت اما روی سلولهای FL تأثیری نداشت. مشخص شده است که تبدیل آمیگدالین به نئو آمیگدالین در محلول آبی اثر ضد سرطانی آن را در سلول های لوسمی پرومیلوسیتیک مهار می کند. عصاره آمیگدالین از مایع منی Persicae شکل فعال D با کروماتوگرافی HPLC نشان داده شد. بنابراین، عصاره قبل از استفاده برای سلولهای لوسمی پرومیلوسیتیک (HL{17}}) برای جلوگیری از اپیمریزاسیون جوشانده شد. افزایش مرگ سلولی نیز ثبت شده است که نشان می دهد آپوپتوز در حال وقوع است.77
علاوه بر این، تغییرات فیزیکی در هسته، و همچنین تکه تکه شدن DNA سلول، شناسایی شده است. علاوه بر این، فعالیت درمانی آمیگدالین بر روی سلولهای H1299 و PALM با سرطان ریه سلول غیر کوچک (NSCLC) در شرایط آزمایشگاهی مشاهده شده است. . نشان داده شده است که آمیگدالین تعداد میکروتوبول های بالغ را در حلقه آئورت موش های دیابتی تحت درمان با آمیگدالین کاهش می دهد و سلول های اندوتلیال ناشی از استرپتوزوتوسین را در سلول های اندوتلیال موش های صحرایی دیابتی ناشی از استرپتوزوتوسین مهار می کند. بدون آمیگدالین درمانی تکثیر می شود. همچنین پیشنهاد شده است که خواص ضد رگ زایی آمیگدالین ممکن است به خواص سرکوب کننده تومور آن کمک کند و نقش های درمانی بالقوه آمیگدالین در شکل 3 نشان داده شده است. 92
12. اثر فلور میکروبی روده بر آمیگدالین
میکروارگانیسمهای GIT، لومن، روده و روده بر متابولیسم داروها و سایر مواد شیمیایی خارجی که وارد بدن میشوند، به ویژه هنگامی که به صورت خوراکی مصرف میشوند، تأثیر میگذارند. فیرمیکوتها، باکتریها و اکتینوباکتریها رایجترین باکتریهای بیهوازی هستند که به آزادسازی سیانید در روده کمک میکنند. کشف شده است که بتا گلوکوزیداز روده ای و بتا گلوکوزیداز میکروبی محصولات متمایزی ایجاد می کنند. بتا گلوکوزیداز که به نام های لاکتاز فلورسین هیدرولاز (LPH) و بتا گلوکوزیداز سیتوزولی (CBG) نیز شناخته می شود، یک تخریب کننده پیوند گلیکوزیدی است که بر روی سایر تخریب کننده های پیوند عمل می کند. مواد، از جمله صفرا. هنگامی که آمیگدالین توسط بتا گلوکوزیداز روده ای به پروناسین تبدیل می شود، اسید هیدروسیانیک تولید نمی شود. یکی دیگر از میکروب های روده، بتا گلوکوزیداز، آمیگدالین را به HCN تبدیل می کند.75 باکتری های روده در تحقیقات متعددی نشان داده شده اند که در آن آمیگدالین به سیانید هیدرولیز می شود که متناسب با ترکیب میکروبی در روده است. سمیت هیدرولیز آمیگدالین در موشهای با دوز 300 میلیگرم بر کیلوگرم کاهش مییابد، اما در موشهای درماننشده باعث ایجاد سمیت و مرگومیر بیشتر میشود.
با مقایسه موش ها و میمون ها، مدفوع انسان به دلیل وجود فلور میکروبی فراوان، تقریباً 50 درصد آمیگدالین را به سیانید هیدرولیز می کند. از باکتری ها بیشتر برای تولید گلوکوزیداز استفاده می شود. جمعیت باکتری در روده تحت تأثیر پری بیوتیک ها و پروبیوتیک ها قرار می گیرد و تنظیم می شود. علاوه بر این، پری بیوتیک ها مولکول های بیولوژیکی هستند، در حالی که پروبیوتیک ها ارگانیسم هایی هستند که اعمال میکروبیوتای روده را به نفع میزبان کنترل می کنند. پری بیوتیک ها می توانند مواد سرطان زا را متصل یا جذب کنند و خطر مسمومیت با سیانید ناشی از آمیگدالین را کاهش دهند. فعالیت بتا گلوکوزیداز باکتریایی توسط لاکتوباسیلوس و بیفیدوباکتریوم کاهش یافت. 56،85،90
13. اثر آمیگدالین بر پیشرفت چرخه سلولی و آپوپتوز
آمیگدالین همچنین دارای خواص ضد سرطانی است زیرا پروتئین های درگیر در چرخه سلولی را تحت تأثیر قرار می دهد یا آن را تغییر می دهد. علاوه بر تحریک آپوپتوز در سلولهای PC3 و LNCaP در سرطان پروستات پس از 24 ساعت و دو هفته درمان، آمیگدالین همچنین سلولهای فاز G0/G1 را افزایش داده و سلولهای فاز G2/M را کاهش میدهد. تعدیل برخی از پروتئینهای چرخه سلولی، مانند کینازهای وابسته به سیکلین (Cdks)، نیز گزارش شده است. پروتئین های چرخه، در درجه اول اگزونوکلئاز، توپوایزومراز، و پروتئین اتصال، تنظیم شدند. محققان بیان پروتئین را با استفاده از تجزیه و تحلیل ریزآرایه cDNA کاهش دادند و همچنین کاهش سطح بیان mRNA ها را با استفاده از تجزیه و تحلیل RT-PCR مشاهده کردند. ثابت شده است که آمیگدالین بیان ژن های مرتبط با چرخه سلولی را در SNU-C4 کولورکتال کاهش می دهد. سلول های سرطانی، مانند اگزونوکلئاز 1 (EXO1)، توپوایزومراز (DNA) I (TOP1)، زیرخانواده F و کاست اتصال ATP. بنابراین، می تواند چرخه سلولی تومور را تحت تاثیر قرار دهد، از تکثیر سلولی جلوگیری کند و اثر ضد توموری خود را نشان دهد. میتوان نتیجه گرفت که آمیگدالین میتواند چرخه سلولی را کنترل کرده و تکثیر سلولی را با تعدیل پروتئینها یا ژنهای چرخه سلولی محدود کند، و بهویژه، آمیگدالین میتواند تکثیر سلولهای تومور بدخیم، به ویژه در سرطان پروستات و روده بزرگ را کاهش دهد.
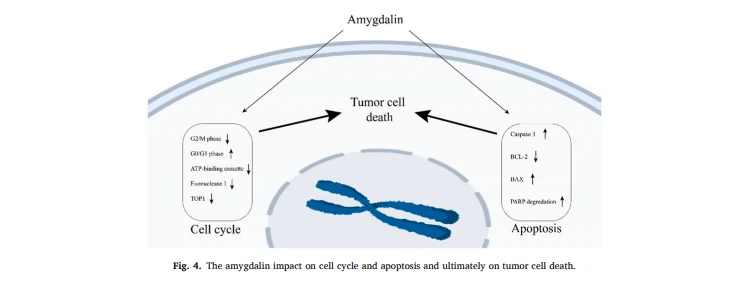
چن و همکاران 49 کشف کردند که آمیگدالین ممکن است با تقویت بیان کاسپاز{2}} باعث آپوپتوز در سلولهای HeLa آغشته به DAPI شود، که بیان BCL{3}} را کاهش داد و بیان Bax را در سلولهای HeLa تیمار شده با آمیگدالین افزایش داد. ، نشان دهنده یک مسیر ضروری در شروع آپوپتوز مبتنی بر آمیگدالین است. همچنین می تواند باعث آپوپتوز در سلول های سرطان پروستات شود. پس از درمان با آمیگدالین، چانگ و همکاران. کشف کردند که بیان آنزیم Bax و فعالیت کاسپاز افزایش مییابد، در حالی که بیان BCL در سلولهای DU145 و LNCaP کاهش مییابد و منجر به آپوپتوز در سلولهای سرطان پروستات میشود. لی و همکاران بیان پروتئینهای آپوپتوز را در سلول های سرطان سینه تحت درمان با آمیگدالین با دوزهای مختلف. آنها کشف کردند که آمیگدالین بیان پروتئین پروآپوپتوز Bax را افزایش می دهد در حالی که بیان پروتئین ضد آپوپتوز BCL-2 پروکاسپاز 3 را کاهش می دهد. تخریب PARP همچنین در سلول های سرطان پستان تحت درمان با آمیگدالین به طور همزمان مشاهده شد. یافته ها حاکی از آن است که آمیگدالین با القای آپوپتوز و تعدیل پروتئین های مرتبط با آپوپتوز، که در سلول های سرطان پروستات و دهانه رحم قابل توجه است، رشد تومور را مهار می کند (شکل 4).74-77.

14. ارتباط بین آمیگدالین و B-گلوکوزیداز
بتا گلوکوزیدازها (-D-glucopyrranoside glucohydrolase) [EC3.2.1.21] آنزیم هایی هستند که پیوندهای گلیکوزیدی کربوهیدرات ها را هیدرولیز می کنند و باقی مانده های گلیکوزیل انتهایی، گلیکوزیدها و الیگوساکاریدها را آزاد می کنند. آنها در طیف گسترده ای از گونه ها، از جمله یوکاریوت ها، باستانی ها، و باکتری ها وجود دارند.30 آنها همچنین در فعالیت های کلیدی مانند تبدیل زیست توده، تجزیه گلیکولیپید، لیگنیکاسیون، دفاع از آفات، فعال سازی هورمون های گیاهی و کاتابولیسم دیواره سلولی مشغول هستند. بیماری گوچر (ناشی از کمبود بتا گلوکوزیداز)، که در آن گلیکوزیدها در بافت های لیزوزومی تجمع می یابند، به همین ترتیب با بتا گلوکوزیدازها درمان می شود. بتا گلوکزیدازها بیشتر به عنوان یک گیاه سلولی برای هیدرولیز سلولز در مقیاس تجاری استفاده می شوند. 90 در دمای تا 90 درجه سانتیگراد، گلوکزیدازهای مقاوم در برابر حرارت برای تولید گلوکز از سلولز استفاده می شود و ایزوفلاون ها همچنین می توانند آگلیکون های مفیدی بسازند. بتا گلوکوزیداز، که به عنوان امولسیون نیز شناخته می شود، در گیاهان خوراکی مانند هسته زردآلو (که دارای آنتی اکسیدان بالایی نیز هستند)، مغز بادام، قارچ، کاهو و فلفل سبز وجود دارد و توسط میکروارگانیسم هایی مانند آسپرژیلوس سیاه تولید می شود. میکروبیوتای روده
گیاهان، قارچها و باکتریها همگی بتا گلوکوزیداز از نظر توالی و ساختار یکسان دارند. فعالیت سوبسترا یا هویت توالی های نوکلئوتیدی آنها می تواند برای طبقه بندی آنها استفاده شود. 88 بتا گلوکوزیدازها را می توان با توجه به ماهیت سوبسترا به سه دسته طبقه بندی کرد: (1) آریل بتا گلوکوزیدازها (که ترجیح قابل توجهی برای آریل دارند. -بتا گلوکزیدها)، (2) سلولز (که فقط دی ساکاریدها را هیدرولیز می کند) و (3) گلوکوزیدازها با ویژگی گسترده (فعالیت روی بسیاری از انواع بسترها نشان می دهد و بتا گلوکوزیدازهای رایج هستند). بتا گلوکوزیدازها بر اساس همگنی توالی به دو زیر خانواده تقسیم می شوند: BGA که شامل بتا گلوکوزیدازها و فسفو بتا گلوکوزیداز (از باکتری ها تا پستانداران) است و BGB که فقط حاوی بتا گلوکوزیدازها (از مخمرها، کپک ها و باکتری ها است). ).{15}} یک چارچوب طبقهبندی جایگزین با توجه به توالی اسید آمینه و شباهت ساختاری نیز برای گلیکوزید هیدرولاز ایجاد شد. آنزیمهای یک خانواده با تشابه گسترده توالی اسید آمینه و توالیهای کاملاً محافظتشده در این روش ارزیابی میشوند.87 وبسایت آنزیم فعال کربوهیدرات (CRAZY) (http://www.cazy.org) اکنون 133 خانواده گلیکوزید هیدرولاز (GH) را فهرست میکند. .84 اکثریت این خانواده ها به زیر گروه ها تقسیم می شوند. یک گروه شامل خانواده هایی با اسیدهای آمینه کاتالیزوری محافظت شده، ساختارهای حوزه کاتالیزوری یکسان، و نژاد و مکانیسم کاتالیزوری مشترک است. خانواده GH-A دارای بیشترین اعضا است، از جمله بتا گلوکوزیدازها از خانواده های GH1، GH5 و GH30.81
خانواده GH1 شناخته شده ترین بتاگلوکوزیدازها را دارد. گلوکوزیدازهای باکتریها، گیاهان و حیوانات به خانواده GH1 تعلق دارند، در حالی که گلوکوزیدازهای باکتریها، کپکها و مخمرها به خانواده GH3 تعلق دارند.73 خانواده GH توسط اتحادیه بینالمللی بیوشیمی و زیستشناسی مولکولی به خانوادههای ساختاری تقسیم میشوند. از آنجایی که تعریف کل طیف بسترها برای آنزیمهای خاص دشوار است، این طرح طبقهبندی، بر اساس ویژگیهای ساختاری آنزیمها، ارزش بیشتری نسبت به خاصیت زیرلایه دارد. از یک خانواده به تجزیه و تحلیل ساختار سایر اعضای همان خانواده کمک می کند، به ویژه در موقعیت فعال، مکانیسم آنزیم و ویژگی های سوبسترا. تکامل گلیکوزید هیدرولاز نیز با طبقه بندی خانواده های آنزیمی توضیح داده می شود. 73 تولید شده، که تنفس سلولی را محدود می کند و باعث مرگ سلولی می شود (شکل 2). سلول های سرطانی غلظت سولفور هیدروکسیلاز کمتری نسبت به سلول های سالم دارند. در نتیجه، توانایی این سلول ها برای سم زدایی اسید هیدروسیانیک آزاد شده با هیدرولیز آمیگدالین محدود می شود. عمل ضد سرطانی آمیگدالین زمانی که با بتا گلوکوزیداز ترکیب می شود افزایش می یابد.56 در سلول های سرطانی، گلیکولیز بی هوازی رایج ترین راه است. شرایط اسیدی فعالیت بتا گلوکوزیداز را افزایش میدهد، که باعث میشود اسید هیدروسیانیک و بنزآلدئید بیشتری در سلولهای سرطانی تولید شود و در نتیجه تأثیر مرگباری به همراه داشته باشد. اسید هیدروسیانیک در مقایسه با سایر داروهای با وزن مولکولی پایین یک عامل غیر اختصاصی است زیرا به دلیل سمیت سیانید منتشر می شود و باعث حذف آن می شود.76 طبق گفته Makarevi´c و همکاران، 29 سلول سرطانی مثانه تحت تأثیر غلظت کمتر آمیگدالین قرار نگرفتند. بیش از 15 میلی مول در لیتر با این وجود، تحریک بتا گلوکوزیداز رشد و مهاجرت سلولی را کاهش داد. آپوپتوز به صورت وابسته به دوز افزایش یافت و سلول ها در مرحله S خاتمه یافتند.77
15. آمیگدالین و بتا گلوکوزیداز در درمان سرطان
آمیگدالین به دلیل خواص ضد توموری آن به عنوان یک کمک کمکی در درمان سرطان استفاده شده است. نشان داده شده است که آمیگدالین به افراد مبتلا به علائم پیشرفته سرطان کمک می کند و عمر آنها را افزایش می دهد. آمیگدالین می تواند تا حدودی کارسینوم پلور یا جانبی را مدیریت و کاهش دهد.76 در شرایط آزمایشگاهی، محصولات هیدرولیتیک آمیگدالین، اسید هیدروسیانیک و بنزآلدئید اثرات ضد سرطانی نشان می دهند. اسید هیدروسیانیک سلول های تومور را با جلوگیری از تشکیل آدنوزین تری فسفات و مهار CCO، آنزیم انتهایی در زنجیره انتقال الکترون میتوکندری، به دلیل فعالیت بتا گلوکوزیداز بر روی آمیگدالین، از بین می برد. آمیگدالین برای درمان موش های دارای تومورهای کاشته شده ارزیابی شده است. آمیگدالین همچنین می تواند در ترکیب با سایر داروها برای درمان سرطان پوست استفاده شود. درمان سلولهای LoVo با ترکیبی از آمیگدالین (0.1، 0.5 و 1.1 mmol/L) و بتا گلوکوزیداز (250 نانومول در لیتر) به مدت 24 ساعت باعث ارتقاء آپوپتوز و نکروز شد. طبق یک تحقیق تغییرات مورفولوژیکی مشخصه ای که در طول آپوپتوز رخ می دهد با استفاده از الکتروفورز ژل DNA و فلوسیتومتری تایید شده است. در نتیجه، آمیگدالین ممکن است یک عامل جدید در درمان تومور با ترویج آپوپتوز باشد. آمیگدالین همچنین برای درمان سرطان روده بزرگ به عنوان یک پیش دارو استفاده شده است. آمیگدالین به عنوان یک سیانید طبیعی تولید کننده پیش دارو در نظر گرفته می شود که بیان Bax و فعالیت کاسپاز{17}} را در سلول های LoVo، که هر دو در آپوپتوز نقش دارند، افزایش می دهد.
ایده اولیه آنزیم درمانی با پیش دارودرمانی در درمان سرطان ها با استفاده از یک کمپلکس خاص آنتی بادی بتا گلوکوزیداز با استفاده از یک عامل اتصال متقابل و یک آنزیم فعال کننده در شرایط آزمایشگاهی، استفاده از یک کمپلکس خاص آنتی بادی بتا گلوکوزیداز با یک آنزیم فعال کننده و یک آنزیم فعال کننده است. عامل اتصال متقابل. 89 آنتی ژن های سطح سلول سرطانی توسط بتا گلوکوزیداز با استفاده از آنتی بادی ها هنگامی که این ترکیب به صورت داخل وریدی داده شود، شناسایی می شود. پیش داروی آمیگدالین توسط بتا گلوکوزیداز فعال می شود و به محل هدف تومور می چسبد و به آن توانایی تخریب آن را می دهد. لیان و همکارانش مدل موش سرطان کولورکتال انسان را توسعه دادند. یک مولکول بتا گلوکوزیداز ضد CEA McAb به رگهای دم موشها تزریق شد و سپس 50 میلیگرم بر کیلوگرم آمیگدالین سه بار در هفته به مدت شش هفته تزریق شد. 19،84–86،88 قبل و بعد از تزریق، تومور مهار، و حجم تومور تعیین شد. از این رو، تغییرات پاتولوژیک در بافتهای تومور موش و اندامهای اولیه شناسایی شد. یافتههای آنها در مدل موش سرطان کولورکتال نشان میدهد که یک سیستم پیش داروی آمیگدالین کونژوگه همراه با مولکول بتا گلوکوزیداز ضد CEA McAb به طور قابلتوجهی توسعه زنوگرافت را محدود میکند. از سوی دیگر، اندام ها هیچ نشانه ای از سمیت سلولی نشان ندادند. پپتیدهای غشای سلولی پلی پپتیدهای 1 با 30 اسید آمینه یا کمتر هستند که ممکن است طیف وسیعی از ترکیبات بیولوژیکی را به داخل سلول منتقل کنند. بتا گلوکوزیداز باعث افزایش نفوذ آنزیم به سلول های اندوتلیال مویرگی و تومورهای جامد خارج سلولی عمیق می شود که منجر به مرگ سلول های تومور می شود.
16. نتیجه گیری
آمیگدالین به عنوان درمانی برای طیف وسیعی از مسائل پزشکی از جمله لوکودرما، جذام، برونشیت، تهوع و سرفه پیشنهاد شده است. مطالعات آزمایشگاهی و حیوانی فواید هضم و تولید مثل و همچنین کاهش سمیت عصبی، هیپرتروفی قلبی و سطوح گلوکز را تایید کردهاند. تحقیقات قبلی عمدتاً بر روی اثربخشی و ایمنی دارویی آمیگدالین متمرکز بوده است، بنابراین دانش ما در مورد مسیرهای مولکولی زیربنای اعمال آن هنوز در مراحل اولیه است. از آنجایی که در حال حاضر اطلاعات کافی برای پشتیبان گیری از این درمان وجود ندارد، باید با احتیاط دنبال شود. اطلاعات کمی در مورد فارماکوکینتیک آمیگدالین یا سمیت سیستمیک آن وجود دارد. برای تعیین پتانسیل درمانی، ایمنی و اثرات نامطلوب این ترکیب، مطالعات ابتکاری مورد نیاز است. برای درک کامل اثرات سلامتی به مطالعه بیشتری نیاز است. برخی از نمونه ها عبارتند از: قلب بیش فعال، دیابت، التهاب، مشکلات گوارشی، تخریب عصبی و تولید مثل. اگرچه اکنون اطلاعات بیشتری نسبت به قبل در دسترس است، اما هنوز برای تجزیه و تحلیل قطعی کافی نیست. تحقیقات اخیر نشان داده است که مصرف خوراکی آمیگدالین خطرناکتر از تزریق آن است. علیرغم نتایج امیدوارکننده در شرایط آزمایشگاهی از جفت شدن آمیگدالین-نانوحامل، تأیید بیشتر in vivo این یافته ها مورد نیاز است. کارآزماییهای بالینی نشان دادهاند که آمیگدالین/-Glu MDEPT یک استراتژی موثر است. فواید درمانی و عوارض جانبی آمیگدالین را می توان با تحقیقات بیشتر در مورد کپسولاسیون و پتانسیل ضد سرطانی آن افزایش داد.

در دسترس بودن داده ها
داده های مورد استفاده برای حمایت از یافته های این مطالعه در صورت درخواست معقول از نویسنده مسئول در دسترس است.
اعلامیه منافع رقابتی
نویسندگان هیچ تضاد منافعی را اعلام نمی کنند.
قدردانی
این پژوهش با پشتیبانی بخش ایمونوژنتیک گروه ایمونولوژی و آلرژی دانشکده پزشکی دانشگاه علوم پزشکی مشهد انجام شد.
منابع
1 Makarevi´c J, Tsaur I, Juengel E, et al. آمیگدالین با کاهش سیکلین A و CDK از رشد سلول های سرطانی مثانه در شرایط آزمایشگاهی جلوگیری می کند.
2. PLoS One. 2016؛ 147 (8): 137-142. https://doi.org/10.1371/journal.pone.0105590. 2 Boehm SMEL، Milazzo S، Horneber M، Ernst E، Stefania MilazzoMarkus HorneberEdzard Ernst. درمان سرطان لاتریل برادر بیومد بول. 2017؛ 5 (4): 296.https://doi.org/10.1002/14651858.CD005476.pub4.
3 جمشیدزاده ع، راسخ HRR، امین LM، و همکاران. فعالیت رودانز و آرژیناز در بافت های طبیعی و سرطانی سینه، مری، معده و ریه انسان. آرک ایران مد. 2001؛ 4(2): 88–92، 242514105_رودانی_و{8}}ARGINASE{9}}فعالیت{10}} در{11}}عادی{12 }} و{ و{21}}ریه.
4 Moon JYY، Kim SWW، Yun GMM، و همکاران. مهار رشد سلولی و کاهش فعالیت تلومراز توسط آمیگدالین در رده های سلولی سرطانی انسان Anim Cell System. 2015؛ 19 (5): 295-304. https://doi.org/10.1080/19768354.2015.1060261.
5 Chen C، Xu F، Yuan S، و همکاران. تجزیه و تحلیل ریسک رقابتی مرگ قلبی عروقی در بیماران مبتلا به سرطان اولیه کیسه صفرا داروی سرطان؛ 2022. https://onlinelibrary. wiley.com/doi/full/10.1002/cam4.5104.
6 Syrigos ON، Rowlinson-Busza G، Epenetos AA، Syrigos KN، Rowlinson-Busza G، Epenetos AA. در شرایط آزمایشگاهی، سمیت سلولی بدنبال فعال سازی خاص آمیگدالین توسط -گلوکوزیداز کونژوگه به یک آنتی بادی مونوکلونال مرتبط با سرطان مثانه. Int J سرطان. 1998؛ 78 (6): 712-719. https://doi.org/10.1002/(sici)1097-0215(19981209) 78:6<712::aid-ijc8>3.0.co;2-د.
7 Chang HK، Shin MS، Yang HY، و همکاران. آمیگدالین از طریق تنظیم بیانهای Bax و Bcl{1}} در سلولهای سرطان پروستات DU145 و LNCaP انسان، آپوپتوز را القا میکند. بیول فارم بول. 2006؛ 29 (8): 1895-1904. https://doi.org/10.1248/bpb.29.1597.
مطالعات سمیت آمیگدالین در موشهای صحرایی، مسمومیت مزمن سیانید را در انسان پیشبینی میکند. وست جی مد. 1981؛ 134 (2): 97.https://pubmed.ncbi.nlm.nih.gov/7222669/.
9 Torre LA، Siegel RL، Ward EM، Jemal A. نرخ و روند جهانی بروز سرطان و مرگ و میر - یک به روز رسانی.
10 Rayan A, Raiyn J, Felah M. Nature بهترین منبع داروهای ضد سرطان است: نمایه سازی محصولات طبیعی برای فعالیت زیستی ضد سرطانی آنها. PLoS One. 2017; 12(11), e0187925.https://doi.org/10.1371/journal.pone.0187925.
11 Makarevi´c J, Tsaur I, Juengel E, et al. آمیگدالین پیشرفت چرخه سلولی را به تاخیر می اندازد و رشد سلول های سرطانی پروستات را در شرایط آزمایشگاهی مسدود می کند. زندگی علمی. 2016؛ 147:137-142. https://doi.org/10.1016/j.lfs.2016.01.039.
12 Ogata K، Volini M. Rhodanese میتوکندری: فعالیت متصل به غشاء و کمپلکس. جی بیول شیمی. 1990؛ 265 (14): 8087-8093. https://pubmed.ncbi.nlm.nih.gov /2335518/.
13 Koˇzich V، Ditroi ´ T، Sokolova ´ J، و همکاران. متابولیسم ترکیبات گوگرد در هموسیستینوریا. Br J Pharmacol. 2019؛ 176 (4): 594-606. https://doi.org/10.1111/ bph.14523. 14 Cipollone R، Ascenzi P، Tomao P، Imperi F، Visca P. سم زدایی آنزیمی سیانید: سرنخ هایی از سودوموناس آئروژینوزا رودانی. جی مول میکروبیول بیوتکنول. 2008؛ 15 (2-3): 199-211. https://doi.org/10.1159/000121331.
15 ایاز ز، زینب ب، خان س، و همکاران. در سیلیکو احراز هویت آمیگدالین به عنوان یک ترکیب ضد سرطانی قوی در هسته تلخ خانواده Rosaceae. عربستان جی بیول Sci. 2020; 27 (9): 2444-2451. https://doi.org/10.1016/j.sjbs.2020.06.041.
16 Kleessen B, Sykura B, Zunft HJ, Blaut M. اثرات اینولین و لاکتوز بر میکرو فلور مدفوع، فعالیت میکروبی و عادت روده در افراد مسن یبوست. من جی کلین نوتر هستم. 1997؛ 65 (5): 1397-1402. https://doi.org/10.1093/ajcn/65.5.1397.
17 البوگامی س، حسن ع، احمد ن، و همکاران. ارزیابی دوز موثر آمیگدالین برای بهبود بیان ژن آنتی اکسیدانی و سرکوب آسیب اکسیداتیو در موش. PeerJ. 2020؛ 8، e9232. https://doi.org/10.7717/peerj.9232.
18 Mani J, Rutz J, Maxeiner S, et al. سطوح سیانید و لاکتات در بیماران در طول مصرف مزمن آمیگدالین خوراکی و به دنبال آن تزریق داخل وریدی آمیگدالین. Compl The Med. 2019؛ 43:295–299. https://doi.org/10.1016/j.ctim.2019.03.002.
19 Li Y طولانی، Xing Li Q، Jiang Liu R، Qian Shen X. داروی چینی آمیگدالین و گلوکوزیداز همراه با سیستم پیش داروی آنزیمی آنتی بادی به عنوان یک درمان ضد تومور عملی. Chin J Integr Med. 2018;24(3):237–240، 0.1007/s11655-015- 2154-x.
20 امینلری مریم، ملکحسینی علی، اکرمی فر، ابراهیم نژاد ح. آنزیم متابولیزه کننده سیانور رودانز در بافت انسان: مقایسه با حیوانات اهلی. کامپ کلین پاتول. 2007؛ 16 (1): 47-51. https://doi.org/10.1007/s00580-006-0647-x.
For more information:1950477648nn@gmail.com
