مصونیت سلول T از قبل موجود در برابر SARS-CoV-2 در کنترلهای سالم در معرض خطر در اکوادور، همانطور که با آزمایش انتشار اینترفرون-گاما COVID{4}} شناسایی شد
Mar 13, 2023
خلاصه
زمینه و هدف: مطالعات پاسخ های ایمنی سلول های T در برابر SARS-CoV-2 در درک وضعیت ایمنی افراد یا جمعیت ها مهم است. در اینجا، ما از یک آزمایش ساده، ارزان و سریع تحریک خون کامل - یک سنجش رهاسازی اینترفرون گاما (IGRA) - برای مطالعه ایمنی سلول T در برابر SARS-CoV-2 در بیماران مبتلا به کووید-19 در حال نقاهت استفاده میکنیم. و تماس های سالم از کیتو، اکوادور. روش ها: تولید اینترفرون گاما (INF-g) در خون هپارینه شده افراد در حال نقاهت و افرادی که در معرض آن قرار نگرفته بودند پس از تحریک به مدت 24 ساعت با پروتئین SARS-CoV{14}} Spike S1، پروتئین دامنه اتصال گیرنده (RBD) یا پروتئین نوکلئوکپسید (NP) به ترتیب. حضور آنتی بادی های پروتئین IgG-RBD در هر دو گروه مورد مطالعه با یک ELISA "در خانه" تعیین شد. یافتهها: همانطور که با تولید INF-g اندازهگیری شد، 80 درصد از بیماران مبتلا به کووید{20}} در حال نقاهت، که همگی IgG-RBD مثبت بودند، پاسخ سلولهای T قوی داشتند.
با این حال، به طور غیرمنتظره، 44 درصد از افراد سالم سالم که در معرض تماس قرار نگرفته بودند، که همگی IgG-RBD منفی بودند، یک پاسخ سلول T ویژه ویروس قوی با COVID{4}} IGRA داشتند، احتمالاً به دلیل قرار گرفتن قبلی در معرض ویروسهای کروناویروس عامل سرماخوردگی معمولی یا موارد دیگر. آنتی ژن های ویروسی یا میکروبی نتیجهگیری و بحث: درصد بالای افراد سالم مواجه نشده با ایمنی از قبل نشان میدهد که بخشی از جمعیت اکوادور احتمالاً دارای سلولهای T واکنشپذیر SARS-CoV{8}} هستند. با توجه به اینکه تکنیک IGRA ساده است و میتواند به راحتی برای تحقیقات در مواردی که تعداد بالایی از بیماران مورد نیاز است، مقیاسبندی شود، این IGRA کووید{10} ممکن است برای تعیین اینکه آیا پاسخ تنها سلول T نشاندهنده مصونیت محافظتی در برابر SARS-CoV است یا خیر. -2 عفونت در یک مطالعه مبتنی بر جمعیت. © 2021 نویسندگان. توسط Elsevier Ltd به نمایندگی از انجمن بین المللی بیماری های عفونی منتشر شده است.
در عین حال، هنگامی که ایمنی بدن ما پایین است، راههای زیادی برای بهبود ایمنی وجود دارد، مصرف غذاهایی که میتوانند ایمنی را تقویت کنند، مانند سیستانچ، پلیساکاریدها، پروتئینها، اسیدهای آمینه و سایر مواد موجود در سیستانچ اغلب میتوانند بدن را تنظیم کنند.iسیستم ایمنی

محصول پودر عصاره cistanche tubulosa را کلیک کنید
معرفی
پاسخ ایمنی به عفونت SARS-CoV{1}} نه تنها شامل تولید آنتی بادی میشود، بلکه عفونت همچنین باعث ایجاد پاسخ سلول T در بیماران میشود (لیپسیچ و همکاران، 2020، نی و همکاران، 2020). به طور کلی، تعیین حضور و میزان پاسخ سلول T حافظه خاص به این عفونت کروناویروس با سنجش ELISPOT با تعیین تعداد لنفوسیتهایی که پس از تحریک با آنتیژنها یا پپتیدهای خاص بیماری (Ni) IFN-g تولید میکنند، انجام میشود. و همکاران، 2020، پای و همکاران، 2014، آبات و همکاران، 2013، براون و همکاران، 2020، گریفونو و همکاران، 2020، لیبرت و همکاران، 2020، سکین و همکاران، 2020).
برای این روش، سلولهای تک هستهای خون محیطی (PBMCs) از خون تازه هپارینه شده با سانتریفیوژ با گرادیان چگالی جدا میشوند. ترشح سیتوکینها توسط سلولهای T منفرد با میکروسکوپ یا با یک دستگاه خاص - صفحهخوان ELISPOT اندازهگیری میشود. روش ELISPOT یک روش «فقط برای آزمایشگاههای تحقیقاتی» است که بسیار پر زحمت، از نظر فنی سخت، نسبتاً گران است و نمیتوان آن را به راحتی در آزمایشگاه بالینی یا در مطالعات مبتنی بر جمعیت به کار برد. با توجه به هزینه، زیرساخت و الزامات آزمایشگاهی مورد نیاز برای انجام سنجش، استفاده از آن در تنظیمات با منابع محدود مانند اکوادور ممکن است حداقل باشد.
پاسخهای ایمنی سلولی را میتوان با یک روش سادهتر نیز تعیین کرد: سنجش آزادسازی اینترفرون-گاما (IGRA). این آزمایش، یک آزمایش خون آزمایشگاهی، سیتوکین های ترشح شده از سلول T (یعنی گاما اینترفرون (IFN-g) را تعیین می کند؛ با این حال، سایر سایتوکین ها مانند TNF یا IL{3}} را نیز می توان با تحریک کل خون تعیین کرد. (نه فقط لنفوسیت های جدا شده) با آنتی ژن های خاص (Pai et al., 2014, Abate et al., 2013). سیتوکین ترشح شده IFN-g با روش الایزا اندازه گیری می شود، روشی که در اکثر آزمایشگاه ها به راحتی در دسترس است، و نتایج با صفحه خوان الایزا خوانده می شود. IGRA ها در آزمایشگاه بالینی کاربرد پیدا کرده اند و برای تعیین عفونت نهفته با مایکوباکتریوم توبرکلوزیس (MTB) و همچنین برای اندازه گیری ایمنی سلولی خاص سیتومگالوویروس (CMV) و پیش بینی عفونت CMV در گیرندگان پیوند استفاده می شوند (Pai et al. ، 2014، Abate و همکاران، 2013). این تستهای IGRA بهطور گسترده مورد ارزیابی قرار گرفتهاند و در مقایسه با روش ELISPOT، قابلیتهای مشابهی را برای پیشبینی عفونت MTB یا CMV نشان میدهند. علاوه بر این، چندین سنجش تجاری و دارای علامت FDA یا CE برای تشخیص ایمنی در برابر سل یا CMV در دسترس است و به طور گسترده انجام می شود.
در مطالعه حاضر، استفاده از COVID{0}} IGRA را بررسی میکنیم و میزان انتشار IFN-g را در بیماران کووید-19 در حال نقاهت و کنترلهای ساده COVID{3}} سالم در پاسخ به موارد خاص ارزیابی میکنیم. آنتی ژن های ویروس SARS-CoV-2: پروتئین RBD. بخش S1 پروتئین اسپایک؛ یا پروتئین نوکلئوکپسید (N). علاوه بر این، ما حضور آنتیبادیهای IgG اختصاصی SARS-CoV-2 را در آن شرکتکنندگان با الایزای داخلی تعیین میکنیم (Amanat et al., 2020, Guevara et al., 2021). ما نشان میدهیم که درصد قابلتوجهی از اهداکنندگان بدون مواجهه، دارای سلولهای T واکنشپذیر SARS-CoV{13}} هستند و این نتایج را مورد بحث قرار میدهیم.
مواد و روش ها
بیماران کووید{0}} در حال نقاهت، کنترلهای سالم، و محیط
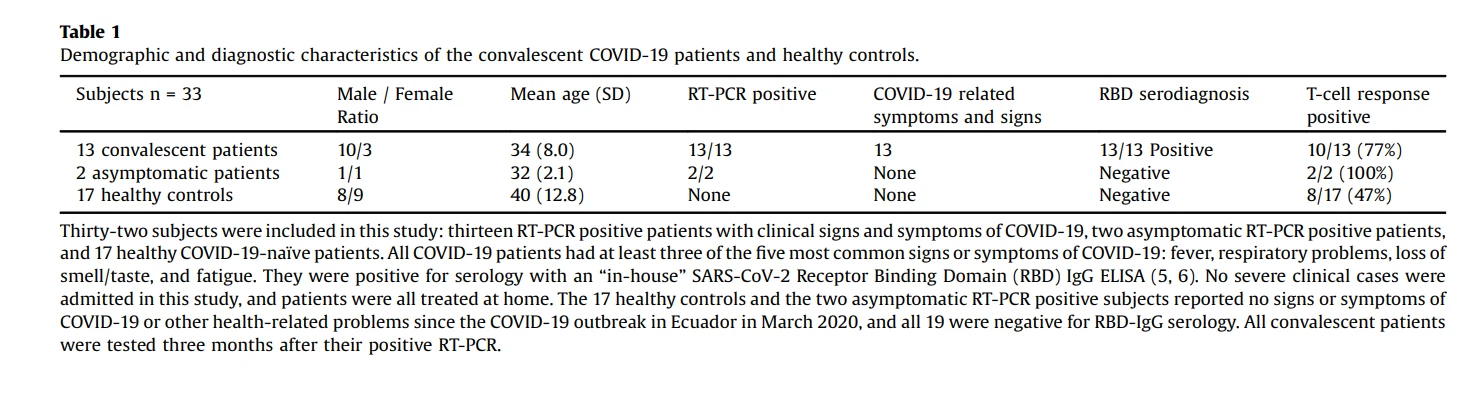
این مطالعه در شهر کویتو، اکوادور، در سپتامبر 2020 انجام شد. هیچ روش آماری برای از پیش تعیین حجم نمونه استفاده نشد. جدول 1 ویژگیهای 32 بیمار در این مطالعه را نشان میدهد: سیزده بیمار مبتلا به کووید-19 در حال نقاهت، همه با علائم/نشانههای COVID{{5} غیر شدید و تشخیص RT-PCR مثبت در ژوئن 2020. و 17 کنترل سالم بدون مواجهه. این کنترلهای سالم در طول همهگیری بسیار محتاط بودند، از تماس با افراد دیگر اجتناب میکردند، و هیچ یک از علائم و نشانههای معمول کووید{10}} را در طول مدت همهگیری، مانند تب، سرفه مداوم، گزارش نکردند. یا از دست دادن بویایی یا چشایی همچنین، دو ناقل بدون علامت SARS-CoV{12}} در این مطالعه وارد شدند. این دو آزمودنی هرگز هیچ علامت یا نشانه ای از بیماری کووید-19 نشان ندادند. با این حال، تکنیک RT-PCR بر روی آنها به عنوان یک نیاز برای مجوز کار در ژوئن 2020 انجام شد و منجر به تشخیص مثبت شد.
سرولوژی
سرولوژی و IGRA برای همه بیماران و گروه کنترل در دو هفته آخر سپتامبر 2020، سه ماه پس از تشخیص RT-PCR بیماران در حال نقاهت انجام شد. برای تعیین حضور آنتیبادیهای IgG اختصاصی کرونا در گروه مطالعه ما، از یک دامنه اتصال گیرنده SARS-CoV{5}} ELISA IgG (9، 10) "داخلی" استفاده شد.

سنجش رهاسازی اینترفرون گاما (IGRA)
برای IGRA، یک نمونه خون هپارینه شده (4 میلی لیتر) گرفته شد و به مقادیر 250 میلی لیتری تقسیم شد و به ترتیب با 2 میلی گرم در میلی لیتر پروتئین RBD (روش جداسازی از مرجع 9) یا 2 میلی گرم بر میلی لیتر از نوکلئوکپسید تجاری موجود تحریک شد. (N) پروتئین یا پروتئین Spike (S1) (ViroGen، شماره کاتالوگ: به ترتیب 00،221-V و 00،226-V). منحنی غلظت-پاسخ دوز با خون بیماران IGRA مثبت و IGRA منفی برای تعیین غلظت بهینه آنتی ژن برای تحریک در IGRA استفاده شد. در 2 میکروگرم در میلیلیتر، حداکثر پاسخ IFN-g در خون افراد مبتلا به کووید{15}} بدون تحریک در گروه کنترل غیر آلوده مشاهده شد. برای هر شرکتکننده، یک کنترل تحریکنشده (NIL) گنجانده شد، و ما یک نمونه خون 250 میلیلیتری را با میتوژن فیتوهاماگلوتینین (PHA)، یک کنترل مثبت برای ارزیابی میزان پاسخ سیتوکین نمونه خون مورد سنجش قرار دادیم. تحریک در یک 96-صفحه ELISA با کف صاف در دمای 37 درجه سانتیگراد به مدت 24 ساعت انجام شد. پلاسما برداشت شد و تولید IFN-g با ELISA انسانی IFN-g تعیین شد (MaxTM Standard Set Biolegen cat. No. 430,101).
نتایج
RBD IgG ELISA نشان داد که همه بیماران علامت دار COVID{{{0}} (RT-PCR مثبت) سه ماه پس از تشخیص RT-PCR از نظر آنتی بادی IgG علیه پروتئین RBD مثبت بودند. دو بیمار بدون علامت RT-PCR مثبت و همه بیماران سالم سالم بدون مواجهه با این الایزا سرم منفی بودند (جدول 1 را ببینید). نتایج تحریک خون کامل در روش COVID{5}} IGRA در شکل 1 نشان داده شده است. القای قوی تولید IFN-g در 80 درصد از بیماران علامت دار COVID-19 با هر سه آنتی ژن، اما پروتئین N و پروتئین S قوی ترین محرک های پاسخ IFN-g بودند (شکل 1 A, B, C). دو بیمار بدون علامت اما RT-PCR مثبت (بیماران 14 و 15)، هر دو بدون آنتی بادی SAR-CoV{17} خاص، همچنین یک پاسخ ایمنی القایی سلول T قوی نشان دادند. از بیماران ساده کووید{19}}، 45 درصد ایمنی سلول T القایی را نشان دادند. پاسخ در این گروه شاهد سالم با پاسخ سلول T از نظر اندازه تفاوت معنیداری با بیماران مبتلا به کووید{23}} در حال بهبودی برای هیچ یک از آنتی ژنهای محرک نداشت (p-value=0.271, 0.437, و 0.719 برای پروتئین های RBD، N و S1 به ترتیب).

شکل 1. تولید IFN-g پس از تحریک خون کامل بیماران مبتلا به کووید-19 در حال نقاهت و افراد سالم سالم با پروتئین RBD، N، یا S1.
نتایج تحریک بیماران در حال نقاهت و گروه شاهد با پروتئین RBD، N یا S1 به ترتیب در شکل 1A، B و C نشان داده شده است. در شکل 1D، پاسخ INF-g هر بیمار و به سه مورد نشان داده شده است. آنتی ژن ها گروه بندی می شوند. بیماران مبتلا به عفونت تایید شده کووید{4} 15-1 شماره دارند که از این تعداد بیماران 14 و 15 بدون علامت بودند. افراد 16 تا 33، بیماران ساده کووید{11}} هستند.
پس از 24 ساعت تحریک، غلظت IFN-g در پلاسما با استفاده از کیت مبتنی بر سنجش ایمنی متصل به آنزیم IFN-g انسانی در دسترس تجاری تعیین شد (Biolegend cat. No. 43{10}},101). بزرگی تحریک به عنوان چگالی نوری در 450 نانومتر (OD450) برای خون تحریک شده با آنتی ژن منهای OD450 برای خون بدون تحریک آنتی ژن بیان شد. OD 1.0 با تقریباً 400 pg/mL IFN-g مطابقت داشت. فیتوهماگلوتینین (PHA) به عنوان میتوژن در غلظت نهایی 5 میلی گرم در میلی لیتر در IGRA برای ارزیابی کیفیت و ظرفیت پاسخ خون استفاده شد. همه بیماران و گروه شاهد حداکثر تولید سیتوکین را با این میتوژن با میانگین چگالی نوری (OD450) 2.54 (SD=0.13) نشان دادند که تقریباً 1000 pg/mL IFN-g را نشان میدهد. هیچ تفاوتی در سطح متوسط IFN-g در خون تحریک نشده بیماران نقاهت و افراد سالم مشاهده نشد (OD{22}}.38، SD=0.14 در مقابل OD450=0.32. SD=0.16). این نتایج نشان داده نشده است. در هر نمودار یک خط افقی برای نشان دادن مقدار برش برای تحریک ترسیم شده است. این مقدار با محاسبه میانگین به علاوه دو انحراف استاندارد پاسخ 9 نفر (بیماران 16، 18، 19، 22، 27-31) از گروه کنترل با کمترین تولید INF-g پس از تحریک تعیین شد.

بحث و نتایج
با استفاده از یک آزمایش خون کامل با انجام آسان که پاسخهای سلول T را ارزیابی میکند، متوجه شدیم که اکثر بیماران در حال نقاهت و بخش قابل توجهی از افراد سالم که در معرض آن قرار نگرفتهاند، پاسخ سلول T خاص و قوی دارند که با تولید INF-g پس از تحریک تعیین میشود. با آنتی ژن های اختصاصی SARS-CoV-2 (شکل 1). چندین مطالعه، که همگی از روش ELISPOT استفاده میکنند، وجود پاسخ سلول T را در اکثر یا همه بیماران مبتلا به کووید{9}} در حال نقاهت گزارش کردهاند (براون و همکاران، 2020، گریفونو و همکاران، 2020، لبرت و همکاران. ، 2020، سکین و همکاران، 2020، مدرباچر و همکاران، 2020، ماتئوس و همکاران، 2020، پنگ و همکاران، 2020).
با این حال، در مورد پاسخ سلول T در افراد سالم سالم، نرخ پاسخ بین 28 تا 50 درصد گزارش شده است (Doshi, 2020, de Vries, 2020, Lipsitch et al., 2020, Sagar et al., 2020) و چندین مورد مطالعات عدم پاسخ سلول T را در بیماران کنترل ساده کووید{8}} گزارش نمیکنند (de Vries, 2020, Moderbacher et al., 2020, Schwarzkopf et al., 2021). بیشتر این مطالعات با روش ELISPOT انجام شد، اما در ایتالیا و ایالات متحده، از IGRA نیز برای تشخیص پاسخ سلول T SARS-CoV استفاده شده است (Petrone et al., 2020, Murugesan et al. .، 2020). در هر دو مطالعه، یک پاسخ خاص سلول T در بیماران در حال نقاهت تشخیص داده شد. با این حال، IGRA پاسخ INF-g را در افراد سالم تشخیص نداد.
ایمنی سلول های T از قبل موجود نسبت به SARS-CoV-2 در افراد ساده کووید{4}} در چندین نشریه بررسی شده است (آلتمن و بویتون، 2020، دوشو و همکاران، 2020، دی وریس، 2020، ست و کروتی، 2020). دلیل اینکه چرا ممکن است پاسخ سلول T خاص کووید{9}} در یک سوژه سالم که در معرض تماس قرار نگرفته باشد، مشخص نیست و موضوع حدس و گمان است. اکثر مطالعات ELISPOT با افراد ساده کووید{11}} از نمونههای خون انسان استفاده میکردند که قبل از کشف ویروس SARS-CoV-2 در سال 2019، بنابراین قبل از هرگونه احتمالی برای قرار گرفتن در معرض قرار گرفتند. به همین دلیل، این مطالعات ELISPOT به این نتیجه رسیدند که پاسخ سلول T در افراد سالم در معرض تماس قبلی احتمالاً از تماس قبلی با ویروسهای «سرماخوردگی معمولی» در گردش (گریفونی و همکاران، 2020، متئوس و همکاران، 2020) یا مواجهه قبلی با آنفولانزا ناشی میشود. و/یا ویروس های CMV (Mahajan et al., 2020) یا سایر آنتی ژن های ویروسی یا میکروبی (Tan et al., 2020). مطالعه ما از خون گرفتهشده در طول همهگیری از داوطلبانی استفاده کرد که تماس صفر را خود گزارش کردند، برای آنتیژن COVID{21} RBD منفی بود و هرگز علائم یا نشانههای COVID-19 را نشان ندادند.
بنابراین، نمیتوانیم این نکته را رد کنیم که پاسخ سلولهای T در برخی از کنترلهای سالم «ساده» COVID{1}} ما ناشی از عفونتهای بدون علامت ویروس SARS-CoV-2 باشد. بیماران 14 و 15 مطالعه ما نمونه ای از این هستند. این افراد به دلیل مثبت بودن RT-PCR به عنوان بیماران کووید-19 طبقه بندی شدند. با این حال، آنها بدون علامت بودند و پاسخ آنتی بادی علیه پروتئین RBD ایجاد نکردند، اما هر دو یک پاسخ سلول T قوی نشان دادند.
این امکان وجود دارد که پس از کلونیزاسیون نازوفارنکس SARS-CoV{1}، سیستم ایمنی این دو بیمار بدون علامت، آنها را با یک پاسخ فقط Tcells حافظه مواجه کرده باشد و هیچ آنتی بادی اختصاصی SARS-CoV{4} وجود نداشته باشد. القاء شده. توضیح دیگر این است که پاسخ سلول T ناشی از یک عفونت مشابه کرونای قبلی است و پاسخ ایمنی سلول T از قبل موجود، از این دو بیمار در برابر ایجاد یک الگوی بیماری تهاجمی تر محافظت می کند. سلولهای T متقابل واکنشی از قبل میتوانند در توضیح برخی از تفاوتها در میزان عفونت یا آسیبشناسی مهم باشند (Le Bert et al., 2020, Sagar et al., 2020). در مورد گروه کنترل های ساده، ما این گروه را مستثنی کردیم که تعداد قابل توجهی از افراد آلوده به SARSCoV{14}} با عفونت بدون علامت شناسایی نشده باشد، اساساً به این دلیل که همه ادغام های گروه کنترل برای آنتی ژن RBD IgG منفی هستند.
دلیل دیگر این است که شیوع عفونت در اکوادور نسبتاً کم است. در زمان انجام این مطالعه، در سپتامبر 2020، اکوادور حدود 200 مورد تایید شده کووید-19 (حدود 1.1 درصد از جمعیت) را گزارش کرده بود. البته، شیوع واقعی عفونت میتوانست چندین برابر بیشتر باشد، اما با این وجود، بعید است که 45 درصد از این گروه کنترل آلوده شده باشند و بنابراین ما به دنبال پاسخ سلول T خاص برای SARS-CoV هستیم. {9}} عفونت.
در نتیجه، یافتن درصد بالایی از افراد سالم مواجه نشده با ایمنی از قبل در کیتو، اکوادور، این انتظار را افزایش میدهد که بخش قابل توجهی از جمعیت ما احتمالاً دارای سلولهای T واکنشی SARS-CoV-2 هستند، زیرا مواجهه قبلی با آنفولانزا، ویروسهای CMV یا کروناویروسهای عامل سرماخوردگی معمولی. هدف تحقیقات آینده باید تعیین این باشد که آیا پاسخ ایمنی از قبل موجود، محافظ است و/یا میتواند بر بیماری شدیدتر کووید{6} غلبه کند یا به بهبودی سریعتر کمک میکند.
اهمیت و محدودیت این مطالعه
مطالعه ما نشان داد که COVID{0}} IGRA یک ابزار جدید مفید و حساس است که میتواند قرار گرفتن در معرض کروناویروسها یا واکنش متقابل به ویروسهای مشابه را با تعیین آزادسازی IFN-g پس از تحریک با آنتیژنهای خاص ویروس ارزیابی کند. این تکنیک ساده، نسبتا ارزان است و می تواند در آزمایشگاه بالینی استفاده شود. این مطمئناً در مورد سنجش ELISPOT صدق نمی کند. علاوه بر این، سنجش IGRA را می توان به راحتی برای مطالعات و تحقیقات مبتنی بر جمعیت که در آن تعداد زیادی بیمار مورد نیاز است، افزایش داد. همراه با سرولوژی، IGRA میتواند برای غربالگری پاسخ آنتیبادی و سلولهای T بیماران منفرد برای درک بهتر ایمنی در سطح جمعیت و تعیین ایمنی از قبل موجود در افراد دارای سرم منفی استفاده شود.
محدودیت مهم مطالعه ما این است که نمونه مورد مطالعه معرف جامعه نیست. هیچ روش آماری برای از پیش تعیین حجم نمونه استفاده نشده است. علاوه بر این، سنجش ما بین تولید IFN-g سلولهای CD4 پلاس یا CD8 پلاس تفاوتی قائل نشد، اما تحریک با پپتیدهای CD8(+) و CD4(+) را میتوان در نظر گرفت (Grifoni et al., 2020, Peng et al.). ، 2020) و در IGRAهای شرح داده شده در Petrone و همکاران، 2020 و Murugesan و همکاران، 2020 استفاده شده است. همچنین، القای سایر سیتوکین ها را می توان با این IGRA اندازه گیری کرد (Petrone et al., 2020). به همین ترتیب، IGRA می تواند برای پیگیری واکسیناسیون برای تعیین توسعه پاسخ سلول T در افراد واکسینه شده استفاده شود یا می تواند برای تعیین اینکه آیا وجود سلول های T حافظه واکنش متقابل با ایمنی محافظتی مرتبط است و می تواند استفاده شود. تظاهرات بیماری ناشی از عفونت SARS-CoV{15}} را کاهش دهد (ساگار و همکاران، 2020).

تایید اخلاق و رضایت مشارکت
خون پس از رضایت کتبی آگاهانه جمع آوری شد. کمیته اخلاق وزارت بهداشت اکوادور پروتکل مطالعه 004-2020 را تایید کرد.
تضاد علایق
نویسندگان اعلام می کنند که هیچ منافع رقابتی ندارند.
مشارکت های نویسنده
طراحی مطالعه؛ JHW و GE; جمع آوری داده ها و آزمایش های آزمایشگاهی: GE، AG، JC، AMR، و MMV. تحلیل داده ها؛ JHW، GE، و ET. نوشتن: JHW، GE، و ET.
قدردانی
ما از همه اهداکنندگان و پرسنل مراقبت های بهداشتی درگیر در این کار، به ویژه Sandra Vivero و Sandra Fonseca، برای کمک در جمع آوری نمونه تشکر می کنیم. این مطالعه توسط یک صندوق تحقیقاتی از Universidad de las Américas حمایت شده است. مؤسسه علوم پایدار، سانفرانسیسکو، کالیفرنیا، ایالات متحده، و بنیاد «پور تودوس» در اکوادور پروتئین RBD و ELISA «داخلی» را ارائه کردند. از Howard E. Takiff و Flor Pujol (IVIC، ونزوئلا)، Paulina E. Andrade (USFQ، اکوادور)، و Lilly Verhagen (UMC، هلند) برای بحثهای پربارشان تشکر میکنیم.

منابع
Abate D، Saldan A، Mengoli C، Fiscon M، Silvestre C، Fallico L، و همکاران. مقایسه نقاط ایمونوسوربنت متصل به آنزیم سیتومگالوویروس (CMV) و سنجش گاما اینترفرون آزادکننده کمیت کننده CMV در ارزیابی خطر عفونت CMV در گیرندگان پیوند کلیه. جی کلین میکروبیول 2013؛ 51 (8): 2501-7.
Altmann DM، Boyton RJ. ایمنی سلول T SARS-CoV{1}: ویژگی، عملکرد، دوام و نقش در حفاظت. Sci Immunol 2020؛ 5(49)eabd6160.
Amanat F، Stadlbauer D، Strohmeier S، Nguyen THO، Chromikova V، McMahon M، و همکاران. یک سنجش سرولوژیکی برای تشخیص تبدیل سرمی SARS-CoV-2 در انسان. Nat Med 2020؛ 26:1033-6.
براون جی، وفادار ال، فرنتچ ام، وندیش دی، گئورگ پی، کورث اف، و همکاران. سلولهای T واکنشپذیر SARS-CoV{1} در اهداکنندگان سالم و بیماران مبتلا به کووید-19. طبیعت 2020؛ 587:270–4.
de Vries RD. سلولهای T خاص SARS-CoV در انسانهایی که در معرض تماس قرار نگرفتهاند: وجود سلولهای حافظه واکنش متقابل با ایمنی محافظتی برابری نمیکند. Sig Transduct Target Ther 2020; 5:224.
Doshi P. Covid-19: آیا بسیاری از افراد از قبل ایمنی دارند؟ BMJ 2020; 370: m3563.
Grifoni A، Weiskopf D، Ramirez SI، Mateus J، Dan JM، Moderbacher CR، و همکاران. اهداف پاسخهای سلولهای سلولی به ویروس SARS-CoV-2 در انسانهای مبتلا به بیماری کووید-19 و افراد در معرض تماس. Cell 2020؛ 181(7)1489-501.
Guevara A، Vivero S، Nipaz V، Guaraca V، Coloma J. یک روش ELISA ارزان SARS-CoV-2 rRBD برای تشخیص سرواستاتوس در جمعیت اکوادور مبتلا به COVID-19. Am J Trop Med Hyg [39_TD$DIFF]2021.
Le Bert N، Tan AT، Kunasegaran K، Tham CYL، Hafezi M، Chia A، و همکاران. ایمنی سلولی خاص SARS-CoV-2- در موارد کووید-19 و SARS و کنترل های غیر آلوده. Nature 2020; 584(7821):457-62.
Lipsitch M، Grad YH، Sette A، Crotty S. سلول های T حافظه واکنش متقابل و ایمنی گله به SARS-CoV-2. Nat Rev Immunol 2020.
Mahajan S، Kode V، Bhojak K، Magdalene CM، Lee K، Manoharan M، و همکاران. اپیتوپهای سلول T ایمنی غالب از آنتیژن سنبله SARS-CoV{2}} ایمنی سلولهای T قوی از قبل موجود را در افراد مواجه نشده نشان میدهند. bioRxiv 2020.
Mateus J، Grifoni A، Tarke A، Sidney J، Ramirez SI، Dan JM، و همکاران. اپی توپ های سلول T انتخابی و واکنش متقابل SARS-CoV-2 در انسان های مواجه نشده. علوم 2020؛ 370 (6512): 89-94.
Moderbacher RC، Ramirez SI، Dan JM، Grifoni A، Hastie KM، Weiskopf D، و همکاران. ایمنی تطبیقی اختصاصی آنتی ژن به SARS-CoV-2 در کووید حاد-19 و ارتباط با سن و شدت بیماری. سلول 2020; S{5}}(20): 31235-6.
Murugesan K، Jagannathan P، Pham TD، Pandey S، Bonilla HF، Jacobson K، و همکاران. سنجش انتشار اینترفرون-گاما برای تشخیص دقیق پاسخ سلول T SARS-CoV-2. Clin Infect Dis 2020;ciaa1537.
Ni L، Ye F، Cheng ML، Feng Y، Deng YQ، Zhao H، و همکاران. تشخیص ایمنی هومورال و سلولی خاص SARS-CoV-2- در افراد بهبودیافته کووید-19. مصونیت 2020؛ 52(6)971-7.
Pai M، Denkinger CM، Kik SV، Rangaka MX، Zwerling A، Oxlade O، و همکاران. سنجش آزادسازی اینترفرون گاما برای تشخیص عفونت مایکوباکتریوم توبرکلوزیس Clin Microbiol Rev 2014؛ 27 (1): 3-20.
پنگ ی، منتزر ای جی، لیو جی، یائو ایکس، یین زی، دونگ دی، و همکاران. سلول های CD4 plus و CD8 plus T حافظه گسترده و قوی ناشی از SARS-CoV-2 در افرادی که در حال نقاهت در بریتانیا هستند به دنبال کووید-19. NatImmunol 2020.
Petrone L، Petruccioli E، Vanini V، Cuzzi G، Fard SN، Alonzi T، و همکاران. یک آزمایش خون کامل برای اندازهگیری پاسخ خاص SARS-CoV-2-در بیماران کووید-19. Clin Microbiol Infect 2020.
Sagar M، Reifler K، Rossi M، Miller NS، Sinha P، White L، و همکاران. عفونت کروناویروس بومی اخیر با کووید کمتر شدید مرتبط است-19. J Clin Invest 2020.
Schwarzkopf S، Krawczyk A، Knop D، Klump H، Heinold A، Heinemann FM، و همکاران. ایمنی سلولی در بیماران کووید{0}} با عفونت تایید شده با PCR اما با SARS-CoV غیرقابل شناسایی-2-IgG خاص. Emerg Infect Dis. 2021؛ 27 (1).
Sekine T، Perez-Potti A، Rivera-Ballesteros O، Strålin K، Gorin JB، Olsson A، و همکاران. ایمنی قوی سلول T در افراد در حال نقاهت مبتلا به کووید بدون علامت یا خفیف{2}}. Cell 2020؛ 183(1)158-68.
Sette A, Crotty S. مصونیت از قبل موجود در برابر SARS-CoV-2: معلوم و ناشناخته. Nat Rev Immunol. 2020؛ 20 (8) 457-8.
Tan CCS، Owen CJ، Tham CYL، Bertoletti A، van Dorp L، Balloux F. واکنش متقاطع با واسطه سلول T از قبل موجود به SARS-CoV-2 را نمیتوان صرفاً با قرار گرفتن در معرض قبلی با کروناویروسهای بومی انسانی توضیح داد. bioRxiv 2020؛ 2020.
For more information:1950477648nn@gmail.com
