همانژیوبلاستومای اولیه کلیه با آنالیزهای مولکولی بر اساس توالی یابی نسل بعدی: گزارش موردی و مروری بر ادبیات
May 24, 2023
خلاصه
1. پس زمینه
همانژیوبلاستوما یک تومور مزانشیمی ضعیف است که اغلب در سیستم عصبی مرکزی (CNS) ایجاد میشود، اما میتواند به صورت خارج عصبی، به عنوان بخشی از بیماری فون هیپل-لیندو (VHL) یا در تومورهای پراکنده ایجاد شود. همانژیوبلاستوم های خارج از اعصاب خارج از سیستم عصبی مرکزی رخ می دهد. این شامل تومورهای ناشی از ساختارهای عصبی پاراآکسیال و اندام های احشایی است. همانژیوبلاستوما پراکنده کلیه، زیرمجموعه نادری از همانژیوبلاستوماهای خارج عصبی، یک نئوپلاسم کلیوی است که کمتر شناخته شده است. تنها 25 مورد تا به امروز در ادبیات زبان انگلیسی شرح داده شده است. ما در اینجا یک تومور پراکنده اضافی را در یک بیمار بدون بیماری VHL گزارش می کنیم.
2. ارائه مورد
در اوروگرام توموگرافی کامپیوتری، یک مرد 61- ساله که با هماچوری شدید مراجعه میکرد، یک توده کلیوی 3.5 سانتیمتری در قطب میانی تا پایینی کلیه چپ داشت. بیمار برای توده نفرکتومی جزئی انجام شد. معاینه پاتولوژیک یک تومور غیر محصور شده به خوبی محصور شده متشکل از ورقه های سلول های چند ضلعی بزرگ را نشان داد که توسط یک شبکه عروقی غنی عبور می کنند. سلولهای تومور سیتوپلاسم ائوزینوفیلیک شفاف و هستههای کلی را نشان دادند. تشخیص همانژیوبلاستوما با رنگ آمیزی مثبت برای آلفا اینهیبین، S100، انولاز اختصاصی نورون و PAX8 تایید شد. با استفاده از توالی یابی نسل بعدی که از تشخیص همانژیوبلاستومای پراکنده کلیه حمایت می کند، هیچ جهش ژنی قابل توجهی، از جمله ژن VHL و تغییرات تعداد کپی، در تومور شناسایی نشد.
3. نتیجه گیری
همانژیوبلاستومای پراکنده کلیه زیرمجموعه نادری از همانژیوبلاستوماهای خارج عصبی است. ما یکی از این تومورها را در یک بیمار بدون شواهد بالینی یا مولکولی بیماری VHL گزارش میکنیم. مقالات برای درک بهتر ویژگی های بالینی، رادیولوژیکی، پاتولوژیک و مولکولی این نئوپلاسم بررسی شد. اکثر همانژیوبلاستوماهای کلیوی دارای رنگ آمیزی ایمونوهیستوشیمی مثبت برای PAX8 بودند که این ایده را تایید می کند که پروفایل ایمنی همانژیوبلاستوماهای خارج عصبی می تواند بسته به محل منشاء متفاوت باشد. تشخیص همانژیوبلاستومای کلیوی به دلیل نادر بودن و همپوشانی ویژگی های میکروسکوپی و ایمونوفنوتیپی با سایر تومورهای کلیوی، از جمله کارسینوم سلول شفاف کلیوی، چالش برانگیز است. در برخی موارد، مطالعات مولکولی یا ژنتیکی ممکن است برای به دست آوردن تشخیص دقیق ضروری باشد. از آنجایی که همانژیوبلاستومای کلیه از نظر بالینی خوش خیم است، شناخت این موجودیت پاتولوژیک برای جلوگیری از درمان بیش از حد غیرضروری مهم است.
کلید واژه ها
همانژیوبلاستومای کلیه، بیماری فون هیپل-لیندو، توالی یابی نسل بعدی

برای دریافت پزشک کلیه اینجا کلیک کنید【Cistanche】
زمینه
همانژیوبلاستوما یک تومور غیرفعال سلول های مزانشیمی است که اغلب در سیستم عصبی مرکزی (CNS) و عمدتاً در مخچه ایجاد می شود. بیشتر تومورها پراکنده هستند، در حالی که 20-30 درصد در بیماران مبتلا به بیماری Von-Hippel-Lindau (VHL) رخ می دهد [1]. همانژیوبلاستوماهای خارج از اعصاب، (همانژیوبلاستوم هایی که در خارج از سیستم عصبی مرکزی رخ می دهند)، شامل تومورهایی است که از ساختارهای پارانوراکسیال، بافت نرم، استخوان و اندام های احشایی به وجود می آیند. به نظر می رسد همانژیوبلاستوماهای خارج عصبی از نظر مورفولوژیکی و ایمونوفنوتیپی با همانژیوبلاستوماهای CNS یکسان هستند، اما تفاوت های خاصی وجود دارد. همانژیوبلاستوما کلیوی یک زیر مجموعه نادر از همانژیوبلاستوماهای خارج عصبی است که معمولاً در شرایط بیماری VHL شناخته شده رخ می دهد. اما، همچنین می تواند به صورت پراکنده رخ دهد. تا به امروز، تنها 25 مورد همانژیوبلاستوماهای پراکنده کلیه در ادبیات زبان انگلیسی شرح داده شده است [2-16]. ما در اینجا یکی از این تومورها را در یک بیمار بدون شواهد بالینی یا مولکولی بیماری VHL گزارش میکنیم و ادبیات را برای درک بهتر ویژگیهای بالینی، رادیولوژیکی، پاتولوژیک و مولکولی آن بررسی میکنیم. از آنجایی که همانژیوبلاستومای کلیوی از نظر بالینی خوش خیم است، شناخت صحیح این موجودیت پاتولوژیک برای جلوگیری از درمان غیر ضروری بالینی مهم است.

Cistanche tubulosa
ارائه پرونده
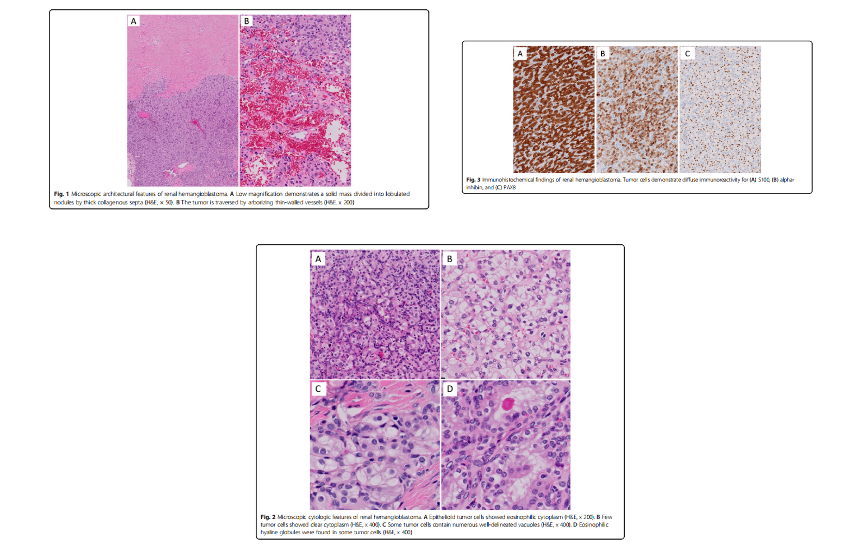
یک مرد {{0}} ساله با یک دوره هماچوری شدید بدون تب، درد پهلو، درد همراه با ادرار، کاهش وزن یا علائم عصبی مراجعه کرد. بیمار سابقه پزشکی گذشته بیماری عروق کرونر و فشار خون بالا را به خوبی کنترل کرده بود. توموگرافی کامپیوتری (CT) اوروگرام تودهای به ابعاد 3.5 × 2.1 × 1.3 سانتیمتر را نشان داد که از نظر شریانی افزایش میدهد، در قطب میانی تا پایینی جانبی کلیه چپ، همراه با یک سنگ منشعب در کالیسهای کلیوی قطب پایین چپ. این یافته ها برای کارسینوم سلول کلیه مشکوک بود. معاینه آزمایشگاهی کراتینین طبیعی را نشان داد. هیچ سابقه خانوادگی بیماری VHL یا بیماری های نئوپلاستیک وجود نداشت. سیستوسکوپی انجام شد و هیچ توموری در مجرای ادرار، مثانه یا حالب مشاهده نشد. یک ماه بعد، بیمار تحت لاپاروسکوپی نفرکتومی جزئی چپ قرار گرفت. یک بررسی کامل از نمونه، یک توده گرد به خوبی محصور شده اما بدون کپسول، به ابعاد 3.0 x 2.1 x 1.3 سانتی متر را نشان داد. سطوح بریده شده نشان داد که تومور سفید مایل به زرد، با فیبروز جزئی و خونریزی خفیف است. از نظر بافت شناسی، تومور تحت قدرت کم، کمی لوبوله شده بود، که توسط یک شبکه عروقی برجسته با رگ های خونی با دیواره نازک (شکل 1B)، در پس زمینه ای از استرومای هیالینیزه و اسکلروتیک (شکل 1A) عبور می کرد. سلولهای تومور با قدرت زیاد، اندازه کمی متغیر بودند، شکل بیضی تا چند ضلعی، و سیتوپلاسم شفاف تا ائوزینوفیلیک (شکل 2A و B) با واکوئلهای ظریف گاه به گاه (شکل 2C) و گلبولهای هیالین ائوزینوفیلیک (شکل 2D) داشتند. ). اکثر هسته های سلول تومور نرم با هسته های نامحسوس بودند، اگرچه پلئومورفیسم خفیف کانونی وجود داشت. هیچ نکروز توموری یا میتوزی وجود نداشت. از نظر ایمونوهیستوشیمی، سلول های تومور به صورت انتشاری S100 (شکل 3A)، آلفا-اینهیبین (شکل 3B)، انولاز اختصاصی نورون (NSE)، ویمنتین و PAX8 (شکل 3C) را بیان کردند. AE1/AE3 فقط رنگ آمیزی سیتوپلاسمی کانونی ضعیف را نشان داد. سلول های تومور از نظر آنتی ژن غشای اپیتلیال (EMA)، کربنیک انیدراز 9 (CA9)، CD10، KRT7، CD117، p504s، سیناپتوفیزین، کروموگرانین، ملانین A، HMB45 و فاکتور استروئیدوژنیک 1 (SF{40}}) منفی بودند. رنگ آمیزی Ki{41}} شاخص پرولیفراتیو بسیار پایینی را نشان داد (<1%). Extracted genomic DNA from formalin-fixed paraffin-embedded material (50% tumor cellularity) was submitted for next-generation sequencing (NGS) using the Oncomine Comprehensive Plus panel (ThermoFisher) enabling the detection of variants in the full coding sequence of 227 genes and hot spots of 165 genes, and the detection of copy number variants of 333 genes, including the entire coding sequence of VHL. Two variants of uncertain significance were detected in NOTCH1 (c.6061G>T, p.V2021F, variant allele frequency = 52%) and APC (c.7459T>C، p.S2487P، فرکانس آلل متغیر=52 درصد)، اما هیچ تغییری در تعداد کپی مشاهده نشد. به طور کلی، یافته های بافت شناسی، ایمونوهیستوشیمی و مولکولی از تشخیص همانژیوبلاستوما پراکنده کلیه پشتیبانی می کند. دوره بعد از عمل بیمار بدون عارضه بود و هیچ شواهدی مبنی بر عود تومور یا متاستاز در پیگیری 10 ماه پس از جراحی وجود نداشت.
بحث
همانژیوبلاستوما یک نئوپلاسم غیر معمول و خوش خیم است که عمدتاً در CNS به ویژه در مخچه ایجاد می شود. همانژیوبلاستوماهای خارج اعصاب زیرمجموعه نادری از همانژیوبلاستوما هستند که خارج از CNS ایجاد می شوند. تا به امروز حدود 200 مورد همانژیوبلاستوماهای خارج عصبی به عنوان بخشی از بیماری VHL یا تومورهای پراکنده گزارش شده است و تا 140 مورد از ساختارهای پارا نوراکسیال عصبی بودند [14]. همانژیوبلاستوم اولیه کلیه یک نئوپلاسم نادرتر است که تنها 25 مورد آن در ادبیات زبان انگلیسی یافت شده است [2-17]. از نظر بالینی، همانژیوبلاستوما پراکنده کلیه یک نئوپلاسم خوش خیم است، شبیه به سایر زیرگروه های همانژیوبلاستوماهای خارج عصبی و همانژیوبلاستومای پراکنده CNS.
همانطور که در جدول 1 توضیح داده شده است، 25 بیمار مبتلا به همانژیوبلاستوماهای پراکنده کلیه بزرگسال بودند و تنها یک نفر کودک بود (در سن 16 سالگی تشخیص داده شد) [5]، با میانگین سنی در تشخیص 48 سال، بین 16 تا 71 سال. 14 بیمار مرد و 12 بیمار زن بودند (M: F=1.17). در 15 بیمار از 26 بیمار، تومورها در کلیه راست قرار داشتند و قطب فوقانی شایع ترین محل بود. متوسط اندازه تومور 4.2 سانتی متر (محدوده 1.2 تا 15 سانتی متر) بود [5، 11]. به طور کلی، 60 درصد بیماران بدون علامت، 24 درصد هماچوری، 12 درصد درد در ناحیه کمر یا شکم داشتند و تنها یک بیمار با علائم سیستمیک مانند تب و کاهش وزن مراجعه کرد [11]. هیچ یک از بیماران وارد شده در این مطالعه بیماری VHL نداشتند. یک بیمار مبتلا به بیماری احتمالی VHL [13] از بررسی حذف شد.
از آنجایی که این تومور بسیار نادر است، توصیفات کمی از ویژگی های رادیولوژیکی مشخصه آن وجود دارد. او و همکاران افزایش ندولر محیطی در فاز کورتیکومدولاری، تقویت پیشرونده گریز از مرکز در فازهای نفروگرافی و تاخیری، و گاهی "پر کردن" کامل در فاز تاخیری در 2 بیمار مبتلا به همانژیوبلاستومای کلیوی [16] را توصیف کرد.
همه تومورهای گزارش شده با جراحی برداشته شدند، تقریباً همه (25/26) توزیع یک طرفه و یک کانونی را نشان دادند، به استثنای یک مورد [11] بیمار با 3 ضایعه در کلیه چپ (کلیه راست بدون درگیری). تمام ضایعات از نظر بافت شناسی به عنوان همانژیوبلاستوما کلیوی تایید شد. از نظر ماکروسکوپی، همانژیوبلاستومای کلیه یک سطح برش جامد و گاهی کیستیک را نشان می دهد [7]. از نظر میکروسکوپی، مشابه همانژیوبلاستوما CNS، همانژیوبلاستومای کلیوی از ورقههای بزرگ و به خوبی مشخص شده از سلولهای چند ضلعی، با یک شبکه عروقی برجسته و درختکاری تشکیل شده است. اندازه سلول های تومور با سیتوپلاسم شفاف تا ائوزینوفیلیک متغیر است که معمولاً حاوی واکوئل های لیپیدی ریز مشخص شده است. ویژگی های رابدوئید در یک تومور گزارش شده است [7]. بیشتر تومورها نرم به نظر می رسند [2]، اما برخی از تومورها پلئومورفیسم هسته ای خفیف تا متوسط را نشان دادند [3]. ارقام میتوز در تومورهای گزارش شده نادر بود.
از نظر ایمونوهیستوشیمی، تقریباً همه همانژیوبلاستوماهای کلیوی دارای مثبت انتشار آلفا اینهیبین (24/26)، NSE (23/23)، پروتئین S100 (25/25) و ویمنتین (19/21) و منفی برای نشانگرهای نورواندوکرین (سیناپتوفیزین) بودند. ، کروموگرانین A)، نشانگرهای ملانوسیتی (HMB45، melan-A)، نشانگرهای اندوتلیال (CD31، CD34) و نشانگرهای مزوتلیال (calretinin، WT{14}}). در 3 مورد از 21 مورد گزارش شده، سلولهای تومور مثبت کانونی و تکهای برای AE1/AE3 [10، 16]، از جمله تومور حاضر، ابراز کردند. اکثر همانژیوبلاستوماهای کلیوی هیچ واکنش ایمنی برای عضله، مانند دسمین [2-4] نشان ندادند، اما دو تومور مشاهده شد که بیان کانونی اکتین عضله صاف را دارند [2، 15]. CD10 در 7/16 تومور مثبت گزارش شد [7، 8، 10، 14، 15]. EMA در 5/15 تومور مثبت بود [4، 7، 8، 14، 15] و CA9 در 3/4 تومور مثبت بود [4، 8، 12].
در مورد حاضر، مثبت بودن هسته ای منتشر و قوی برای PAX8 در 8/14 تومور [10-12، 14-16] مشاهده شد و PAX2 در 2 تومور گزارش شده مثبت بود [8، 12]. PAX8 و PAX2 فاکتورهای رونویسی مخصوص دودمان سلولی هستند که نقش مهمی در ارگانوژنز کلیه دارند [17]. هر دو عامل در کلیه های طبیعی و همچنین در بسیاری از نئوپلاسم های اپیتلیال کلیه مانند کارسینوم سلول کلیه (RCC) بیان می شوند. ژائو و همکاران، فرضیهای را مطرح کردهاند که نشان میدهد مشخصات ایمنی همانژیوبلاستومهای خارج عصبی میتواند با محلهای مختلف منشأ متفاوت باشد [10]. با یافته های مثبت برای PAX8 و/یا PAX2 در 9 تومور فوق، ما با این فرضیه موافقیم که همانژیوبلاستوماهای کلیوی قادر به بیان آنتی ژن های خاص کلیه هستند.

هربا سیستانچوعصاره سیستانچ
همانژیوبلاستومای کلیه به دلیل نادر بودن، احتمالاً یک تومور ناشناخته کلیه است. این نئوپلاسم ضعیف را می توان با بدخیمی های مختلف، از جمله RCC سلول شفاف یا آنژیومیولیپوم اپیتلیوئید اشتباه گرفت. Clear cell RCC خصوصیات مورفولوژیکی مشابهی با همانژیوبلاستوماهای کلیوی دارد، مانند یک سیتوپلاسم شفاف و یک شبکه عروقی برجسته. مفیدترین ویژگی برای افتراق RCC سلول شفاف از همانژیوبلاستومای کلیوی، عدم وجود واکوئل های لیپیدی سیتوپلاسمی ریز است که عمدتاً در همانژیوبلاستومای کلیوی وجود دارد. از نظر ایمونوهیستوشیمی، RCC سلول شفاف معمولاً برای AE1/AE3، EMA، CA9، CD10 و PAX8 مثبت است، اما برای آلفا اینهیبین، S100 و NSE منفی است. با این حال، برای اضافه کردن سردرگمی، مونتیرونی و همکاران [18] RCC های سلولی شفاف را در 2 بیمار با 60-70 درصد از سلول های تومور که ویژگی های مشابه همانژیوبلاستوم را نشان می دادند، گزارش کردند. در آن موارد گزارش شده، سلول های تومور آلفا اینهیبین و S100 را فقط در قسمت مشابه همانژیوبلاستوما بیان کردند (نه در قسمت RCC سلول شفاف)، اما PAX8، CD10 و RCC در هر دو جزء تومور مثبت بودند. پس از بررسی دقیق مورفولوژی بافت شناسی در مورد فعلی ما، حدود 10 درصد از سلول های تومور را یافتیم که سیتوپلاسم شفاف را نشان می دهند، اما تمام سلول های تومور به طور مداوم برای S100، آلفا اینهیبین، NSE، Vimentin و برای CD10 و CA9 منفی رنگ آمیزی شده اند. این یافته ها از تشخیص همانژیوبلاستوما کلیوی پشتیبانی می کند. یکی دیگر از تقلید کننده های اصلی همانژیوبلاستومای کلیه، آنژیومیولیپوم اپیتلیوئیدی است که دارای صفحاتی از سلول های چند ضلعی با سیتوپلاسم فراوان و شبکه عروقی غنی است. ویژگی کلیدی برای افتراق همانژیوبلاستومای کلیوی از آنژیومیولیپوم های اپیتلیوئیدی این است که آنژیومیولیپوم های اپیتلیوئیدی معمولاً به جای سیتوپلاسم واکوئله حاوی لیپید، سیتوپلاسم شبکه ای را نشان می دهند. از نظر ایمونوهیستوشیمی، آنژیومیولیپوم های اپیتلیوئیدی معمولا HMB45 مثبت و ملان-A مثبت، اما آلفا اینهیبین منفی هستند. سایر تشخیص های افتراقی شامل انکوسیتوم کلیوی و بافت نابجای آدرنال داخل کلیه است. انکوسیتوما خصوصیات مورفولوژیکی مشابهی با همانژیوبلاستوما دارد، مانند سیتوپلاسم ائوزینوفیلیک و گلبول های هیالین ائوزینوفیلیک، اما واکوئل های لیپیدی سیتوپلاسمی ظریف در انکوسیتوما وجود ندارند. از نظر ایمونوهیستوشیمی، انکوسیتوما معمولاً برای EMA، CD117 و PAX8 مثبت است اما برای CD10، آلفا اینهیبین و ویمنتین منفی است. بافت نابجای آدرنال داخل کلیه در 6 درصد از جمعیت عمومی یافت می شود. معمولاً از صفحات یا غدد سلولی با مرزهای سلولی مشخص و سیتوپلاسم کفی فراوان تشکیل شده است که توسط رگ های خونی پراکنده در یک الگوی سینوسی عبور می کند که ویژگی های آن شبیه همانژیوبلاستوم است. اگرچه سلولهای قشر آدرنال برای a-inhibin مثبت هستند، اما برای سایر نشانگرهای قشر آدرنال مانند melan-A و SF{31}} نیز ایمنی واکنش نشان میدهند، اما برای PAX8، S100 و ویمنتین منفی هستند.
در برخی موارد گزارش شده، مطالعات ژنتیک مولکولی انجام شد، از جمله آنالیز واکنش زنجیره ای پلیمراز (PCR) برای اگزون های ژن VHL (تست شده در 6 مطالعه، 9 بیمار) [3، 6، 8، 12، 14، 15]، از دست دادن هتروزیگوسیتی تجزیه و تحلیل (LOH) برای ژنهای کروموزوم 3p (تست شده در 2 مطالعه، 5 بیمار) [12، 14]، و هیبریداسیون فلورسانس درجا (FISH) برای حذف کروموزوم 3p (تست شده در 1 مطالعه، 1 بیمار) [8]. به طور کلی، هیچ جهش ژن VHL، از دست دادن هتروزیگوسیتی (LOH) کروموزوم 3p، یا حذف کروموزوم 3p در 9 تومور گزارش شده مشاهده نشد. ما با فرضیه ارائه شده توسط Muscarella و همکاران موافق هستیم. که 1) تغییرات ژنتیکی ممکن است در ناحیه اینترونیک یا تنظیم کننده ژن VHL باشد. 2) ناهنجاری ژنتیکی ممکن است شامل ژن های دیگری باشد که با بیان ژن VHL تداخل دارند. 3) مکانیسم های ژنتیکی تومور جایگزین [14]. از آنجایی که NGS می تواند یک رویکرد پروفایل مولکولی جامع را ارائه دهد، ما تومور را برای NGS ارائه کردیم که تغییرات DNA را در بیش از 400 ژن مورد بررسی قرار داد، بدون اینکه هیچ تغییر قابل توجهی شناسایی شود. در زمان مطالعه ما، این اولین باری است که آنالیز NGS در همانژیوبلاستومای پراکنده کلیه توصیف شده است. با این حال، هیچ جهش ژنی قابل توجهی از جمله ژن VHL در تومور ما شناسایی نشد. دو نوع با اهمیت نامشخص در NOTCH1 و APC شناسایی شد، اما هیچ تغییری در تعداد کپی مشاهده نشد. ممکن است نیاز به یک مطالعه کوهورت بزرگ برای پرداختن به اهمیت این دو نوع در همانژیوبلاستومای کلیوی باشد. بنابراین، مکانیسم ژنتیکی تومور همانژیوبلاستومای کلیه، حداقل در تومور ما، نامشخص باقی مانده است.

سیستانچ استاندارد شده
نتیجه
همانژیوبلاستومای پراکنده کلیه زیرمجموعه نادری از همانژیوبلاستوماهای خارج عصبی است. ما در اینجا یکی از این تومورها را در یک بیمار بدون شواهد بالینی یا مولکولی بیماری VHL گزارش میکنیم و ادبیات را برای درک بهتر ویژگیهای بالینی، رادیولوژیکی، پاتولوژیک و مولکولی این نئوپلاسم مرور میکنیم. از موارد بررسی ما و مورد حاضر، متوجه شدیم که اکثر همانژیوبلاستوماهای کلیوی دارای رنگ آمیزی ایمونوهیستوشیمی مثبت برای PAX8 هستند، که این ایده را تایید می کند که مشخصات ایمنی همانژیوبلاستوماهای خارج عصبی می تواند بسته به محل منشأ متفاوت باشد. تشخیص همانژیوبلاستومای کلیوی به دلیل نادر بودن و همپوشانی ویژگی های میکروسکوپی و ایمونوفنوتیپی با تومورهای سلول کلیوی (PAX8 plus و CD10 plus)، به ویژه کارسینوم سلول کلیوی شفاف، چالش برانگیز است. با این حال، تشخیص دقیق ضروری است، زیرا همانژیوبلاستومای کلیوی یک تشخیص بالینی خوش خیم است و شناخت صحیح این موجودیت پاتولوژیک برای جلوگیری از درمان غیر ضروری مهم است.
منابع
1. Byun J، Yoo HJ، Kim JH، Kim YH، Cho YH، Hong SH، و همکاران. نرخ رشد و سرنوشت همانژیوبلاستومای درمان نشده: ارزیابی بالینی تجربه یک موسسه J Neurooncol. 2019؛ 144 (1): 147-54.
2. Nonaka D, Rodriguez J, Rosai J. همانژیوبلاستوما خارج عصبی: گزارش 5 مورد. J Surg Pathol هستم. 2007؛ 31 (10): 1545-51.
3. آی پی YT، یوان جی کیو، چونگ اچ، چان جی کی. همانژیوبلاستوما پراکنده کلیه: یک تومور بدخیم کاذب شناخته نشده؟ J Surg Pathol هستم. 2010؛ 34 (11): 1695-700.
4. Verine J، Sandid W، Miquel C، Vignaud JM، Mongiat-Artus P. همانژیوبلاستوم پراکنده کلیه: یک تومور بدخیم کاذب شناخته نشده؟ J Surg Pathol هستم. 2011؛ 35 (4): 623-4.
5. Liu Y، Qiu XS، Wang EH. همانژیوبلاستومای پراکنده کلیه: یک تومور نادر کلیه. تشخیص پاتول 2012؛ 7:49.
6. Wang CC، Wang SM، Liau JY. همانژیوبلاستوما پراکنده کلیه در یک مرد 29- ساله. Int J Surg Pathol. 2012؛ 20 (5): 519-22.
7. Yin WH، Li J، Chan JK. همانژیوبلاستوم پراکنده کلیه با ویژگی های رابدوئید و بیان کانونی CD10: گزارش یک مورد و بررسی ادبیات. تشخیص پاتول 2012؛ 7:39.
8. Jiang JG، Rao Q، Xia QY، Tu P، Lu ZF، Shen Q، و همکاران. همانژیوبلاستوما پراکنده کلیه با بیان PAX2 و کانونی CD10: گزارش یک مورد. Int J Clin Exp Pathol. 2013؛ 6 (9): 1953-6.
9. Wang Y، Wei C، Mou L، Zhang Q، Cui Z، Li X، و همکاران. همانژیوبلاستومای پراکنده کلیه: گزارش مورد و بررسی ادبیات. اونکول لت. 2013؛ 5 (1): 360-2.
10. Zhao M، Williamson SR، Yu J، Xia W، Li C، Zheng J، و همکاران. بیان PAX8 در همانژیوبلاستوما پراکنده کلیه از دودمان سلولی اولیه کلیوی پشتیبانی می کند: پیامدهایی برای تشخیص افتراقی. هوم پاتول. 2013؛ 44 (10): 2247-55.
11. دویل لس آنجلس، سی دی فلچر. همانژیوبلاستوم محیطی: خصوصیات بالینی پاتولوژیک در مجموعه ای از 22 مورد. J Surg Pathol هستم. 2014؛ 38 (1): 119-27.
12. Kuroda N، Agatsuma Y، Tamura M، Martinek P، Hes O، Michal M. همانژیوبلاستوما پراکنده کلیه با بیان CA9، PAX2، و PAX8: یک دام تشخیصی در تشخیص افتراقی از کارسینوم سلول کلیوی شفاف. Int J Clin Exp Pathol. 2015؛ 8 (2): 2131-8.
13. وو یو، وانگ تی، ژانگ پی پی، یانگ ایکس، وانگ جی، وانگ سی اف. همانژیوبلاستوما خارج عصبی کلیه: چالش تشخیص بالینی پاتولوژیک جی کلین پاتول. 2015؛ 68 (12): 1020-5.
14. Muscarella LA، Bisceglia M، Galliani CA، Zidar N، Ben-Dor DJ، Pasquinelli G، و همکاران. همانژیوبلاستوم خارج اعصاب: یک مطالعه بالینی آسیب شناسی 10 مورد با تجزیه و تحلیل مولکولی ژن VHL. Pathol Res Pract. 2018؛ 214 (8): 1156-65.
15. Oberhammer L، Mitterberger MJ، Lusuardi L، Kunit T، Drerup M، Colleselli D، و همکاران. همانژیوبلاستومای پراکنده کلیه: گزارش موردی از یک تومور خوش خیم کلیوی نادر. Clin Case Rep. 2019؛ 7 (12): 2321–6.
16. He J، Liu N، Liu W، Zhou W، Wang Q، Hu H. CT و MRI یافته های مشخصه همانژیوبلاستومای پراکنده کلیه: دو گزارش مورد. پزشکی (بالتیمور). 2021؛ 100 (6): e24629.
17. چی ان، اپستین ج.ا. درست کردن Pax شما: پروتئین های Pax در حال توسعه و بیماری. روند ژنت. 2002؛ 18 (1): 41-7.
18. Montironi R، Lopez-Beltran A، Cheng L، Galosi AB، Montorsi F، Scarpelli M. کارسینوم سلول کلیوی شفاف (ccRCC) با ویژگی های مشابه همانژیوبلاستوم: یک الگوی گزارش نشده قبلی از ccRCC با اهمیت بالینی احتمالی. یورو اورول. 2014؛ 66 (5): 806-10.
Xintong Wang، George K. Haines III، Meenakshi Mehrotra، Jane Houldsworth و Qiusheng Si.
