استفاده آینده نگر از پروبیوتیک ها برای حفظ سلامت فضانوردان در طول پرواز فضایی
Sep 28, 2023
خلاصه:حفظ سلامت فضانورد در طول سفر فضایی بسیار مهم است. مطالعات متعدد تغییرات مختلفی را در میکروبیوم روده و سلامت فیزیولوژیکی مشاهده کردهاند. فضانوردان در ایستگاه فضایی بین المللی (ISS) تغییراتی در جوامع میکروبی در روده، بینی و پوست خود داشتند. علاوه بر این، تغییرات سلولی سیستم ایمنی در فضانوردان با تغییرات در نوتروفیل ها، مونوسیت ها و سلول های T مشاهده شده است. پروبیوتیک ها با مهار پایبندی پاتوژن ها، افزایش عملکرد سد اپیتلیال با کاهش نفوذپذیری و ایجاد اثر ضد التهابی، به رفع این مشکلات سلامتی ناشی از پرواز فضایی کمک می کنند. هنگامی که پروبیوتیک ها در معرض میکروگرانش قرار گرفتند، فاز تاخیر کوتاه تر، رشد سریع تر، بهبود تحمل اسید و مقاومت در برابر صفرا را نشان دادند. یک کپسول لاکتوباسیلوس کازئی سویه Shirota یخ زده برای پایداری آن به مدت یک ماه در ISS مورد آزمایش قرار گرفت و نشان داده است که ایمنی ذاتی را تقویت کرده و میکروبیوتای روده را متعادل می کند. ثابت می کند که استفاده از اسپورهای خشک شده یخ زده B. subtilis برای پروازهای فضایی طولانی مدت مفید است زیرا برای تمام جنبه های آزمایش شده برای پروبیوتیک های تجاری تحت شرایط شبیه سازی شده واجد شرایط است. این نتایج نشاندهنده نیاز به مطالعه بیشتر اثر پروبیوتیکها در شرایط ریزگرانشی شبیهسازی شده و شرایط پرواز فضایی و استفاده از آنها برای غلبه بر اثرات ناشی از دیسبیوز میکروبیوم روده و مسائلی است که ممکن است در طول پرواز فضایی رخ دهد.

گیاه سیستانچ سیستم ایمنی را افزایش می دهد
کلمات کلیدی: فضانورد پرواز فضایی؛ پروبیوتیک ها؛ میکروبیوم؛ ریزگرانش شبیه سازی شده (SMG)
1. معرفی
اکتشافات فضایی انسانی اخیراً افزایش یافته است زیرا مأموریت های بیشتری توسط آژانس های فضایی مختلف بین المللی برنامه ریزی شده است. "برنامه تحقیقات انسانی" اداره ملی هوانوردی و فضایی در حال حاضر در حال برنامه ریزی برای ماموریت های طولانی مدت انسان در فضا به مریخ و ماه است. مطالعات مختلف نشان میدهد که فضانوردان به دلیل قرار گرفتن در معرض عوامل استرسزای متعدد مانند گرانش و تشعشعات، حفظ سلامتی خود را دشوار میدانند و در طول پروازهای فضایی کوتاه و طولانی با مشکلات سلامتی زیادی مواجه میشوند. بنابراین، درک خطرات سلامتی انسان مرتبط با سفر فضایی ضروری است. فضانوردانی که 6 تا 12 ماه را در ایستگاه فضایی بین المللی (ISS) سپری می کنند، تغییراتی در میکروبیوتای روده و تغییرات فیزیولوژیکی متفاوتی را تجربه کرده اند. این تغییرات شامل عفونتهای دستگاه تناسلی ادراری، مشکلات قلبی عروقی، تغییر در مقاومت و بیماریزایی باکتریها، تغییر در پاسخ ایمنی و ایجاد سرطانها به دلیل قرار گرفتن در معرض تشعشعات است [1،2]. بسیار مهم است که اقدامات احتیاطی لازم برای حفظ سلامت فضانوردان انجام شود زیرا ماموریت های فضایی مدت زمان بسیار طولانی به طول می انجامد [3]. سازمان بهداشت جهانی پروبیوتیک ها را به عنوان "میکروارگانیسم های زنده ای که در صورت مصرف به مقدار کافی، فواید سلامتی را برای میزبان به همراه دارد" توصیف کرده است [4]. نشان داده شده است که مصرف چند سویه پروبیوتیک سیستم ایمنی و فلور روده را تنظیم می کند و منجر به افزایش باکتری های خوب مانند لاکتوباسیل ها و بیفیدوباکتری ها و کاهش میکروب های مضر می شود. پروبیوتیکهایی مانند لاکتوباسیلوس کازئی سویه Shirota (LcS) میتوانند ایمنی ذاتی را بهبود بخشند و فعالیت سلولهای کشنده طبیعی را با افزایش تولید اینترلوکین توسط مونوسیتها و ماکروفاژها افزایش دهند. LcS، پس از مصرف، به شکل زنده به میکروبیوم روده می رسد و میکروبیوم روده را حفظ می کند [5،6]. نشان داده شده است که پروبیوتیک ها بر سنتز و آزادسازی مواد عصبی فعال تأثیر می گذارند. نشان داده شده است که لاکتوباسیلوس اسیدوفیلوس بیان گیرنده های کانابینوئید را تعدیل می کند [7]. Akkermansia muciniphila به عنوان یک پروبیوتیک بالقوه که می تواند از موسین دستگاه گوارش به خوبی استفاده کند، به طور جدایی ناپذیری با متابولیسم میزبان و پاسخ ایمنی مرتبط است. این پتانسیل را دارد که یک هدف درمانی در بیماریهای مرتبط با میکروبیوتا مانند کولیت، سندرم متابولیک، بیماریهای ایمنی و سرطان باشد [8]. در نتیجه، یک مطالعه نشان می دهد که پروبیوتیک های نسل بعدی مشتق شده از Akkermansia ممکن است خطر بیماری های مرتبط با التهاب مزمن را کاهش دهند [7]. مصرف خوراکی میکروب برجسته روده Faecalibacterium prausnitzii اخیراً کشف شده است که با افزایش تولید IL{16}} (یک سیتوکین) و فاکتور نکروز تومور (TNF) در روده بزرگ برای بهبود بیماری روده، خواص ضد التهابی نشان میدهد [9] ]. مطالعه دیگری همچنین پتانسیل ضد التهابی سویه های لاکتوباسیلوس بولگاریکوس و استرپتوکوکوس ترموفیلوس جدا شده از ماست خانگی بلغاری را نشان می دهد. سویه های پروبیوتیک لاکتوباسیلوس، بیفیدوباکتریوم و استرپتوکوک عمدتاً برای پیشگیری یا درمان عفونت های دهان استفاده می شوند [10]. برخی از میکروبیوتای روده نقش مهمی در عملکرد تغذیه ای ایفا می کنند و به در دسترس بودن ویتامین و تولید اسیدهای چرب با زنجیره کوتاه کمک می کنند. میکروارگانیسم های روده می توانند ویتامین B12، ویتامین K، پیریدوکسین، فولات، بیوتین، اسید نیکوتین و تیامین تولید کنند [11]. پلاک یا بیوفیلم های دندانی در حفره باکال باعث سلامت دهان و دندان می شود. با این حال، باکتری های اسید لاکتیک (LAB) با آن بیوفیلم/پلاک تعامل می کنند و از طریق فعالیت ضد میکروبی، عوامل ایجاد کننده را از بین می برند [12]. در طول یک پرواز فضایی طولانی مدت، قابلیت اطمینان مدیریت کارآمد سلامت ضروری است. طبق تحقیقات انجام شده، پرواز فضایی باعث تغییراتی در فیزیولوژی انسان می شود [13]. این تغییرات می توانند ماهیت های مختلفی داشته باشند: فیزیولوژیکی از جمله ناراحتی های گوارشی، درماتیت، و عفونت های تنفسی. ایمونولوژیک [14] و میکروبیوم [15]. مطالعات روی زمین نشان داده است که پروبیوتیک ها در بهبود مشکلات سلامتی که در طول پروازهای فضایی با آن مواجه می شوند، مفید هستند. آنها با رقابت با پاتوژن ها، کاهش مشکلات گوارشی، تقویت اتصالات محکم در سلول های اپیتلیال روده، تولید متابولیت های ضروری، و تعامل با سلول های میزبان برای ارتقاء تغییرات فیزیولوژیکی و ایمنی کمک می کنند [16-18]. این بررسی بر مشکلات مختلف پروازهای فضایی که فضانوردان با آنها مواجه میشوند و اینکه چگونه مصرف پروبیوتیکها میتواند به کاهش این مشکلات کمک کند، تمرکز دارد، که میتواند به فضانوردان در غلبه بر مشکلات پرواز فضایی کمک کند.

مزایای مکمل سیستانچ - افزایش ایمنی
2. مسائل بهداشتی در طول پرواز فضایی
فضا یک محیط خشن است و پیشرفت در علم مواد، تولید برق، روباتیک و الزامات پزشکی برای اطمینان از بقای فضانوردان در طول سکونتگاه ها و سفرهای بین سیاره ای ضروری است. هدف حوزه نوظهور زیست فضانوردی پرداختن به برخی از مسائل پزشکی است که فضانوردان در فضا با آن مواجه هستند. به دلیل محیط خصمانه در فضا، فضانوردان در طول پروازهای فضایی بلندمدت و کوتاه مدت با خطرات متعددی برای سلامتی مواجه هستند [19،20]. یک نمایش نموداری از مسائل بهداشتی که فضانوردان در طول پرواز فضایی با آن مواجه می شوند در (شکل 1) نشان داده شده است.

شکل 1. نمایش نموداری مسائل بهداشتی که فضانوردان در طول پرواز فضایی با آن مواجه می شوند. تصویر با استفاده از BioRender.com ایجاد شده است.
2.1. تغییرات در میکروبیوم
جاشوا لدربرگ اصطلاح "میکروبیوم انسانی" را در سال 2001 ایجاد کرد. او آن را به عنوان "شبکه طبیعی میکروارگانیسم های مشترک، همزیست و بیماری زا که واقعاً فضای بدن ما را به اشتراک می گذارند" توصیف کرد. میکروبیوم انسان متشکل از همزیستهای مفید مختلف، عمدتاً باکتریها است که به طور فعال سلامت را تقویت میکنند. با تغییر در میکروبیوتا، افزایش پاتوژن ها می تواند بر هموستاز تأثیر بگذارد و باعث بیماری های مختلف شود. در هر دو ماموریت فضایی بلند مدت و کوتاه مدت، تغییراتی در پروفایل باکتریایی روده، بینی و دهان فضانوردان مشاهده شده است. این پیشرفتها به کاهش ثروت کلی میکروبهای سودمند از جنسهای لاکتوباسیلوس و بیفیدوباکتریوم و گسترش میکروارگانیسمهای فرصتطلب مربوط میشوند، بهعنوان مثال، اشریشیا کلی، کلستریدیوم اسپ، استافیلوکوکوس اورئوس، فوزوباکتریوم نوکلئاتوم [3] ae Pseudomsaona [3] ae Pseudomsaona. بررسی میکروبیوتای 9 فضانوردی که یک سال را در ایستگاه فضایی بین المللی سپری کردند، شواهدی را نشان می دهد که نشان دهنده تغییر در جمعیت میکروبی دستگاه گوارش (GI)، بینی، زبان و پوست در طول ماموریت های فضایی است. DNA جمعآوریشده از نمونههای میکروبی در این مطالعه برای تعیین ترکیب میکروبی، تحت توالییابی ژن 16S rRNA قرار گرفت. این مطالعه افزایش مربوط به فضا در Parasutterella sp را مشخص کرد. عدد. این به طور قطعی با تشدید مزمن روده در افراد مبتلا به بیماری التهابی روده مرتبط است. این مطالعه همچنین کاهش مرتبط با فضا را در جمعیت سه جنس باکتریایی با خواص ضدالتهابی نشان داد: Fusicatenibacter روده، Pseudobutyvibrio، و Akkermansia. تغییرات کمتری در هنگام پرواز در میکروبیوتای بینی مشاهده شد [1،6].

cistanche tubulosa - بهبود سیستم ایمنی
برای مشاهده محصولات Cistanche Enhance Immunity اینجا را کلیک کنید
【بیشتر بخواهید】 ایمیل:cindy.xue@wecistanche.com / Whats App: 0086 18599088692 / Wechat: 18599088692
مطالعه لیو و همکاران. [15] اولین کسی بود که تأثیر ماموریت های کوتاه مدت پرواز فضایی را بر میکروبیوم روده انسان نشان داد. این مطالعه نشان داد که فراوانی Bacteroides پس از پرواز فضایی با کاهش لاکتوباسیلوس و بیفیدوباکتریوم افزایش یافت. باکتریوئیدها به طور موثر فیبرهای غذایی را در روده انسان تجزیه می کنند و تولید کننده اسید فنولیک و پروپیونات ضروری هستند. جنس Bacteroides دارای چندین گونه باکتریایی بیماریزا است که در شرایط استرس زا به سرعت تکثیر می شوند. محیط فضایی سیستم ایمنی انسان را ضعیف می کند و تعداد باکتری ها می تواند افزایش یابد. در روده انسان، لاکتوباسیل ها مسئول تولید مقدار زیادی اسید لاکتیک هستند. علاوه بر این، مطالعات نشان می دهد که بیفیدوباکتریوم اسیدهای لاکتیک و استیک را از قندها تولید می کند. کاهش جمعیت گونههای لاکتوباسیلوس و بیفیدوباکتریوم میتواند در عملکرد سیستم ایمنی میزبان در روده و عملکرد میکروبیوتای روده اختلال ایجاد کند و سیستم ایمنی متاثر از پرواز فضایی میتواند باعث فعال شدن مجدد ویروسهای نهفته و افزایش تعداد پاتوژنهای فرصتطلب شود. روده. مطالعه دوقلو همچنین نشان داد که متابولیتهایی مانند 3-ایندول پروپیونیک اسید که اثرات ضدالتهابی دارد، در طول مطالعه در سطوح پایین در پرواز مشاهده شدند. مطالعه زیر همچنین تغییری را در عملکرد میکروبیوم در سوژه پرواز در مقایسه با موضوع زمینی مربوط به جوامع میکروبی بیان کرد [21]. مطالعه صدیقی و همکاران. [22] از یک مدل موش تخلیه اندام عقبی (HU) روی زمین برای شبیه سازی شرایط ریزگرانش برای بررسی تغییرات در ترکیب باکتریایی میکروبیوتای روده استفاده کرد. آنها دریافتند که تخلیه اندام عقبی باعث تغییراتی در میکروبیوتای روده می شود، از جمله کاهش تنوع میکروبیوتای مفید روده که می تواند منجر به افزایش نفوذپذیری و التهاب روده شود. این مطالعه کاهش میزان Akkermansia muciniphila، Eubacterium coprostanoligenes و Burkholderiales را در موش هایی که در معرض ریزگرانش شبیه سازی شده در مقایسه با موش های معمولی قرار داشتند، نشان داد. این جنس های باکتریایی با خواص ضد التهابی، هموستاز روده و مزایای سلامتی مانند پیشگیری از سنگ کلیه مرتبط هستند. این مطالعه همچنین اهمیت نسبت متعادلی از Firmicutes و Bacteroidetes را در حفظ سلامت کلی با تغییراتی در نسبت آنها که منجر به dysbiosis و مسائل مربوط به سلامتی می شود، برجسته کرد. فیرمیکوت ها در متابولیسم و تغذیه میزبان نقش دارند، در حالی که باکتریوئیدها با تعدیل ایمنی مرتبط هستند. این نتایج نشان می دهد که تغییرات در میکروبیوتای روده ممکن است به اثرات منفی سلامتی که در پرواز فضایی تجربه می شود کمک کند [22]. ابزار تحلیلی «تست تشابه برای الگوهای فراوانی میکروبیوم سازگار و تکرارپذیر» یا STARMAP شباهت را در مجموعه دادههای تحقیقاتی دوفضایی برای یافتن تغییرات میکروبیوتا آزمایش میکند. این مطالعه همچنین کشف کرد که تغییرات میکروبیوتای مربوط به پروازهای فضایی در طول مأموریتهای RR-1 (پژوهش جوندگان 1) و STS{13}} (ماموریت انسانی) مشابه بودند، که نشاندهنده تغییر شدید در میکروبیوتای روده پستانداران به دلیل پرواز فضایی است [ 23]. اثر میکروگرانش بر میکروبیوتای روده فضانوردان در طول پرواز فضایی نیز در جدول 1 خلاصه شده است.
2.1.1. محور میکروبیوتا – روده – مغز و ارتباط آن با سلامت روان فضانوردان
میکروبیوتای روده از 106 سلول ویروسی، باکتریایی و تک یاخته تشکیل شده است که آن را به پرتعدادترین جامعه میکروبیوتای انسانی تبدیل می کند. مغز با تغییر نفوذپذیری روده بر عملکرد و ترکیب میکروبیوتا تأثیر می گذارد. مغز از طریق سیستم عصبی خودمختار (ANS) نیز ممکن است بر عملکرد سیستم ایمنی تأثیر بگذارد. محور روده – مغز (GBA) یک مسیر ارتباطی دو طرفه بین سیستم عصبی مرکزی و روده است. مراکز عاطفی و شناختی مغز را با عملکردهای روده محیطی مرتبط می کند. پیشرفت های تحقیقاتی اخیر اهمیت میکروبیوتای روده را در تأثیرگذاری بر این فعل و انفعالات برجسته کرده است [24]. ترکیب میکروبیوتای روده در طول عمر تغییرات زیادی را تجربه می کند که به موازات دوره های پویای رشد، پیری و بلوغ مغز است. دیس بیوز می تواند ناشی از عوامل محیطی مانند رژیم غذایی، گرانش، استرس و تشعشع باشد. علاوه بر این، میکروبیوتای روده نقش مهمی در ایجاد پاسخهای ایمنی سازگار و ذاتی دارد. میکروارگانیسم های دستگاه گوارش به عنوان ایستگاه های رله تجمع و انتقال اطلاعات به نواحی خاصی از مغز به ویژه مخچه عمل می کنند و بر سلامت روان تأثیر می گذارند. تأثیر عوامل محیطی مرتبط با سفرهای فضایی بر روی این میکروارگانیسم ها همگرا می شود [25].
2.1.2. چالش های سلامت روان فضانوردان در طول پرواز فضایی
پرواز فضایی یک محیط منحصر به فرد و دشوار است که می تواند تأثیر قابل توجهی بر سلامت روان فضانوردان داشته باشد [26]. انزوا، حبس، گرانش ریز، اختلال در ریتم های شبانه روزی، و تاخیرهای ارتباطی همگی می توانند به استرس روانی، اضطراب، افسردگی و سایر مسائل مربوط به سلامت روان کمک کنند [27،28]. تحقیقات نشان میدهد که فضانوردان زمانی که در فضا هستند بیشتر احساسی هستند و دچار اختلالات روانی میشوند [29]. فقدان حمایت اجتماعی و انزوا که در طول پرواز فضایی اتفاق می افتد یکی از دلایل اصلی مشکلات سلامت روان برای فضانوردان است. فضانوردان برای دوره های طولانی از خانواده و دوستان خود منزوی می شوند و درگیر شدن در تعاملات اجتماعی منظم را برای آنها دشوار می کند. این ممکن است منجر به احساس انزوا، کسالت و اضطراب روانی شود [28]. چالش اصلی دیگر، اختلال در چرخه خواب و بیداری ناشی از قرار گرفتن در معرض مداوم نور مصنوعی و عدم وجود چرخه طبیعی روز و شب در فضا است [30]. مطالعه اخیر ما و همکاران. [31] همچنین ارتباط بین میکروبیوم روده ناشی از پروبیوتیک و سطوح استرس کاهش یافته در بزرگسالان را نشان داد، بنابراین نقش محور روده-مغز در کاهش اثرات استرس را ثابت کرد.
جدول 1. اثر ریزگرانش بر میکروبیوتای روده فضانوردان در طول پرواز فضایی.

سلامت روان بخش مهمی از پروازهای فضایی است و فضانوردان بیشتر احتمال دارد استرس روانی، اضطراب و سایر مسائل مربوط به سلامت روان را تجربه کنند. ادامه کاوش و اتخاذ تکنیک هایی برای بهبود سلامت روان فضانوردان در فضا بسیار مهم است.
2.2. عفونت دستگاه ادراری تناسلی
در ماموریت های فضایی طولانی مدت، فضانوردان با چالش های فیزیکی زیادی مواجه می شوند که می تواند بر سلامت دستگاه تناسلی آنها تأثیر بگذارد. در طول پرواز فضایی، محیط ریزگرانش باعث کاهش حجم پلاسما و افزایش خروجی ادرار به دلیل جابجایی مایعات از اندام تحتانی به سمت بالاتنه میشود که منجر به خطر عفونتهای دستگاه ادراری (UTIs) به دلیل کاهش جریان ادرار و استاز ادراری میشود. . علاوه بر این، استرس و تغییر چرخه خواب و بیداری در طول پرواز فضایی ممکن است به افزایش بروز شب ادراری کمک کند [33]. فضانوردان مرد ممکن است به دلیل قرار گرفتن در معرض تشعشعات در طول پرواز فضایی با کاهش سطح تستوسترون مواجه شوند که منجر به کاهش میل جنسی و اختلال نعوظ می شود. از سوی دیگر، فضانوردان زن ممکن است بی نظمی های قاعدگی و سندرم احتقان لگن را تجربه کنند که باعث درد، فشار و ناراحتی در ناحیه لگن می شود [33،34]. عفونتهای مجاری ادراری مشکلات رایجی در فضا هستند و فضانوردان زن نسبت به فضانوردان مرد فراوانی بیشتری را تجربه میکنند. عوامل بیماریزای ادراری مانند استافیلوکوکوس ساپروفیتیکوس و اشریشیا کلی به دلیل توانایی آنها برای اتصال به سلول های اوروپیتلیال از طریق مولکول های چسبنده، علل مهم همه عفونت های دستگاه ادراری هستند. بررسیهای آزمایشگاهی نشان دادهاند که هر دو سویه E. coli بیماریزا و غیر بیماریزا چسبندگی و تهاجم بهتری را تحت گرانش میکروبی نشان میدهند. این چسبندگی بالاتر، همراه با سینتیک رشد تسریع شده E. coli در فضا، ممکن است مسئول پیشرفت بیماری باشد [3].

مزایای مکمل سیستانچ - افزایش ایمنی
2.3. فعال سازی مجدد ویروس در پرواز فضایی
مطالعه ای توسط Sonnenfeld & Shearer [35] به خطر افتادن سیستم ایمنی، احتمال ایجاد شرایط بدخیم و عفونت فعال شدن مجدد ویروس نهفته در انسان در طول پرواز فضایی را روشن کرد. در طول پرواز فضایی، تعداد قابل توجهی از این علائم مربوط به تضعیف سیستم ایمنی بدن به دلیل فعال شدن مجدد دو ویروس است: ویروس اپشتین بار و ویروس واریسلا-زوستر [1]. فعال شدن مجدد ویروس نهفته یک نشانگر زیستی برای وضعیت سیستم ایمنی فضانوردان است و عوامل موثر در آن افزایش ترشح گلوکوکورتیکوئید، تغییر در تولید سیتوکین و کاهش عملکرد سلولهای ایمنی هدف از بین بردن ویروسها است. وجود DNA ویروسی در مایعات بدن نشان دهنده فعال شدن مجدد ویروس است [36].
2.4. مقاومت باکتری ها و تغییرات در بیماری زایی باکتریایی
ژانگ و همکاران [37] تغییرات مقاومت ضد میکروبی سویه S. enteritidis را که توسط فضاپیمای Shenzhou{1}} به فضا منتقل شد، مورد مطالعه قرار دادند. در مقایسه با کرنش زمینی، کرنش پروازی افزایش مقاومت آمیکاسین، افزایش سرعت رشد و برخی تغییرات متابولیسم را نشان داد. اشریشیا کلی MG1655 هنگامی که در معرض میکروگرانش مدل شده با برش کم (LSMMG) و آنتی بیوتیک های پس زمینه مانند کلرامفنیکل، سفالوتین، تتراسایکلین، سفوکسیتین، سفوروکسیم و سفوکسیتین قرار گرفت، مقاومت آنتی بیوتیکی نشان داد. این سویه برای بیش از 110 نسل، حتی پس از حذف محیط LSMMG و قرار گرفتن در معرض آنتی بیوتیک، مقاومت به کلرامفنیکل و سفالوتین نشان داد. سویه اقتباس شده از توالی ژنوم اشرشیاکلی حدود 25 تغییر را نشان داد. این تغییرات ژنومی با مقاومت آنتی بیوتیکی همراه بود، با تغییر در چهار ژن مقاومت آنتی بیوتیکی: ompF، acrB، mdfA و Marr [38]. طبق مطالعه لیو و همکاران. [15] پرواز فضایی قدرت بیماریزایی باکتری ها را تغییر می دهد. هنگام بررسی ژنهای حدت، آنها دریافتند که میکروبیوم روده بر برخی از فاکتورهای حدت (VF) تأثیر میگذارد. نمونه ای از چنین تغییری افزایش فاکتور VF0367 مرتبط با توسعه لیپوپلی ساکارید بود که یک لایه محافظ در بروسلا را تشکیل می دهد [15]. مطالعه اخیر نشان داد که تعداد قرائت نشانگر جهش Streptomyces EF-Tu پس از سفر فضانورد به میزان قابل توجهی افزایش یافته است. این نشانگر تغییرات توالی القاکننده مقاومت به ریفامایسین فاکتور طویل شدن استرپتومایسس cinnamoneus Tu را شناسایی می کند. افزایش جهش های EF-Tu پس از پرواز فضایی نشان می دهد که مقاومت به ریفامایسین ممکن است به دلیل شرایط پرواز فضایی افزایش یافته باشد [39]. این مطالعات حاکی از افزایش بیماری زایی میکروب های خاص پس از قرار گرفتن در معرض پرواز فضایی است.
2.5. اختلال سد اپیتلیال و بیماری التهابی روده (IBD)
بیماری التهابی روده (IBD) یک بیماری التهابی مزمن و عود کننده در دستگاه گوارش است که با اختلال در سد اپیتلیال و اختلال در تنظیم ایمنی مشخص می شود. تحقیقات اخیر نشان داده است که فضانوردان هنگام حضور در فضا، ناراحتی گوارشی، از جمله علائم مشابه IBD را تحمل میکنند، که به احتمال زیاد در نتیجه تأثیر گرانش روی اپیتلیوم روده است. تغییرات در پروتئینهای اتصال محکم (TJ) باعث ایجاد اختلال در سد اپیتلیال میشود که منجر به افزایش نفوذپذیری روده و انتقال متعاقب آن آنتی ژنهای مجرا در سراسر اپیتلیوم میشود [40،41]. تغییر در بیان یا محلی سازی TJ ها ممکن است منجر به یک وضعیت نشتی روده به دلیل افزایش نفوذپذیری به مولکول هایی شود که از لومن به لایه پروپریا منتشر می شوند [42]. آلوارز و همکاران در مطالعه خود. [43] تاخیری را در محلی سازی پروتئین های TJ-اکلودین و ZO-1 تحت شرایط ریزگرانش شبیه سازی شده یافتند. یافتهها نشان میدهد که ریزگرانش شبیهسازیشده به سد اپیتلیال آسیب رسانده و حساسیت زمینهای به مانع حتی پس از برداشتن شرایط ریزگرانش همچنان ادامه دارد. این اختلال زمینه ای باعث می شود که فضانوردان مستعد ابتلا به بیماری های مختلف نقص سد سلولی اپیتلیال روده مانند بیماری کرون، کولیت اولسراتیو، بیماری سلیاک و دیابت نوع I شوند [44]. IBD در فضانوردان در طول پروازهای فضایی با افزایش نفوذپذیری پاراسلولی روده در نتیجه اختلال پروتئین TJ گزارش شده است [1،45]. یک مطالعه کاهش بیان و توزیع پروتئینهای TJ مانند اکلودین، کلودین{9}}، کلودین 04 و JAM-A و افزایش بیان کلودین{12}} [46] را گزارش کرد. مطالعه دیگری توسط یی و همکاران. [47] پیشنهاد کرد که Lactobacillus reuteri LR1 می تواند اختلالات روده ای مرتبط با اختلال عملکرد سد اپیتلیال را درمان کند. عفونت با انتروتوکسیژن E. coli K88 باعث افزایش نفوذپذیری تکلایههای سلولی IPEC{17}} شد. پروبیوتیک LR1 به طور قابل توجهی عملکرد سد اپیتلیال را بهبود بخشید و چسبندگی و کلونیزاسیون توسط کلیفرم ها را کاهش داد.

cistanche tubulosa - بهبود سیستم ایمنی
2.6. تغییرات ایمنی در طول پرواز فضایی
Astronauts face the issue of immune cell alteration during spaceflight. Innate immunity, or the first line of defense, plays a vital role in prolonging healthcare among astronauts. Immunological changes observed in astronauts during space flight have been shown in (Table 2). A study conducted at Johnson Space Center, Houston, showed an 85% increase in neutrophils during a 5–11-day spaceflight mission as compared to pre-flight levels along with remarkably lower values in phagocytosis [48]. An increase in the number of white blood cells, polymorphonuclear leukocytes, was also observed in short-duration spaceflight missions to the ISS [49]. Similar effects have been observed in astronaut long-duration spaceflight missions. An increase in the level of white blood cells [14]. Another study by Makedonas et al. [50] reported an increased inflammation in the astronauts during 1-year NASA "twins" study aboard the International Space Station. Cosmonauts on a long duration (>140 روز) پروازهای فضایی افزایش آزادسازی اندوکانابینوئیدها همراه با فعال شدن سیستم ایمنی را نشان داده است که خطر اختلالات مرتبط با التهاب را در انسان تقلید می کند. افزایش التهاب تا 30 روز پس از پرواز ادامه داشت [51]. تغییرات گرانشی که فضانوردان تجربه میکنند میتواند بر ریزمحیطهای دو اندام لنفوئیدی اصلی، تیموس و مغز استخوان تأثیر بگذارد. این اندام ها مسئول تولید لنفوسیت ها یا گلبول های سفید هستند. تغییرات در تولید لنفوسیتها میتواند تأثیر غیرمستقیم بر پاسخهای ایمنی اکتسابی داشته باشد و نحوه واکنش سیستم ایمنی به التهاب، عفونتها و تومورها را تغییر دهد [52].
جدول 2. تغییرات ایمونولوژیکی مشاهده شده در فضانوردان در طول پرواز فضایی.


2.7. تغییرات در عملکرد قلب و عروق
فضانوردان در فضا با بی وزنی مواجه می شوند که منجر به توزیع مجدد مایعات بدن به ناحیه سینه-سفالیک از نیمه پایینی بدن می شود. این انتقال مایع مسئول یک سندرم بی شرایط قلبی عروقی است که با افت فشار خون، احتمال پیش سنکوپ یا سنکوپ و کاهش توانایی استرس مشخص می شود [57]. فضانوردان در فضا استرس متابولیک را تجربه می کنند. استرس متابولیک پیش بینی کننده قوی بیماری قلبی و دیابت نوع 2 است [58]. پرواز فضایی همچنین خطر ایجاد آریتمی های بدخیم را به همراه دارد، زیرا تغییرات ایجاد شده در طول پرواز فضایی بر افزایش ناهمگنی رپلاریزاسیون تاکید می کند. مطالعات بیشتری برای درک تغییرات فیزیولوژیکی رخ داده در بدن مورد نیاز است، که همچنین به ارائه بینش عمیق تر در مورد تغییرات در سلامت انسان پس از تجاری سازی پرواز فضایی کمک می کند [59].
2.8. تأثیر تشعشعات کیهانی بر فضانوردان
انسان ها در فضا در معرض تشعشعات فضایی قرار می گیرند. اینها پرتوهای کیهانی کهکشانی تولید شده در خارج از منظومه شمسی، ذرات خورشیدی آزاد شده از خورشید، و تابش محدود به دلیل میدان مغناطیسی زمین هستند. این تشعشعات فضایی فضانوردان را به خطر می اندازند زیرا باعث ایجاد چندین نوع سرطان می شوند. احتمال ابتلا به سرطان در فضانوردان زن 20 درصد بیشتر از فضانوردان مرد است. این بیشتر به این دلیل است که سرطان سینه و تخمدان در زنان شایع تر است. در طول سفر، افراد می توانند اثرات کوتاه مدتی مانند تغییرات در خون، اسهال، حالت تهوع و استفراغ را تجربه کنند [3]. تابش تنوع فلور روده را کاهش می دهد و ترکیب میکروبیوتای روده را تغییر می دهد [60]. گزارشهای مربوط به پروازهای قبلی آپولو، اسکایلب و ایستگاه فضایی مدولار روسیه (MIR) نشان میدهد که فضانوردان شاهد فلاشهایی از نور بودند که در میدان بینایی خود حرکت میکردند، احتمالاً به دلیل تغییر در ادراک تولید شده توسط تشعشعات یونیزان، که نشان میدهد به نظر میرسد اختلالات بینایی نیز مرتبط هستند. با قرار گرفتن در معرض تابش [61]. در طی یک مأموریت 6-ماهه به ایستگاه فضایی بینالمللی، ماه و فراتر از آن، یک فضانورد در معرض تشعشعات حدود 50 تا 2000 میلیسیورت (mSv) قرار میگیرد. دوز تشعشع بالاتر از mSv 100 باعث سرطان می شود [62]. مطالعه تجزیه و تحلیل آماری STARMAPs نشان داد که تغییرات میکروبیوتای مربوط به پرواز فضایی در مقایسه با تغییرات ناشی از تشعشعات فضایی بر روی زمین متفاوت است. آنها پیشنهاد کردند که این تفاوت می تواند به این دلیل باشد که ایستگاه فضایی بین المللی در مدار پایین تری در داخل کمربند ون آلن قرار دارد. از این رو، افراد مورد تحقیق در این مطالعه در معرض تشعشعات کیهانی قرار نگرفتند. این مطالعه ثابت می کند که درک تشعشعات فضایی دور از کمربندهای ون آلن در آینده نزدیک حیاتی است [23]. واکنش های پیش التهابی به بی وزنی، تشعشع، هایپرترمی ناشی از استرس، یا ترکیبی از این عوامل در طول پرواز فضایی می تواند باعث "تب فضایی" شود که می تواند بر سلامت و انرژی، نیاز به مواد مغذی و مایعات و عملکرد فیزیکی و شناختی فضانوردان در طول طولانی مدت تاثیر بگذارد. مدت زمان پرواز فضایی [63].
3. پروبیوتیک ها و نقش آنها در زیست شناسی فضایی
اکتشافات فضایی از دانشمندان خواسته است تا مأموریتهای خدمه انسان به ماه و مریخ را توسعه دهند و برنامهریزی کنند. چنین ماموریت های طولانی مدت نیاز به دانش گسترده ای از چگونگی تأثیر سفر فضایی بر سلامت فضانوردان دارد. ظهور آپولو 11 و آزمایشهای شبیهسازی مختلف روی زمین و ایستگاه فضایی بینالمللی به ما این امکان را میدهد که بفهمیم فضا چگونه بر میکروبها و انسانها تأثیر میگذارد. همانطور که در بخش 2.1 ذکر شد، حفظ میکروبیوم روده انسان یک جنبه ضروری از سفرهای فضایی طولانی مدت است. عدم تعادل در میکروبیوم روده باعث بسیاری از بیماری ها شده است و نشان داده شده است که سفر به فضا باعث تغییراتی در میکروبیوم روده می شود. پروبیوتیک ها می توانند به مشکلات گوارشی مانند اسهال عفونی حاد، عفونت هلیکوباکتر پیلوری، اسهال مرتبط با آنتی بیوتیک، سندرم روده تحریک پذیر، کولیت اولسراتیو و یبوست کمک کنند و همچنین عملکرد سد روده را بهبود بخشند [64،65]. پروبیوتیک ها همچنین به حفظ سیستم ایمنی، پیشگیری از سرطان و کمک به مسائل روانی کمک می کنند [66]. پرمصرف ترین پروبیوتیک ها شامل اعضایی از گونه های لاکتوباسیلوس، بیفیدوباکتریوم یا ساکارومایسس است [67]. ما بیشتر می بینیم که چگونه پروبیوتیک ها می توانند یک مکمل مفید باشند (جدول 3).
3.1. مکانیسم کلی عمل پروبیوتیک ها
3.1.1. مهار اتصال پاتوژن
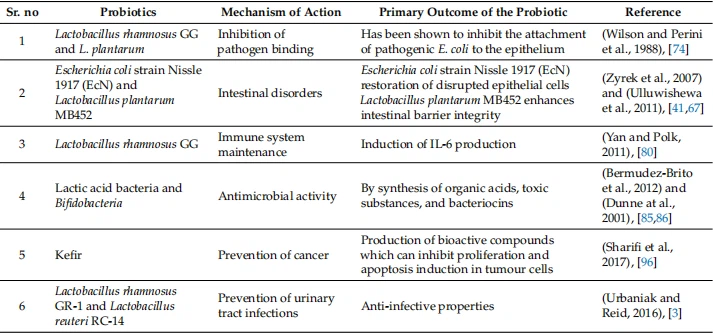
سویه های پروبیوتیک با تغییر سطح ترشح موکوس، اتصال پاتوژن به لایه اپیتلیال را مهار می کنند. پروبیوتیک ها می توانند با افزایش تعداد سلول های جامی (موسین ترشحی) که از لایه مخاطی حمایت می کنند، استحکام سد روده را بهبود بخشند. لایه مخاطی نقشی در کاهش اتصال باکتریهای بیماریزا به سلولهای اپیتلیال مخاطی دارد و پروبیوتیکها با القای ترشح مخاطی عمل میکنند [68،69]. Otte و Podolsky [70] دریافتند که سویه های لاکتوباسیلوس نحوه بیان MUC2، MUC3 و MUC5AC در سلول های HT29 را تغییر دادند. سویه های پروبیوتیک همچنین می توانند با رقابت برای محل چسبندگی، اتصال پاتوژن به لایه اپیتلیال را مهار کنند. پیلیهای متصلکننده مخاط انسان این امکان را برای برخی از پروبیوتیکها فراهم میکند که بدن را بهتر استعمار کنند [71]. پروبیوتیک ها برای مکان های اتصال لکتین بر روی گیرنده های گلیکوکونژوگیت موجود در سطوح میکروویلی سلول های اپیتلیال رقابت می کنند [72،73]. نشان داده شده است که L. plantarum و لاکتوباسیلوس rhamnosus سویه GG از اتصال باکتری E. coli بیماریزا به اپیتلیوم جلوگیری می کنند [74].
3.1.2. استفاده از پروبیوتیک ها برای اختلالات روده ای
پاتوژنز سندرم روده تحریکپذیر (IBS) ممکن است شامل تغییر فعالسازی سیستم ایمنی روده، دیسبیوز میکروبیوم روده، تغییر محور مغز – روده و افزایش نفوذپذیری سلولهای اپیتلیال روده باشد [75]. پروبیوتیک ها بر علائم دخیل در IBS، مانند نفخ، نفخ، تغییر حرکات روده، دیس بیوز میکروبیوتای روده و درد شکمی تأثیر می گذارند [76]. پروبیوتیک ها با مهار چسبندگی پاتوژن، افزایش عملکرد سد اپیتلیال با کاهش نفوذپذیری آن و ایجاد یک اثر ضد التهابی عمل می کنند [77]. یکپارچگی GIT توسط سلول های اپیتلیال حفظ می شود که به عنوان یک مانع بین سیستم ایمنی میزبان و محیط خارجی عمل می کنند. در پروبیوتیک اشرشیاکلی سویه Nissle 1917 (EcN)، یک اثر سیگنال دهی مهم منجر به ترمیم سلول های اپیتلیال مختل شده می شود. این باعث می شود پروبیوتیک EcN در درمان بیماری التهابی روده موثرتر باشد [41]. پروبیوتیک لاکتوباسیلوس پلانتاروم MB452 همچنین یکپارچگی سد روده ای را با افزایش بیان پروتئین های اتصال محکم - سینگولین و اکلودین بهبود می بخشد. این پروتئین ها به حفظ ترمیم سلول های اپیتلیال کمک می کنند [67]. Bifidobacterium sp. گروه دیگری از پروبیوتیک ها هستند که به حفظ یکپارچگی اتصالات محکم در مخاط دستگاه گوارش کمک می کنند. آنها با جلوگیری از توزیع مجدد پروتئین های اکلودین و TJ از سد اپیتلیال در برابر کولیت حاد محافظت می کنند [78].
3.1.3. نگهداری سیستم ایمنی
پروبیوتیک ها می توانند سیستم ایمنی بدن را عمدتاً با (1) تغییر ترشح ایمونوگلوبولین/سیتوکین، (2) تقویت سد روده اپیتلیال، (3) افزایش فعالیت سلول های ماکروفاژها یا سلول های کشنده طبیعی، (4) اتصال رقابتی به لایه اپیتلیال و جلوگیری از میکروب های بیماری زا تعدیل کنند. اتصال، و (5) تعدیل ترشح موکوس. ذرات آنتی ژنی تولید شده توسط پروبیوتیک ها، نه باکتری های کامل، می توانند وارد سلول های اپیتلیال شوند و با سلول های ایمنی تماس بگیرند [79]. تعداد کمی از سویههای پروبیوتیک، مانند لاکتوباسیلوس رامنوسوس GG و بیفیدوباکتریا، تولید سیتوکین را از انواع مختلف سلول تعدیل میکنند و پاسخهای ایمنی ذاتی و سازگاری مخاطی و سیستمیک را تغییر میدهند [80]. پروبیوتیک ها با سلول های اپیتلیال تعامل دارند و با تغییر مسیرهای انتقال سیگنال سلولی، انتشار سیتوکین را تعدیل می کنند [81]. سویه های مختلف پروبیوتیک با تحریک تولید اجزای مختلف سیستم ایمنی عمل می کنند. اینها شامل تحریک تولید IL-10 و-20 توسط سلولهای تک هسته ای در باکتریهای اسید لاکتیک [82]، القاء تولید IL-6 در لاکتوباسیلوس رامنوسوس GG [80] و پیشگیری از آپوپتوز ناشی از سیتوکین و فعال سازی غیرفعال کننده پروتئین کیناز فعال شده با میتوژن p38 پرو آپوپتوز توسط TNF، IL{17}} یا گاما اینترفرون در لاکتوباسیلوس رامنوسوس GG [83]، که نشان دهنده افزایش بقای سلول های روده است [79]. با توجه به تأثیرات روی ایمنی، استفاده از پروبیوتیک ها برای ترویج تشکیل SCFA منابع تغذیه ای و متابولیکی و همچنین ظرفیت لنفوسیت ها را برای از بین بردن ویروس افزایش می دهد و به طور بالقوه انتشار مجدد ویروس های نهفته را کاهش می دهد [84].
3.1.4. فعالیت ضد میکروبی پروبیوتیک ها
مکانیسم های دیگری که توسط آن پروبیوتیک ها رشد میکروبی را مهار می کنند عبارتند از سنتز اسیدهای آلی، مواد سمی و باکتریوسین ها [85]. باکتریهای اسید لاکتیک (LAB)، باکتریهای اسید پروپیونیک و بیفیدوباکتریها برای قرنها در صنایع نگهداری و تخمیر استفاده میشوند. عواملی که آنها را برای استفاده در نگهداری کارآمد می کند را می توان به pH پایین، کاهش مقادیر کربوهیدرات ها و تولید ترکیبات ضد میکروبی نسبت داد. این باکتری ها می توانند مواد ضد میکروبی تولید کنند و آنها را کاندید مناسبی برای انتخاب به عنوان یک پروبیوتیک می کند [86]. LAB اسیدهای آلی مانند اسید استیک، اسید لاکتیک و اسید پروپیونیک را از طریق تخمیر گلوکز تولید می کند. اسید لاکتیک و اسید استیک اثر مهاری بر مخمر، کپک ها و باکتری ها دارند [87]. علاوه بر افزایش pH، اسید تفکیک نشده روی غشای سلولی پخش می شود. تجزیه می شود و یون های H+ را در سیتوپلاسم آزاد می کند و باعث فروپاشی گرادیان الکتروشیمیایی و متعاقب آن باکتریوستاز یا مرگ باکتری ها می شود [88]. باکتریوسین های تولید شده توسط LAB پپتیدهای ضد میکروبی هستند که توسط ریبوزوم ها سنتز می شوند [89]. باکتریوسین ها عمدتاً غشای سلولی را هدف قرار می دهند، جوانه زنی هاگ را مهار می کنند، باعث غیرفعال شدن حامل های آنیونی می شوند و فعالیت آنزیمی را با اثر باکتریواستاتیک یا باکتری کشی بسته به حساسیت سلول تغییر می دهند. این پپتیدها معمولاً بر روی گونه های باکتریایی نزدیک به هم و باکتری های گرم مثبت مؤثر هستند [90].
3.1.5. پروبیوتیک های مورد استفاده برای اسهال مرتبط با آنتی بیوتیک
میکروبیوتای روده در طول پرواز فضایی در معرض تغییر قرار می گیرد و از آنتی بیوتیک ها برای درمان استفاده می شود [1]. اگرچه آنتی بیوتیک ها برای ریشه کن کردن عفونت های باکتریایی بسیار مهم هستند، اما آسیب قابل توجهی به میکروارگانیسم های موجود در میکروبیوتای روده وارد می کنند [91]. مصرف آنتی بیوتیک می تواند باعث مشکلات مختلفی مانند کلونیزاسیون توسط کلستریدیوم دیفیسیل بیماری زا شود که باعث مشکلات مزمن دستگاه گوارش و اسهال شدید می شود. در شرایط عادی، C. difficile با رقابت با باکتریهای مشترک در دستگاه گوارش مواجه میشود، اما وقتی میکروبیوتای روده در معرض خطر قرار میگیرد (همانطور که در طول سفر فضایی مشاهده شد)، C. difficile میتواند دستگاه را مستعمره کند [92]. پروبیوتیک ها را می توان برای پرکردن میکروبیوتای دستگاه گوارش استفاده کرد و همچنین می توان از آنها برای درمان عفونت های C. difficile استفاده کرد [93]. از پروبیوتیک ها می توان برای درمان اسهال ناشی از آنتی بیوتیک استفاده کرد.
3.1.6. پروبیوتیک ها به عنوان پیشگیری از سرطانr
به دلیل قرار گرفتن در معرض تشعشعات، احتمال ابتلا به سرطان در فضانوردان بیشتر است. مصرف شیر سویا تخمیر شده با پروبیوتیک ها به عنوان یک اقدام پیشگیرانه در برابر سرطان سینه از طریق اثر ضد استروژنی ایزوفلاون ها عمل می کند [94]. ایجاد سرطان روده بزرگ به عوامل مختلفی بستگی دارد. شواهد نشان داده است که بین تغییرات در ساختار میکروبیوم روده و ایجاد سرطان کولورکتال ارتباط وجود دارد. پروبیوتیک ها ممکن است بر نحوه ارتباط سیستم ایمنی و میکروبیوتای روده تأثیر بگذارند و ممکن است به پیشگیری از سرطان کولورکتال کمک کنند [95]. کفیر (شیر تخمیر شده با پروبیوتیک ها) حاوی ترکیبات فعال زیستی مانند پلی ساکاریدها و پپتیدها است که می تواند از تکثیر و القای آپوپتوز در سلول های تومور جلوگیری کند. مطالعات نشان داده اند که کفیر می تواند روی سرطان روده بزرگ و سینه تاثیر بگذارد [96].

گیاه سیستانچ سیستم ایمنی را افزایش می دهد
3.1.7. پروبیوتیک ها برای استرس/اضطراب
حفظ شرایط عاطفی و فیزیکی فضانوردان یک عامل حیاتی برای ماموریت های فضایی طولانی مدت آینده است. استرس بدون شک یکی از نگرانکنندهترین عواملی است که به دلیل اثراتی که بر سلامت و عملکرد انسان دارد، میتواند بر رفاه کلی خدمه تأثیر بگذارد [97]. اضطراب و استرس با دیس بیوز روده مرتبط است. مطالعه ما و همکاران. [31] گزارش کردند که مصرف لاکتوباسیلوس پلانتاروم P{4}} علائم اضطراب/استرس را در انسان بهبود می بخشد. همچنین کشف شد که مصرف پروبیوتیک مسیر سنتز متابولیت گاما آمینوبوتیریک اسید (GABA) را توسط Bifidobacterium adolescentis غنی می کند، GABA و هیستامین انتقال دهنده های عصبی مهمی هستند که از طریق عصب واگ به محور روده-مغز حرکت می کنند.
3.1.8. پروبیوتیک ها برای عفونت دستگاه ادراری
پروبیوتیکهایی مانند Lactobacillus rhamnosus GR-1 و Lactobacillus reuteri RC-14 دارای خواص ضد عفونی هستند که در زنان آزمایش شده است و به نظر میرسد که به میزان قابل توجهی از UTI جلوگیری میکند. ضد میکروبی بدون واکنش [3].
جدول 3. پروبیوتیک ها: مکانیسم اثر و مزایای سلامتی آنها.
3.1.9. اسیدهای چرب با زنجیره کوتاه و نقش آنها در نگهداری میکروبیوتای روده
پروبیوتیک ها می توانند اسیدهای چرب با زنجیره کوتاه (SCFAs) تولید کنند [98]. SCFA ها محصولات جانبی آلی تخمیر هستند. هنگامی که کربوهیدرات های غیرقابل هضم در محیط بی هوازی توسط میکروبیوتای روده به طور ناقص تجزیه می شوند، در مجرای روده تولید می شوند. SCFA ها عمدتاً از استات، بوتیرات و پروپیونات تشکیل شده اند [99,100]. SCFA ها نقش مهمی در تنظیم سیستم ایمنی دارند. نگهداری، ساختار و تولید مخاط روده به میکروبیوتای روده و رژیم غذایی بستگی دارد. یک رژیم غذایی غنی از فیبر منجر به تولید SCFAs توسط میکروبیوتای روده می شود که باعث بهبود تولید موکوس و پپتید ضد میکروبی و بیان بالاتر پروتئین های TJ می شود. رژیم غذایی با کمبود فیبر منجر به تغییر میکروبیوتای روده می شود که منجر به افت لایه مخاطی و افزایش حساسیت به عفونت ها و بیماری های التهابی مزمن می شود [100]. SCFA ها همچنین مولکول های سیگنالی هستند که با اتصال به گیرنده های GPR41 و GPR43 سلول های اپیتلیال روده و سلول های ایمنی، تشکیل اینترلوکین را تنظیم می کنند [101]. مطالعه سیلوا و همکاران. [102] گزارش کرده است که SCFA ها ممکن است با حمایت از یکپارچگی سد خونی مغزی (BBB)، تعدیل انتقال عصبی، تأثیر بر سطوح فاکتور نوروتروفیک و تقویت حافظه، تأثیر مستقیمی بر مغز داشته باشند. یک مطالعه گزارش داد که SCFA بوتیرات عملکرد سد روده را افزایش می دهد. پروتئین کیناز فعال شده با آدنوزین مونوفسفات (AMPK) پس از فعال شدن، مونتاژ اتصال محکم را تسهیل می کند و مسیرهای متابولیک را در متابولیسم اسیدهای چرب و سنتز پروتئین تنظیم می کند [103]. MARS 500 یک آزمایش زمینی شش ماهه بود که شامل معاینه مدفوع شش خدمه بود. نتایج یک تغییر مداوم در فراوانی نسبی Faecalibacterium prausnitzii و Roseburia faecis تولیدکننده بوتیرات را در میکروبیوتای روده همه اعضای خدمه نشان داد. این نشان دهنده تغییر در تولید SCFA و پیامدهای احتمالی برای حمایت از رابطه متقابل میکروبیوتا-میزبان است [7]. قصر قمری 1 آزمایش دیگری است که روی زمین انجام شد. از سه خدمه برای آزمایش عملکرد سیستم پشتیبانی حیات زیستی (BLSS) استفاده شد. آنها یک رژیم غذایی با فیبر بالا مصرف کردند و یک جدول زمانی ثابت را دنبال کردند که شامل کارهای دستی قابل توجهی در کابین گیاه بود. نتایج تغییرات مشابهی را در ترکیب میکروبیوتای روده در اعضای خدمه با تنوع و تعداد میکروارگانیسمهای Lachnospira، Faecalibacterium و Blautia نشان داد. این همچنین تصریح می کند که یک رژیم غذایی با فیبر بالا و سبک زندگی ممکن است برای حمایت از میکروبیوتای سالم روده مفید باشد [32].
3.2. میکروگرانش/مطالعات ریزگرانشی شبیه سازی شده بر روی پروبیوتیک ها
برای اینکه یک پروبیوتیک موثر باشد، باید ویژگی های خاصی داشته باشد. برخی از این موارد عبارتند از: پایداری در برابر اسید و صفرا، چسبیدن به سلول های روده انسان، تضاد با پاتوژن های روده ای و تولید مواد ضد میکروبی. با این حال، این ویژگی ها می توانند بر اساس عوامل محیطی و ریزگرانش تغییر کنند. مطالعات متعددی برای آزمایش پروبیوتیکها در شرایط in vitro و in vivo برای درک مزایای سلامتی بالقوه و ایمنی آنها برای سلامت فضانوردان در طول پرواز فضایی انجام شده است. برخی از این مطالعات را در پاراگراف های زیر خلاصه می کنیم. مطالعه ای که توسط شائو و همکاران انجام شد. [104] برای بررسی تأثیر شرایط ریزگرانش شبیهسازیشده بر لاکتوباسیلوس اسیدوفیلوس، تأثیر قابلتوجهی بر برخی فعالیتها و ویژگیهای بیولوژیکی نشان داد. یافته های کلیدی عبارت بودند از (1) عدم تغییر قابل توجه در مورفولوژی L. acidophilus، (2) کوتاه شدن فاز تاخیر، (3) افزایش سرعت رشد، (4) افزایش تحمل به اسیدها (pH 2.5) با مقاومت در برابر صفرا، (5) کاهش یافت. حساسیت به سدیم پنی سیلین، سفالکسین و جنتامایسین سولفور، (6) تغییر قابل توجهی در توانایی چسبندگی L. acidophilus، و (7) افزایش فعالیت ضد میکروبی علیه استافیلوکوکوس اورئوس و استافیلوکوکوس تیفی موریوم. این تغییرات ناشی از ریزگرانش شبیه سازی شده (SMG) روی پروبیوتیک های L. acidophilus می تواند برای فضانوردان در طول پرواز فضایی مفید باشد. این پروبیوتیک ها می توانند شرایط استرس زا را تحمل کنند و برای مدت طولانی تری در دستگاه گوارش باقی بمانند. از آنجایی که هیچ تغییری در توانایی چسبندگی آن ایجاد نمی شود، می تواند به حفظ عملکرد سد اپیتلیال روده و جلوگیری از ورود پاتوژن ها کمک کند [103]. در مطالعه دیگری، Senatore و همکاران. [105] لاکتوباسیلوس رویتری را برای متابولیسم و بیان ژن آن در شرایط SMG مورد بررسی قرار داد. آنها هیچ تغییری در رشد باکتری، اندازه و شکل سلول نسبت به شاهد پیدا نکردند. از سوی دیگر، افزایش تحمل برای عبور دستگاه گوارش و افزایش تولید ترکیب فعال زیستی روترین مشاهده شد [32]. کپسول لاکتوباسیلوس کازئی سویه Shirota (LcS) منجمد خشک شده برای پایداری آن در ISS به مدت یک ماه آزمایش شد. کپسولهای LcS از پرواز فضایی در پروفایلهای ژنتیکی، الگوهای رشد، تخمیر کربوهیدرات، واکنشپذیری به آنتیبادیهای خاص LcS و توانایی القای سیتوکین با توجه به نمونههای کنترلی که در آزمایشگاه زمینی نگهداری میشوند، تفاوتی نداشتند. LcS نشان داده است که ایمنی ذاتی را تقویت می کند و میکروبیوتای روده را متعادل می کند و می تواند برای مبارزه با مشکلات ایمنی مرتبط با پرواز فضایی استفاده شود [6،44].
3.3. ماندگاری و بقای پروبیوتیک های تجاری در یک دستگاه گوارش شبیه سازی شده
سه پروبیوتیک تجاری، یعنی لاکتوباسیلوس اسیدوفیلوس سویه DDS-1، بیفیدوباکتریوم لانگوم سویه BB536 و هاگ باسیلوس سوبتیلیس سویه HU58 برای بقا در شرایطی که انتظار میرود در طی یک سفر رفت و برگشت سالانه 3- به مریخ با آنها مواجه شویم، آزمایش شدند. پارامترهای مورد آزمایش قرار بقا برای: 1. ذخیره سازی طولانی مدت در شرایط محیطی. 2. تشعشعات کیهانی شبیه سازی شده کهکشانی و تابش رویداد ذرات خورشیدی. 3. قرار گرفتن در معرض مایع معده شبیه سازی شده. 4. قرار گرفتن در معرض مایع روده شبیه سازی شده. طبق این مطالعه، قرار گرفتن در معرض تابش تاثیر کمی بر سویه های پروبیوتیک مورد بررسی داشت. با این حال، عمر مفید و نرخ بقای سه سویه به طور قابل توجهی در طول شبیهسازی عبور آنها از دستگاه گوارش فوقانی متفاوت بود. بر اساس یافته ها، تنها هاگ های باسیلوس سوبتیلیس می توانند در همه شرایط زنده بمانند. این نشان می دهد که پروبیوتیک های ساخته شده از هاگ های باکتری ممکن است یک انتخاب مناسب برای سفر طولانی مدت انسان به فضا باشد [106].
4. نتیجه گیری
برای سفرهای فضایی طولانی مدت، یک عامل مهم حفظ سلامت فضانورد است. تغییرات فیزیولوژیکی مختلفی در سلامت خدمه پرواز مشاهده شده است که شامل مواردی مانند تغییر در میکروبیوم روده است که منجر به تغییر اثر محور MGB بر سلامت روان، عفونتهای دستگاه تناسلی، فعال شدن مجدد ویروس، مقاومت باکتریها و... تغییرات در حدت، کاهش ایمنی و تغییر در پاسخ ایمنی، مشکلات قلبی عروقی و ایجاد سرطان به دلیل قرار گرفتن در معرض اشعه. این بررسی تلاش میکند تا کاربرد احتمالی پروبیوتیکها را که میتواند برای مقابله با این مسائل بهداشتی ناشی از پرواز فضایی مورد استفاده قرار گیرد، درک کند. حفظ میکروبیوم روده برای سفرهای فضایی طولانی مدت مهم است و بسیاری از بیماری ها به دلیل تغییر یا عدم تعادل در میکروبیوم روده ایجاد می شوند. با توجه به مزایای شناخته شده پروبیوتیک ها برای میکروبیوم روده و سلامت کلی، استفاده از آنها به عنوان یک مکمل غذایی یا به عنوان افزودنی به غذا در طول پرواز فضایی می تواند جایگزینی امیدوارکننده برای مقابله با اختلالات و پیامدهای سلامتی باشد که مسافران فضایی تجربه می کنند. با این حال، آزمایشهای انجامشده بر روی پروبیوتیکها در شرایط ریزگرانشی شبیهسازیشده، به طور کامل سفر فضایی طولانیمدت را تقلید نمیکند. مطالعات بیشتری باید بر روی پروبیوتیک ها انجام شود تا استفاده از آنها در فضا تأیید شود، اثربخشی آنها به عنوان اقدامات متقابل برای مسائل بهداشتی ذکر شده در بالا بررسی شود، و خواص پروبیوتیک ها که ممکن است در طول پرواز فضایی رخ دهند تغییر دهند.
منابع
1. Voorhies, AA; مارک اوت، سی. مهتا، س. پیرسون، دی ال. Crucian، BE; فیسون، ا. Oubre، CM; تورالبا، م. مونسرا، ک. ژانگ، ی. و همکاران مطالعه تاثیر ماموریت های فضایی طولانی مدت در ایستگاه فضایی بین المللی بر میکروبیوم فضانوردان. علمی نسخه 2019، 9، 9911. [CrossRef] [PubMed]
2. ییم، ج. چو، SW; کیم، بی. پارک، اس. هان، YH; Seo, SW پروفایل رونویسی سویه پروبیوتیک اشرشیاکلی موضوع 1917 تحت ریزگرانش شبیه سازی شده. بین المللی جی. مول. علمی 2020، 21، 2666. [CrossRef]
3. اوربانیاک، سی. Reid, G. تأثیر بالقوه میکروبیوتا و پروبیوتیک ها بر زنان در طول پروازهای فضایی طولانی. سلامت زنان 2016، 12، 193-198. [CrossRef]
4. هیل، سی. گارنر، اف. رید، جی. گیبسون، GR; مرنشتاین، دی جی؛ پات، بی. مورلی، ال. کنانی، RB; فلینت، اچ جی; سالمینن، اس. و همکاران بیانیه اجماع انجمن علمی بین المللی پروبیوتیک ها و پری بیوتیک ها در مورد دامنه و استفاده مناسب از اصطلاح پروبیوتیک. نات. Rev. Gastroenterol. هپاتول. 2014، 11، 506-514. [CrossRef]
5. ماتسوموتو، ک. تاکادا، تی. شیمیزو، ک. کادو، ی. کاواکامی، ک. ماکینو، آی. یامائوکا، ی. هیرانو، ک. نیشیمورا، ا. کاجیموتو، او. و همکاران اثرات یک فرآورده شیر پروبیوتیک حاوی لاکتوباسیلوس کازئی سویه Shirota بر دفعات دفع و میکرو فلور روده داوطلبان وضعیت سلامتی پایین: یک مطالعه متقاطع تصادفی شده با کنترل دارونما. Biosci. میکرو فلورا 2006، 25، 39-48. [CrossRef]
6. ساکائی، ت. متکی، ی. تاکاهاشی، تی. شیدا، ک. کیواکی، م. شیماکاوا، ی. ماتسویی، ا. چونان، او. موریکاوا، ک. اوتا، تی. و همکاران پروبیوتیکها در فضای بیرونی: ارزیابیهای امکانسنجی پروبیوتیکهای خشک انجمادی محصور شده در طی یک ماه ذخیرهسازی در ایستگاه فضایی بینالمللی. علمی 2018، 8، 10687. [CrossRef] [PubMed]
7. تورونی، س. رامپلی، اس. بیاگی، ای. کنسلندی، ج. سورگنینی، م. پیانو، سی. کوئرسیا، اس. سوورینی، م. Carbonero، FG; بیانکونی، جی. و همکاران پویایی زمانی میکروبیوتای روده در افرادی که یک محیط محدود را به اشتراک می گذارند، یک 520-شبیه سازی فضایی زمینی روزانه، MARS500. Microbiome 2017, 5, 39. [CrossRef] [PubMed]
8. ژانگ، تی. لی، کیو. چنگ، ال. بوچ، اچ. Zhang, F. Akkermansia muciniphila یک پروبیوتیک امیدوارکننده است. میکروب. بیوتکنول. 2019، 12، 1109–1125. [CrossRef] [PubMed]
9. سوکول، ح. پیگنور، بی. واترلوت، ال. لخدری، ا. Bermúdez-Humarán، LG; Gratadoux، JJ; بلوجون، اس. بریدونو، سی. Furet، JP; کورتیر، جی. و همکاران Faecalibacterium prausnitzii یک باکتری ضد التهابی مشترک است که با تجزیه و تحلیل میکروبیوتای روده بیماران مبتلا به بیماری کرون شناسایی شده است. Proc. Natl. آکادمی علمی ایالات متحده آمریکا 2008، 105، 16731-16736. [CrossRef]
10. گوتووا، آی. دیمیتروف، ز. Najdenski، H. لاکتوباسیلوس بولگاریکوس و استرپتوکوکوس ترموفیلوس انتخاب شده از ماست بلغاری پتانسیل ضد التهابی قابل توجهی را نشان می دهد. Acta Microbiol. Bulg 2017, 33, 137-142.
11. روز، RL; هارپر، ای جی؛ Woods, RM; دیویس، OG; Heaney، LM Probiotics: چشم انداز فعلی و افق های آینده. علوم آینده OA 2019, 5, FSO391. [CrossRef] [PubMed]
12. صراف، ک. Shashikanth، MC; پری، تی. سلطانا، ن. Chaitanya، NC پروبیوتیک ها در پزشکی و دندانپزشکی نقش دارند. J. Assoc. پزشکان هند 2010، 58، 488-490.
13. داگلاس، جی. Voorhies، A. انتخاب مبتنی بر شواهد گونههای پروبیوتیک برای ارتقای سلامت فضانوردان یا کاهش علائم بیماری در ماموریتهای طولانی مدت پرواز فضایی. سود. Microbes 2017, 8, 727-737. [CrossRef] [PubMed]
14. کروسیان، بی. استو، RP; مهتا، س. کیریارته، اچ. پیرسون، دی. سامز، سی. تغییرات در ایمنی تطبیقی در طول پروازهای فضایی طولانی مدت ادامه دارد. npj Microgravity 2015، 1، 15013. [CrossRef] [PubMed]
15. لیو، ز. لو، جی. دو، آر. سان، دبلیو. لی، جی. لان، اچ. چن، پی. یوان، ایکس. کائو، دی. لی، ی. و همکاران اثرات پرواز فضایی بر ترکیب و عملکرد میکروبیوتای روده انسان میکروب های روده 2020، 11، 807-819. [CrossRef]
16. O'Flaherty، S. Klaenhammer، TR نقش و پتانسیل باکتری های پروبیوتیک در روده، و ارتباط بین میکرو فلور روده و روده/میزبان. بین المللی Dairy J. 2010, 20, 262-268. [CrossRef]
17. تورونی، ف. ونتورا، ام. Butto، LF; دورانتی، س. O'Toole، PW; Motherway، MO; ون سیندرن، دی. گفتگوی مولکولی بین میکروبیوتای روده انسان و میزبان: دیدگاه لاکتوباسیلوس و بیفیدوباکتریوم. سلول. مول. زندگی علمی. 2014، 71، 183-203. [CrossRef]
18. دیوار، ر. کریان، جی اف. راس، RP; فیتزجرالد، GF; دینان، TG; Stanton, C. ترکیبات عصبی باکتریایی تولید شده توسط سایکوبیوتیک ها. Adv. انقضا پزشکی Biol. 2014، 817، 221-239.
19. بلابر، ای. مارچال، اچ. Burns، BP Bioastronautics: تاثیر ریزگرانش بر سلامت فضانوردان. Astrobiology 2010, 10, 463-473. [CrossRef]
20. کروسیان، بی. بابیاک وازکز، ا. جانستون، اس. پیرسون، دی ال. Ott، CM; Sams, C. بروز علائم بالینی در طول پروازهای فضایی مداری طولانی مدت. بین المللی جی ژنرال مد. 2016، 2016، 383–391. [CrossRef]
21. Garrett-Bakelman، FE; درشی، م. گرین، اس جی. Gur، RC; لین، ال. Macias، BR; مک کنا، ام جی؛ میدان، سی. میشا، ت. نسرینی، ج. و همکاران دوقلوهای ناسا تجزیه و تحلیل چند بعدی از یک سال پرواز فضایی انسان را مطالعه می کنند. Science 2019, 364, 6436. [CrossRef]
22. صدیقی، ر. قیصر، ر. خان، ن.ا. الحربی، ع.م. الفهمی، ح. الموسلحی، الف. اثر ریزگرانش بر ترکیب باکتری میکروبیوتای روده در مدل تخلیه اندام عقبی. Life 2022، 12، 1865. [CrossRef] [PubMed]
23. جیانگ، پی. گرین، اس جی. چلیپالا، جنرال الکتریک؛ تورک، FW; Vitaterna، MH تغییرات قابل تکرار در میکروبیوم روده نشان دهنده تغییر در متابولیسم میکروبی و میزبان در طول پرواز فضایی است. Microbiome 2019, 7, 113. [CrossRef] [PubMed]
24. کارابوتی، م. سیروکو، آ. Maselli، MA; Severi, C. محور روده-مغز: تعاملات بین میکروبیوتای روده، سیستم عصبی مرکزی و روده ای. ان گاستروانترول 2015، 28، 203-209. [PubMed]
25. Sajdel-Sulkowska، اختلال EM در محور میکروبیوتا-روده-مغز (MGB) و سلامت روان فضانوردان در طول سفرهای فضایی طولانی مدت. در کتابچه راهنمای اختلالات مخچه و مخچه; Manto, M., Gruol, D., Schmahmann, J., Koibuchi, N., Sillitoe, R., Eds.; Springer: Cham، سوئیس، 2019. [CrossRef]
26. پالینکاس، لس آنجلس مسائل روانی اجتماعی در پرواز طولانی مدت فضایی: بررسی اجمالی. گراویت. بیول فضایی گاو نر 2001، 14، 25-33.
27. مالیس، م.م. DeRoshia، CW ریتم های شبانه روزی، خواب، و عملکرد در فضا. هوانوردی. محیط فضایی پزشکی 2005، 76، B94–B107. [PubMed]
28. اولوافمی، FA; عبدالباکی، ر. لای، JCY؛ Mora-Almanza، JG; Afolayan، EM مروری بر سلامت روان فضانوردان در ماموریت های سرنشین دار: مداخلات بالقوه برای چالش های شناختی و سلامت روان. زندگی علمی. Space Res. 2021، 28، 26-31. [CrossRef]
29. آرون، ا. ایوالدی، تی. لوگانوفسکی، ک. پالرمو، اس. پارا، ای. فلامینی، دبلیو. مارازیتی، دی. بار اکتشاف فضایی بر سلامت روان فضانوردان: مروری روایی. کلین Neuropsychiatry 2021, 18, 237. [PubMed]
30. زیوی، ص. دی جنارو، ال. Ferlazzo، F. خواب در ایزوله، محدود و شدید (ICE): مروری بر عوامل مختلف مؤثر بر خواب انسان در ICE. جلو. نوروسک. 2020, 14, 851. [CrossRef]
31. ما، ت. جین، اچ. Kwok، LY; سان، ز. لیونگ، MT; Zhang، H. مصرف پروبیوتیک استرس و علائم اضطراب انسان را احتمالاً از طریق تعدیل پتانسیل عصبی میکروبیوتای روده کاهش داد. نوروبیول. استرس 2021، 14، 100294. [CrossRef]
32. هائو، ز. لی، ال. فو، ی. لیو، اچ. تأثیر ساختار رژیم غذایی و سبک زندگی سیستم حمایت از زندگی احیاکننده بر میکروبیوتای روده: شبیهسازی فضایی زمینی 105-روزانه در قصر قمری 1. محیط زیست. میکروبیول. 2018، 20، 3643–3656. [CrossRef] [PubMed]
33. جونز، ج.ا. جنینگز، آر. پیتریزک، آر. چیفتچی اوغلو، ن. Stepaniak، P. مسائل مربوط به دستگاه ادراری تناسلی در طول پرواز فضایی: بررسی. بین المللی جی. ایمپوت. Res. 2005، 17 (ضمیمه 1)، S64–S67. [CrossRef] [PubMed]
34. مشرا، ب. Luderer, U. خطرات باروری سفر فضایی در زنان و مردان. Nat Rev Endocrinol. 2019، 15، 713-730، Erratum در Nat. کشیش اندوکرینول. 2019، 15، 713–730. [CrossRef] [PubMed]
35. سوننفلد، جی. شیرر، عملکرد ایمنی WT در طول پرواز فضایی. تغذیه 2002، 18، 899-903. [CrossRef] [PubMed]
36. رونی، BV; Crucian، BE; پیرسون، دی ال. Laudenslager، ML; مهتا، SK فعال شدن مجدد ویروس هرپس در فضانوردان در طول پرواز فضایی و کاربرد آن بر روی زمین. جلو. میکروبیول. 2019، 10، 16. [CrossRef]
37. ژانگ، بی. بای، پ. ژائو، ایکس. یو، ی. ژانگ، ایکس. لی، دی. لیو، سی. افزایش نرخ رشد و مقاومت آمیکاسین سالمونلا انتریتیدیس پس از یک ماه پرواز فضایی در فضاپیمای Shenzhou-11 چین. MicrobiologyOpen 2019, 8, e00833. [CrossRef]
38. تیرومالی، م.ر. کارویا، ف. تران، کیو. استپانوف، وی.جی. بروس، RJ; Ott، CM; پیرسون، دی ال. فاکس، جنرال الکتریک ارزیابی مقاومت آنتیبیوتیکی اکتسابی در اشریشیا کلی که در معرض میکروگرانش مدلسازی شده با برش کم طولانیمدت و قرار گرفتن در معرض آنتیبیوتیک پسزمینه قرار گرفته است. MBio 2019, 10, e02637-18. [CrossRef]
39. موریسون، MD; Thissen, JB; کارویا، ف. مهتا، س. اوربانیاک، سی. ونکاتسواران، ک. اسمیت، دی جی; جین، سی. بررسی تغییرات ناشی از پرواز فضایی در میکروبیوم فضانوردان. جلو. میکروبیول. 2021, 12, 659179. [CrossRef]
40. Turner, JR عملکرد سد مخاطی روده در سلامت و بیماری. نات. کشیش ایمونول. 2009، 9، 799-809. [CrossRef]
41. زیرک، ع.ا. سیچون، سی. هلمز، اس. اندرز، سی. سوننبورن، یو. Schmidt, MA مکانیسمهای مولکولی زیربنای اثرات پروبیوتیک اشرشیاکلی Nissle 1917 شامل توزیع مجدد ZO-2 و PKCζ است که منجر به اتصال محکم و ترمیم سد اپیتلیال میشود. سلول. میکروبیول. 2007، 9، 804-816. [CrossRef]
42. جانسون-هنری، KC; دوناتو، کالیفرنیا؛ شن تو، جی. گردنپور، م. شرمن، PM Lactobacillus rhamnosus سویه GG از تغییرات انتروهموراژیک اشریشیا کلی O157:H7- در عملکرد سد اپیتلیال جلوگیری می کند. آلوده کردن ایمنی 2008، 76، 1340-1348. [CrossRef] [PubMed]
43. آلوارز، ر. لک لک، کالیفرنیا؛ Sayoc-Becerra، A. مارچلتا، RR; Prisk، GK; McCole، DF یک محیط ریزگرانشی شبیه سازی شده باعث ایجاد نقص پایدار در عملکرد سد اپیتلیال می شود. علمی جمهوری 2019، 9، 17531. [CrossRef] [PubMed]
44. Arrieta، MC; بیستریتس، ال. Meddings، JB تغییرات در نفوذپذیری روده. روده 2006، 55، 1512-1520. [CrossRef]
45. لی، SH تنظیم نفوذپذیری روده توسط اتصال محکم: مفهوم بر بیماری های التهابی روده. intest. Res. 2015، 13، 11. [CrossRef]
46. Blair, SA; کین، اس وی؛ کلیبورگ، DR; Turner, JR بیان و فعالیت کیناز زنجیره سبک میوزین اپیتلیال در بیماری التهابی روده تنظیم می شود. آزمایشگاه. تحقیق کنید. 2006، 86، 191-201. [CrossRef]
47. یی، اچ. وانگ، ال. Xiong، Y. وانگ، ز. کیو، ی. ون، ایکس. جیانگ، ز. یانگ، ایکس. Ma، X. Lactobacillus reuteri LR1 بیان ژنهای پروتئینهای اتصال محکم را از طریق مسیر MLCK در سلولهای IPEC{2}} در طی عفونت با انتروتوکسیژنیک اشریشیا کلی K88 بهبود بخشید. واسطه التهاب 2018, 2018, 6434910. [CrossRef] [PubMed]
48. Kaur، I. سیمونز، ای آر. کاسترو، ویرجینیا; مارک اوت، سی. پیرسون، DL تغییرات در عملکرد نوتروفیل در فضانوردان. رفتار مغز. ایمنی 2004، 18، 443-450. [CrossRef]
49. Stowe, RP; Sams، CF; پیرسون، DL اثرات مدت زمان ماموریت بر پاسخ های عصبی ایمنی در فضانوردان. هوانوردی. محیط فضایی پزشکی 2003، 74، 1281-1284.
50. Makedonas، G. مهتا، س. چوکر، آ. سیمپسون، RJ; مارشال، جی. نارنجی، JS؛ Aunon-Chancellor، S. اسمیت، اس ام. زوارت، اس آر. استو، RP; و همکاران پروتکل مقابله ایمونولوژیک ویژه برای ماموریت های اکتشاف در اعماق فضا. جلو. ایمونول. 2019، 10، 2407. [CrossRef]
51. بوخهایم، جی. ماتزل، اس. رایکوا، م. واسیلیوا، جی. پونومارف، اس. نیچیپوروک، آی. هورل، ام. موزر، دی. بییر، ک. فویرکر، ام. و همکاران تغییر ناشی از استرس به سمت التهاب در فضانوردان پس از پرواز طولانی مدت فضایی. جلو. فیزیول. 2019، 10، 85. [CrossRef]
52. آکیاما، ت. هوری، ک. هینوی، ای. هیرایوا، م. کاتو، ا. مائکاوا، ی. تاکاهاشی، ا. Furukawa، S. چگونه پرواز فضایی بر سیستم ایمنی اکتسابی تأثیر می گذارد؟ npj Microgravity 2020، 6، 14. [CrossRef]
53. Kaur، I. سیمونز، ای آر. کاسترو، ویرجینیا; Ott، CM; پیرسون، DL تغییرات در عملکرد مونوسیت فضانوردان. رفتار مغز. ایمنی 2005، 19، 547-554. [CrossRef] [PubMed]
54. Voss، EW بی وزنی طولانی مدت و ایمنی هومورال. Science 1984, 225, 214-215. [CrossRef] [PubMed]
55. Mills, PJ; Meck, JV; واترز، WW; D'Aunno، D. Ziegler، MG زیرجمعیتهای لکوسیت محیطی و سطوح کاتکول آمین در فضانوردان به عنوان تابعی از مدت مأموریت. روانی پزشکی 2001، 63، 886-890. [CrossRef] [PubMed]
56. استو، RP; Sams، CF; مهتا، SK; کائور، آی. جونز، ام ال. بازخورد، DL; پیرسون، زیرمجموعه های لکوسیت DL و عملکرد نوتروفیل پس از پرواز فضایی کوتاه مدت. J. Leukoc. Biol. 1999، 65، 179-186. [CrossRef]
57. گوئل، ا. براک، L. سندرم بی شرایطی قلبی عروقی در طول پروازهای فضایی. ان کاردیول D'angéiol. پاریس 1989، 38، 499-502.
58. تانگ، اچ. افزایش، HH; مججی، م. براون، RD تغذیه درازمدت فضایی: بررسی محدوده. مواد مغذی 2021، 14، 194. [CrossRef]
59. کیانی، EG; مارتین-یبرا، ا. لندرانی، ف. بولیا، جی. لاگونا، پی. وایدا، پی. بی وزنی و اختلالات ریتم قلبی: دانش فعلی از مطالعات پرواز فضایی و استراحت در بستر. جلو. اختر. علوم فضایی 2016، 3، 27. [CrossRef]
60. ژیان، ی. ژانگ، دی. لیو، ام. وانگ، ی. خو، Z.-X. تأثیر میکروبیوتای روده بر آنتریت ناشی از تشعشع. جلو. سلول. آلوده کردن میکروبیول. 2021, 11, 586392. [CrossRef]
61. تسه ای، د. جوچینکو، ا. لینچ، ا. Urbaniak, C. درک پیچیدگیها و تغییرات میکروبیوم فضانورد برای مأموریتهای فضایی طولانی مدت موفق. Life 2022, 12, 495. [CrossRef]
62. دورانته، م. کوسینوتا، FA سرطان زایی یون سنگین و اکتشاف فضای انسانی. نات. Rev. Cancer 2008, 8, 465-472. [CrossRef] [PubMed]
63. Stahn، AC; ورنر، آ. اوپاتز، او. Maggioni، MA; استایناچ، ام. فون اهلفلد، فولکس واگن؛ مور، ا. Crucian، BE; اسمیت، اس ام. زوارت، اس آر. و همکاران افزایش دمای هسته بدن در فضانوردان در طول ماموریت های فضایی طولانی مدت. علمی Rep. 2017, 7, 16180. [CrossRef] [PubMed]
64. کلیگلر، بی. Cohrsen, A. پروبیوتیک ها. 2008. در دسترس آنلاین: www.aafp.org/afp (در 25 ژانویه 2022 قابل دسترسی است).
65. کانینگهام، م. Azcarate-Peril، MA; بارنارد، ا. بنوا، وی. گریمالدی، آر. گیونت، دی. Holscher، HD; هانتر، ک. مانورونگ، اس. اوبیس، دی. و همکاران شکل دادن به آینده پروبیوتیک ها و پری بیوتیک ها Trends Microbiol. 2021، 29، 667-685. [CrossRef]
66. شی، الح. بالاکریشنان، ک. تیاگارجاه، ک. محمد اسماعیل، NI; یین، OS خواص مفید پروبیوتیک ها. تروپ زندگی علمی. Res. 2016، 27، 73-90. [CrossRef]
67. اوللوویشوا، د. اندرسون، آرسی مک نب، WC; موگان، پی جی. ولز، جی.ام. روی، NC تنظیم نفوذپذیری اتصال محکم توسط باکتری های روده و اجزای غذایی. J. Nutr. 2011، 141، 769-776. [CrossRef] [PubMed]
68. Mack, DR; آرنه، اس. هاید، ال. وی، اس. Hollingsworth، MA ترشح موسین خارج سلولی MUC3 به دنبال چسبیدن سویه های لاکتوباسیلوس به سلول های اپیتلیال روده در شرایط آزمایشگاهی است. روده 2003، 52، 827-833. [CrossRef]
69. Caballero-Franco، C. کلر، ک. دی سیمون، سی. Chadee, K. فرمول پروبیوتیک VSL#3 بیان و ترشح ژن موسین را در سلول های اپیتلیال کولون القا می کند. صبح. J. Physiol.-Gastrointest. فیزیول کبد 2007، 292، G315–G322. [CrossRef]
70. اوت، جی.ام. Podolsky، DK مدولاسیون عملکردی انتروسیت ها توسط میکروارگانیسم های گرم مثبت و گرم منفی. صبح. J. Physiol.-Gastrointest. فیزیول کبد 2004، 286، G613–G626. [CrossRef]
71. کانکاینن، م. پائولین، ال. تینکینن، اس. فون اسوفسکی، آی. ریونانن، جی. پارتانن، پ. ساتوکاری، ر. وسترلوند، اس. هندریککس، APA؛ لبیر، اس. و همکاران تجزیه و تحلیل مقایسه ای ژنومی لاکتوباسیلوس رامنوسوس GG پیلی حاوی پروتئین اتصال انسان به مخاط را نشان می دهد. Proc. Natl. آکادمی علمی ایالات متحده آمریکا 2009، 106، 17193-17198. [CrossRef]
72. موکای، ت. کانکو، اس. ماتسوموتو، ام. Ohori، H. اتصال Bifidobacterium bifidum و Lactobacillus reuteri به بخشهای کربوهیدراتی گلیکولیپیدهای روده که توسط آگلوتینین بادام زمینی شناسایی شدهاند. بین المللی جی. میکروبیول غذایی. 2004، 90، 357-362. [CrossRef]
73. تالون، آر. آریاس، س. برسلیه، پی. Urdaci، MC چسبندگی وابسته به سویه و ماتریکس لاکتوباسیلوس پلانتاروم توسط ترکیبات باکتریایی پروتئینی انجام می شود. J. Appl. میکروبیول. 2007، 102، 442-451. [CrossRef] [PubMed]
74. ویلسون، خ. Perini، F. نقش رقابت برای مواد مغذی در سرکوب کلستریدیوم دیفیسیل توسط میکرو فلور کولون. آلوده کردن ایمنی 1988، 56، 2610-2614. [CrossRef] [PubMed]
75. دای، سی. ژنگ، سی کیو; جیانگ، م. Ma، XY; جیانگ، ال جی پروبیوتیک ها و سندرم روده تحریک پذیر. World J. Gastroenterol. 2013، 19، 5973-5980. [CrossRef] [PubMed]
76. تویی، م. هیروتا، اس. توموتکی، ع. ساتو، ن. حظومی، ی. عنان، ک. ناگاشیما، تی. توکودا، ی. ماسودا، ن. اوسومی، س. و همکاران نوشیدنی پروبیوتیک با مصرف ایزوفلاون سویا برای پیشگیری از سرطان پستان: مطالعه مورد شاهدی. Curr. Nutr. علوم غذایی 2013، 9، 194-200. [CrossRef]
77. باکلی، ND; شامپاین، CP; ماسوتی، هوش مصنوعی؛ واگار، LE; تامپکینز، TA; Green-Johnson، JM مهار استراتژیهای غذایی کاربردی برای چالشهای سلامتی سفر فضایی - سویای تخمیر شده برای تغذیه فضانوردان. فضانورد Acta. 2011، 68، 731-738. [CrossRef]
78. رائو، RK; سمک، جی. حفاظت و بازیابی سد روده توسط پروبیوتیک ها: پیامدهای تغذیه ای و بالینی. Curr. Nutr. علوم غذایی 2013، 9، 99-107. [CrossRef] [PubMed]
79. Galdeano، CM; پردیگón، G. نقش زنده ماندن سویه های پروبیوتیک در ماندگاری آنها در روده و سیستم ایمنی داخل مخاطیتحریکJ. Appl. میکروبیول.2004, 97, 673–681. [CrossRef]
