خطر افزایش فشار خون و بیماری قلبی عروقی پس از اهدای کلیه زنده: آیا از نظر بالینی مرتبط است؟ قسمت 1
Apr 20, 2023
خلاصه
اولین پیوند موفقیت آمیز کلیه اهداکننده زنده در سال 1954 انجام شد. دریافت پیوند کلیه از اهداکننده کلیه زنده بهترین گزینه برای افزایش امید به زندگی و کیفیت زندگی در بیماران مبتلا به مرحله نهایی بیماری کلیوی است. با این حال، از سال 1954، سؤالات متعددی در مورد اخلاق اهدای کلیه زنده از نظر تأثیرات منفی بر امید به زندگی اهداکنندگان مطرح شده است. با توجه به رابطه نزدیک بین کاهش عملکرد کلیه در بیماران مبتلا به بیماری مزمن کلیه (CKD) و فشار خون بالا، بیماری قلبی عروقی و مرگ و میر قلبی عروقی، اطلاعات در مورد تأثیر اهدای کلیه بر این موارد به ویژه مرتبط است. در این مقاله، ما شواهد موجود را با تمرکز بر مطالعات جدیدتر در مورد تأثیر اهدای کلیه بر مرگ و میر همه علل، مرگ و میر قلبی عروقی، بیماری های قلبی عروقی و فشار خون بالا و همچنین نشانگرهای آسیب قلبی عروقی از جمله سفتی شریانی و کاردیومیوپاتی اورمیک بررسی می کنیم. . ما همچنین در مورد شباهتها و تفاوتهای بین کاهش پاتولوژیک عملکرد کلیه که در CKD رخ میدهد و کاهش عملکرد کلیه که به دلیل نفرکتومی اهداکننده رخ میدهد، بحث میکنیم. اهداکنندگان کلیه اقدامی نوع دوستانه انجام می دهند که به نفع بیماران فردی و همچنین جامعه گسترده تر است. آنها سزاوار داشتن شواهد با کیفیت بالا برای تصمیم گیری آگاهانه هستند.
طبق مطالعات مربوطه،سیستانچیک گیاه سنتی چینی است که قرن هاست برای درمان بیماری های مختلف استفاده می شود. داشتن آن از نظر علمی ثابت شده استضد التهاب، ضد پیری،وآنتی اکسیدانخواص مطالعات نشان داده اند که سیستانچ برای بیماران مبتلا به آن مفید استبیماری کلیوی. مواد فعال سیستانچ به عنوان کاهش دهنده شناخته شده استالتهاب, بهبود عملکرد کلیهوبازگرداندن سلول های آسیب دیده کلیه. بنابراین، ادغام cistanche در aبیماری کلیویطرح درمانی می تواند مزایای زیادی را برای بیماران در مدیریت شرایط خود ارائه دهد.سیستانچبه کاهش پروتئینوری کمک می کند، سطح BUN و کراتینین را کاهش می دهد و خطر ابتلا به آن را کاهش می دهدآسیب کلیه. علاوه بر این، سیستانچ همچنین به کاهش سطح کلسترول و تری گلیسیرید کمک می کند که می تواند برای بیماران مبتلا به بیماری کلیوی خطرناک باشد.

روی Cistanche Tubulosa For Kidney Disease کلیک کنید
برای اطلاعات بیشتر:
david.deng@wecistanche.com WhatApp:86 13632399501
کلید واژه ها:مرگ و میر همه علل، سفتی شریان، فشار خون، بیماری قلبی عروقی، مرگ و میر قلبی عروقی، بیماری مزمن کلیه، فشار خون بالا، اهدای کلیه، پیوند، کاردیومیوپاتی اورمیک
معرفی
در سال 1954، در سن 23 سالگی، رونالد هریک یک کلیه به برادر دوقلوی خود ریچارد اهدا کرد [1، 2]. این اولین پیوند موفقیت آمیز عضو جامد در انسان بود. با این حال، رونالد به مرحله نهایی بیماری کلیه (ESKD) مبتلا شد که نیاز به دیالیز داشت، دچار سکته مغزی شد، نیاز به آنژیوپلاستی عروق کرونر داشت و در نهایت در سن 79 سالگی بر اثر بیماری قلبی عروقی درگذشت [2]. این و اهداهای بعدی، سؤالات اخلاقی را در مورد ایمنی اهدای کلیه، به ویژه در مورد خطرات ابتلا به بیماری قلبی عروقی [3-6] ایجاد کرد. شصت و هفت سال پس از اهدای رونالد هریک، آیا اکنون میتوانیم این ابهامات را حل کنیم؟ در این مقاله، شواهد موجود در حال حاضر را با تمرکز بر خطرات فشار خون بالا و بیماری قلبی عروقی مرتبط با اهدای کلیه برای پاسخ به این سؤالات بررسی خواهیم کرد.
مرگ و میر و رویدادهای قلبی عروقی
مرگ و میر همه علل
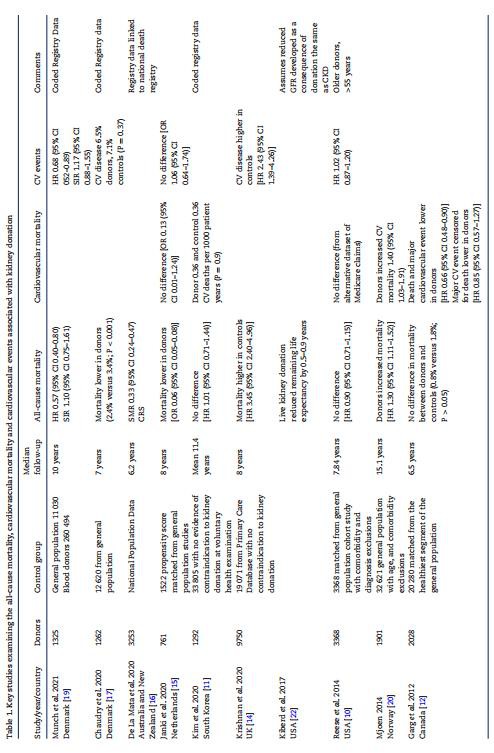
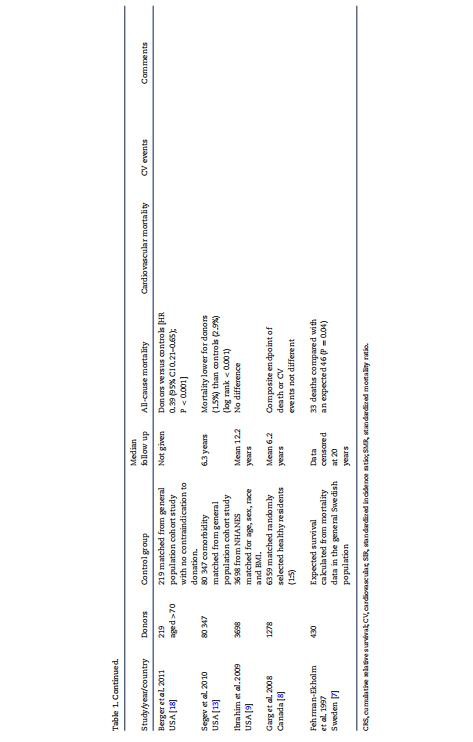
عبارت " اهداکنندگان کلیه بیشتر عمر می کنند " در ادبیات پزشکی پس از یک مطالعه سوئدی منتشر شده در سال 1997 ظاهر شد [7]. این مطالعه 430 اهداکننده را تا 31 سال پیگیری کرد و میزان بقای آنها را با میزان مرگ و میر ملی مقایسه کرد. شاید تعجب آور نباشد، با توجه به اینکه اهداکنندگان به طور گسترده از نظر بیماری غربالگری شده اند و در صورت مشاهده هر گونه ناهنجاری قابل توجهی از روند اهدا حذف شده اند، میزان بقای اهداکنندگان بهتر است. این یکی از ویژگی های ثابت تحقیق در مورد بقای اهداکنندگان بوده است. یافته های مطالعات متعدد، با حداکثر 40 سال پیگیری، شواهدی مبنی بر کاهش بقا در مقایسه با جمعیت عمومی نشان نداده است [8-12]، و در واقع بسیاری از آنها امید به زندگی بهتری را گزارش کرده اند [7، 13-19]. چندین مطالعه به دنبال غلبه بر این با استفاده از جمعیتهای «شاهد» انتخاب شده، تلاش برای حذف افراد مبتلا به شرایطی هستند که مانع اهدای کلیه میشوند، مانند فشار خون کنترلنشده، دیابت شیرین و سرطان (جدول 1 و 2). بنابراین، این گزارشها اغلب میزان رویدادهای سلامتی را در اهداکنندگان کلیه و افراد کنترل بسیار کمتر از جمعیت عمومی توصیف میکنند. این مطالعات همچنین عمدتاً مدت زمان نسبتاً کوتاهی دارند، با میانگین پیگیری<10 years. The highly selected nature of kidney donors means that it should not be surprising that adverse events are rare, at least in the medium to short term.
نگرانیهای مربوط به اثرات نامطلوب درازمدت ممکن است در 2{18}}14 مقاله در مقالهای که نتایج سالانه 1901 اهداکننده نروژی و 32 621 بیمار کنترل را بررسی میکرد، مطرح شد. که به طور بالقوه واجد شرایط اهدا بودند [20]. نسبت های خطر (HRs) برای مرگ و میر ناشی از همه علل {HR 1.30 [95 درصد فاصله اطمینان (CI) 1.11-1.52)]} در اهداکنندگان با منحنی های واگرا پس از حدود 10 سال به طور قابل توجهی افزایش یافت. محدودیتهای این مطالعه شامل حذف اهداکنندگان حاشیهای، گروه اهداکننده مسنتر (8 سال) نسبت به گروه کنترل، و پیگیری طولانیتر اهداکنندگان در مقایسه با گروه شاهد بود. علاوه بر این، منطقه روستایی نروژ مورد استفاده برای انجام این مطالعه دارای امید به زندگی غیرمعمول بالایی است [21]. با این وجود، این داده ها حداقل باعث نگرانی هستند و حداقل، مطمئناً نسبت به رضایت خاطر هشدار می دهند. تجزیه و تحلیل تصمیم پزشکی مارکوف نشان داد که اهداکنندگان به عنوان یک پیامد مستقیم اهدا، امید به زندگی 0.5 تا 1 سال کاهش یافته است [22]. با این حال، این تا حد زیادی بر اساس اهداکنندگان مبتلا به بیماری مزمن کلیوی (CKD) بود و، همانطور که بعداً بحث خواهد شد، این لزوماً صحیح نیست. با این وجود، در حال حاضر، اکثر شواهد موجود به نظر نمی رسد که نشان دهد اهدای کلیه با افزایش قابل توجهی در مرگ و میر به هر علت مرتبط است. در واقع، یک متاآنالیز اخیر از چهار مطالعه [12، 13، 18، 20]، از جمله مطالعه نروژی، که بین سالهای 2010 و 2016 با 84 495 اهداکننده و 62 484 کنترل منتشر شد، هیچ شواهدی از افزایش مرگ و میر ناشی از همه علل در اهداکنندگان [خطر نسبی تعدیل شده ترکیبی (RR) 0.60 (95 درصد فاصله اطمینان (CI): 0.31-1.10)] [23]. با این حال، باید توجه داشت که دو مورد از این مطالعات که در 97 درصد اهداکنندگان مشارکت داشتند، فقط به طور متوسط 6.3 و 6.5 سال پیگیری داشتند [12، 13]. پیگیریهای فشردهتر و طولانیمدت جمعیتهای اهداکننده با گروههای کنترل مناسب مورد نیاز است. این مطالعات برای مشاوره با اهداکنندگان بالقوه جوانتر در مورد خطرات موجود و هرگونه کاهش بالقوه در امید به زندگی مورد نیاز است. آنها طبیعتاً تأمین مالی، اداره و نگهداری آنها دشوار خواهد بود.
بیماری های قلبی عروقی و حوادث قلبی عروقی
مطالعات مشاهده ای اصلی که رابطه بین اهدای کلیه و مرگ و میر و رویدادهای قلبی عروقی را بررسی می کند در جدول 1 نشان داده شده است. به طور کلی، مطالعات کاهش یا عدم افزایش در مرگ و میر قلبی عروقی را نشان داده اند [1{24}}، 11، 15]. به طور مشابه، مطالعات افزایش حوادث قلبی عروقی یا خطر ابتلا به بیماری قلبی عروقی را نشان نداده است [12، 14، 17، 19]. یک متاآنالیز اخیر از چهار مطالعه [9، 12، 20، 24] که بین سالهای 2009 و 2016 با مجموع 4274 اهداکننده و 53 246 کنترل منتشر شد، و میانگین زمان پیگیری بین 6 تا 15 سال، هیچ شواهدی مبنی بر افزایش خطر قلبی عروقی در اهداکنندگان یافت نشد [RR ادغام شده با تنظیم 1.11 (95 درصد فاصله اطمینان (CI 0.64-1.70)] [23].

این یافته ها در زمینه رابطه قوی بین CKD و بیماری قلبی عروقی شاید تعجب آور باشد. با این حال، اکثر این مطالعات مدت زمان نسبتا کوتاهی دارند، به این معنی که افزایش خطر طولانی مدت قلبی عروقی را نمی توان کنار گذاشت. تا به امروز، اکثر مطالعات دارای دوره های پیگیری متوسط 6 تا 8 ساله هستند، که ممکن است برای تشخیص اثرات نامطلوب قلبی عروقی اهدا بر فرآیندهای بیماری که ممکن است چندین دهه طول بکشد، بسیار کوتاه باشد. علاوه بر این، محدودیتهایی که برای مطالعاتی اعمال میشود که مرگ و میر ناشی از همه علل را بررسی میکنند، در مورد مطالعاتی که رویدادهای قلبی عروقی را بررسی میکنند، اعمال میشود، بهویژه آنهایی که مربوط به انتخاب اهداکننده و مقایسه گروه کنترل، و همچنین مدت زمان پیگیری هستند. سایر توضیحات بالقوه مربوط به درجه و ماهیت کاهش عملکرد کلیه مشاهده شده در اهداکنندگان است. این موارد در زیر بررسی می شوند.
رابطه بین عملکرد کلیه و مرگ و میر ناشی از همه علل و حوادث قلبی عروقی
رابطه بین CKD و افزایش مرگ و میر و رویدادهای قلبی عروقی به دلایل مختلف به خوبی ثابت شده است، با چندین مطالعه مشاهده ای بزرگ که نشان دهنده افزایش خطر در نرخ های تخمینی فیلتراسیون گلومرولی (eGFRs) است.<60 mL/min/1.73 m2 [25–28]. However, the really large increases in cardiovascular disease start to occur at an eGFR <45 mL/min/1.73 m2. For example, in a study of over 1 million patients followed up for a median of 2.84 years, the age-standardized all-cause mortality per 100 person-years was 0.76, 1.08, 4.76, and 11.36 for the eGFR ranges of >60, 45–59, 30–44 and 15–29 mL/min/ 1.73 m2, respectively [25]. Similarly, the age-standardized rates of cardiovascular events per 100 person-years were 2.11, 3.65, 11.29, and 21.80 for the eGFR ranges of >60، 45-59، 30-44 و 15-29 میلی لیتر در دقیقه / 1.73 متر مربع، به ترتیب [25]. علاوه بر این، همچنین باید توجه داشت که بیمارانی که فقط با کاهش خفیف eGFR بدون پروتئینوری یا سیستاتین C بالا مواجه هستند، خطر قلبی عروقی بسیار ضعیفی دارند [29، 30].
نفرکتومی اهداکننده نشان دهنده از دست دادن ناگهانی تقریباً 50 درصد از توده نفرون با کاهش همزمان و متناسب اولیه در GFR است. با این حال، کلیه باقی مانده می تواند درصد قابل توجهی را جبران کند، معمولاً بین 20 تا 40 درصد از عملکرد از دست رفته [31-35]. به عنوان یک نتیجه از این "هیپرفیلتراسیون تطبیقی" مطالعات نشان داده است که تنها تعداد کمی از اهداکنندگان دارای GFR اندازه گیری شده مطابق با مرحله 3 CKD هستند. به عنوان مثال، مطالعه ای با استفاده از کلیرانس آیوهگزول برای اندازه گیری GFR در 255 اهدا کننده به طور متوسط 12.2 سال پس از اهدا، نشان داد که تنها 15 درصد از اهداکنندگان دارای GFR اندازه گیری شده بودند.<60 mL/min/1.73 m2 and none had a measured GFR <30 mL/min/1.73 m2 [9]. Furthermore, only 11% had microalbuminuria and only 1% had macroalbuminuria [9]. No donor had an eGFR <45 mL/min/1.73 m2 and albuminuria [9]. In a prospective study of 68 donors measuring GFR isotopically, one-third had a measured GFR <60 mL/min/1.73 m2, whereas half had an eGFR <60 mL/min/1.73 m2 1-year post-donation [36]. Only 7% of this cohort developed microalbuminuria. The cardiovascular risk of the large proportion of donors who have an eGFR in the range of CKD stage 2 remains uncertain and again requires further long-term study, particularly given data suggesting abnormalities in cardiac function at this level of eGFR [42, 43].
در جمعیت عمومی، کاهش eGFR در طول زمان نیز با افزایش خطر قلبی عروقی همراه است [44، 45]. همچنین نکته قابل توجه این است که بیماران مبتلا به eGFR پایدار در اندازهگیریهای مکرر نیز خطر قلبی عروقی را به طور قابل توجهی کاهش میدهند [46-48]. با این حال، در اهداکنندگان کلیه، کاهش معمول در طول زمان در GFR به نظر نمی رسد اتفاق بیفتد [37، 40، 41، 49]. برای مثال، در یک مطالعه آیندهنگر بر روی 203 اهداکننده و 205 کنترل که با دقت انتخاب شده بودند، اهداکنندگان کاهش بیشتری در GFR اندازهگیری شده با آیوهگزول از 6 ماه تا 9 سال پس از اهدا تجربه نکردند، در حالی که GFR در گروه کنترل به طور متوسط 1.26 میلیلیتر کاهش یافت. /min/ 1.73 متر مربع در سال [40]. آلبومینوری در اهداکنندگان طی این 9 سال نیز افزایش نیافته است [40]. همچنین یافتههای مشابهی در یک مطالعه آیندهنگر 5- ساله اهداکنندگان کلیه با استفاده از GFR ایزوتوپی برای اندازهگیری عملکرد کلیه مشاهده شد. در 48 اهداکننده که 5 سال پس از اهدا مورد مطالعه قرار گرفتند، هیچ کاهش بیشتری در eGFR یا eGFR اندازهگیری شده ایزوتوپی در اهداکنندگان مشاهده نشد، در حالی که 45 فرد کنترل سالم میانگین سالانه کاهش eGFR را 2±1 میلیلیتر در دقیقه / 1.73 متر مربع داشتند [37]. ].
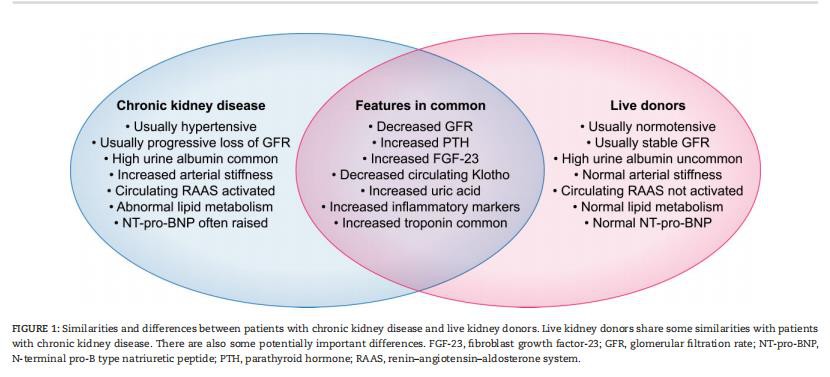
اگرچه شباهت های زیادی بین اهداکنندگان کلیه و بیماران مبتلا به CKD وجود دارد، اما تفاوت های مهمی نیز وجود دارد (شکل 1). در حالی که اکثر آنها یک eGFR غیرطبیعی و یک ناهنجاری ساختاری دارند، این موضوع بحث است که آیا اهداکنندگان کلیه باید طبقه بندی شوند یا نه، زیرا داشتن CKD با تمام همراهان ضمنی خطرات را برای سلامتی افزایش می دهد. مکانیسمهای زیربنایی «هیپرفیلتراسیون تطبیقی» که در کلیه باقیمانده رخ میدهد پیچیده است و تحت تأثیر عوامل متعددی از جمله سن، جنس، نژاد و اندازه بدن است [32، 50]. علاوه بر این، اگرچه کاهش GFR مرتبط با پیری وجود دارد، اما اینکه آیا و زمانی که این فرآیند از یک فرآیند فیزیولوژیکی به یک فرآیند پاتولوژیک تغییر میکند نیز نامشخص است [51-54]. به طور مشابه، مشخص نیست که آیا میکروآلبومینوری مشاهده شده در اقلیت اهداکنندگان دارای ارتباط بالینی است و باید برای طبقه بندی اهداکنندگان به عنوان مبتلا به CKD، صرف نظر از GFR استفاده شود [50]. اساسا، اهداکنندگان از طریق فرآیندی که کلیه باقیمانده را درگیر نمی کند، GFR کاهش یافته و میکروآلبومینوری ایجاد می کنند. ارتباط پیش آگهی این تغییرات، بر خلاف بیماران مبتلا به CKD که از طریق فرآیندهای مختلف بیماری به دست میآیند، هنوز مشخص نیست.
فشار خون
In the general population, every 10 mmHg increase in systolic and 5 mmHg increase in diastolic blood pressure is associated with a 1.5-fold increase in death from ischaemic heart disease and stroke [55]. It is well established that blood pressure increases with age [56] and that >80 درصد از بیماران مبتلا به CKD فشار خون بالا دارند [57]. بنابراین اهدای کلیه می تواند به طور بالقوه خطر ابتلا به فشار خون را در طول زمان افزایش دهد و احتمالاً از طریق تغییرات فیزیولوژیکی مانند هایپرفیلتراسیون کلیه، تغییرات در تون عروق و فعال شدن سیستم رنین-آنژیوتانسین-آلدوسترون [58]. دادههای مربوط به فشار خون و ایجاد فشار خون در اهداکنندگان کلیه هنوز بهطور شگفتانگیزی نامشخص است و به دلیل تماسهای بیشتر با خدمات پزشکی پس از اهدای خون و اندازهگیریهای مکرر فشار خون، در معرض سوگیری عمیق «نظارت» هستند [8، 58].

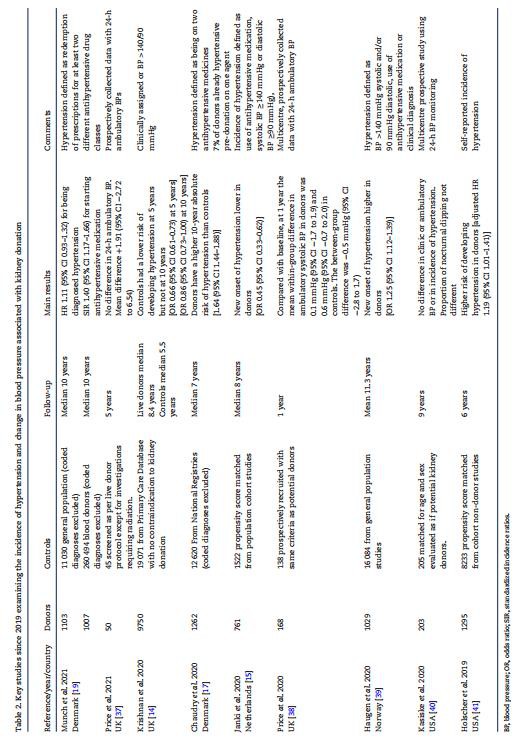
Multiple studies have been published examining the incidence and prevalence of hypertension post-kidney donation. Most are generally small and vary greatly in methodological rigor, blood pressure measurements, duration of follow-up, selection of the control group, the information presented on pre-donation characteristics, and the conclusions they present on whether donation increases blood pressure and the future risk of developing hypertension. A meta-analysis and systematic review published in 2006 found 48 studies from 28 countries with a total of 5145 donors followed up for an average of 7 years post-donation [59]. On average, 31% of surviving donors were lost to follow-up, potentially biasing results in either direction. Ten of these studies had healthy volunteers as control subjects. In nine of these studies, the control group appeared to be assembled at the time of donor follow-up evaluation, with only one study following up with control participants prospectively. Studies with >5 سال پیگیری (محدوده 6 تا 13 سال) برای تعیین اینکه آیا افزایش فشار خون پس از اهدای خون بالاتر از آنچه می تواند به پیری طبیعی نسبت داده شود، بررسی شد. برای فشار خون سیستولیک، چهار مطالعه [60-63] (157 اهداکننده، 128 فرد کنترل) و برای فشار خون دیاستولیک، پنج مطالعه [60-64] (196 اهداکننده، 161 کنترل) وجود داشت. تقریباً 10 سال پس از اهدا، اهداکنندگان به ترتیب 6 میلیمتر جیوه (95 درصد فاصله اطمینان (CI 2-11 میلیمتر جیوه) و 4 میلیمتر جیوه (95 درصد فاصله اطمینان 1-7 میلیمتر جیوه) در فشار خون سیستولیک و دیاستولیک در مقایسه با گروه کنترل داشتند. شش مطالعه [61، 62، 65-68] خطر ابتلا به فشار خون بالا را با یک دوره پیگیری متوسط از 2 تا 13 سال در 249 اهدا کننده و 161 فرد کنترل مورد بررسی قرار دادند. تنها یک مطالعه [66] افزایش خطر ابتلا به فشار خون را گزارش کرد. ناهمگونی آماری مشخصی بین مطالعات وجود داشت، بنابراین آنها ادغام نشدند. با این حال، این نوع مطالعات منجر به پذیرش گسترده این واقعیت شد که اهدای کلیه با فشار خون بالاتر و نرخ بالقوه بالاتر فشار خون همراه است.
با این حال، یک متاآنالیز و مرور سیستماتیک بعدی که در 2{15}}18 [23] منتشر شد، مطالعات مشاهدهای اهداکنندگان کلیه زنده را با حداقل 1- سال پیگیری پس از اهدا، مورد بررسی قرار داد که یک گروه مقایسه را ارائه کرد. از افراد کنترلی که کلیه اهدا نکرده بودند. شش مطالعه، منتشر شده بین 20{{20}}7 و 2016، در متاآنالیز فشار خون سیستولیک و دیاستولیک [9، 36، 69] وارد شدند. –72] با مجموع 712 اهداکننده و 830 کنترل. هیچ تفاوتی در فشار خون سیستولیک بین اهداکنندگان و گروه شاهد وجود نداشت، با یک تفاوت میانگین استاندارد شده 0.14 (95 درصد فاصله اطمینان (CI): 0.10- تا 0.40 mmHg. اهداکنندگان دارای فشار خون دیاستولیک کمی بالاتر هستند، با اختلاف میانگین استاندارد شده 0.17 (95 درصد فاصله اطمینان (CI 0.03-0.34) mmHg. چهار مطالعه بروز فشار خون را با مجموع 1726 اهداکننده و 6949 فرد کنترل و یک دوره پیگیری 6 تا 10 سال مورد بررسی قرار دادند [8، 9، 24، 71]. هیچ خطر افزایشی برای اهداکنندگان مبتلا به فشار خون بالا با ریسک نسبی تعدیل شده ادغام شده 1.08 (95 درصد فاصله اطمینان (CI): 0.46-2.34) مشاهده نشد. نویسندگان این متاآنالیز پیشنهاد کردند که نتایج متفاوتی که در مقایسه با مرور سیستماتیک قبلی [59] گزارش کردند، میتواند با انتخاب و تطبیق بهتر گروههای اهداکننده و کنترل در این مطالعات جدیدتر و با کیفیت بهتر توضیح داده شود [23].
چندین مطالعه دیگر از زمان انتشار این متاآنالیز دوم در سال 2018 منتشر شده است. مطالعات کلیدی منتشر شده پس از سال 2018 در جدول 2 خلاصه شده و نتایج متفاوتی را گزارش می کنند. برخی در مقایسه با گروه شاهد، بروز بالاتر فشار خون را گزارش کرده اند [17، 39، 41]. مونک و همکاران [19] هیچ تفاوتی در بروز پرفشاری خون بین اهداکنندگان انتخاب شده از جمعیت عمومی گزارش نکردند، اما در مقایسه با گروه کنترل انتخاب شده از اهداکنندگان خون، یک بار دیگر اهمیت انتخاب گروه اهداکننده در این نوع مطالعات را برجسته کرد. کریشان و همکاران [14] گزارش کردند که اهداکنندگان در 5 سالگی در مقایسه با گروه شاهد خطر ابتلا به فشار خون بالا را داشتند اما در 10 سالگی نه. جانکی و همکاران [15] در یک مطالعه از هلند بر روی 761 اهداکننده و 1522 گروه کنترل همسان امتیاز گرایش از مطالعات همگروهی جمعیت عمومی و یک دوره پیگیری متوسط 8 ساله نشان داد که بروز فشار خون بالا در اهداکنندگان کمتر است. سه مطالعه شاید شایسته ذکر ویژه باشند [37، 38، 40]. هر سه این مطالعات، کنترلهایی را انتخاب کردند که معیارهای انتخاب اهدایی را گذرانده بودند، به جز آنهایی که نیاز به قرار گرفتن در معرض تشعشع داشتند. آنها همچنین 24-ساعت اندازه گیری فشار خون سرپایی را انجام دادند که یک استاندارد طلایی برای اندازه گیری فشار خون و تشخیص فشار خون بالا ارائه می کرد. پس از 1 [38]، 5 [37] و 9 [40] سال پیگیری، هیچ یک از این مطالعات هیچ تفاوتی در 24-ساعت فشار خون سیستولیک یا دیاستولیک و همچنین بروز فشار خون بالا پیدا نکردند.
با توجه به ارتباط نزدیک بین CKD و فشار خون، شاید تعجب آور باشد که کاهش GFR پس از نفرکتومی به وضوح در اهداکنندگان مشاهده نمی شود. با این حال، همانطور که قبلاً گفته شد، هنوز مشخص نیست که کاهش GFR که از طریق یک فرآیند غیر پاتولوژیک رخ می دهد، CKD باشد. افزایش فشار خون در بیماری مزمن کلیه ناشی از چندین فرآیند از جمله فعالیت بیش از حد سیستم عصبی سمپاتیک، افزایش کلسیم داخل سلولی، احتباس سدیم، معکوس شدن اتساع عروق ناشی از هیپوکسی و فعال شدن سیستم رنین-آنژیوتانسین-آلدوسترون است [73]. مشخص نیست که آیا این فرآیندها در نتیجه اهدای کلیه اتفاق میافتند، اگرچه حداقل یک مطالعه شواهدی از فعال شدن سیستم رنین-آنژیوتانسین در اهداکنندگان نشان نداد [36]. جالب توجه است، بیماران مبتلا به سرطان کلیه که با نفرکتومی جزئی درمان میشوند، فشار خون بالاتری دارند، خطر ابتلا به بیماریهای قلبی عروقی افزایش مییابد و در مقایسه با بیمارانی که با نفرکتومی رادیکال درمان شدهاند، در برخی از مطالعات مشاهدهای، اما نه همه آنها، و تنها در موارد تصادفی کنترلشده، شواهدی دال بر افزایش بقا وجود ندارد. آزمایشی تا به امروز [74-78]. این در حالی بود که بیماران تحت درمان با نفرکتومی نسبی GFR بالاتری بعد از عمل داشتند، که نشان میدهد وجود پارانشیم آسیبدیده کلیوی ممکن است به جای کاهش GFR فی نفسه، باعث افزایش فشار خون شود.
در حال حاضر، شواهد موجود نشان می دهد که هرگونه افزایش بالقوه فشار خون پس از اهدای کلیه، احتمالاً اندک است. مطالعات بلندمدت با کیفیت بالا و آینده نگر فشار خون در اهداکنندگان کلیه گران بوده و انجام آنها دشوار است. موانع قابل توجهی در مورد یافتن کنترل های مناسب و نیاز به دوره های چند دهه مشاهده وجود دارد. علاوه بر این، پیوند اهداکنندگان زنده اغلب در مراکز بیمارستانی بزرگ انجام می شود که شامل زمان سفر طولانی است. برای مثال، در کره، با وجود بیش از 80 درصد پیوند کلیه در آن کشور که شامل اهداکنندگان زنده بود، تنها 11 درصد از بیماران پیگیری شدند [79]. با این وجود، این موانع باید برطرف شوند تا اهداکنندگان بالقوه اطلاعات مورد نیاز خود را داشته باشند.
سفتی شریانی
آئورت و سیستم شریانی بسیار قابل انبساط، تغییرات نوسانی فشار خون را که در نتیجه جهش متناوب بطن ایجاد میشود، بافر میکند و تضمین میکند که اکثر بافتها جریان تقریباً ثابتی را بدون قرار گرفتن در معرض حداکثر فشار سیستولیک دریافت میکنند [80، 81]. سفتی آئورت و شریان بزرگ با افزایش سن و قرار گرفتن در معرض عوامل خطر از جمله فشار خون بالا، دیابت و CKD افزایش می یابد [80-84]. در حالی که مطالعات متعدد ارتباط بین کاهش عملکرد کلیه، حتی در محدوده طبیعی، و افزایش سفتی شریانی [82-85] را نشان دادهاند، در مورد اینکه آیا سفتی شریانی مستقل از فشار خون و سایر بیماریهای همراه، در CKD افزایش مییابد اختلاف نظر وجود دارد. 7}}، 87].

سرعتی که موج فشار به سمت پایین یک شریان حرکت می کند با انبساط آن رابطه معکوس دارد، یعنی هر چه رگ سفت تر باشد، سرعت موج پالس (PWV) سریعتر است [80، 81]. در حال حاضر PWV کاروتید-فمورال یا آئورت به عنوان اندازه گیری استاندارد طلایی سفتی شریان در نظر گرفته می شود [88، 89]. افزایش PWV آئورت با همه علل و مرگ و میر قلبی عروقی در جمعیت عمومی و بیماران مسن، دیابتی و فشار خون بالا، و همچنین در بیماران مبتلا به CKD، از جمله کسانی که دیالیز می شوند و دریافت کنندگان پیوند کلیه مرتبط است [90-100].
در یک مطالعه مقطعی، PWV آئورت در 1{3}}1 اهداکننده (12.{5}} ± 2.0 m/s) در مقایسه با 134 داوطلب سالم (1.5 ± 8.5 متر) افزایش یافت. /s؛ P < 0.001) [101]. در یک مطالعه کنترل نشده روی 45 اهداکننده، تفاوتی در PWV آئورت 12 ماه پس از اهدا وجود نداشت (7.2 ± 1.3 m/s در مقابل 6.8 ± 1.1 m/s؛ P=0.74) [1{56}} 2]. نتایج مشابهی در مطالعه کنترل نشده دیگری روی 21 اهداکننده در 12 ماه مشاهده شد [103]. در یک مطالعه کنترلشده آیندهنگر، انبساط آئورت، که با استفاده از تصویربرداری رزونانس مغناطیسی اندازهگیری شد، در 45 اهداکننده در مقایسه با 40 گروه کنترل اندکی کاهش یافت [تفاوت در تغییر بین گروهها 0.57- (95 درصد فاصله اطمینان (CI): 1.09- تا -0.06 × 10-3 mmHg-1). ; P=0.03] در 12 ماه پس از نفرکتومی [36]. با این حال، در زیرگروهی از این گروه با 42 اهداکننده و 42 کنترل که 5 سال پس از اهدای کلیه مجدداً تحت مراقبت قرار گرفتند، PWV آئورت در هر دو گروه در طول زمان افزایش یافته بود، اما هیچ تفاوت قابل تشخیصی بین گروهها در 5 سال وجود نداشت [-0.24 (95 درصد فاصله اطمینان (CI) -0.69 تا 0.21 m/s)] [37]. این نتایج 5-سال با یافتههای یک مطالعه آمریکایی بر روی 205 اهداکننده و 203 فرد کنترل که به مدت 9 سال پیگیری شدند، مطابقت دارد. در زیرمجموعه ای از 100 اهداکننده و 113 کنترل، هیچ تفاوتی در PWV بین گروه ها در این دوره وجود نداشت [PWV در 9 سال: اهداکنندگان 7.69 (95 درصد فاصله اطمینان (CI): 7.28-8.10 متر بر ثانیه). کنترل 7.90 (95 درصد فاصله اطمینان (CI): 7.44-8.36 m/s)] [40].
It has been estimated that the required sample size to adequately power a study to determine a 0.4 m/s change in PWV is >350 بیمار در هر گروه [104]. هیچ مطالعه ای در این اندازه وجود ندارد. بنابراین شاید تعجب آور نباشد که ادبیات متناقض است. با این حال، کار اخیر برخی از اطلاعات را ارائه کرده است. مطالعه EARNEST (اثر کاهش نرخ فیلتراسیون گلومرولی پس از نفرکتومی بر سفتی شریانی و همودینامیک مرکزی) یک طراحی طولی چند مرکزی، کنترلشده و آیندهنگر در بریتانیا داشت [38، 104]. این هدف بلندپروازانه جذب 400 اهداکننده و شاهد بود، اما در نهایت با جذب 469 نفر پایان یافت و 306 نفر (168 اهداکننده و 138 کنترل) در 12 ماه پیگیری شدند. به طور کلی، این مطالعه شواهدی مبنی بر تغییرات مهم پیش آگهی در سفتی شریانی در 12 ماه پس از اهدای کلیه ارائه نکرد، اما نیاز به مطالعات دقیق طولانیمدت بیشتری را نشان داد. اینها گران هستند و انجام آنها دشوار است، بنابراین داده های بیشتر در مورد سفتی شریانی در اهداکنندگان کلیه ممکن است به کندی جمع آوری شوند [105، 106].
به طور خلاصه، اثرات اهدای کلیه بر عملکرد شریانی هنوز نامشخص و در مراحل اولیه تحقیقات است. تعداد کمی از دادههای موجود از نظر اندازه و/یا مدت زمان پیگیری محدود هستند، اما هیچ سیگنال واضحی از اثرات نامطلوب عمده اهدای کلیه بر سفتی شریانی نشان ندادهاند، اگرچه مطالعات بزرگتر و طولانیمدت مورد نیاز است.
برای اطلاعات بیشتر: david.deng@wecistanche.com WhatApp:86 13632399501
