Sidt2 یک پروتئین کلیدی در مسیر تخریب اتوفاژی-لیزوزومی است و برای حفظ ساختار کلیه و عملکرد فیلتراسیون ضروری است.
Nov 07, 2023
تنظیم و هموستاز اتوفاژی برای حفظ مورفولوژی و عملکرد اندام ضروری است. به عنوان یک پروتئین غشای لیزوزومی، اثرSidt2برساختار کلیهواتوفاژی کلیههنوز ناشناخته است در این مطالعه متوجه شدیم که کلیه هایSidt2−/-موشها تغییراتی را در ضخیم شدن غشای پایه، همجوشی فرآیند پا و تورم میتوکندری نشان دادند که نشان میدهدساختار کلیه آسیب دیده است. افزایش پروتئین ادرار در 24 ساعت نشان داد کهعملکرد کلیهنیز آسیب دیده بود. در عین حال عدم وجودSidt2باعث کاهش تعداد لیزوزوم های اسیدی، کاهش فعالیت هیدرولاز اسید و بیان آن در لیزوزوم و افزایش pH در لیزوزوم شد که نشان می دهد عملکرد لیزوزومی پس از آن مختل شده است.Sidt2حذف تجمع اتوفاگولیزوزوم ها، افزایش سطح پروتئین LC3-II و P62 و کاهش سطح mRNA P62 نشان داد که عدم وجودSidt2ژن باعث ایجاد مسیر اتوفاژی غیرطبیعی می شودflاوه آزمایش کلروکین، ایمونوflUorescence autophagosome، سنجش همجوشی لیزوزوم، و Ad-mcherry-GFP-LC3B بیشتر نشان داد که، پس ازSidt2حذف، تولید اتوفاگوزوم ها افزایش پیدا نکرد، اما ادغام اتوفاگوزوم ها و لیزوزوم ها و تخریب اتوفاگولیزوزوم ها مختل شد. هنگام جوجه کشیSidt2−/-سلولهای دارای راپامایسین فعال کننده اتوفاژی، متوجه شدیم که میتواند اتوفاژی را فعال کند، که به صورت افزایش اتوفاگوزومها ظاهر میشود، اما نمیتواند تخریب اتوفاگولیزوزوم را بهبود بخشد. در همین حال، بیشتر نشان داد کهSidt2ژن نقش مهمی در پیشرفت روان فرآیندهای اتوفاگولیزوزوم ایفا می کند. به طور خلاصه، عدم وجودSidt2ژن باعث اختلال در عملکرد لیزوزوم و کاهش تعداد لیزوزوم های اسیدی می شود که منجر به اختلالات تشکیل و تخریب اتوفاگولیزوزوم ها می شود که در نهایت به صورت تظاهر می یابد.ساختار و عملکرد غیر طبیعی کلیه. Sidt2برای حفظ عملکرد طبیعی لیزوزوم ها و ثبات فیزیولوژیکی کلیه ها ضروری است.

معرفی
دیدگاه سنتی این است که لیزوزوم ها محل دفع زباله سلول ها برای حذف زباله های تولید شده توسط سلول ها هستند [1-3]. با این حال، بسیاری از مطالعات نشان دادهاند که نقش لیزوزومها بسیار پیچیدهتر است و ممکن است شامل انتقال سیگنال سلولی، تومورزایی، رشد و سایر جنبههایی باشد که بر فعالیتهای زندگی بدن تأثیر میگذارد [4-10]. لیزوزوم ها معمولاً در بافت هایی مانند کبد و کلیه غنی می شوند [11]. بنابراین، اختلال عملکرد لیزوزومی نیز ارتباط نزدیکی با بیماری های بافتی کبد و کلیه دارد، مانند بیماری گوچر [12]، موکوپلی ساکاریدوز [13]، بیماری نیمن پیک [14]، گلومرولواسکلروز تاخیری [15]، نفروپاتی غشایی ایدیوپاتیک [6] پروتئین های غشایی لیزوزوم (LMPs) اجزای غشایی هستند که عملکرد آنها نه تنها حفظ یکپارچگی لیزوزوم است، بلکه در جنبه های مختلفی مانند انتقال سیگنال درون سلولی و تنظیم که برای حفظ عملکرد لیزوزوم ضروری است، دخیل هستند. و فعالیت های حیات سلولی [17-19].
تا به امروز، بیش از 100 LMP کشف شده است، اما عملکرد بیشتر آنها هنوز ناشناخته است [20]. غشای 7 ابرخانواده 1 (TM7SF1) برای حفظ عملکرد پودوسیت کلیه ضروری است [21] و نقش مهمی در روند رشد کلیه ایفا می کند [22]. کانال 5 با ولتاژ کلرید (ClC{10}}) یک کانال یون کلرید (Cl(-)) است که در لولههای کلیوی بیان میشود، که برای عملکرد طبیعی لولههای کلیوی ضروری است [23]. هنگامی که جهش یافته باشد، ممکن است باعث بیماری دنت شود [24]. بیان بیش از حد کانال 7 دارای ولتاژ کلرید (ClC{15}}) از آپوپتوز سلول های اپیتلیال لوله های کلیوی ناشی از اختلال در حالت ردوکس جلوگیری می کند [25]. این مطالعات نشان می دهد که به عنوان اجزای بافت کلیه غنی شده با لیزوزوم، LMP ها برای حفظ عملکرد طبیعی ضروری هستند، اما مکانیسم خاص بیماری زایی مرتبط با آنها هنوز نامشخص است.
خانواده گذر غشایی SID1، عضو 2 (Sidt2) یک LMP جدید کشف شده است که به شدت در بافت های کبد و کلیه بیان می شود [26]. مطالعات قبلی نشان دادهاند که حذف Sidt2 میتواند باعث بیماریهای مرتبط با کبد شود که به صورت استئاتوز کبد و اختلالات متابولیسم لیپیدهای کبدی ظاهر میشوند [11، 18]. در یک مطالعه اخیر، متوجه شدیم که کلیههای موش Sidt2-/- نیز آسیب دیدهاند، اما مکانیسم خاص آن نامشخص است. لیزوزوم ها اندام اجرایی مهمی برای اتوفاژی هستند [10]. آیا تنظیم اتوفاژی دخیل است؟ در این مطالعه، ما ارتباط بین عملکرد لیزوزومی (اتوفاژی) و بیماری را بررسی کردیم و مکانیسم زمینهای مربوط به Sidt2 که باعث آسیب کلیه میشود را بررسی کردیم، که کمک بزرگی برای مطالعه ارتباط بین LMP و بیماری خواهد بود.

نتایج
مدل Sidt2-/- این را نشان می دهدآسیب کلیهبا تجمع اتوفاگولیزوزوم همراه است
روش ساخت موش های Sidt2-/- در شکل 1A نشان داده شده است. DNA دم موش هموزیگوت به دست آمده توالی یابی شد و نتیجه توالی یابی یک وجهی بود (شکل 1B) و از دست دادن قطعه 199 جفت باز در اگزون دوم رخ داد. از طریق شناسایی ژنوتیپ PCR، متوجه شدیم که موشهای Sidt{4}}/+ (Wild Type, WT) دارای 685 جفت باز قطعه DNA بودند، در حالی که موشهای Sidt2-/- 486 جفت باز داشتند (شکل 1C). همانطور که در شکل 1D نشان داده شده است، پروتئین Sidt2 را به سختی می توان در موش های Sidt2-/- نسبت به WT تشخیص داد، که نشان می دهد مدل با موفقیت ساخته شده است. با آزمایش ادرار، مشخص شد که پروتئین ادرار 24 ساعته در موش های Sidt2-/- به طور قابل توجهی در مقایسه با WT افزایش یافته است (شکل 1E)، که نشان می دهد پس از حذف Sidt2، سد فیلتراسیون کلیه مختل شده است. مشاهدات میکروسکوپ الکترونی عبوری (شکل 1F) نشان داد که در مقایسه با موشهای WT (a-f)، کلیههای موش Sidt2-/- همجوشی پراکنده فرآیندهای پا، ضخیم شدن غشای پایه گلومرولی (g, h)، اپیتلیال لولهای کلیوی را نشان دادند. ادم سلولی، آسیب میکروویلی (i، j)، ادم میتوکندری، تغییرات شبه واکوئل، و ناپدید شدن خارها (k، l). جالب توجه است که موشهای Sidt2-/- تعداد زیادی تجمع اتوفاگولیزوزوم (که با فلشهای قرمز، m، n نشان داده شدهاند) را به نمایش گذاشتهاند، و این تعداد بهطور قابلتوجهی بیشتر از گروه کنترل بود (شکل 1G). در سطح سلولی، ما دریافتیم که Sidt2 برای بقای سلول های کلیه نیز ضروری است. حذف ژن Sidt2 باعث کاهش تکثیر و افزایش آپوپتوز سلول های MPC5 و SV40 MES 13 می شود (شکل تکمیلی 1).
حذف ژن Sidt2 منجر به تغییر در تعداد و عملکرد لیزوزوم های اسیدی در سلول های کلیه موش می شود.
فناوری Crispr-Cas9 برای از بین بردن ژن Sidt2 در سلول های MPC5 و SV40 MES 13 برای به دست آوردن مدل های سلولی استفاده شد. تایید سطح mRNA و پروتئین (شکل 2A-C) به ترتیب توسط qRT PCR و وسترن بلات انجام شد که نشان میدهد مدلها با موفقیت ساخته شدهاند. سیستم تخریب با واسطه لیزوزوم یک مرحله کلیدی در تخریب اتوفاژی است. به عنوان یک LMP ضروری، آیا حذف Sidt2 بر بیان پروتئین های مرتبط با لیزوزوم تأثیر می گذارد؟ ما پروتئین غشایی 1 مرتبط با لیزوزومی LMP (LAMP1) را اندازه گیری کردیم. نتایج نشان داد که بیان LAMP1 پس از حذف Sidt2 در سلول های MPC5 و SV40 MES 13 کاهش یافت (شکل 2D، E). ما بیشتر از LysoTracker برای برچسب زدن لیزوزومهای اسیدی استفاده کردیم و دریافتیم که تعداد لیزوزومهای اسیدی پس از حذف Sidt2 در هر دو نوع سلول کاهش یافت (شکل 2F، G). متعاقبا، ما کاتپسین لیزوزومی B (CTSB) را اندازهگیری کردیم و دریافتیم که در بافت کلیه موش (شکل 2H، I)، سلولهای MPC5 (شکل 2J، K) و سلولهای SV40 MES 13 (شکل 2L، M)، عبارات از CTSB در مدل های Sidt2 - / - همه کاهش یافتند، که نشان می دهد که فعالیت آنزیم پروتئولیتیک در لیزوزوم ها با حذف ژن Sidt2 کاهش یافته است. به طور مشابه، بیان پیش ساز CTSB در دو نوع سلول از گروه Sidt2-/- به طور قابل توجهی کاهش یافت، که نشان می دهد CTSB نیز پس از حذف Sidt2 تحت تأثیر قرار گرفته است. ما بیشتر از LysoSensor برای تشخیص محیط اسیدی لیزوزوم ها استفاده کردیم. هر چه نسبت شدت فلورسانس کمتر باشد، مقدار pH در لیزوزوم بالاتر است. نتایج نشان داد که پس از حذف Sidt2، مقدار pH افزایش یافت (شکل 2N, O) و اسیدی شدن غیر طبیعی بود. برای بررسی بیشتر اینکه آیا ناهنجاریهای لیزوزومی بالا به دلیل تعداد غیرطبیعی لیزوزومها یا عملکردهای غیرطبیعی لیزوزوم است، سلولها را با میکروسکوپ الکترونی بررسی کردیم (شکل 2P). ما دریافتیم که هیچ تغییر آشکاری در تعداد لیزوزوم های اولیه و تعداد کل لیزوزوم ها (شامل لیزوزوم های اولیه و ثانویه) پس از حذف Sidt2 وجود ندارد (شکل 2Q).
مسیر اتوفاژی کلیه پس از حذف Sidt2 غیر طبیعی است
همانطور که در بالا ذکر شد، تعداد زیادی تجمع اتوفاگولیزوزوم در سلول های کلیه موش های Sidt2-/- مشاهده شد که نشان می دهد مسیر اتوفاژی غیر طبیعی است. با استفاده از تجزیه و تحلیل وسترن بلات، نشان داده شد که افزایش قابل توجهی در سطح پروتئین LC3- فسفاتیدیل اتانول آمین مزدوج (LC3-II) و Sequestosome 1 (P62) در کلیه Sidt2-/- وجود دارد. موش، و افزایش بیان پروتئین مربوط به اتوفاژی مربوط به اتوفاژی 5 (Atg5)، مربوط به اتوفاژی 7 (Atg7)، و مربوط به اتوفاژی 12 (Atg12) (شکل 3A، B). با این حال، سطح mRNA P62 به طور قابل توجهی کاهش یافت (شکل 3C)، که نشان می دهد مسیر اتوفاژی پس از حذف Sidt2 در داخل بدن غیر طبیعی است. سپس دریافتیم که بیان پروتئین های اتوفاژی LC3-II، P62، Atg5، Atg7، و Atg12 نیز در دو نوع سلول کلیه پس از حذف Sidt2 افزایش یافته است (شکل 3D-G) که سازگار بود. با in vivo. افزایش LC{26}}II نشاندهنده افزایش اتوفاگوزومها در سلولهای کلیه پس از حذف Sidt2 است که ممکن است در اثر فعال شدن اتوفاژی یا تخریب مسدود شده اتوفاگوزومها ایجاد شود. ایمونوفلورسانس P62 (شکل 3H) به وضوح افزایش محتوای P62 را در سلول های Sidt2-/- نشان داد (شکل 3I). برخلاف سطح پروتئین، qRT-PCR نشان داد که P62 به طور قابل توجهی در سطح mRNA کاهش می یابد (شکل 3J)، که نشان می دهد افزایش P62 به تخریب ناکافی مربوط می شود. افزایش در Atg5، Atg7، و Atg12 نشان داد که اتوفاژی شروع شده و به طور طبیعی شکل میگیرد، اما تجمع P62 موانع فرآیند اتوفاژی را نیز مطرح میکند، و این تناقض ما را ملزم به بررسی بیشتر وضعیت واقعی شار اتوفاژی میکند.
در شرایط آزمایشگاهی، کاربرد کلروکین نشاندهنده کاهش شار اتوفاژی پس از از دست دادن Sidt2 است. آزمایش کلروکین یکی از آزمایشهای کلاسیک برای مشاهده شار اتوفاژی است. برای درک دلایل افزایش LC3-II و P62 پس از حذف Sidt2، از کلروکین (CQ)، یک مهارکننده پایین دستی اتوفاژی، استفاده کردیم تا روی سلولها برای مشاهده شار اتوفاژی عمل کند. ابتدا، ما از گرادیان های غلظت مختلف استفاده کردیم تا تأیید کنیم که غلظت اشباع مهار شده توسط CQ 50 میکرومولار (شکل 4A-F) در سلول های MPC5 و SV40 MES 13 بود. علاوه بر این غلظت، زمانی که غلظت CQ به افزایش ادامه داد، LC3-II و P62 برای رسیدن به اشباع بیشتر افزایش پیدا نکردند. بنابراین، ما از تحریک 50 میکرومولار CQ در طول 16 ساعت برای مهار کامل شار اتوفاژی استفاده کردیم، و در این زمان، تفاوتهای LC{13}}II بین گروه Sidt2+/+گروه و گروه Sidt2-/- ناپدید شد. سلول های MPC5 و SV40 MES 13. به طور مشابه، پس از پردازش 50 میکرومولار CQ، تفاوتهای P62 ناشی از حذف Sidt2 نیز ناپدید شدند (شکل 4G، H، J، K). آمار مربوط به شار اتوفاژی نشان داد که وقتی Sidt2 از بین رفته بود کاهش می یابد (شکل 4I, L)، که بیشتر تایید می کند که افزایش بیان LC{26}}II و P62 پس از حذف Sidt2 به دلیل شکست در پاکسازی اتوفاژی بوده است. به جای افزایش سطح اتوفاژی (فعال شدن اتوفاژی).
اختلال در همجوشی اتوفاگوزوم- لیزوزوم در شرایط آزمایشگاهی پس از حذف Sidt2 پاکسازی و تخریب مراحل میانی و اواخر در فرآیند اتوفاژی است که شامل همجوشی اتوفاگوزوم با کاهش پس از حذف Sidt2 است (شکل 5D)، که نشان میدهد همجوشی اتوفاگوزوم ها و لیزوزوم ها دچار اختلال شد.
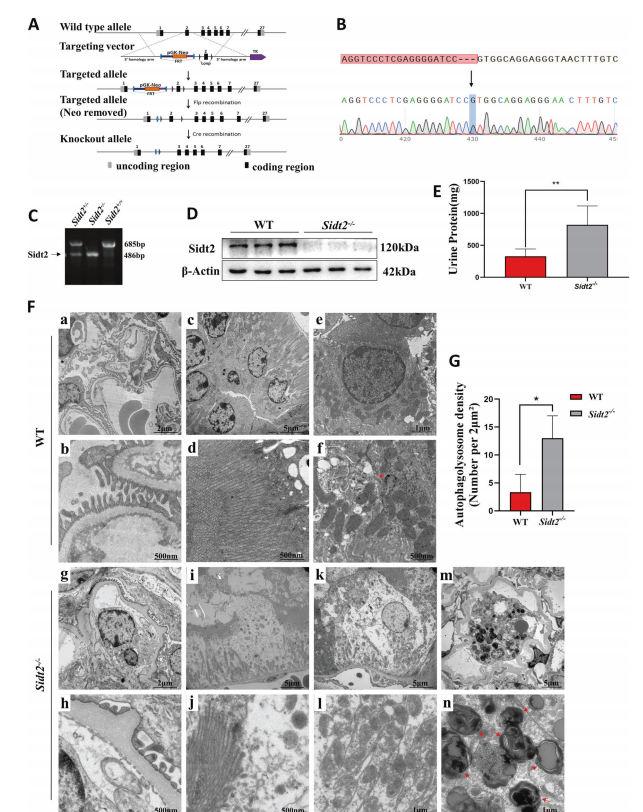
عکس. 1آسیب کلیهو تجمع اتوفاگولیزوزوم در موش Sidt2-/-. یک شماتیک هدف قرار دادن ژن سیستم Cre-LoxP. B بالا نمودار توالی صادر شده DNA دم موش حذفی ژن Sidt2 است. در زیر نقشه توالی، فلش نشان دهنده محل ژن گم شده است. در مقایسه با موش های WT، از دست دادن ژن 199 جفت باز در اگزون 2 رخ می دهد. بررسی سطح DNA C از Sidt2 (استخراج شده از بافت دم). محصول تقویت شده پرایمر حاوی ناحیه ناک اوت پایه است که به صورت Sidt2+ /+(WT)، Sidt2+/−، یا Sidt2−/− نشان داده شده است. تأیید سطح پروتئین D برای تشخیص سطح بیان پروتئین Sidt2 توسط وسترن بلات. E کلیه پروتئین ادرار 24 ساعته در موش WT و Sidt2-/-. ساختار فوق میکرو مورفولوژیکی کلیه موش های WT (a، f) و موش Sidt2-/- (g-n). در مقایسه با موش WT، کلیه موش Sidt2-/- همجوشی فرآیند پا، ضخیم شدن غشای پایه (g، h)، ادم سلول های اپیتلیال لوله های کلیوی، آسیب میکروویلی (i، j)، تخریب میتوکندری (k، l) و تجمع اتوفاگولیزوزوم (m, n)؛ G تعداد کل اتوفاگولیزوزوم های کلیوی در موش WT و Sidt2-/-. *P < 0.{20}}5، **P <0.01.
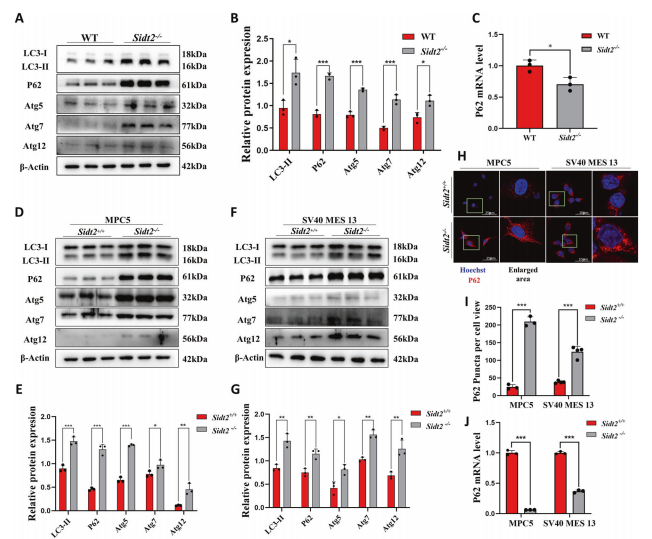
شکل 3 حذف Sidt2 مسیر اتوفاژی را مختل می کند. تشخیص WT و Sidt2-/- سطوح بیان پروتئین مربوط به اتوفاژی سلولی توسط وسترن بلات. نمودارهای آماری B نتایج تست وسترن بلات. سطح بیان mRNA ژن C P62 در بافت کلیه موش WT و Sidt2-/-. سطح بیان D پروتئین های مسیر اتوفاژی سلول MPC5 قبل و بعد از ناک اوت Sidt2. E نمودار آماری نمودار (D). سطوح بیان F پروتئین های مسیر اتوفاژی در سلول های SV40 MES 13 قبل و بعد از ناک اوت Sidt2. G نمودار آماری نمودار (F); ایمونوفلورسانس H P62 در سلول های MPC5 و SV40 MES 13 قبل و بعد از ناک اوت Sidt2. من نمودارهای آماری از نتایج ایمونوفلورسانس. سطوح بیان mRNA ژن J P62 در سلول های MPC5 و SV40 MES 13 قبل و بعد از ناک اوت Sidt2. *P <0.05، **P <0.01، ***P <0.001.

Ad-mCherry-GFP-
نشانگذاری دوگانه فلورسانس LC3B نشان میدهد که تشکیل اتوفاگولیزوزوم و مسیر تخریب آن پس از حذف Sidt2 مسدود شده است. در طی فرآیند اتوفاژی، mCherry-GFP-LC3B روی غشای اتوفاگوزوم جمع می شود و به شکل لکه های زرد زیر میکروسکوپ فلورسانس ظاهر می شود. هنگامی که اتوفاگوزوم ها و لیزوزوم ها با هم ترکیب می شوند تا اتوفاگولیزوزوم ها را تشکیل دهند، محیط اسیدی درون لیزوزوم فلورسانس GFP را خاموش می کند به طوری که خود را به شکل لکه های قرمز نشان می دهد. بنابراین، GFP متصل به LC3 فقط می تواند برای تشخیص اتوفاگوزوم ها استفاده شود، در حالی که mCherry می تواند همزمان اتوفاگوزوم ها و اتوفاگولیزوزوم ها را تشخیص دهد. هنگامی که لکه های فلورسانس سبز و قرمز با هم ترکیب می شوند و به صورت لکه های فلورسانس زرد نشان داده می شوند، این مربوط به اتوفاگوزوم ها است. در این زمان، فلورسانس قرمز می تواند نشان دهنده اتوفاگولیزوزوم ها باشد و همچنین می تواند صافی تشکیل اتوفاگولیزوزوم را نشان دهد [27]. سلولهای MPC5 و سلولهای SV40 MES 13 در هر دو گروه Sidt2+/+ و Sidt2-/- با آدنوویروس Ad-mCherry GFP-LC3B ترانسفکت شدند و با میکروسکوپ لیزری کانفوکال عکسبرداری شدند (شکل 6A). مشخص شد که تعداد نقاط فلورسنت زرد افزایش یافته و تعداد نقاط فلورسنت قرمز کاهش یافته است (شکل 6B، C) پس از حذف Sidt2، نشان داد که تعداد اتوفاگوزوم ها افزایش یافته و اتوفاگولیزوزوم ها در گروه Sidt2-/- کاهش یافته است. این به این دلیل است که موانعی برای تشکیل اتوفاگولیزوزوم وجود داشت و مسیرهای تخریب اتوفاگولیزوزوم مسدود شده بود که منجر به موانع تخریب اتوفاگوزومی شد.

راپامایسین تجمع P62 ناشی از حذف Sidt2 را بهبود نداد، بلکه آن را تشدید کرد راپامایسین (RAPA) یک مهارکننده mTOR است و اتوفاژی را فعال میکند. هنگامی که RAPA روی سلولهای MPC5 و SV40 MES 13 گروههای Sidt2+/+ و Sidt2-/- عمل کرد، مقدار LC3-II را در هر دو گروه افزایش داد. این بدان معنی است که RAPA می تواند مسیر بالادست اتوفاژی را فعال کند. به طور مشابه، ما دریافتیم که افزایش سطح LC3-II در گروه Sidt2-/- با RAPA آشکارتر از آن در گروه کنترل (Sidt2+/+گروه) بود، که نشان میدهد زمانی که RAPA عمل کرد در گروه Sidt2-/-، تخریب اتوفاگوزوم ها هنوز بهبود نیافته است. در همین حال، ما همچنین تغییرات را در P62 مشاهده کردیم و متوجه شدیم که وقتی RAPA روی گروه Sidt{15}}/+ سلولهای MPC5 و SV40 MES 13 عمل میکند، P62 تغییر قابلتوجهی نداشته است، که نشان میدهد شار اتوفاژی طبیعی است. هنگامی که RAPA بر روی گروه Sidt2-/- عمل کرد، سطح بیان P62 در مقایسه با قبل از تجویز بیشتر افزایش یافت و همچنین نسبت به کنترل پس از درمان با RAPA آشکارتر بود (شکل 7A، B، D، E). متعاقبا، به منظور بررسی دلایل بیان ناسازگار پروتئین P62 پس از تیمار Sidt2+/+ و گروه Sidt2-/- با RAPA، سطوح mRNA P62 را اندازه گیری کردیم و دریافتیم که سطح افزایش یافته است. پس از درمان RAPA در هر دو گروه Sidt2+/+ و Sidt2-/-، و گروه Sidt2+/+ سطح بالاتری نسبت به گروه Sidt2-/- داشتند (شکل 7C ، F)، که می تواند بیشتر ثابت کند که جریان اتوفاژی در گروه Sidt2+/+ صاف بود، در حالی که اختلال جریان اتوفاژی در گروه Sidt2-/- در پایان اتوفاژی رخ داد، یعنی تخریب اتوفاگولیزوزوم ها. ارتباط دادن. ما همچنین اثر Sidt2 را بر تکثیر و آپوپتوز سلولهای کلیه تحت شرایط اتوفاژی فعال مورد مطالعه قرار دادیم و دریافتیم که پس از فعالسازی سلولی اتوفاژی ناشی از محیط بدون سرم، در مقایسه با گروه کنترل، تکثیر Sidt2-/- گروه بیشتر مهار شد و آپوپتوز آشکارتر بود (شکل تکمیلی 2).
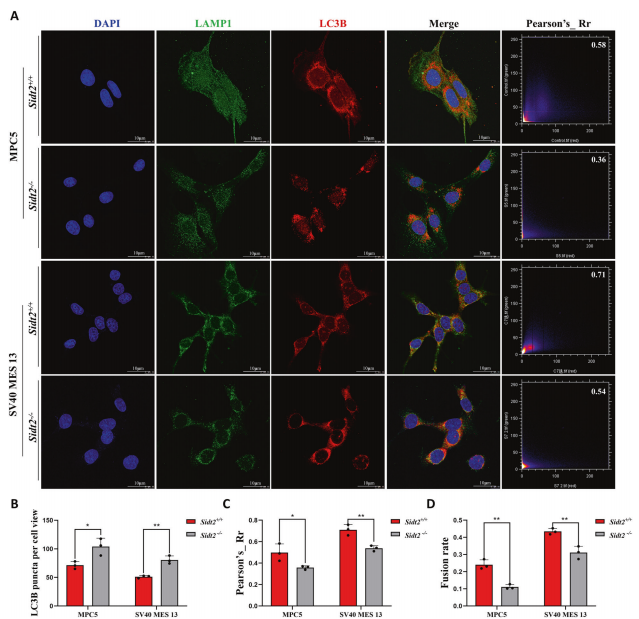
شکل 5 از همجوشی اتوفاگوزوم و لیزوزوم پس از حذف Sidt2 جلوگیری می شود. هممحلیسازی ایمونوفلورسانس LC3B و LAMP1 در سلولهای MPC5 و SV40 MES 13 قبل و بعد از ناک اوت Sidt2، تجزیه و تحلیل با ضریب همبستگی پیرسون. مقایسه B نقاط فلورسانس LC3B قبل و بعد از ناک اوت Sidt2 در سلول های MPC5 و SV40 MES 13. مقایسه C ضریب همبستگی پیرسون قبل و بعد از ناک اوت Sidt2 در سلول های MPC5 و SV40 MES 13. D مقایسه سرعت همجوشی قبل و بعد از ناک اوت Sidt2 در سلول های MPC5 و SV40 MES 13 (نسبت تعداد نقاط فلورسنت هم موضعی LAMP1 و LC3B به تعداد لکه های فلورسنت LAMP1). *P <0.05، **P <0.01.
خدمات حمایتی Wecistanche - بزرگترین صادرکننده سیستانچ در چین:
ایمیل:wallence.suen@wecistanche.com
واتساپ/تلفن:+86 15292862950
خرید برای جزئیات بیشتر مشخصات:
https://www.xjcistanche.com/cistanche-shop






