سلول های بنیادی برای پزشکی احیا کننده و ضد پیری بخش 1
Jun 01, 2022
لطفا تماس بگیریدoscar.xiao@wecistanche.comبرای اطلاعات بیشتر
خلاصه:برای بررسی روشهای بهبود پردازش ضایعات خوک، پوست خوک با استفاده از پروتئازهای مختلف تجاری (آلکالاز، فلوورزیم، نوتراز، بروملین، پروتامکس و پاپائین) تحت چندین شرایط بهینه هیدرولیز شد. پس از هیدرولیز آنزیمی، هیدرولیزهای کلاژن (CHS) با وزن مولکولی (3 کیلو دالتون) از طریق اولترافیلتراسیون غشایی تکه تکه شدند. CHS برای خواص فیزیکی (pH، بازیابی پروتئین، محتوای گروه آمینه آزاد، توزیع وزن مولکولی، و ترکیب آمینو) و همچنین برای خواص عملکردی (فعالیتهای آنتی اکسیدانی و فعالیتهای ضد پیری) آنالیز شد. در میان CH ها، CH های هیدرولیز شده توسط آلکالاز (CH-Alcalase) بالاترین درجه هیدرولیز را در مقایسه با سایر CH ها نشان دادند. هر دو "CH-Alcalase" و "CH-Alcalase".<3 kda"="" fractions="" showed="" a="" considerably="" high="" antioxidant="" activity="" and="" collagenase="" inhibition="" activity.="" therefore,="" resulting="" bioactive="" have="" the="" potential="" for="" development="" as="" antioxidants="" and="" anti-aging="" ingredients="" in="" the="" food,="" cosmetics,="" and="" pharmaceuticals,="" from="" animal="">
کلید واژه ها:هیدرولیز؛ پروتئازهای تجاری؛ هیدرولیز کلاژن؛ آنتی اکسیدان؛ ضد پیری

لطفا برای دانستن بیشتر اینجا کلیک کنید
1. مقدمه
با افزایش امید به زندگی، روش های ضد پیری پوست مورد توجه زیادی قرار گرفته است. کلاژن، که در محصولات مراقبت از پوست به عنوان یک ماده آرایشی برای ضد پیری استفاده می شود، به طور گسترده ای در بازار لوازم آرایشی استفاده می شود. کلاژن یک پروتئین فیبری با وزن مولکولی بالا با منشاء حیوانی است که به وفور در بافت همبند، پوست، تاندون ها، غضروف ها، رباط ها، دندان ها، ناخن ها و موی انسان و حیوانات یافت می شود. دام ها منبع اصلی کلاژن صنعتی هستند[1]. سالانه مقادیر زیادی از محصولات جانبی دام در سراسر جهان به عنوان زباله توسط صنایع فرآوری غذا و گوشت دور ریخته می شود. با این حال، اینها ممکن است به عنوان منابع پروتئینی مهم برای مواد غذایی جدید مورد استفاده قرار گیرند یا از طریق هیدرولیز به محصولات با ارزش افزوده تبدیل شوند، که به طور گسترده برای بهبود و ارتقاء خواص عملکردی و تغذیه ای پروتئین ها استفاده می شود [2،3]. کلاژن نیز به طور فزاینده ای به عنوان منبعی از پپتیدهای فعال زیستی در نظر گرفته می شود که به عنوان ترکیبات مفیدی برای استفاده در برنامه های غذایی یا دارویی نشان داده اند.فواید سیستانچ،بنابراین، هیدرولیز کلاژن ممکن است نقش مهمی در بهبود فراهمی زیستی و مناسب بودن آن برای استفاده در فرآیندهای تجاری مختلف داشته باشد.
فعالیت های فیزیولوژیکی پپتیدهای فعال زیستی، که معمولاً حاوی 2-20 باقی مانده اسید آمینه (<6000 da),="" are="" based="" on="" the="" composition="" and="" sequence="" of="" their="" amino="" acids="" [2,4].="" due="" to="" their="" structural="" properties="" such="" as="" molecular="" weight,="" bioactive="" peptides="" may="" possess="" specific="" characteristics="" that="" affect="" numerous="" physiological="" processes="" related="" to="" antimicrobial,="" antioxidant,="" emulsifying,="" antihypertensive,="" antidiabetic,="" and="" immunomodulatory="" functions="" in="" organisms[1,5,6].="" generally,="" low="" molecular="" weight="" hydrolysates="" display="" lower="" viscosity,="" better="" dispersion,="" higher="" hydrophobicity,="" and="" smaller="" particle="" size="" [7].="">کلسترول سیستانچدرجه هیدرولیز مستقیماً بر وزن مولکولی و ترکیب اسید آمینه هیدرولیزها تأثیر می گذارد [8]. بنابراین، فرآیند هیدرولیز ممکن است برای تولید پپتیدهای زیست فعال جدید ضروری باشد.

سیستانچ می تواند ضد پیری باشد
هیدرولیز پروتئین، که منجر به جدا شدن پیوندهای پپتیدی می شود، ممکن است از طریق فرآیندهای آنزیمی یا شیمیایی انجام شود [9]. فرآیندهای شیمیایی، از جمله هیدرولیز قلیایی یا اسیدی با استفاده از استخراج با حلال، نه تنها برای محیط زیست، بلکه برای انسان هایی که محصولات حاصل را مصرف می کنند نیز مضر هستند [4،10]. فرآیندهای شیمیایی که کنترل آنها دشوار است، محصولاتی حاوی آمینو اسیدهای اصلاح شده تولید می کنند [9]. در مقابل، هیدرولیز آنزیمی ممکن است در شرایط ملایم انجام شود، بنابراین از محیط های شدید که توسط تیمارهای شیمیایی مورد نیاز است اجتناب می شود. علاوه بر این، فرآیندها نه واکنشهای جانبی ایجاد میکنند و نه ارزش غذایی منبع پروتئین را کاهش میدهند [8]. چندین پروتئاز از جمله آلکالاز، پپسین، پروتامکس، تریپسین و نوتراز معمولاً برای هیدرولیز پروتئین ها استفاده می شوند که در نتیجه انواع مختلفی از پروتئین ها و پپتیدهای هیدرولیز شده با انواع فعالیت های زیست عملکردی تولید می شوند. یک مطالعه تولید هیدرولیزهای کلاژن با فعالیت آنتی اکسیدانی از ژلاتین پوست خوک را با استفاده از هیدرولیز آنزیمی توسط پپسین و پانکراتین گزارش کرد [11].عوارض جانبی cistanche deserticolaمحصولات فرعی ماهی قزل آلا برای تولید هیدرولیزهای پپتیک با استفاده از پروتئازهای مختلف هیدرولیز شدند، جایی که پپتیدهای نهایی خواص آنتی اکسیدانی و ضد التهابی عالی را نشان دادند [12].
هدف از این تحقیق این بود: (الف) شناسایی فعال ترین هیدرولیزهای کلاژن تولید شده توسط هیدرولیز آنزیمی با استفاده از پروتئازهای مختلف تجاری موجود (آلکالاز، فلوورزیم، نوتراز، پروتامکس، بروملین و پاپائین)؛ (ب) برای تأیید اثر شکنش هیدرولیزهای کلاژن به دست آمده از هیدرولیز آنزیمی، و (ج) برای تعیین فعالیت های آنتی اکسیدانی و ضد پیری آنها در شرایط آزمایشگاهی.
2. نتایج و بحث
2.1. اثر هیدرولیز آنزیمی بر هیدرولیزهای کلاژن
2.1.1.pH
خواص عملکردی پروتئین ها ممکن است از طریق هیدرولیز توسط پروتئازهای خاص افزایش یابد. در این مطالعه، شش پروتئاز مختلف (آلکالاز، فلوورزیم، نوتراز، بروملین، پروتامکس و پاپائین) برای هیدرولیز کلاژن از پوست خوک به منظور به دست آوردن هیدرولیزهای کلاژن فعال با وزن مولکولی پایین استفاده شد.دوز cistanche redditتغییر pH در هیدرولیزهای کلاژن (CH) در شکل 1 نشان داده شده است. pH سوسپانسیون کلاژن (5 درصد مخلوط پوست خوک) در ابتدا 6.{3}} . CH-Alcalase و CH-Flavorzyme در 12 ساعت انکوباسیون به pH بهینه (pH 8.{9}}) رسیدند. CH- Protamex، CH-Bromelain و CH-Papain در 6 ساعت انکوباسیون به pH بهینه (pH7.{15}}) رسیدند، در حالی که CH-Flavorzyme به مدت 24 ساعت انکوباسیون از pH6.39 به pH5.69 کاهش یافت (شکل 1). pH هیدرولیز پروتئین عامل مهمی است که واکنش های هیدرولیز آنزیمی را تنظیم می کند[13]. بنابراین، تولید کلاژن هیدرولیز شده در شرایط pH متفاوت ممکن است به دلیل تغییرات وابسته به pH در ترکیب آنزیم باشد، که ممکن است بر فعال شدن زیستی و خواص فیزیکوشیمیایی آنها تأثیر بگذارد.

2.1.2. الکتروفورز ژل دودسیل سولفات سدیم-پلی آکریل آمید (SDS-PAGE)
پروفیل های الکتروفورز ژل دودسیل سولفات-پلی آکریل آمید (SDS-PAGE) CHهای تیمار شده با پروتئازهای مختلف به مدت 24 ساعت نشان داده شده است (شکل 2). نمایه پپتیدی سوسپانسیون کلاژن (در 0 ساعت) یک نوار قابل مشاهده در محدوده وزن مولکولی کم تا بالا را نشان داد. نتایج نشان داد هیدرولیز سریع در CH-Alcalase، CH-Neutrase، CH-Bronneline و CH-Protamex، زیرا هیچ باندی پس از 3 ساعت انکوباسیون وجود نداشت. باندهای محدوده وزن مولکولی بالا CH-Alcalase، CH-Neutrase، و CH-Protamex به روش انکوباسیون وابسته به زمان کاهش یافت. با این حال، CH-بروملین با زمان جوجه کشی متفاوت نیست زیرا آبجو پس از تنها 1 ساعت انکوباسیون کاملاً هیدرولیز شده است. جالب توجه است، CH ها به طور کامل ناپدید شدند زمانی که نمونه با آلکالاز یا نوتراز به مدت 6 ساعت واکنش نشان داد، که نشان می دهد کلاژن به عنوان یک بستر مناسب برای برخی از آنزیم های دیگر آزمایش شده عمل می کند.فواید عصاره سیستانچ،با این حال، باندهای CH-Flavorzyme و CH-Papain در محدوده وزن مولکولی کم تا بالا پس از 24 ساعت ظاهر شدند. بسته به نوع پروتئاز، زمان انکوباسیون و نسبت پروتئاز به سوبسترا (مقدار پروتئین) می توان تا حدی با هیدرولیز آنزیمی به پپتیدها یا اسیدهای آمینه هیدرولیز کرد. فرآیند هیدرولیز آنزیمی عمدتاً با این که آیا نوع پروتئاز درگیر یک اندوپپتیداز یا یک اگزوپپتیداز است تعیین می شود [15،16]. از آنجایی که آلکالاز، نوتراز و پروتامکس اندوپپتیدازهایی هستند، فرآیندهای هیدرولیز آنها ممکن است انتظار داشته باشد که پیوندهای پپتیدی از اسیدهای آمینه غیر پایانی را به طور تصادفی بشکند و در نتیجه هیدرولیز بیشتر پروتئین ها را تسهیل کند. از سوی دیگر، Flavorzyme هم یک اندو و هم اگزوپپتیداز است که غیر یا N-ترمینال زنجیره های پپتیدی را می شکند. در این مطالعه، پروتئین کلاژن حاوی محلهای اتصال بود که نسبت به فعالیت آندوپپتیداز Flavorzyme حساستر به فعالیت اگزوپپتیداز بود. بنابراین، به دلیل فعالیت اگزوپپتیداز، هیدرولیز پروتئین های کلاژن توسط Flavorzyme شامل شکستن گام به گام پیوندهای پپتیدی از ترمینال N آمینو اسیدها بود که هیدرولیز پروتئین را کاهش داد.

2.1.3. بازیابی پروتئین و محتوای گروه آمینو رایگان
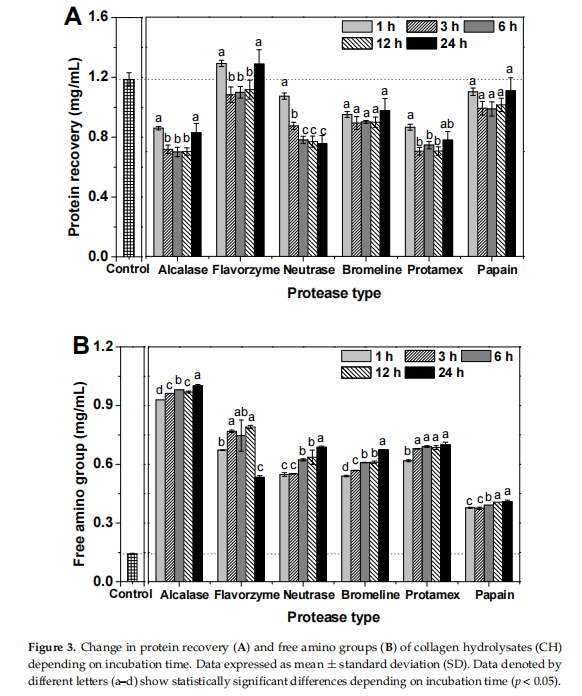
بازیابی پروتئین CHهای بدست آمده از طریق پروتئازهای تجاری مختلف نشان داده شده است (شکل 3A). شاهد (سوسپانسیون کلاژن) دارای محتوای بازیابی پروتئین 1.19 میلی گرم بر میلی لیتر بود. بازیابی پروتئین پارامتری از کارایی هیدرولیز آنزیمی است. محتوای بازیابی پروتئین کم CH نشان دهنده افزایش تجزیه پروتئین است. علاوه بر این، بازیابی پروتئین به خوبی با حلالیت پروتئین ارتباط دارد. فعالیت هیدرولیتیک بالاتر ممکن است به دلیل افزایش زنجیره های جانبی آبگریز در معرض، منجر به افزایش فعل و انفعالات آبگریز بین پروتئین ها و/یا پپتیدها شود. این زنجیره های جانبی آبگریز ممکن است منجر به کاهش حلالیت پروتئین شود، بنابراین منجر به افزایش بازیابی پروتئین هیدرولیزها می شود. در مطالعه ما، محتوای بازیابی پروتئین به خوبی با تغییرات در الگوهای SDS-PAGE همبستگی داشت. کمترین و بالاترین میزان بازیابی پروتئین به ترتیب برای هیدرولیز آلکالاز و فلوورزیم ثبت شد. برای راندمان هیدرولیز مربوط به زمان انکوباسیون، CH-Alcalase، CH-Bromelain و CH-Protamex در یک ساعت پس از انکوباسیون نسبت به شاهد به شدت کاهش یافتند. کاهش محتوای بازیابی پروتئین ناشی از هیدرولیز پروتئین رابطه معکوس با محتوای گروه آمینه نشان داد. علاوه بر این، اکثر CH ها، به جز CH-Neutrase، محتوای پروتئین کم را بین 3 ساعت و 12 ساعت نشان دادند. پس از 24 انکوباسیون، محتوای پروتئین آنها دوباره در CH-Alcalase، CH-Flavorzyme، CH-Neutrase، CH-Bromeline، CH-Protamex و CH-Papain به شرح زیر افزایش یافت:{18}}. میلیلیتر، 75.75. برخی گزارشها نشان میدهند که زمان هیدرولیز بهینه به عوامل متعددی مانند گونه انتخابشده، ماده خام، آنزیم مورد استفاده، نرخ ماده خام/آنزیم، غلظت آنزیم و درجه هیدرولیز مورد نظر و غیره بستگی دارد. ]. برخی گزارش ها نشان می دهد که هیدرولیز آنزیمی طولانی مدت (بیش از 24 ساعت) ممکن است منجر به کاهش فعالیت پروتئاز شود. بنابراین، هیدرولیز آنزیمی باید در عرض 24 ساعت از هیدرولیز آنزیمی انجام شود [17،18].

The free amino group content of CH, which is an indicator of enzymatic hydrolysis efficiency, was estimated(Figure 3B). The expected outcome of protein breakdown is that protein may be hydrolyzed into shorter peptide products. The free amino group content of the control was initially 0.14 mg/mL. The free amino group content of all CHs dramatically increased with increasing incubation time. After 24 h incubation, the free amino group content by descending order was: CH-Alcalase (1.00 mg/mL)>CH-Protamex(0.70 mg/mL)> CH-Neutrase(0.68 mg/mL)>CH-Bromeline (0.67 mg/mL)>CH-Flavorzyme (0.53 mg/mL)>CH-Papain (0.40 mg/mL). تفاوتهای رایج در پروتئین کل یا محتوای گروه آمینه آزاد نمونههای هیدرولیز شده آنزیمی ممکن است به ویژگی آنزیم مربوط باشد. این به خواص آنزیم در طول فرآیند هیدرولیز آنزیمی وابسته است [16،17]. به عنوان مثال، پروتئازهای قلیایی (مانند آلکالاز) در مقایسه با پروتئازهای اسیدی یا خنثی، فعالیت هیدرولیتیک بالاتری از خود نشان می دهند.
2.2. اثر اولترافیلتراسیون بر خواص هیدرولیز کلاژن
یک فرآیند اولترافیلتراسیون ممکن است یک روش مفید و سودمند صنعتی برای تولید فراکسیون های پپتیدی کوچک با اندازه مولکولی مطلوب و زیست فعالی بالا باشد، بسته به ترکیب هیدرولیز اولیه و فعالیت مورد مطالعه [19]. حلالیت، محتوای گروه آمینه آزاد و بازده CH ها پس از لیوفیلیزاسیون نشان داده شده است (جدول 1). میزان حلالیت و محتوای گروه آمینو آزاد گروه شاهد به ترتیب 95/11 درصد و 79/9 درصد 0 بود. پس از هیدرولیز آنزیمی و اولترافیلتراسیون با وزن مولکولی 3 کیلو دالتون، بیشترین حلالیت (21.17 درصد) و محتوای گروه آمینه آزاد (14.17 درصد) در CH-Alcalase مشاهده شد.<3 kda.="" however,=""><3kda was="" the="" lowest="" field="" (12.42%)observed.="" therefore,="" although="" ultrafiltration="" is="" useful="" in="" separating="" chs="" with="" low="" molecular="" weight,="" it="" may="" cause="" a="" reduction="" in="">

میانگین وزن مولکولی هیدرولیزهای پروتئین عامل مهمی است که خواص بیولوژیکی آنها را تعیین می کند [19]. به طور کلی، کسری متوسط با مگاوات<3 kda="" represents="" a="" collagen="" hydrolysate;="" an="" average="" fraction="" with="" mw=""> 50 kDa represents gelatin, and an average fraction with MW>300 کیلو دالتون نشان دهنده کلاژن است [20،21]. توزیع وزن مولکولی نسبی کنترل (نمونه پیش تیمار)، CH-Alcalase و CH-Alcalase<3 kda="" is="" depicted="" in="" figure="" 4.="" the="" molecular="" weight="" distribution="" was="" over="" 20,100="" da="" for="" the="" control,="" which="" did="" not="" include="" the="" collagen="" hydrolysate=""><3 kda).="" this="" could="" not="" be="" numerically="" provided="" in="" this="" study,="" as="" the="" detection="" limit="" of="" the="" index="" detector="" system="" only="" ranged="" from="" 106="" to="" 20,100="" da.="" however,="" ch-alcalase="" showed="" detectable="" values="" in="" a="" higher="" range="" of="" relative="" molecular="" weight="" distribution,="" which="" ranged="" from="" 20,100="" da="" to="" 4270="" da="" (maximum="" peak:12,600="" da).in="" ch-alcalase=""><3 kda,="" the="" molecular="" weight="" distribution="" mainly="" showed="" three="" peaks:="" one="" with="" an="" mw="" of="" approximately="" 4270="" da(maximum="" peak),="" one="" with="" an="" mw="" of="" approximately="" 424="" da,="" and="" one="" with="" an="" mw="" of="" approximately="" 222="" da="" and="" 102="" da.="" ultrafiltration="" is="" an="" effective="" purification="" method="" used="" to="" obtain="" low="" molecular="" weight="" peptides="" from="" crude="" hydrolysates.="" results="" indicated="" that="" enzymatic="" hydrolysis="" by="" alcalase="" clearly="" reduced="" the="" high="" mw="" of="" the="" control="" (either="" collagen="" or="" gelatin),="" and="" that="" ultrafiltration="" was="" an="" effective="" purification="" method="" that="" can="" be="" used="" to="" obtain="" low="" molecular="" weight=""><3 kda)="" from="" crude="" collagen="" hydrolysates.="" reportedly,="" low="" molecular="" weight="" peptides="" (2-20="" amino="" acids)="" are="" more="" biologically="" active="" compared="" to="" their="" parent="" polypeptide/="" proteins,="" which="" are="" larger="">

ترکیب اسید آمینه در CH ها نشان داده شده است (جدول 2). CHS توسط پروتئازهای مختلف دارای ترکیب اسید آمینه و خواص آنتی اکسیدانی متفاوتی بود [23]. ترکیب اسید آمینه کلاژن سرشار از گلیسین (Gly)، پرولین (Pro) و اسید گلوتامیک (Glu) بود. محتوای اسید آمینه CHs (CH-Alcalase و CH-Alcalase).<3 kda)="" increased="" more="" than="" that="" of="" the="" control,="" following="" enzymatic="" hydrolysis="" with="" or="" without="" ultrafiltration.="" in="" particular,="" the="" content="" of="" gly,="" pro,="" and="" glu="" was="" much="" higher="" in=""><3 kda(gly="" 218="" mg/g,="" pro="" 152="" mg/g,="" and="" glu="" 120="" mg/g)="" than="" ch-alcalase(gly149="" mg/g,="" pro="" 95mg/g,="" and="" glu78="" mg/g).="" an="" increase="" in="" the="" content="" of="" these="" amino="" acids="" is="" strongly="" related="" to="" enhanced="" antioxidant="" capabilities="" 16,20].="" gly="" and="" pro="" contain="" hydrophobic="" amino="" acid="" groups,="" and="" glu="" contains="" negatively="" charged="" amino="" acid="" groups.="" these="" amino="" acids="" have="" been="" reported="" to="" enhance="" antioxidant="" activity="" because="" of="" their="" increased="" solubilities="" in="" lipids="" or="" via="" free="" radical="" reactions="">


این مقاله از Molecules 2019, 24, 1104 استخراج شده است. doi:10.3390/molecules24061104 www.mdpi.com/journal/molecules
