تعیین ساختاری NMR بدون ابهام محصولات واکنش دیمری (به علاوه)-کاتچین-لاکاز به عنوان نشانگرهای بالقوه اکسیداسیون انگور و شراب
Mar 12, 2022
برای جزئیات بیشتر تماس بگیرید:tina.xiang@wecistanche.com
خلاصه:( بعلاوه )-کاتچین-لاکازاکسیداسیوناستانداردهای دیمری با استفاده از لاکاز از Trametes Versicolor یک محلول آب-اتانول در pH 3.6 است. هشت بخش مربوط به هشت محصول دایمر اکسیداسیون بالقوه شناسایی شد. پروفایل های فراکسیون ها با پروفایل های به دست آمده با دو اکسیدوردوکتاز دیگر مقایسه شد:پلی فنل اکسیدازاستخراج شده از انگور و لاکاز از Botrytis cinerea. پروفایل ها بسیار مشابه بودند، اگرچه برخی از تفاوت های جزئی تفاوت های احتمالی را در واکنش پذیری این آنزیم ها نشان می دهد. سپس پنج بخش جدا شده و با طیفسنجی NMR 1D و 2D آنالیز شدند. افزودن ردپای نیترات کادمیوم در نمونههای حلشده در استون به سیگنالهای NMR کاملاً حلشده پروتونهای فنلی منجر شد، که امکان تعیین ساختاری بدون ابهام شش محصول واکنش، یکی از فراکسیونهای حاوی دو انانتیومر را فراهم کرد. این محصولات بیشتر می توانند به عنوان نشانگرهای اکسیداسیون برای بررسی حضور و تکامل آنها در شراب در طول شراب سازی و پیری شراب مورد استفاده قرار گیرند.
کلید واژه ها: نشانگر اکسیداسیون؛ (به علاوه) -کاتچین. سیگنال های NMR فنولی؛ لاکاز؛ نیترات کادمیوم؛ پلی فنل اکسیداز

برای دریافت اطلاعات بیشتر کلیک کنید
1. مقدمه
پلی فنول هاخانواده ای از ترکیبات شیمیایی هستند که به طور گسترده در طبیعت وجود دارند. آنها به مقدار قابل توجهی در چای [1]، کاکائو [2،3]، زغال اخته [4]، انگور [5 لیتر، و محصولات تخمیر شده مانند شراب [6] یافت می شوند. ساختار شیمیایی پلی فنل ها به عنوان اهداف اولیه اکسیداسیون J7,8] به طور مداوم تکامل می یابد. این تغییرات بر خواص ارگانولپتیکی بسیاری از انواع مواد غذایی تأثیر می گذارد. آنها مسئول پدیده هایی مانند قهوه ای شدن غذا [9] و اصلاح ویژگی های حسی شراب هستند [10،11. در انولوژی، این پدیده اکسیداسیون در انگور یا شراب اتفاق می افتد. در مورد اکسیداسیون آنزیمی، آنزیم های اصلی مسئول قهوه ای شدن اکسیدوردوکتازها هستند، به طور دقیق تر،پلی فنل اکسیدازموجود در انگور و لاکاز تولید شده توسط Botrytis cinerea [12].
آنزیمیاکسیداسیونعمدتاً در گل انگور رخ می دهد، اما قهوه ای شدن بیشتر شراب ممکن است به دلیل واکنش های اکسیداسیون شیمیایی |7،13] یا بوتریتیس سینرئا لاکاز باشد که می تواند در طول پیری شراب بسیار پایدار باشد. دو فعالیت آنزیمی اکسیداسیون ممکن است روی بسترهای فنلی رخ دهد: فعالیت مونوفنل اکسیداز که با هیدروکسیلاسیون یک گروه هیدروکسیل موجود در موقعیت مجاور مشخص می شود و فعالیت دی فنل اکسیداز مربوط به اکسیداسیون ارتو دی هیدروکسی بنزن ها به ارتو بنزوکینون ها.
طبق کمیته نامگذاری اتحادیه بینالمللی بیوشیمی و زیستشناسی مولکولی (NC-IUBMB)، این فعالیتهای آنزیمی توسط آنزیمهای کلاس{1} EC مربوط به اکسیدوردوکتازها کاتالیز میشوند. در میان آنها، سه دسته اصلی اکسیدوردوکتازها که اکسیداسیون پلی فنل را کاتالیز می کنند عبارتند از EC1.14.18.1 (مونوفنول مونواکسیژناز)، EC1.11.1 (پراکسیداز/POD) و EC1.10.3 (اکسیدوردوکتازهای اثر بر دی فنل ها).
این کلاس آخر به زیر کلاسهای مختلفی تقسیم میشود، و دو مورد از آنها برای این مطالعه جالب به نظر میرسند: EC1.10.3.1 (پلی فنل اکسیداز/PPO) و EC1.10.3.2 (لاکاز) (به مواد تکمیلی شکل S1 مراجعه کنید).
PPO، لاکاز و پراکسیداز اکسیدوردوکتازهایی هستند که عمدتاً مسئول قهوه ای شدن در طی فرآوری انگور هستند [13]. قهوه ای شدن ناشی از POD در میوه ها ناچیز است اما می تواند تجزیه فنل ها را در صورت ترکیب با PPO افزایش دهد[15]. PPO به طور طبیعی در انگور وجود دارد و قادر است اکسیداسیون مونوفنول ها را به کاتکول ها و کاتکول ها را به رنگدانه های قهوه ای کاتالیز کند [8،13،16]. لاکازها که در انگورهای آلوده به بوتریتیس یافت میشوند، طیف عمل گستردهتری دارند، زیرا میتوانند اکسیداسیون بسیاری از بسترهای مختلف را کاتالیز کنند. اهداف اصلی اکسیداسیون لاکازها 1-2 و 1-4 دی هیدروکسی بنزن باقی می مانند.
در شراب، بنزوکینون تولید شده توسط اکسیداسیون (PPO یا لاکازها) بسته به خواص اکسیداسیون و کاهش و وابستگی های الکترونیکی به راحتی می تواند تحت واکنش های بیشتری قرار گیرد [15]. آنها می توانند به عنوان الکتروفیل عمل کنند و با مشتقات آمینه واکنش دهند [18] یا به عنوان اکسیدان عمل کنند و از جمله با سوبستراهای فنلی واکنش نشان دهند. بسته به ترکیب شیمیایی آنها (کینون یا نیمه کینون)، بنزوکینون می تواند منجر به محصولات مختلف واکنش اکسیداسیون شود. در یک pH خنثی، (+)-کاتچین در موقعیت حلقه A C5 یا C7 به کینون اکسید می شود و منجر به تشکیل شش ایزومر دایمری ممکن می شود که دلالت بر پیوند بین موقعیت حلقه B C2'، C5'، یا C6' واحد کاتچین بالایی و موقعیت حلقه A C6 یا C8 واحد پایینی [19,20]. دهیدرودیکاتچین محصول شناخته شده این جفت است [21]. موقعیتهای برچسبگذاری ساختارها در شکل 1 نشان داده شده است. در شرایط اسیدی، اشکال نیمهکینونی نیز میتواند روی حلقه B (موقعیت OH3' یا OH4') وجود داشته باشد و منجر به چهار ایزومر دیمری احتمالی شود [20،22] با واحد کاتچین بالایی و حلقه A واحد پایینی (موقعیت C6 یا C8). اکسیداسیون آنزیمی کاتچین در مطالعات قبلی مورد بررسی قرار گرفت [22،23]، و محصولات اکسیداسیون مرتبط با HPLC [24] مشخص شد، اگرچه به ندرت جدا شده و هرگز به طور کامل توسط NMR مشخص نشد.

هدف از این کار ابتدا با UHPLC-MS مقایسه پروفایل های محصولات اکسیداسیون دیمریک (به علاوه) - کاتچین در حضور سه عصاره اکسیدوردوکتاز، یعنی PPO استخراج شده از انگور، لاکاز از قارچ Botrytis cinerea موجود در شراب های شیرین بوتریتیزه شده بود. [14] و لاکاز از Trametes Versicolor.
هدف دوم نیم سنتز و مشخص کردن ساختارهای برخی از محصولات اکسیداسیون دایمر توسط طیف سنجی NMR به دست آمده با لاکاز از Trametes Versicolor بود.

2. نتایج و بحث
2.1. مقایسه پروفایل های محصولات واکنش دایمر با سه اکسیدوردوکتاز مختلف و (به علاوه) -کاتچین
(به علاوه) -کاتچین برای اولین بار در حضور لاکاز از Trametes Versicolor در pH3.6 در محلول شراب مدل اکسید شد. پس از جداسازی کسر دیمری از باقیمانده (بعلاوه)-کاتچین و سایر فراکسیون های پلیمری، هشت فراکسیون اصلی جمع آوری و توسط UHPLC-UV-MS مورد تجزیه و تحلیل قرار گرفت که از N1 تا N8 به ترتیب زمان ماند افزایشی ذکر شد (جدول 1). طیف جرمی الکترواسپری در حالت مثبت پیک های یونی [M به علاوه H] به علاوه در m/z 579 برای N1 تا N6 را نشان داد، که به طور فرضی مربوط به یک دایمر تشکیل شده توسط یک پیوند واحد بین دو واحد کاتچین، و [M به علاوه H] به علاوه در m/577 برای N7 و N8، به طور فرضی نشان دهنده تشکیل یک پیوند اضافی است.

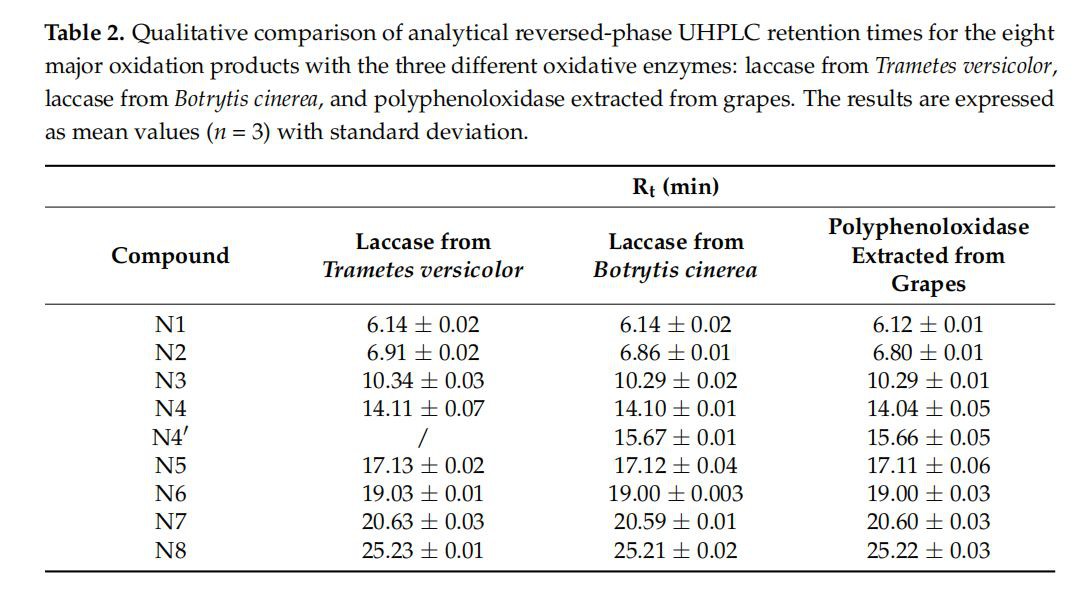
این هشت تااکسیداسیونکسری به طور بالقوه پس از پلیمریزاسیون شیمیایی یک بخش تانن در کارهای قبلی [25،26] مشاهده شد و احتمالاً می تواند همان مواردی باشد که قبلا توسط Guyot و همکارانش توضیح داده شده است. [20]، حتی اگر شرایط تجربی کمی متفاوت باشد. در واقع، در این مطالعه قبلی، یک عصاره خام PPO در pH 3 و 6 برای به دست آوردن هشت فراکسیون استفاده شد. در مطالعه حاضر، سه آنزیم مختلف در pH 3.6 در محلول شراب مدل مقایسه شدند. تجزیه و تحلیل مقایسه ای LC-MS از فراکسیون های اکسیداسیون اصلی به دست آمده با سه آنزیم مختلف (لاکاز از Trametes Versicolor، لاکاز از Botrytis cinerea، و پلی فنل اکسیداز استخراج شده از انگور) در جدول 2 ارائه شده است. زمان ماند تقریباً با آنزیمهای مختلف یکسان بود و m/z مشابه با آنالیز MS تعیین شد. این نتایج این فرضیه را تایید میکند که بخشهای یکسانی برای هر آنزیم، حاوی محصولاتی با ساختارهای مشابه با فرضیههای Guyot و همکاران، به دست آمده است. [20]. Lopez-Serrano و Ros Barcel6 [27] همچنین یک مطالعه مقایسه ای روی محصولات اکسیداسیون (+)-کاتچین با دو آنزیم مختلف انجام دادند: پراکسیداز و پلی فنل اکسیداز، که هر دو از توت فرنگی استخراج می شدند. آنها به این نتیجه رسیدند که محصولات به دست آمده با دو آنزیم از نظر کیفی یکسان هستند. یک ترکیب اضافی به نام N4' با m/z=578 Th و Rt=15.66 دقیقه در آزمایشها با لاکاز از Botrytis cinerea و PPO استخراج شد، اما نه با لاکاز از Trametes Versicolor، که تفاوتهای احتمالی را نشان میدهد. در واکنش پذیری برای این آنزیم ها.
2.2. بررسی و بهینهسازی پارامترهای فیزیکوشیمیایی بر روی سیگنالهای فنلی و آلیفاتیک OH 1H-NMR
خصوصیات ساختاری دیمرهای پروسیانیدین را می توان با تجزیه و تحلیل NMR به دست آورد. به طور خاص، موقعیت پیوند دقیق بین واحدها ممکن است با استفاده از طیف های همبستگی HMBC و/یا ROESY [28،29] تعیین شود (شکل های S2 و S3). در مورد پیوند نوع اتری (COC)، نسبت پروتون های سیگنال هیدروکسیل ضروری است. اگر برخی از پروتونهای آلیفاتیک یا آروماتیک با هم همپوشانی داشته باشند یا برخی از همبستگیهای کلیدی وجود نداشته باشند، ممکن است در مورد پیوندهای CC بسیار مهم باشد. با این حال، حتی در یک حلال آپروتیک، پروتون های هیدروکسیل پلی فنل ها اغلب به عنوان سیگنال های گسترده ای ظاهر می شوند که هیچ اطلاعات ساختاری از آنها نمی توان به دست آورد [30]. این موضوع به طور آزمایشی با افزودن آثاری از
Cd(NO3)2 در محلول های نمونه. در واقع، سیگنال های گسترده H گروه های OH به دلیل تبادل بین مولکولی بین این پروتون های OH و سایر پروتون های موجود در حلال یا املاح است. با کاهش پیوندهای بین مولکولی، حضور نیترات کادمیوم در نمونه ها ممکن است این تبادلات را کاهش دهد، بنابراین وضوح سیگنال های پروتون OH را بهبود می بخشد.
2.2.1.اثر افزودن کادمیوم
پس از خشک کردن انجمادی، پنج بخش N2، N3، N4، N6 و N8 در استون-dg حل شدند. سپس، طیف پروتون NMR 1D در 25 درجه قبل (شکل 2A) و پس از افزودن مقادیر کمی کادمیوم (شکل 2B) بدست آمد. در استون خالص، پروتونهای OH فنلی همه فراکسیونها بهعنوان قلههای وسیع ظاهر شدند. پس از افزودن کادمیوم، این پروتونها در مورد بخشهای N6 و N8 سیگنالهایی با وضوح بالا نشان دادند، در حالی که برای بخشهای N2، N3 و N4 سیگنالها فقط کمی واضحتر بودند. همچنین لازم به ذکر است که افزایش محتوای Cd هیچ تاثیری بر وضوح سیگنال OH نداشت، زیرا هیچ وضوح یا وسعتی از پهنای خط پیک مشاهده نشد که مقادیر کمی از سی دی به نمونهها اضافه شد (دادهها نشان داده نشده است).
سیگنالهای OH فنولی بسیار تفکیکشده از محصولات N2، N3، و N4 به لطف خشک کردن و حلسازی مجدد اضافی به دست آمد (شکل 2C،D).

تفاوت رفتار پس از افزودن کادمیوم بین بخشها را میتوان با قدرت برهمکنشهای مولکولی توضیح داد: در مورد N2، N3، و N4 در مقایسه با N6 و N8 قویتر است، مرحله دیگری برای شکستن این پیوندها ضروری است.
این مرحله اضافی ممکن است مرحله کلیدی در هنگام استفاده از کادمیوم برای به دست آوردن سیگنال های OH فنولی بسیار تفکیک شده در هر موقعیتی باشد، صرف نظر از منشاء نمونه ها، واکنش سنتز، یا محصولات پلی فنلی طبیعی.
کار قبلی که با خصوصیات ساختاری بدون ابهام سروکار داردپلی فنولدایمرها با استفاده از سیگنالهای NMR فنلی OH با تفکیک بالا به لطف افزودن نیترات کادمیوم در سال 1996 منتشر شد [30]. تا آنجا که ما می دانیم، از آن زمان تاکنون هیچ مقاله پژوهشی دیگری با استفاده از این روش منتشر نشده است. تحقیقات دیگری متعاقباً برای رسیدن به این هدف، یا با افزودن دوز اسید پیکریک [31] یا با استفاده از دمای اکتساب پایین [32] انجام شد. این ممکن است با گام بعدی لازم برای به دست آوردن یک اثر تعیین کننده بر وضوح اوج OH با افزودن Cd توضیح داده شود، همانطور که در بالا توضیح داده شد. با این حال، به نظر می رسد کادمیوم از ارزش بالایی برخوردار است، زیرا سیگنال های بسیار تفکیک شده را می توان بدون نیاز به افزودن مقادیر دقیق به دست آورد، برخلاف اسید پیکریک یا کسب طیف NMR در دماهای پایین.
2.2.2. اثر دما
کاهش دما از 25 درجه سانتیگراد به 15 درجه تأثیری بر وضوح سیگنالهای OH فنلی یا آلیفاتیک OH نداشت. با این وجود، جابجاییهای پایینزمینی پیکهای پروتونی مبادلهای به ما این امکان را داد که برخی از سیگنالهای فنلی و آلیفاتیک OH را از هم جدا کنیم و شناسایی آنها را واضحتر نشان دهیم (شکل 3). با کاهش دما، نرخ تبادل پروتون کاهش مییابد و میتوان انتظار پیکهای آلیفاتیک OH شدیدتر را داشت [31]. بدیهی است که دمای 15 درجه به اندازه کافی پایین نیست تا سیگنال های OH آلیفاتیک را به خوبی حل کند. با این حال، به ما اجازه داد تا به وضوح تشدید دو پروتون OH آلیفاتیک در نمونههای N3 و N6 و یکی در نمونه N8 را شناسایی کنیم. طیف نمونه N2 همچنین دو سیگنال پروتون آلیفاتیک OH را نشان داد که در دمای 25 درجه سانتیگراد بیشتر از 15 درجه قابل تشخیص بودند (شکل 2E). طیف، چه دما روی 25 درجه تنظیم شده باشد یا روی 15 درجه سانتیگراد، به دلیل همپوشانی مداوم (شکل 2E).

2.3. خصوصیات ساختاری استانداردهای دایمر - تجزیه و تحلیل طیف NMR
طیف NMR بخشهای N2، N3، N4، N6 و N8 نشان داد که محصولات اکسیداسیون خلوص بالایی دارند زیرا شدت سیگنال سایر ترکیبات شناساییشده کمتر از 10 درصد در مقایسه با این محصولات بود.
در همه طیفها، چهار ناحیه تغییر شیمیایی lH معمولی واحدهای کاتچین را میتوان متمایز کرد (شکل 2C): سیگنالهای پروتونهای آلیفاتیک حلقههای پیران (حلقههای C) در منطقه از 2.3 تا 50 ppm یافت میشوند. و پروتون های سیگنال معطر حلقه های رزورسینول (حلقه A) و حلقه های کاتکول (به ارمغان می آورد) به ترتیب از 5.5 تا 6.3 ppm و 6.3 تا 7.1 ppm. سیگنال های فنل OH هر دو حلقه A و B از 7.1 تا 10 ppm ظاهر شدند. طیف NMR هر دو بخش وجود مجموعه سیگنال مجزا از واحدهای کاتچین را در نسبت شدت ثابت نشان داد: دو مجموعه سیگنال در طیف کسرهای N2، N3، N6 و N8 مطابق با حضور دایمرها مشاهده شد، و چهار مجموعه در طیف N4، که می تواند مربوط به یک تترامر، دو دایمر، یا مخلوطی از الیگومرهای مختلف باشد، یعنی یک تریمر به اضافه یک مونومر. به منظور تعیین درجه الیگومریزاسیون محصولات موجود در کسر N4، آزمایش H DOSY با استفاده از مخلوطی حاوی مقدار کمی از هر دو بخش N4 و N2 انجام شد. ضرایب انتشار همه سیگنال ها مقادیر مشابهی را نشان می دهد (شکل 4) که نشان دهنده وجود دو دیمر کاتچین در کسر N4 است.

به لطف سیگنال های فنل OH کاملاً حل شده که نتایج کمی قابل اعتمادی را ارائه می دهد، نوع پیوند بین واحدهای کاتچین ممکن است مستقیماً از ادغام سطح پیک استنتاج شود. بنابراین، برای هر دو فراکسیون، N3 و N6، فقدان یک OHphenol (متعلق به رزورسینول یا حلقه کاتکول) و فقدان یک پروتون آروماتیک رزورسینول نشان دهنده یک پیوند بین فلاوانی (IFL) از نوع اتر است که به معنای مخالفت در A است. یا حلقه B و موقعیت C6 یا C8 در یک حلقه A. در مورد نمونه N2، دو پروتون معطر وجود نداشت، یکی از یک حلقه B و دیگری از یک حلقه A، که دلالت بر CA-CB IFL دارد. طیف 1D'H کسر N4 نشان داد که دو پروتون از حلقه B و همچنین دو پروتون از حلقه A وجود ندارد. بنابراین پیوندهای بین واحدهای دایمر کسر N4 هر دو از انواع CC هستند. طیف کسر N8 کاملاً متفاوت از چهار بخش دیگر بود. برخی سیگنالها نمونهای از واحدهای کاتچین بودند که در آنها سه فنل OH، یک حلقه A آروماتیک و یک پروتون حلقه B و همچنین یک OH آلیفاتیک وجود نداشت. از سوی دیگر، برخی دیگر از سیگنالهای NMR غیر معمول واحد کاتچین هستند: متیلن با شیفتهای شیمیایی 13C (~40ppm) و یک گروه کتون (~192ppm).
سیستمهای اسپین پروتون حلقههای C، A، و B با استفاده از هر دو طیف TOCSY H 1D و 1H 2D تعیین شدند (نمایش داده نشده است). دو سیستم چرخش حلقه C ABMX (معمولاً کاتچین) در طیف فراکسیونهای N2، N3، N6 و N8 و چهار سیستم برای کسر N4 مشاهده شد. در طیف فراکسیون های N2، N3، N6 و N8، دو دوتایی متا جفت شده (J~2Hz) و یک تک در ناحیه حلقه آروماتیک A به ترتیب به پروتون های حلقه A واحد کاتچین غیر مرتبط اختصاص داده شدند. و به پروتون باقیمانده حلقه A واحد کاتچین C6-یا C{17}}پیوند داده شده است. در طیف N4، به دلیل وجود دو دایمر، چهار دوتایی متا کوپل شده و دو سینگل شناسایی و به شرح بالا اختصاص داده شدند. سیستمهای پروتون حلقه B نیز به راحتی از این طیفها تعیین شدند و به ما اجازه دادند دو سیستم اسپین پروتون ABM را برای دیمرهای بخشهای N3 و N6 شناسایی کنیم، در حالی که یک سیستم اسپین پروتون ABM و یک AB برای دایمر N2 و یک ABM و یک سیستم اسپین پروتون AM برای دایمر N4. دایمر N8 تنها یک سیستم چرخش حلقه B ABM معمولی یک مونومر کاتچین را نشان داد.
2.3.1. تعیین موقعیت حلقه A از IFL دیمرهای کسری N2، N3، N4 و N6
ایجاد پل بر روی حلقه A از دایمرها (یعنی موقعیت C6A یا C8A) مستلزم نسبت دادن پروتون HA باقیمانده واحد کاتچین متصل به CA است. به لطف سیگنال های OH فنولی بسیار حل شده، یک نقطه شروع آسان، شناسایی دو پروتون OHفنول از واحدهای متصل به حلقه A بود، یعنی حلقه A که
had one isolated lHspin. This may be achieved using lH-13C long-range correlations, as illustrated in Figure5. The OH5A has readily been identified thanks to a correlation with the C4aC. This quaternary carbon is indeed characterized by both its chemical shift at~100 ppm and a long-range correlation observed with the H4Cprotons. OH5A also correlated with two other carbons∶ the most deshielded (δ>145 ppm) was obviously C5A, while the other (6>125 ppm) was C6A, which also showed a correlation with the other OHA phenol proton,i.e., OH7A. This latter correlated with two other carbons: a deshielded quaternary carbon(δ>145ppm) and a more shielded carbon(δ>125 ppm) که به راحتی به C7A و C8A نسبت داده شد. هنگامی که C6A و C8A اختصاص داده شدند، پروتون باقیمانده HA ممکن است مستقیماً به طیف HSQC نسبت داده شود. بنابراین مشخص شد که این پروتون HA باقیمانده برای همه بخشهای N2، N3، N4، N6 H6A بود. بنابراین IFL بین واحدهای کاتچین یک موقعیت C8A را برای همه دایمرها نشان می دهد.
2.3.2. تعیین موقعیت حلقه B IFL
دیمرهای کسرهای N2 و N4. طیف کسر N2 دو نوع مختلف از سیستم اسپین پروتون حلقه B را نشان داد: یکی AMX مربوط به حلقه B واحد غیر پیوندی، و دیگری AM با ثابت جفت شدن حدود 8 هرتز، مشخصه H6'B و H5'. B از یک واحد متصل به C2'B. بنابراین پیوند بین واحدهای دایمر N2 C2'B-C8A است. طیف NMR کسر N4 نیز سیستمهای اسپین B متفاوتی را نشان داد: دو AMX، مربوط به حلقه B غیر مرتبط، و دو سیستم AXspin، که هر دو ثابتهای جفتی حدود 2 هرتز را نشان میدهند که مشخصه H2'B و H6' هستند. پروتون های B واحدهای مرتبط با C5'B. وجود همبستگی های دوربرد'H/13C بین H6'Band C8A، که در طیف HMBC دو دیمر مشاهده شد، مطابق با پیوند C5/'B-C8A است (شکل 5).

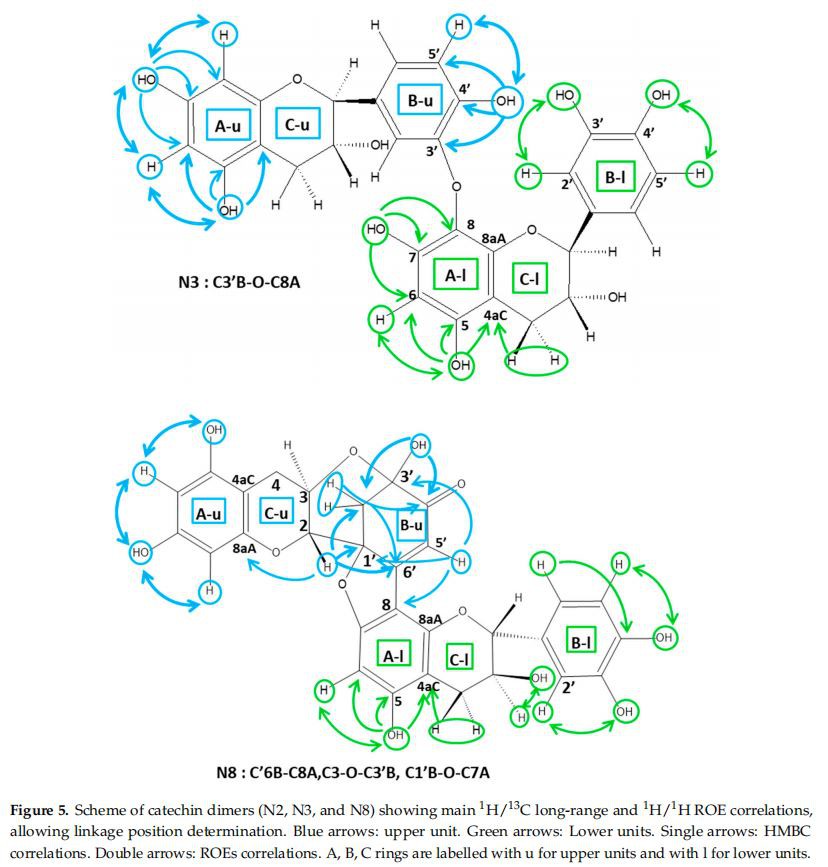
دیمرهای کسرهای N3 و N6. طیف فراکسیون های N3 و N6 حضور دو سیستم پروتون حلقه B AMX و عدم وجود یک سیگنال فنل OH را نشان داد. از آنجایی که همه پروتونهای فنلی OHA واحدهای دایمر شناسایی شدند (همانطور که در بالا توضیح داده شد)، سیگنال فنلی OH از دست رفته میتواند سیگنال OH3'B یا OH4'B باشد.
موقعیت OH (3'B یا 4'B) را می توان به راحتی از طریق همبستگی های ROE با H2'Bor H5'B به ترتیب یا با استفاده از همبستگی های HMBC دوربرد همانطور که در شکل 5 نشان داده شده است تعیین کرد.
انتساب باقیمانده OH حلقه های B به آسانی با استفاده از همبستگی های دوربرد HMBC یا ROESY، همانطور که در شکل 5 نشان داده شده است، انجام شد. در مورد دایمر N3، یک همبستگی ROE بین H5'B و OH باقی مانده مشاهده شد. B از واحد کاتچین از طریق حلقه B آن به هم وصل شده است. بنابراین این OH به عنوان OH4'B شناخته شد. در مورد کسر N6، OH'B باقی مانده به OH3'B اختصاص داده شد، زیرا یک همبستگی ROE بین این OH و H2'B مشاهده شد. همبستگی های دوربرد HMBC مطابق با این اسناد است. سپس موقعیت پیوند این دو دایمر به شرح زیر تعیین شد: CO3'B-C8A و CO4'B-C8A برای N3 و N6. به ترتیب.
کسر N8. تجزیه و تحلیل طیف دایمر N8 نشان داد که یک واحد از این دایمر کاتچین است با دو موقعیت پیوند یکی حلقه A، یکی در موقعیت C8A و دیگری در موقعیت C-O7A، زیرا پروتون های H8A و OH7A هستند. گم شده واحد دیگر این دایمر ویژگیهای طیفی منفرد را نشان میدهد که نشاندهنده از دست دادن آروماتیک بودن حلقه B و وجود چندین موقعیت پیوند در هر دو حلقه B و C است.
سیگنالهای NMR برخاسته از حلقه B دو دوتایی در 2.49 و 2.71 پیپیام بودند که یک جفت جمینال تقریباً 15 هرتز (12.03 ppm) معمولی یک گروه متیلن و یک تکی در ppm 6.38 ناشی از یک پروتون اتیلنی را نشان میدادند. از آنجایی که این پروتون های متیلن و اتیلن جفت نشده اند، احتمالاً در موقعیت های 2'B و 5'B قرار دارند. طیف HIMBC همه همبستگیها را نشان میدهد، و اجازه میدهد نسبتهای دقیقی از کربنهای حلقه B، همانطور که در شکل 5 نشان داده شده است، نشان دهد. C2'B، و دو مورد باقیمانده، با کربنهایی که در ~90ppm و~162ppm تشدید میشوند، که میتوان به C1'B و C6'B.H5'B نسبت داد. : یکی کربنی است که قبلا به C3'B (~95ppm) اختصاص داده شده بود، و دیگری که در ~90ppm طنین انداز شد، بنابراین می توان به C1'B نسبت داد. سپس کربن در ~ 162 ppm به C6'B استنباط شد.
حضور یک OH آلیفاتیک (~ 5.8ppm) در موقعیت C3'B (~95ppm) از طریق همبستگی ROE آن با هر دو پروتون H2'B تعیین شد. علاوه بر این، OH3/B همبستگی HMBC را با یک کربن چهارتایی در 192.5 ppm، مشخصه یک گروه کتون در موقعیت C4'B داد.
محافظ این C1'B در حدود 40 ppm مطابق با کاهش آروماتیک بودن حلقه B است. علاوه بر این، فقدان OH در موقعیت C7A واحد دیگر با یک پیوند اتری C1'BO-C7A مطابقت دارد.
داده های NMR نشان داد که حلقه C این واحد فاقد OH3C است. وجود یک پیوند C3C-O-C3'B مطابق با محافظ C3C حدود 1.5ppm و همچنین تغییر شیمیایی C3'B است که نمونه کربن همیکتال (95ppm) است.
در مجموع، داده های طیفی NMR به ما این امکان را می دهد که نتیجه بگیریم که این دایمر با دهیدروکاتچین A که قبلا توسط Winges و همکارانش توضیح داده شد مطابقت دارد.[33] و سپس توسط Guyot و همکاران.[20].
ساختارهای شش ترکیب دیمری تعیین شده توسط این آنالیزهای NMR در شکل 6 نشان داده شده است، N2، N3، N6 و N8 محصولات خالص هستند و N4 مخلوطی از دو ایزومر است.


3. مواد و روشها
3.1.مواد شیمیایی
(به علاوه) - کاتچین هیدرات بزرگتر یا مساوی 98 درصد; لاکاز از Trametes Versicolor(0.94 U·mg-1); دی هیدرات دی بازیک فسفات سدیم بزرگتر یا مساوی 98 درصد; اسید سیتریک (معرف ACS، نیترات کادمیوم تتراهیدرات 99.997 درصد؛ اسید فرمیک و Amberlite XAD7HP از سیگما-آلدریچ) (سنت لوئیس، MO، ایالات متحده آمریکا) به دست آمدند. اسید (TFA) از Roth Labo (کارلسروهه، آلمان). آب LC-MS، استونیتریل LC-MS (ACN)، و متانول LC-MS (MeOH) همه از VWR (Radnor، PA، ایالات متحده آمریکا) بودند.
3.2. تهیه محلول شراب مدل
محلول شراب مدل یک محلول اتانول/آب (12/88؛ o/o) با 0.033 M اسید تارتاریک بود که با PH 3.6 با NaOH 1 M تنظیم شده بود [34].
3.3. عصاره های PPO انگور خام
عصاره PPO همانطور که قبلا توسط Singleton و همکارانش توضیح داده شد، تهیه شد.[35]. انگورهای منجمد ابتدا در یک بافر استات (1.5 مولار، pH5؛ 10 gL-I اسید اسکوربیک) مخلوط شدند. سپس مخلوط فیلتر شده و سانتریفیوژ شد (3000 گرم؛ 10 دقیقه). باقیمانده در نهایت با استون (80 درصد) شسته و در هوا خشک شد.
3.4.لاکاز از Botrytis Cinerea
لاکاز از Botrytis cinerea همانطور که توسط Quijada-Morin و همکارانش توضیح داده شد به دست آمد.[36]. از سویه VA612 (جمع آوری شده در 2005 در تاکستانی در Hautvillers، Champagne، فرانسه، از رقم Pinot Noir) تولید شد. به طور خلاصه، کشتها روی محیط مخمر جامد مالت به مدت یک هفته در دمای 24 درجه زیر نور آبی قرار گرفتند. سپس هاگ ها خراشیده شدند و در یک بالن 5{22}}0 میلی لیتری ارلن مایر حاوی 125 میلی لیتر محیط کشت (4{{3{37}}}} gL-1گلوکز، 7) تلقیح شدند. gL{1{41}}}}گلیسرول، 0.5 g·L-1L-histidine، 0.1 g:L{17}} CuSO، 1.8gL-1 NaNO3، 0.5g:L -1 KCl, 0.5gL-1 CaCl2·H2O,0.05g:L-1 FeSO4.7H2O,1.0g L-1KH2PO4 و 0.7gL-1 MgSO 4-7H2O). پس از 3 روز انکوباسیون و 2 روز رشد در همان محیط قبلی، اسید گالیک (2 گرم در لیتر-1) به پیش کشت ها اضافه شد. پس از 5 روز، محیط مایع فیلتر شد، و مایع رویی در یک سیستم فیلتراسیون Quixstand (GE Healthcare UK، Little Chalfont، انگلستان) مجهز به یک غشاء با وزن مولکولی 30 کیلو دالتون به فیلتراسیون مماس فرستاده شد. کنسانتره در نهایت تحت یک دیافیلتراسیون در برابر آب مقطر قرار گرفت و تنها بخش هایی که فعالیت اکسیدانی علیه ABTS داشتند ({54}} درجه) حفظ شدند.
3.5. روش اکسیداسیون
یک محلول لاکاز (1 گرم در لیتر-1) در بافر فسفات-سیترات قبلاً تهیه شده بود و به یک محلول 6 گرم در لیتر-1 (بعلاوه) -کاتچین (شراب مدل) اضافه شد تا غلظت نهایی لاکاز به دست آید {6}}.3 گرم لیتر-1. سپس محلول به دست آمده به مدت 2 ساعت به آرامی (180 دور در دقیقه) در دمای اتاق هم زده شد. غلظت ها قبلاً بهینه شده بودند و آزمایش در سه تکرار انجام شد.
3.6. توقف واکنش در Resin Amberlite XAD7HP
یک ستون کهربایی لایت با اتانول (مطلق) تهویه شد و با دو حجم ستونی آب میلیاکسی شسته شد. محیط واکنش لاکاز/(بعلاوه)-کاتچین قبلی روی ستون ریخته شد و ابتدا با دو حجم ستون میلیکیواتر [37] شسته شد. سپس ستون با اتانول شسته شد تا زمانی که کسر جمعآوری شده بدون رنگ شود. فقط فراکسیون های اتانول نگهداری، تبخیر و لیوفیلیزه شدند. پودر تا زمان استفاده در -80 درجه نگهداری شد.
3.7. روش خالص سازی کسر دیمری با استفاده از کروماتوگرافی فلش
پودر لیوفیلیزه شده ابتدا با استفاده از یک سیستم کروماتوگرافی فلش puriflash430 مجهز به آشکارساز UV در 280 نانومتر و یک ستون Puriflash diol 50 um f0025 خالص شد. فاز متحرک دوتایی شامل استونیتریل (حلال A) و متانول (حلال B) بود که هر دو با 0.1 درصد TFA اسیدی شده بودند. یک سری تزریق با سرعت جریان ثابت 20 میلی لیتر در دقیقه{7}} با استفاده از گرادیان زیر انجام شد: 100 درصد A به مدت 4.4 دقیقه. 0-10 درصد B در 10 دقیقه؛ 10 درصد B برای 5 دقیقه; 10-90 درصد B در 5 دقیقه؛ 90 درصد B برای 3 دقیقه؛90-10 درصد B در 2 دقیقه؛ 10 درصد B برای 10 دقیقه. حجم تزریق 1 میلی لیتر (300 میلی گرم پودر لیوفیلیزه حل شده در 1 میلی لیتر از حلال A) بود. هر بار سه کسر مجزا جمع آوری شد. مورد اول مربوط به باقیمانده (بعلاوه) - کاتچین بود و سومی مخلوطی از پلی فنل های با وزن مولکولی بالا بود. بخش دوم شسته شده، حاوی مخلوطی از محصولات اکسیداسیون دایمر، تبخیر و قبل از مرحله دوم تصفیه لیوفیلیز شد.
3.8. روش خالص سازی محصولات اکسیداسیون از کسر دیمری با استفاده از یک سیستم کروماتوگرافی نیمه آماده سازی
بخش حاوی محصولات اکسیداسیون دایمر با استفاده از سیستم کروماتوگرافی فشار متوسط نیمه آماده سازی Bio-Rad NGC 10 مجهز به ستون Varian Dynamax C18 Microsorb فاز معکوس (250 × 21.2 میلی متر؛ 3 um) خالص شد. فاز متحرک دوتایی شامل میلیO آب (حلال A) و 80 درصد استونیتریل، 20 درصد میلیکیو آب (حلال B) بود که هر دو با 0.05 درصد TFA اسیدی شده بودند. یک سری از تزریق (300 میکرولیتر) از پودر لیوفیلیزه (20 میلی گرم محلول در 200 میکرولیتر حلال A و 100 میکرولیتر ACN) تحت شرایط شستشوی زیر انجام شد: 100 درصد A به مدت 4 دقیقه. 0-35 درصد B در 46 دقیقه؛35-100 درصد B در 2 دقیقه؛ 100 درصد B برای 5 دقیقه. هشت بخش مجزا در هر بار، مربوط به سیگنال های UPLC خالص در 280 نانومتر جمع آوری شد. هر بخش قبل از تجزیه و تحلیل NMR تبخیر و لیوفیلیز شد.
3.9. آماده سازی نمونه برای آنالیز NMR
حدود 1 میلی گرم از هر پودر لیوفیلیزه وزن شده در لوله های اپندورف در 500 میکرولیتر استون-dg حل شد. سپس، 10 میکرولیتر از محلول غلیظ نیترات کادمیوم در استون-d به نمونه ها اضافه شد و محلول های به دست آمده برای تجزیه و تحلیل NMR به لوله های NMR 5 میلی متری منتقل شدند. یک مرحله اضافی برای برخی از نمونه ها انجام شد: پس از حل شدن پودرهای لیوفیلیزه در استون-dg در حضور آثار کادمیوم، نمونه ها تا خشک شدن تبخیر شدند و سپس بدون افزودن بیشتر کادمیوم در استون-d مجدد حل شدند.
3.10. مشخصات ابزار
تجزیه و تحلیل UPLC-MS. واکنش ها با استفاده از دو سیستم UPLC-MS بررسی شدند. اولین مورد برای شناسایی دقیق زمانهای نگهداری محصولات با استفاده از روش گرادیان طولانی استفاده شد. به عنوان مثال، کروماتوگرافی مایع با عملکرد فوقالعاده معکوس واترز همراه با طیفسنجی جرمی (UHPLC-MS). سیستم کروماتوگرافی مایع یک Acquity UPLC (Waters, Milford, MA, USA) مجهز به آشکارساز آرایه فتودیود بود. ما از ستون Acquity UPLC HSS T3 (1.8 um, 2.1 × 150 mm) استفاده کردیم. دمای ستون 25 درجه بود. فاز متحرک دوتایی شامل 0.1 درصد اسید فرمیک در آب (حلال A) و استونیتریل (حلال B) بود. جداسازی با سرعت جریان ثابت 0.25mL·min-1 با استفاده از گرادیان زیر انجام شد:8-11 درصد B در 2 دقیقه؛ 11 درصد B برای 8 دقیقه. 11-25 درصد B در 15 دقیقه;25-55 درصد Bin 5 دقیقه;55-99 درصد Bin 1 دقیقه;99 درصد B برای 4 دقیقه;99-8 درصد Bin1 دقیقه;8 درصد B به مدت 4 دقیقه حجم تزریق 5 میکرولیتر بود. طیف سنج جرمی یک چهار قطبی ساده یونیزاسیون الکترواسپری QDa Waters Acquity (ESI) بود (واترز، میلفورد، MA، ایالات متحده). ولتاژ مویرگی روی 0.8 کیلو ولت تنظیم شد. طیف جرمی در محدوده جرمی 200-900 حالت یون مثبت نازک به دست آمد.
دومین سیستم UHPLC-MS که برای تأیید سریع در مراحل تصفیه استفاده میشود، همان چیزی است که قبلاً توضیح داده شد، با یک ستون Acquity UHPLC HSS T3 (1.8 میکرومتر، 2.1×100 میلیمتر) گرم شده است. در 38 درجه جداسازی با سرعت جریان ثابت 0.55 میلیلیتر در دقیقه{10}} با استفاده از گرادیان سریع زیر انجام شد: 0.{12}} درصد B در 5 دقیقه. 40-99 درصد B در 2 دقیقه; 99 درصد B برای 1 دقیقه؛ 99-0.1 درصد B در 1 دقیقه. حجم تزریق 2 میکرولیتر بود. طیف سنج جرمی یک تله یونی یونیزاسیون الکترواسپری بروکر آمازون X (ESI) بود (Bruker Daltonics، برمن، آلمان). ولتاژ مویرگی روی -5.5 کیلو ولت تنظیم شد. طیف جرمی در محدوده جرمی 50-2000 حالت یون مثبت نازک به دست آمد.
تمام آنالیزهای UPLC-MS در سه تکرار انجام شد.
ابزار NMR. تمام طیفهای NMR روی یک طیفسنج Agilent DD{{0}} MHz (Agilent Technologies، Santa Clara، CA، USA) ثبت شد که در فرکانسهای 500.05 و 125.74 مگاهرتز برای هستههای پروتون و کربن-13 کار میکند. به ترتیب، با استفاده از یک کاوشگر تشخیص غیرمستقیم 5 میلی متری مجهز به یک سیم پیچ گرادیان. آزمایش های 1D'H و 13C، 2Dhomonuclear1H TOCSY و ROESY، و lH/13C HSQC و HMBC با استفاده از توالی های پالس کلاسیک انجام شد و با استفاده از هر دو سکانس MessJ4N2 و Mess1M. نرم افزار .1 (Mestrelab Research، اسپانیا). اندازه گیری های DOSY همانطور که قبلاً توضیح داده شد 38 بدست آمد و پردازش شد. پارامترهای اکتساب توالی پالس DgcsteSL به شرح زیر بود: زمان تأخیر انتشار و عرض پالس گرادیان به ترتیب 50 میلیثانیه و 2 میلیثانیه تنظیم شد، قدرت گرادیان (g) در 16 مرحله با فاصله g2 برابر از 0.3 به افزایش یافت. 32G·cm-I. پس از تصحیح فاز، طیف دو بعدی DOSY از اندازه گیری ارتفاع پیک با استفاده از نرم افزار VNMRJ4.2 ساخته شد.
همه طیفها به سیگنالهای حلال استون-dg ارجاع داده شدند (سیگنال H باقیمانده در ppm 2.05 و سیگنال 13C در 29.92 ppm).

4. نتیجه گیری
اثر سه اکسیدوردوکتاز مختلف (پلی فنل اکسیداز استخراج شده از انگور، لاکاز از Botrytis cinerea، و لاکاز از Trametes Versicolor) بر روی (بعلاوه) -کاتچین مورد بررسی قرار گرفت و پروفایل های حاصل از LC-UV-MS بسیار مشابه بود، اگرچه برخی تفاوت های جزئی وجود داشت. تفاوت های احتمالی در واکنش پذیری این آنزیم ها را پیشنهاد کرد.
ساختار شش محصول اکسیداسیون کاتچین-لاکاز (با استفاده از لاکاز از Trametes Versicolor) بر اساس امضاهای خاص NMR (چهار محصول خالص، به عنوان مثال، N2، N3، N6، و N8، و N4، مربوط به مخلوطی از NMR) به دست آمد. دو ایزومر). انتساب کامل سیگنالهای OH فنلی به لطف افزودن نیترات کادمیوم با یک روش آمادهسازی نمونه امکانپذیر شد که امکان انتساب بدون ابهام پیوندهای بین واحدهای کاتچین را برای برخی از ترکیبات مورد نظر فراهم کرد. این روش تجزیه و تحلیل NMR مخلوط های پلی فنل را، چه سنتز شده و چه استخراج شده از محصولات طبیعی، بسیار ساده می کند.
استانداردهای به دست آمده در این کار ممکن است در آینده به عنوان نشانگرهای اکسیداسیون برای بررسی حضور و تکامل آنها در طول رسیدن انگور و پیری شراب مورد استفاده قرار گیرند. علاوه بر کاتچین، سایر ترکیبات پلی فنول، از جمله فلاونوئیدها و غیر فلاونوئیدها نیز ممکن است به عنوان بسترهای لاکاز برای به دست آوردن استانداردهای جدید اضافی استفاده شوند.
اختصارات
NMR: تشدید مغناطیسی هسته ای،
سی دی: کادمیوم،
TOCSY: طیف سنجی همبستگی کل،
ROESY: طیفسنجی اثر Overhauser هستهای با چارچوب چرخشی،
HSQC: آزمایش همبستگی تک کوانتومی هترونوکلی،
HMBC: اتصال چند بانده هترونکلئر،
DOSY: طیفسنجی دستوری انتشار.
منابع
1. خان، ن. مختار، اچ. پلی فنول های چای برای ارتقای سلامت. زندگی علمی. 2007، 81، 519-533. [CrossRef]
2. فایول، ن. Vallverdu-Queralt، A.; میدک، ای. Hue, C.; بولانجر، آر. شاینیر، وی. سامرر، ن. خصوصیات مشتقات جدید فلاوون{2}}در دانه های تخمیر شده کاکائو. مواد شیمیایی مواد غذایی 2018، 259، 207–212. [CrossRef] [PubMed]
3. ریمباخ، جی. ملچین، م. مورینگ، جی. واگنر، AE Polyphenols از کاکائو و سلامت عروق - یک بررسی انتقادی. بین المللی جی. مول. علمی 2009، 10، 4290-4309. [CrossRef]
4. Avram, AM; مورین، پ. براون میلر، سی. هوارد، ال آر. سنگوپتا، ا. Wickramasinghe، SR غلظت پلی فنول ها از عصاره تفاله بلوبری با استفاده از نانوفیلتراسیون. Food Bioprod. روند. 2017، 106، 91-101. [CrossRef]
5. آنتونیولی، آ. فونتانا، آر. پیکولی، پی. بوتینی، R. خصوصیات پلی فنول ها و ارزیابی ظرفیت آنتی اکسیدانی در تفاله انگور Cv. مالبک مواد شیمیایی مواد غذایی 2015، 178، 172-178. [CrossRef]
6. Saucier, C. چگونه پلی فنول های شراب در طول پیری شراب تکامل می یابند؟ سرویزیا 2010، 35، 11-15. [CrossRef]
7. اولیویرا، سی ام. فریرا، ACS؛ دی فریتاس، وی. سیلوا، مکانیسم های اکسیداسیون AMS که در شراب ها اتفاق می افتد. مواد غذایی Res. بین المللی 2011، 44، 1115-1126. [CrossRef]
8. Singleton، VL Oxygen با فنل ها و واکنش های مرتبط در بایدها، شراب ها، و سیستم های مدل: مشاهدات و مفاهیم عملی. صبح. J. Enol. ویتیک 1987، 38، 69-77.
9. Mathew, AG; پارپیا، قهوه ای شدن مواد غذایی HAB به عنوان یک واکنش پلی فنل. در پیشرفت در تحقیقات مواد غذایی؛ Chichester، CO، Mrak، EM، Stewart، GF، Eds. مطبوعات دانشگاهی: کمبریج، MA، ایالات متحده آمریکا، 1971; جلد 19، ص 75–145. [CrossRef]
10. گامبوتی، ا. رینالدی، ا. اوگلیانو، ام. Moio، L. تکامل ترکیبات فنلی و قابض در طول پیری شراب قرمز: اثر قرار گرفتن در معرض اکسیژن قبل و بعد از بطری. جی. آگریک. مواد شیمیایی مواد غذایی 2013، 61، 1618-1627. [CrossRef] [PubMed]






