تکامل مولکولی پروتئین باکتری کش/افزایش نفوذپذیری (BPIFA1) تنظیم کننده پاسخ های ایمنی ذاتی در پستانداران قسمت 2
May 29, 2023
3. نتایج
توالی پروتئین BPIFA1 کدگذاری شده در ژنوم پستانداران برای تعیین نقش انتخاب تطبیقی و تکامل مورد مطالعه قرار گرفت. پروتئین BPIFA1 واسطه اصلی سیگنالدهی ذاتی در برابر عفونتهای میکروبی توسط باکتریها و قارچها است. هنگامی که توالی ها با استفاده از MSA ترکیب شدند، از آنها برای ایجاد درختان فیلوژنتیک بیزی و انجام تحقیقات بیشتر استفاده شد. برای شروع آبشارهای سیگنال دهی درون سلولی، فعال کردن مجموعه ای از ژن های شناسایی شده در گونه های پستانداران مناسب و داشتن یک دامنه عملکردی (LBP-BPI) ضروری است. برای سورفکتانت فسفولیپید دی پالمیتوئیل فسفاتیدیل کولین (DPPC)، این دامنه اتصال به چربی دارای درجه انتخابی بسیار بالایی است. سیستم ایمنی ذاتی راه هوایی فوقانی در پاسخ به سیگنالهای ژنتیکی متعدد، مانند افزایش نرخ جایگزینی غیر مترادف، هاپلوتیپهای همولوگ قابل توجه و عدم وجود تنوع ژنتیکی در پروتئینهای BPIFA1 فعال میشود، که نشان میدهد که حضور این پروتئینها به دلیل مثبت بودن مثبت بوده است. انتخاب.
دامنه اتصال لیپید (LBD) یک دامنه ساختاری است که در بسیاری از پروتئین ها وجود دارد، که می تواند برخی از مولکول های لیپیدی خاص را برای تنظیم عملکرد یا محلی سازی پروتئین ها متصل کند.
چندین مطالعه نشان داده اند که دامنه های اتصال به لیپید می توانند بر ایمنی تأثیر بگذارند. به عنوان مثال، در برخی از اندامهای لنفاوی ثانویه مانند طحال و غدد لنفاوی، یک مولکول چربی به نام S1P (اسفنگولیپید-1-فسفات) مهاجرت و مهاجرت سلولهای T و سلولهای B را با تعامل با حوزههای اتصال به چربی تنظیم میکند. حفظ. علاوه بر این، برخی از گیرندههای مهم سطح سلولهای ایمنی مانند TLR4، TLR7، و TLR8 نیز حاوی حوزههای اتصال به چربی هستند که میتوانند انواع مختلفی از مولکولهای لیپیدی را متصل کرده و فعال شدن و پاسخ سلولهای ایمنی را تنظیم کنند.
بنابراین، رابطه مشخصی بین حوزههای اتصال به لیپید و ایمنی وجود دارد که ایدههای جدیدی را برای مطالعه تنظیم پاسخهای ایمنی توسط حوزههای اتصال به چربی ارائه میدهد. مشاهده می شود که ما باید ایمنی خود را برای مقاومت در برابر ویروس ها تقویت کنیم. سیستانچ می تواند به طور قابل توجهی ایمنی را بهبود بخشد. سیستانچ همچنین دارای اثرات ضد ویروسی و ضد سرطانی است که می تواند توانایی سیستم ایمنی را برای مبارزه و بهبود ایمنی بدن تقویت کند.

روی فواید سلامتی سیستانچ کلیک کنید
3.1. تکامل مولکولی ژن BPIFA1
در این کار، ما برای نشانههای سازگاری در ژن BPIFA1، از سیگنالهای انتخاب تدریجی ضعیف تا قوی در طول تکامل تطبیقی در ژنوم پستانداران، جستجو کردیم. درصد معمولی کدونها در ژن BPIFA1 که تحت تکامل تطبیقی قرار میگیرند، تعیین شد. با پیروی از همان رویه برای هر دنباله کدگذاری، میانگین نسبت کدون های انتخاب شده مثبت را در همه شاخه ها محاسبه کردیم. با استفاده از تغییرات نرخ BUSTED و مترادف در شاخههای آزمایشی با دقت انتخاب شده فیلوژنی BPIFA1، ما ردپایی از انتخاب تنوعبخش اپیزودیک در سطح ژن را تعیین کردیم. در نتیجه، به این نتیجه رسیدیم که انتخاب واگرا در امتداد سه خط فرود مورد بررسی قرار گرفته است. با استفاده از تنوع نرخ مترادف، ما انتخاب تنوع بخشی اپیزودیک در سطح ژن را در شاخههای آزمایشی فیلوژنی BPIFA1 مشاهده کردیم. برای دستیابی به این هدف از یک انتخاب متنوع اپیزودیک در سطح ژن استفاده شد. دو شاخه آزمایش شواهدی از تنوع بخشیدن به انتخاب را نشان دادند که نشان میدهد سایت در معرض این نوع تکامل قرار گرفته است (شکل 1).
میانگین نسبتهای dN/dS برای BPIFA1 در تمام سایتها و دودمانها بیشتر از یک بود. در نتیجه تحقیقاتی بر روی این پروتئین برای شناسایی نشانه های انتخاب مثبت انجام شد. مشخص شد که پروتئین دارای ساختار حفاظت شده اسیدهای آمینه است که امکان خالص سازی را فراهم می کند و دارای ارزش امگا بیشتر از 1 است. یک آزمایش احتمال ورود به سیستم بر روی این پروتئین انجام شد، همه مکان های آن مورد تجزیه و تحلیل قرار گرفتند و نرخ تعویض محاسبه شد. برای ارزیابی اینکه آیا انتخاب مثبت رخ داده است یا خیر، از سه مجموعه مختلف از مدلهای احتمال استفاده کردیم: M0 در مقابل M3، M1 در مقابل M2، و M7 در مقابل M8. برآورد پارامترهای تحت M1 و M2 مقایسه شد و مشخص شد که مقدار M2 برای این پروتئین ها مثبت است. درصد سایتهای انتخاب شده مثبت برای سه مدل با مقادیر 422، 64.5 و 93.63 به ترتیب معنیدار بود (جدول 1).

برای ارائه شواهد اضافی برای حمایت از یافتههای انتخاب مثبت، ما مدل ترکیب مکانیکی-تجربی را با استفاده از سرور انتخاب در سایتهای خاص اعمال کردیم. در طی این فرآیند، ما متوجه شدیم که چندین مکان در نقاط مختلف در طول تکامل تحت فشار انتخابی قرار گرفتهاند (شکل 1). به همین دلیل، میتوانیم میزان حفظ تکاملی این ژن را تخمین بزنیم. ما دریافتیم که اکثریت قریب به اتفاق سایتهای انتخاب شده مثبت در سرتاسر کلادهای پستانداران حفظ شدهاند. این به این دلیل بود که آمینو اسیدهای حفظ شده بیشتر سیگنال های مورد استفاده برای انتخاب مثبت در الگوریتم شبکه عصبی را به خود اختصاص دادند (جدول 2).

روش انتخاب مدل کدون 9113 مدل مختلف را ارزیابی کرد. بهترین مدل (log(L)=−18,910, mBIC=39,340.92) دارای سه نرخ بود و دقیقترین بود. با این مدل، بهبودهای 218.66 log(L) و 398.33 mBIC امتیاز در مقایسه با یک مدل نرخ واحد به دست آمد، که در آن همه جانشینیهای غیر مترادف با همان سرعت اتفاق افتادند، همانطور که در جدول 1 نشان داده شده است. هر مدل در مجموعه معتبر دارای نسبت شواهد حداقل 0.01 در مقایسه با بهترین مدل، به این معنی که در 9.21 واحد mBIC بهترین مدل قرار داشت، یا به طور معادل، نسبت شواهد حداقل 0.01 در مقایسه با بهترین مدل داشت. میانگینگیری مدل، نرخ تغییر را در این مجموعه از مدلها تخمین زد (شکل 2). الگوی انتخاب تکاملی در موقعیتهای اسید آمینه در پروتئین BPIFA1 نیز با استفاده از تحلیل انتخاب مدل کدون ارزیابی شد، که نشان داد جایگزینی محلهای اسید آمینه در طول تکامل تطبیقی در پروتئینها رخ داده است. ما نشان دادیم که موقعیتهای اسید آمینه پایه پروتئینها به دلیل نسبتهای جایگزینی متفاوت، تکامل تطبیقی را نشان میدهند. بر اساس توزیع محل های اسید آمینه در BPIFA1، حداکثر نرخ جایگزینی تقریباً 1.19 و کمترین آن 14.1 بود (شکل 2).


شناسایی نواحی مهم فیزیولوژیکی پروتئین را می توان با تقابل فراوانی تعویض های مترادف (Ks) و غیر مترادف (Ka) در پروتئین انجام داد. این مبنایی را برای نتیجه گیری وجود انتخاب خالص و انتخاب داروینی مثبت موضعی فراهم می کند. ما از Selecton نسخه 2.2 (قابل دسترسی در http://selection-bio info-tau.ac.il، در 29 سپتامبر 2021) استفاده کردیم، یک وب سرور که به طور خودکار نسبت Ka به Ks (u) را در هر سایت در پروتئین رنگهای مختلف نشاندهنده انواع مختلف انتخاب (انتخاب مثبت، انتخاب خالصکننده و عدم انتخاب) هستند و برای نمایش گرافیکی این نسبت در هر سایت استفاده میشوند. مدل انتخاب مجموعه ای از فرضیه های مختلف تکاملی است که می تواند برای آزمایش آماری احتمال اینکه یک پروتئین معین در معرض انتخاب مثبت قرار گرفته است مورد استفاده قرار گیرد. از طریق یک رابط کاربری گرافیکی عمل می کند. مدل مکانیکی-تجربی اخیراً ایجاد شده بر خواص فیزیکی اسید آمینه تأثیر گذاشته است (جدول 3).

3.2. انتخاب تطبیقی ژن BPIFA1
برای تعیین میزان سازگاری گونههای مختلف پستانداران با محیطهایشان، از همترازیهای متعددی از توالیهای کدکننده ژن BPIFA1 از هر یک از ۳۴ گونه استفاده کردیم. این تست ها را می توان به صورت جداگانه یا ترکیبی انجام داد. رایج ترین انواع آزمون ها به عنوان آزمون شاخه ای شناخته می شود. در طول تکامل گونههای مهرهداران، انتخاب دودمانهای خاص برای تشخیص دودمانهای متمایز تحت فشار انتخاب مورد استفاده قرار گرفت. احتمال انتخاب خاص دودمان برای هر گروه فیلوژنتیکی با استفاده از مدل احتمال اثرات تصادفی شاخه-محل تطبیقی (aBS-REL) محاسبه شد. علاوه بر این، از تکنیک aBS-REL برای تشریح هر ژن استفاده شد تا مشخص شود کدام دودمان در زمانهای مختلف تاریخ تکامل در معرض انتخاب تطبیقی قرار گرفتهاند.
هنگامی که برای دودمان پستانداران اعمال شد، مدل aBS-REL تأیید کرد که ژنهای پیشبینیشده BUSTED تحت انتخاب مثبت بودند. نتایج ما، که نشان میدهد فشار انتخابی بر روی ژنهای BPIFA1 در دودمان پستانداران اثر میگذارد، نشان داد که این دو فرضیه مطابقت دارند (جدول 4). در فیلوژنی ژن BPIFA1، شواهدی مبنی بر انتخاب تنوع اپیزودیک در هشت شاخه وجود داشت. اهمیت یافتهها با استفاده از آزمون نسبت درستنمایی (p > 0.{10}}5) ارزیابی شد که پس از بررسی نتایج بسیاری از آزمونهای دیگر انجام شد (شکل 3). در مجموع، 63 خط مجزا از طریق این آزمون خاص برای تنوع بخشیدن به انتخاب قرار گرفتند. آزمونهای چندگانه انجام شد و اهمیت یافتهها با استفاده از آزمون نسبت درستنمایی با آستانه p-value 05/0 مشخص شد.

این جدول یک خلاصه آماری از تناسب مدل ها با داده ها را گزارش می دهد. Baseline MG94xREV به مدل پایه MG94xREV اشاره دارد که یک دسته نرخ ω را در هر شاخه استنباط می کند. مدل تطبیقی کامل به مدل تطبیقی aBS-REL اشاره دارد که بر تعداد بهینهشدهای از دستههای نرخ ω در هر شاخه دلالت دارد.
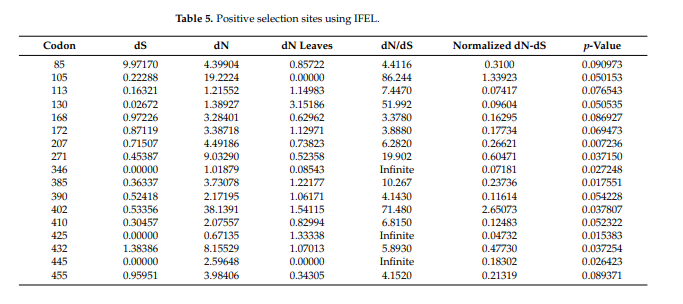
در طول فرآیند تکاملی، ما مقادیر امگا را با استفاده از روشهای SLAC، FUBAR، MEME و FEL برای یافتن نشانههای انتخاب مثبت بررسی کردیم (جدول 5). بر اساس یافته های ما، ژن BPIFA1 در کلادهای پستانداران در معرض انتخاب تکاملی مثبت قرار گرفته است. ما توانستیم با استفاده از روش بیزی تشخیص دهیم که کدام مناطق ژنوم تحت فشار انتخابی قرار می گیرند. این تکنیک شامل تعیین احتمال خلفی برای هر کدون است. سایتهایی با تعداد احتمالات بیشتر به احتمال زیاد تحت انتخاب متنوعی قرار گرفتهاند، که منجر به نرخهای بالاتر جایگزینی غیر مترادف و مترادف نسبت به سایتهایی با تعداد احتمالات کمتر میشود (جدول 2). با استفاده از تجزیه و تحلیل BEB، ما متوجه شدیم که چندین مکان در سراسر دامنه LBP-BPI پروتئین باکتری کش در معرض انتخاب مثبت با احتمال بالای 95 درصد قرار گرفته است. این مورد برای همه سایت ها بود. سایت ها در سراسر دامنه در مکان های مختلف پراکنده شدند. یافته های PAML با استفاده از مجموعه داده موجود در سرور انتخاب مورد بررسی قرار گرفت. این سرور قادر به شناسایی انتخاب تطبیقی در مکانهای خاصی در پروتئین بود که به ما اجازه داد وجود انتخاب مثبت را تأیید کنیم. برای تعیین نرخ جایگزینی، از مدل MEC استفاده شد. یافته ها نشان داد که انتخاب تطبیقی در چندین مکان در BPIFA1 رخ داده است (جدول 5).

3.3. تجزیه و تحلیل نوترکیبی
برای ژن BPIFA1، تجزیه و تحلیل نوترکیبی برای یافتن پیوندهای تکاملی بالقوه بین ژن ها انجام شد. این تحقیق سه رویداد نوترکیبی را نشان داد. هر یک از توالی های نوترکیبی، از جمله والدین اصلی و فرعی، از ژن BPIFA1 می آیند. ما نقاط شکست نوترکیبی را با استفاده از تجزیه و تحلیل GARD شناسایی کردیم. با سرعت 3{9}}.30 مدل در ثانیه، GARD 5120 مدل را بازرسی کرد. فضای جستجوی 72874879 مدل با حداکثر سه نقطه شکست توسط 759 نقطه شکست احتمالی تراز ایجاد شد که الگوریتم ژنتیک تنها 0.01 درصد از آنها را بررسی کرد. با نسبت شواهد 100 یا بالاتر، مدل چند درختی به مدل تک درختی ترجیح داده شد، که نشان می دهد حداقل یکی از نقاط شکست منعکس کننده ناهماهنگی توپولوژیکی است. این با مقایسه نمرات AICc بهترین مدل GARD، که توپولوژی های متغیر را در سراسر بخش ها مجاز می کرد (37,996.2) و مدلی که درخت یکسان را برای همه پارتیشن های تعیین شده توسط GARD فرض می کرد، اما طول شاخه های مختلف را مجاز می کرد، تأیید شد. بین پارتیشن ها به طور خاص، امتیاز AICc بهترین مدل GARD 37996.2 بود، در حالی که امتیاز AICc مدل 37996.2 بود. (شکل 4 و 5).

3.4. برهمکنش های پروتئین-پروتئین و تجزیه و تحلیل اتصال لیگاند
ما از پایگاه داده STRING برای جستجوی پروتئین های بیان شده با BPIFA1 استفاده کردیم و چندین جفت تعامل پروتئین-پروتئین را شناسایی کردیم. 13 گره و 35 لبه وجود داشت که با پروتئین بیان شده با BPIFA1 نشان داده شد. لبه های نمودار PPI شبکه های خطی هستند که گره های جداگانه را به هم پیوند می دهند (شکل 6). میانگین مقدار ضریب خوشه بندی محلی 0.978 بود. غنیسازی PPI دارای مقدار p 5.25 × 10-12 بود. شبکه PPI نشان دهنده برهمکنش های ژن BPIFA1 با سایر ژن های ایمنی بیان شده است. COX7B2، BPIFB6، BPIFB4، BPIFB2، BPIFB3، PLTP، CETP، BPI، LBP، و ODF2L 10 ژن درگیر در شبکه PPI BPIFA1 بودند (شکل 6).

ژنهای BPIFB6، BPIFB4، BPIFB2 و BPIFB3 مهمترین ژنها بودند زیرا در مسیرهای سیگنالدهی بیولوژیکی نقش دارند که نقش اساسی در ایمنی ذاتی در برابر عفونت باکتریایی دارند. علاوه بر این، این ژن ها توسط BPIFA1 تنظیم مثبت می شوند، که دلیل دیگری است که آنها بسیار مهم در نظر گرفته می شوند (جدول 6). مسیرهای مولکولی در ریشه کن کردن میکروب های مهاجم از طریق فعالیت مختل کننده غشاء که از تمام پروتئین های مرتبط با نقش های متنوع تشکیل شده است، ضروری هستند. فعالیت مختل کننده غشاء برای از بین بردن میکروب های مهاجم ضروری بود. دو پروتئین مهم در میانجیگری سیگنالها در پاسخ به لیپوپلیساکاریدها عبارتند از پروتئین باند شونده LPS (LPSBP) و پروتئین افزایشدهنده نفوذپذیری باکتریکشی (BPI). آنها تمایل زیادی به لیپید A، مادهای که در LPS یافت میشود، نشان دادند و بهطور چشمگیری شبیه یکدیگر بودند. علیرغم داشتن ساختارهای مشابه، LBP و BPI عملکردهای بیولوژیکی مختلفی را انجام می دهند که به طور مشخص با یکدیگر متفاوت هستند. به عنوان مثال، LBP اغلب به LPS متصل می شود و ارائه LPS به سلول های CD14 پلاس، مانند ماکروفاژها و مونوسیت ها را بسیار تسهیل می کند، در حالی که BPI فعالیت زیستی LPS را مهار و کاهش می دهد. این دو پروتئین هر دو در باکتری ها وجود دارند.

لیگاندها اجزای حیاتی در فرآیند کنترل بیان و فعالیت پروتئین ها هستند. نیروهای اتصال بین مولکولی، مانند پیوندهای یونی، پیوندهای هیدروژنی، برهمکنش آبگریز و نیروهای واندر-والس، در فرآیند اتصال لیگاند نقش دارند. به دلیل تعامل بین لیگاندها و پروتئین ها، ساختار سه بعدی پروتئین تغییر خواهد کرد. به دلیل این تغییرات در وضعیت ساختاری پروتئین، برخی از عملکردهای پروتئین ممکن است مهار یا فعال شوند. بنابراین، ما یک مطالعه برهمکنش اتصال پروتئین-لیگاند را با استفاده از ویژگیهای فیزیکوشیمیایی اسید آمینه انجام دادیم تا مشخص کنیم کدام باقیماندهها با لیگاند تعامل دارند و کدام نه. برای انجام این کار، ما از یک وبسایت (http://crdd.osdd.net/raghava/lpicom، دسترسی به 18 اکتبر 2021) استفاده کردیم که کسری از باقیماندههایی را که با لیگاند معین تعامل میکنند محاسبه میکند. باقیمانده های کلیدی مانند سیستئین، گلیسین، آلانین، لیزین، اسید آسپارتیک، هیستیدین، لوسین، والین آرژنین، تریپتوفان، سرین، ترئونین و تیروزین با هفت لیگاند (1BP1، BPH، XE، NEH، CLA، CU و MG) و PC1. در مقایسه با برهمکنش با PC1، اسیدهای آمینه باردار، به ویژه اسیدهای آمینه ضروری، مزیت بیشتری در تعامل با 1BP1، BPH، XE، NEH، CLA، CU و MG داشتند (شکل 7). اسیدهای آمینه کوچک و قطبی که با آنها در ارتباط بودند در هر یک از سه لیگاند مشخص شدند.
ما از دو رویکرد متمایز برای پیشبینی در مورد مکانهای اتصال مکمل استفاده کردیم: اولی بر اساس مقایسه زیرساختهای اتصال خاص (TM-SITE) بود، در حالی که دومی بر اساس همترازی پروفایلهای توالی (S-SITE) بود. این تکنیک ها پروتئین BPIFA1 را در برابر 500 پروتئین غیر زائد که با 814 ترکیب یونی آلی، مصنوعی و فلزی ترکیب شده بودند، ارزیابی کردند. با شروع پیشبینی ساختارهای پروتئینی با وضوح پایین، رویکردها با موفقیت بقایای اتصال BPIFA1 را شناسایی کردند و به میانگین ضریب همبستگی متیوز (MCC) دست یافتند که بسیار بالاتر بود. بهعلاوه، این تکنیکها لیگاندهایی را که با باقیماندهها متصل میشوند، کشف کردند (جدول 7).


4. بحث
پسزمینههای ناهمگن پلتفرمهایی را ارائه میدهند که در آن جمعیتهایی که تحت انتخاب متفاوت قرار میگیرند را میتوان به زیرجمعیتهای سازگار بومی متمایز کرد [44]. تأثیر انتخاب بر جریان ژن در بین جمعیت ها، مانند تعادل مهاجرت-انتخاب، امکان سازگاری ذاتی و واگرایی مداوم را تعیین می کند. این همچنین به عنوان تعادل انتخاب مهاجرت شناخته می شود. تمایلی برای تنوع ژنتیکی محلی در جمعیت ها وجود دارد که به دلیل جریان ژنی زمانی که تأثیر انتخاب کمتر از تأثیر جریان ژن است، همگن شود. در عوض، اگر فشار انتخابی بیشتر از نیروی یکپارچه جریان ژن باشد، واریانتهای ژنتیکی ممکن است در مکانهای خاص مستعد انتخاب واگرای قدرتمند تجمع یافته و حفظ شوند [45].
در نتیجه جایگزین احتمالی، مزایای جریان ژن با انتخاب در برابر مهاجرانی که تناسب ژنتیکی ضعیفی دارند، محدود میشود، که همچنین راه را برای سازگاری محلی هموار میکند [45،46]. برای درک تفاوت های جمعیت در فرکانس جریان ژن، باید بین جریان ژن و انتخاب ارتباط وجود داشته باشد [46]. در چنین شرایطی، انتخاب تعیین می کند که آیا جمعیت به عنوان یک گروه متمایز به تکامل یا واگرایی ادامه می دهد. رویکرد تجربی بیز، LRT را در هر سایت شعبه محاسبه کرد و تمام سایتهای مختلف را که در آن انتخاب متنوع ممکن است رخ دهد، قرار داد. بر اساس رویکرد تجربی بیز، تقریب بیزی سریع و بدون محدودیت، که به عنوان FUBAR نیز شناخته می شود، برای تعیین محل انتخاب متنوعی که در ژن BPIFA1 رخ می دهد، استفاده شد. FUBAR امکان پراکندگی مکان به مکان و شاخه به شاخه کدون ها را فراهم کرد و برای کشف تکامل تطبیقی که در سطح ژن رخ داد استفاده شد. روش MEME برای بررسی تکامل تطبیقی که در سطح ژن رخ داده است مورد استفاده قرار گرفت [25،32،47]. سایتهای کدگذاری متنوع اپیزودیک توسط SLAC با مقدار p کمتر از 0.01 پیدا شد (جدول 1).
این مدل برای تخمین نرخ جایگزینی مترادف و غیر مترادف مورد استفاده قرار گرفت و سایتهای کدگذاری با نرخ جایگزینی مترادف بیشتر یا برابر با نرخ غیرمترادف برای شناسایی سایتهایی که در حال انتخاب متنوع بودند، قابل توجه در نظر گرفته شدند. در MEME، برآوردهای حداکثر احتمال برای کدون های 130، 167، 168، 190، 243، 265 و 289 ژن BPIFA1 به دست آمد (جدول 2). بر اساس سیگنال های غیر قابل توجه آنها، این کدون ها به عنوان مکان های انتخاب شده مثبت شناسایی نشدند، که به دلیل ویژگی اپیزودیک انتخاب طبیعی است. انتخاب طبیعی که بهطور پراکنده در طول فواصل کوتاه تکامل تطبیقی انجام میشد، با وقوع مکرر انتخاب طبیعی یا خالصکننده پوشانده شد. در نتیجه، علائم تکامل تطبیقی را نمی توان از طریق تست حساسیت و انتخاب مثبت یافت [48].
ما هفده سایت را پیدا کردیم که با استفاده از روش PAML به طور مطلوب انتخاب شدند، پانزده سایت با استفاده از الگوریتم IFEL و چهار سایت با استفاده از الگوریتم FEL انتخاب شدند. فشار انتخاب تطبیقی بر روی توالی کدون ژن BPIFA1 با استفاده از مدل MEC محاسبه شد. این منجر به شناسایی هفتاد و چهار اسید آمینه شد (شکل 1). یک مدل تکامل مبتنی بر انتخاب مثبت استفاده شد که تفاوتها را در سطح کدون (M8) آشکار کرد. برنامه MrBayes در سرور Selection از یک مدل MCMC برای تعیین تفاوتهای ژن MAVS در پستانداران در سطح کدون استفاده کرد [49].
بر اساس نتایج همراستایی پروتئین MAFFT، مطالعات قبلی نشان داده اند که دامنه Ig در توالی های کد کننده MAVS باقی می ماند. این نتایج نشان میدهد که سوئیچهای پروتئین جایگزین در خالصسازی نواحی انتخابشده مضر هستند و بنابراین بعید به نظر میرسد که در طول تکامل حفظ شوند [50،51]. مکانهای مسیرهای تکاملی متعدد با استفاده از توزیع نرخ چند پارامتری، یک مدل اثر تصادفی با فاصله اطمینان 95 درصد و مقادیر قابلتوجه Pr [>] شناسایی شدند. سپس به لطف این روش، سایت ها می توانند مکان یابی شوند (جدول 3). در مورد انتخاب مثبت، وزن نرخ کلاس با استفاده از توزیع گسسته عمومی دو متغیره برای هر سایت کدگذاری تعیین شد. همگرایی مدل MCMC با این واقعیت نشان داده شد که میانگین تخمینهای پسین برای BPIFA1 نزدیکتر به مقدار عامل کاهش در نظر گرفته شده است (جدول 2).
این مقادیر از {{0}}.95 تا 0.99 متغیر بودند. در طول فرآیند تنوع بخشیدن به انتخاب، تنها مکان های کدگذاری با مقادیر تجربی بیز (EBF) بیش از 50 در نظر گرفته شد. محاسبات با استفاده از حجم نمونه موثر خالص برای تعیین مقادیر EBF برای هر سایت کدگذاری ارزیابی شده با استفاده از انتخاب مثبت انجام شد. استنباط توزیع پارامترهای انتخاب خاص ژن می تواند انتخاب های شناسایی شده را در تعداد زیادی از سایت های کدگذاری بهبود بخشد. مناطق کدگذاری که به طور مثبت انتخاب و شناسایی شدند، شواهد قابل توجهی از تنوع بخشیدن به انتخاب در ژنهای BPIFA1 ارائه میدهند که اکنون در حال گذراندن دودمان انتخابی هستند. در نتیجه، برخی از جهشهایی که در ابتدا خنثی به نظر میرسند (و هیچ تأثیر فوری بر تناسب اندام ندارند) میتوانند «مجاز» باشند و به پروتئین اجازه میدهند تا تغییرات بعدی را که در غیر این صورت مضر بوده و باعث تفاوتهای فنوتیپی میشوند، مقاومت کند [52]. جهشهای خنثی در اپیستاز پایهای را برای انتخاب و سازگاری بعدی میگذارد، که اخیراً توجه زیادی را به خود جلب کرده و به عنوان راهی برای آشتی دادن مدلهای خنثی و انتخابی تکامل ارائه شده است [53].
نرخ تعویض برای جفت FWY و HKR تقریبا 50 درصد بود، نرخ تعویض برای DENQ 50 درصد و نرخ تعویض برای ACGILMPSTV 90 درصد بود. شبکه PPI نشاندهنده تعاملات پروتئین BPIFA1 با سایر پروتئینهای ایمنی بیانشده است. COX7B2، BPIFB6، BPIFB4، BPIFB2، BPIFB3، PLTP، CETP، BPI، LBP، و ODF2L ده ژنی بودند که ما تعیین کردیم که مسئول این برهمکنش های پروتئینی هستند (شکل 6). ژنهای BPIFB6، BPIFB4، BPIFB2 و BPIFB3 مهمترین ژنها هستند زیرا در مسیرهای سیگنالدهی بیولوژیکی نقش دارند که نقش اساسی در ایمنی ذاتی در برابر عفونت باکتریایی دارند. علاوه بر این، این ژنها توسط BPIFA1 تنظیم میشوند و دلیل دیگری برای اهمیت آنها ارائه میکند (جدول 6). رابطها شامل خوشههایی از باقیماندههای حفاظتشده با ترکیب اسید آمینه سازگار با هسته مشترک (باقیماندههایی با بیشترین تغییر در دفن پس از اتصال) و یک منطقه حفاظتشده [54] هستند، و مناطق داغی که از خوشهبندی نقاط داغ به وجود میآیند مطابق با بستهبندی محکم هستند. و مناطق حفاظت شده
بنابراین، رابط ها تحت فشار تکاملی هستند تا اتصالات جاری را حفظ کنند و در عین حال از تعاملات نامطلوب و غیر اختصاصی جلوگیری کنند. برخی از ویژگیهای فیزیکوشیمیایی را میتوان تغییر داد تا احتمال اینکه رابطهای پروتئین-پروتئین ممکن است برهمکنشهای ناکارآمد ایجاد کنند [55] کاهش یابد. در نتیجه بررسی ما، متوجه شدیم که مقادیر برای کدون های انتخاب شده مثبت ارائه شده در جدول 1 بیش از 1 است. این نشان می دهد که توسعه سایت های مترادف به زمان بیشتری نسبت به توسعه سایت های غیر مترادف (سایت های dN) نیاز دارد. این تأثیر مفید انتخاب داروینی، که تغییرات جدید و چندشکلی آللی بیشتر را تشویق میکند، بهعنوان متعادلکننده یا تصفیهکننده انتخاب عمل میکند [56] که باعث تغییر در پروتئین ساختاری میشود و بر مسیر سیگنالینگ تأثیر میگذارد [57]. حتی اگر آنها از یک اصل و نسب منشا می گیرند، جایگزینی اسید آمینه در فرزندان گونه های مختلف ممکن است پیامدهای بسیار متفاوتی داشته باشد [56،57]. این در تضاد با این واقعیت است که شجره نامه آنها با ارسال های قبلی مطابقت دارد. ژنهای BPIFA1 انتخاب شده در این مطالعه اطلاعاتی را برای تجزیه و تحلیل زیستی فراهم میکنند که هدف آن انتخاب ژنها بر اساس مقیاس زمانی تکاملی از دورههای اخیر تا طولانیمدت است.
علاوه بر این، مکانیسم تکاملی اساسی که در نتیجه تحقیقات اخیر کشف شده است ممکن است به دلیل عدم وجود ویژگیهای ساختاری و عملکردی تعداد زیادی از پروتئینها در ژنوم ناکافی باشد. تکامل و انطباق ژنهای کدکننده پروتئین در مگس سرکه به طور کامل مورد بررسی قرار گرفت تا مرتبطترین عوامل تعیینکننده تکامل و سازگاری در سطح ژنهای کدکننده پروتئین مشخص شود. این با مقایسه D. melanogaster با گونه های نزدیک و جمعیت آنها انجام شد. برنامه های کاربردی در مقیاس بزرگ بیوانفورماتیک و تجزیه و تحلیل ساختاری توسط تیم ما برای تعیین ویژگی های ساختاری و عملکردی پروتئین ها انجام شد. متعاقبا، با استفاده از سیستم طبقه بندی خود، باقیمانده ها را به انواع سایت های ساختاری و عملکردی تقسیم کردیم. سرعت تکامل و انطباق توالی در بین پروتئینها و مکانهای مختلف مقایسه شد که شناسایی نقاط داغ سازگاری را در کل ژنوم ممکن کرد. علاوه بر این، نشان داده شده است که پروتئینهای تطبیقی سریع با سرعتهایی بالاتر از آنچه که بهطور تصادفی پیشبینی میشود، با یکدیگر تعامل دارند. این کشف نشان میدهد که همانطباق احتمالاً در بین پروتئینهای تطبیقی سریع وجود دارد.
در نتیجه اتصالات فیزیکی آنها، موارد زیر نمونههایی از مکانیسمهایی هستند که پتانسیل مشارکت در سازگاری را دارند: (1) پروتئینهای تطبیقی سریع اغلب در فعالیتهای شیمیایی مشابه غنی میشوند و در معرض فشار انتخاب مشابه قرار میگیرند، و (2) ) پروتئین های سریع تطبیقی همزمان تکامل می یابند. دو نمونه متفاوت از تکامل تطبیقی در PPIها در این تحقیق نشان داده شد، که نویسندگان را به این فرضیه سوق داد که این فعل و انفعالات فیزیکی ممکن است نقشی در سازگاری پروتئینهای تطبیقی سریع در D. melanogaster داشته باشند. علاوه بر این، ما نشان دادیم که پدیده همانطباق ممکن است در یک مفهوم کلیتر از فقط بین پروتئینهای تطبیقی سریع رخ دهد. سرعت انطباق معمولاً در پروتئین هایی که با پروتئین های تطبیقی سریع در تعامل هستند بیشتر است. با توجه به اینکه فعل و انفعالات مولکولی در تکامل تطبیقی نقش دارند، منصفانه است که پیش بینی کنیم که این برهمکنش ها ممکن است بر هم انطباق در سطح جهانی تر نیز حاکم باشد. فرض شده است که تکامل همزمان تماسهای فیزیکی مکانیسمی است که مسئول نرخهای تکاملی مشابه مشاهدهشده در پروتئینهای متقابل است.

5. نتیجه گیری ها
هدف ما شناسایی فشارهای انتخابی بود که به توسعه سیستم BPIFA1 گیاه و پستانداران کمک کرده است، که بیان آن در طیف گسترده ای از بیماری ها تعدیل می شود. پروتئین BPIFA1 به سرعت در پاسخ به فشار انتخابی در اصل و نسب انسان تکامل یافت و ما توانستیم عوامل تعیین کننده انتخاب ژنتیکی را که عامل فعالیت باکتری کشی آن هستند مشخص کنیم. در طول تاریخچه تکاملی خود، انتخاب مثبت ممکن است نقش مهمی در بهبود پاسخ حدت به محرک های مختلف داشته باشد، که می تواند تنوع مشاهده شده در ثبات عملکرد ژن را توضیح دهد. یافتههای ما درک جامعتری از تاریخچه تکاملی ژنهای BPIFA1 ارائه میدهد که تجزیه و تحلیل ژنومیک عملکردی بیماریزایی در فرآیندهای بیولوژیکی را افزایش میدهد. پیشبینی میشود که این یافتهها ممکن است به بهبود درک پیشگیری از بیماری نیز کمک کند. علاوه بر این، مطالعه این ژن ها ممکن است طراحی یک روش منحصر به فرد را تسهیل کند که می تواند به تعیین پروتئین های حدت مختلف موجود در پاتوژن های باکتریایی کمک کند. یافتههای ما ما را به این فرضیه سوق میدهد که محدودیتها در طول فرآیند تکاملی نقش کلیدی در شکلدهی اکتشافات ما داشتهاند. در نتیجه این محدودیتها، زمانی که ویژگیهایی مانند طول پروتئین را با کمپلکسهای پیچیده جفت کردیم، توانستیم برخی از مرزهای عددی را شناسایی کنیم. ویژگیهای منحصربهفرد پروتئینها جالب است زیرا ممکن است نشانهای از عوامل استرسزای غیرمعمول یا تنظیمات هموستاتیکی باشد که حضور آنها را در سلولها ممکن کرده است. بنابراین، آنها یک انتخاب امیدوارکننده برای تحقیقات بیشتر هستند.
مشارکت نویسنده:
مفهوم سازی، HIA، و JC. روش، HIA، MAK، FAK، SI، RWA و NSP. نرم افزار، HIA، WN، NSP، RWA، و SI. اعتبارسنجی، MAK، JC، FAK، و HIA. تجزیه و تحلیل رسمی، HIA، MAK، FAK، SI، RWA، و NSP. تحقیقات، HIA، MAK، FAK، SI، RWA، و NSP. منابع، HIA، MAK و JC. مدیریت داده، HIA، MAK، FAK، SI، RWA، و WN. نوشتن - آماده سازی پیش نویس اصلی، HIA; نوشتن - بررسی و ویرایش، HIA، SI، RWA، WN و NSP. تجسم، JC و MAK. نظارت، MAK، FAK، NSP، و WN همه نویسندگان نسخه منتشر شده نسخه خطی را خوانده و با آن موافقت کرده اند.
منابع مالی:
این تحقیق هیچ بودجه خارجی دریافت نکرد.
بیانیه هیئت بررسی نهادی:
قابل اجرا نیست.
بیانیه رضایت آگاهانه:
قابل اجرا نیست.
بیانیه در دسترس بودن داده ها:
تمام داده های مربوط به این مقاله باید به طور آشکار در دسترس خوانندگان باشد.
قدردانی ها:
این مطالعه توسط پروژه ویژه مالی استان گوانگدونگ در سال 2022 برای ساخت و ساز جنگلداری اکولوژیکی پشتیبانی شد.
تضاد علاقه:
نویسندگان هیچ تضاد منافع را اعلام نمی کنند.
منابع
1. لی، جی. خو، پی. وانگ، ال. فنگ، ام. چن، دی. یو، ایکس. Lu, Y. بیولوژی مولکولی BPIFB1 و پیشرفت های آن در بیماری. ان ترجمه پزشکی 2020, 8, 651. [CrossRef] [PubMed] 2. Saferali, A.; تانگ، AC؛ Strug، LJ; Quon، BS; زلوسنیک، جی. سندفورد، ای جی. بررسی، عملکرد تعدیل کننده ایمنی ژن BPIFA1 اصلاح کننده فیبروز کیستیک. PLoS ONE 2020, 15, e0227067. [CrossRef] [PubMed]
3. نام، ب.-ح. ماه، J.-Y. پارک، ای.-اچ. کیم، Y.-O. کیم، دی.-جی. کنگ، اچ جی. کیم، دبلیو-جی. جی، YJ; An، CM؛ پارک، NG; و همکاران فعالیت ضد میکروبی پپتیدهای مشتق شده از پروتئین اتصال دهنده لیپوپلی ساکارید چوب زیتون / نفوذپذیری باکتریایی افزایش دهنده پروتئین (LBP/BPI). Mar. Drugs 2014, 12, 5240-5257. [CrossRef] [PubMed]
4. Kirschning، CJ; او-یونگ، جی. لامپ، N.; رویتر، دی. پفیل، دی. سیلهمر، جی جی. Schumann، RR سازماندهی مشابهی از ژن های پروتئین متصل شونده به لیپوپلی ساکارید (LBP) و پروتئین انتقال فسفولیپید (PLTP) یک خانواده ژنی مشترک از پروتئین های اتصال به لیپید را نشان می دهد. ژنومیکس 1997، 46، 416-425. [CrossRef] [PubMed]
5. بالاکریشنان، ع. Marathe، SA; جوگلکار، م. Chakraborty، D. باکتری کش/پروتئین افزایش دهنده نفوذپذیری: یک پروتئین چندوجهی با عملکردی فراتر از خنثی سازی LPS. ایمنی ذاتی 2012، 19، 339-347. [CrossRef]
6. رایت، SD; راموس، RA; توبیاس، PS; اولویچ، آر.جی. Mathison، JC CD14، یک گیرنده برای مجتمع های لیپوپلی ساکارید (LPS) و پروتئین اتصال LPS. Science 1990, 249, 1431-1433. [CrossRef]
7. شائو، ی. لی، سی. چه، ز. ژانگ، پی. ژانگ، دبلیو. دوان، ایکس. Li، Y. شبیه سازی و شناسایی دو ژن پروتئین متصل شونده به لیپوپلی ساکارید/پروتئین افزایش دهنده نفوذپذیری باکتری (LBP/BPI) از خیار دریایی Apostichopus japonica با عملکرد متنوع در تعدیل تولید ROS. توسعه دهنده Comp. ایمونول. 2015، 52، 88-97. [CrossRef]
8. شفر، ن. لی، ایکس. سیبولد، MA; جرجور، NN; دنلینگر، ال سی؛ کاسترو، ام. کاورستون، AM; تیگ، WG; بومر، جی. Bleecker, ER تأثیر تنوع ژنتیکی BPIFA1/SPLUNC1 بر بیان و عملکرد آن در اپیتلیوم راه هوایی آسم. JCI Insight 2019, 4, e127237. [CrossRef]
9. بریتو، سی جی; Cohn، L. ضد باکتری / افزایش نفوذپذیری پروتئین حاوی عضو خانواده A1 در حفاظت از میزبان راه هوایی و بیماری تنفسی. صبح. J. Respir. سلول مول. Biol. 2015، 52، 525-534. [CrossRef]
10. موسی، م. ویلسون، ک. سان، ال. مولای، ع. بینگل، ال. ماریوت، اچ ام. LeClair، EE; Bingle، CD محلی سازی دیفرانسیل BPIFA1 (SPLUNC1) و BPIFB1 (LPLUNC1) در حفره بینی و دهان موش. سلول Tissue Res. 2012، 350، 455-464. [CrossRef]
11. Tsou، Y.-A.; تونگ، ام.-سی. الکساندر، کا. چانگ، دبلیو. Tsai، M.-H. چن، اچ.-ال. چن، سی.-ام. نقش BPIFA1 در عفونت های میکروبی راه هوایی فوقانی و بیماری های مرتبط BioMed Res. بین المللی 2018، 2018، 2021890. [CrossRef] [PubMed]
12. Caikauskaite، R. BPIFA1 تعامل با باکتری ها و اهمیت آنها برای دفاع میزبان راه هوایی. Ph.D. پایان نامه، دانشگاه شفیلد، شفیلد، انگلستان، 2018.
For more information:1950477648nn@gmail.com
