شناسایی سیستماتیک و مقایسه نمایه های بیان شده MiRNA های اگزوزومی در خوک های آلوده به NADC{0}}مانند سویه PRRSV
Dec 27, 2023
خلاصه ساده:اگزوزوم ها نقش منحصر به فردی در عفونت ویروسی، ارائه آنتی ژن و سرکوب/ ارتقای ایمنی بدن دارند. ویروس سندرم تولید مثل و تنفسی خوک (PRRSV) یکی از مضرترین پاتوژن ها در صنعت خوک است. در اینجا، ما از سویه PRRSV NADC30-مانند CHsx1401 برای آلوده کردن مصنوعی خوکهای یک روزه، جداسازی اگزوزومهای سرم و شناسایی 33 miRNA اگزوزومی با بیان متفاوت (DE) بین گروههای عفونت و کنترل استفاده کردیم، و 18 miRNA DE مرتبط با عفونت و ایمنی PRRSV به عنوان مولکول های عملکردی بالقوه درگیر در تنظیم عفونت ویروس PRRSV توسط اگزوزوم ها غربالگری شدند.
خلاصه:اگزوزوم ها وزیکول های بیولوژیکی هستند که توسط سلول ها ترشح و آزاد می شوند که به عنوان واسطه های ارتباط بین سلولی عمل می کنند و نقش منحصر به فردی در عفونت ویروسی، ارائه آنتی ژن، و سرکوب / ارتقای ایمنی بدن دارند. ویروس سندرم تناسلی و تنفسی خوک (PRRSV) یکی از آسیبزاترین پاتوژنها در صنعت خوک است و میتواند باعث اختلالات تولید مثل در خوکها، بیماریهای تنفسی در خوکها، کاهش عملکرد رشد و سایر بیماریهایی شود که منجر به مرگ و میر خوکها میشود. در این مطالعه، ما از سویه PRRSV NADC30-مانند CHsx1401 برای آلوده کردن مصنوعی خوکهای یک روزه و جداسازی اگزوزومهای سرم استفاده کردیم. بر اساس فناوری توالییابی با توان عملیاتی بالا، 305 miRNA در اگزوزومهای سرم قبل و بعد از عفونت شناسایی شدند که در میان آنها 33 miRNA به طور قابلتوجهی بین گروهها بیان شد (13 نسبتاً تنظیم شده و 20 نسبتاً پایین تنظیم شده). تجزیه و تحلیل حفظ توالی ژنوم CHsx1401 8 منطقه حفاظت شده را شناسایی کرد، که در مجموع 16 miRNA با بیان متفاوت (DE) پیش بینی شد که به نزدیک ترین منطقه حفاظت شده به 3 منطقه متصل شوند.0 UTR ژنوم CHsx1401، شامل 5 miRNA DE که قادر به اتصال به CHsx هستند{2}}0 UTR (ssc-miR-34c، ssc-miR-375، ssc-miR-378، ssc-miR-486، ssc-miR-6529). تجزیه و تحلیل بیشتر نشان داد که ژن های هدف miRNA های بیان شده متفاوت به طور گسترده در مسیرهای سیگنال دهی مرتبط با عملکرد اگزوزومی و مرتبط با ایمنی ذاتی و 18 miRNA DE (ssc-miR{14}}p, ssc-miR{16}} دخیل بودند. ، ssc-miR-320، ssc-miR-10b، ssc-miR-124a، ssc-miR-128، و غیره) مرتبط با عفونت و ایمنی PRRSV غربالگری شدند به عنوان مولکول های عملکردی بالقوه در تنظیم عفونت ویروس PRRSV توسط اگزوزوم ها.

گیاه سیستانچ سیستم ایمنی را افزایش می دهد
کلید واژه ها:PRRSV; اگزوزوم سرم؛ miRNA ها
1. معرفی
ویروس سندرم تولید مثل و تنفسی خوک (PRRSV) یک ویروس RNA مثبت تک رشته ای با ساختار پوششی متعلق به راسته Nidovirales، خانواده Arteriviridae، جنس Betaarterivirus است [1،2]. کروی یا بیضی شکل با قطر 50 تا 65 نانومتر در زیر میکروسکوپ الکترونی انجمادی است [3،4]. طول ژنوم PRRSV حدود 15 کیلوبایت با یک کلاهک 50 و یک دم پلیA 30 است و شامل حداقل 10 فریم خواندن باز (ORFs) است که توسط مناطق ترجمه نشده (UTRs) در هر دو انتهای 50 و 30 احاطه شده اند [5،6] و توسط پروتئین نوکلئوکپسید، با پوشش دو لایه لیپیدی برای تشکیل ذرات ویروس پیچیده شده است. اگزوزوم ها متعلق به وزیکول هایی با ساختار غشایی تک لایه هستند و ساختار توپولوژیکی مشابهی با سلول ها دارند [7]. شکل زیر میکروسکوپ الکترونی "فنجانی شکل" یا "دیسکی شکل" است [8،9]. اگزوزوم ها می توانند برای مدت طولانی در سیستم گردش خون وجود داشته باشند و مواد موجود در اگزوزوم ها می توانند توسط سلول های مجاور یا سلول های گیرنده دور جذب شوند و سپس سلول های گیرنده را تنظیم کنند تا در تبادل مواد ژنتیکی بین سلول ها شرکت کنند [10،11]. آنها عمدتاً از مواد سطح غشاء و محتویات حمل شده تشکیل شده اند، از جمله گیرنده های سطح سلول، پروتئین های غشایی، پروتئین های محلول، لیپیدها، RNA (mRNA، miRNA، lncRNA، و RNA ویروسی و غیره)، DNA ژنومی، DNA میتوکندری [12-14]. ]. MicroRNA ها (miRNAs) یک کلاس از 18 تا 25 نوکلئوتید (nt) هستند که به طور تکاملی حفظ شده اند RNA های تک رشته ای کوچک درون زا غیر کدکننده، که با القای تخریب mRNA هدف یا با اتصال به 30 UTR از mRNA هدف، فرآیند ترجمه را مهار می کنند. به خاموش کردن ژن پس از رونویسی، سپس تنظیم بیان ژن در سطح پس از رونویسی [15-17]. تخمین زده می شود که miRNA ها بیش از 60 درصد از ژن های پستانداران را پس از رونویسی تنظیم می کنند [18،19]. MiRNA ها نقش مهمی در ارتباطات بین سلولی دارند و همچنین می توانند به عنوان یک مولکول عملکردی بالقوه برای عفونت، انتقال و دفاع بیماری و ویروس استفاده شوند [20]. تعداد فزاینده ای از مطالعات نشان داده اند که miRNA ها می توانند در مایعات بدن مانند بزاق، ادرار، شیر مادر و خون وجود داشته باشند و از طریق سیستم گردش خون مایع بدن عمل کنند [21،22]. miRNA های اگزوزومی به عنوان تنظیم کننده های درون زا بیان ژن و متابولیسم در نظر گرفته می شوند و می توانند شرایط پاتولوژیک مختلفی را نشان دهند [23،24].

cistanche tubulosa - بهبود سیستم ایمنی
در طول دو دهه گذشته، نشان داده شده است که miRNA ها نقش مهمی در تنظیم رشد سلول های ایمنی، پاسخ های ایمنی ذاتی و پاسخ های ایمنی اکتسابی دارند. برخی دیگر از miRNA ها از طریق راه های زیر به عفونت PRRSV آسیب می رسانند، مستقیماً ژنوم PRRSV یا گیرنده PRRSV را هدف قرار می دهند یا با تنظیم پاسخ ایمنی ذاتی میزبان نقش دارند. خانواده miR-26 میتواند به طور قابلتوجهی به تکثیر ویروس آسیب برساند و miR-26a میتواند تکثیر سویههای PRRSV نوع 1 و نوع 2 را در ماکروفاژهای آلوئولی خوک (PAM) با تنظیم اینترفرون نوع I (IFN) مهار کند. مسیر، که کارآمدتر از miR-26b [25،26] است. miR-30c و miR{8}}b برای تعدیل پاسخ ایمنی ذاتی میزبان با هدف قرار دادن مسیر IFN نوع I و مسیر NF-kB، به ترتیب شناسایی شدهاند [27-29]. MiR{12}}، miR-378، و miR-505 عوامل میزبان ضد ویروسی هستند که PRRSV را هدف قرار میدهند و دارای سایتهای هدف محافظهکارانه در سویههای PRRSV نوع 2 هستند [30]. در همان زمان، miR میزبان شناسایی شده است که با هدف قرار دادن مستقیم گیرنده PRRSV CD151 در سلولهای MARC، تکثیر PRRSV را مهار میکند [31]. miR{21}} همچنین میتواند بهطور غیرمستقیم تکثیر PRRSV را با تنظیم پایین گیرنده PRRSV CD163 در مونوسیتهای خون و PAMها مهار کند [32]. علاوه بر این، miRNA ها می توانند همانندسازی PRRSV را با تداخل در فیزیولوژی سلولی پایه ترویج کنند. MiR-24-3p و miR-22 مستقیماً 30 UTR HO-1 را در طول عفونت PRRSV هدف قرار میدهند تا از مهار هم اکسیژناز (HO{30}}) فرار کنند. پروتئین شوک حرارتی (همچنین به عنوان HSP32 شناخته می شود) در PRRSV [33،34]. خوکها نسبت به PRRSV حساستر هستند و کمتر قادر به دفاع از خود در برابر ورود این پاتوژن به ارگانیسم هستند [35]. در مطالعه حاضر، ایمنی ذاتی و ایمنی اکتسابی خوکهای آلوده به این ویروس در سطح مولکولی با استفاده از یک سویه رایج در مزرعه مورد بررسی قرار گرفت. یک کیت جداسازی اگزوزوم سرم، میکروسکوپ الکترونی عبوری (TEM)، آنالیز ردیابی نانوذرات (NTA) و وسترن بلات (WB) برای جداسازی و شناسایی اگزوزومهای سرم قبل و بعد از عفونت با PRRSV، به دنبال آنالیز توالی RNA کوچک، شناسایی، استفاده شد. و تجزیه و تحلیل نتایج بیان دیفرانسیل با استفاده از روشهای بیوانفورماتیک برای به دست آوردن چندین miRNA اگزوزوم سرم مرتبط با PRRSV، و به دنبال آن شناسایی نتایج دادهها با استفاده از PCR کمی (qRT-PCR).
2. مواد و روشها
2.1. آزمایش های حیوانی
شش آنتی ژن PRRSV و آنتی بادی دو منفی سالم 42- خوک سفید بزرگ یک روزه برای جداسازی، مراقبت های بهداشتی و سازگاری با محیط در سیستم تغذیه تمیز خوک قرار گرفتند. همه خوک ها برای خوردن و نوشیدن بدون محدودیت آزاد بودند. هنگامی که آنها با شرایط موجود در جداساز آشنا شدند، خوک ها با 2 میلی لیتر 105 TCID50/mL PRRSV NADC{6}}مانند CHsx1401 که توسط پیشینیان ذکر شده بود از طریق بینی تلقیح شدند [36،37]. خون خوکها قبل از (گروه شاهد، n=6) و 7 روز پس از (گروه درمان، n=6) تلقیح ویروس از ورید اجوف قدامی برای جداسازی سرم جمعآوری شد. بقایای سلولی در سرم با سانتریفیوژ در 3000 گرم به مدت 15 دقیقه حذف شد. همه آزمایشهای حیوانی در مطالعه ما توسط کمیته اخلاق حیوانی مؤسسه علوم دامی، آکادمی علوم کشاورزی چین (CAAS) (پکن، چین)، IAS تأیید شد{15}}.
2.2. جداسازی و خالص سازی اگزوزوم های سرم
جداسازی و خالص سازی اگزوزوم با استفاده از کیت exoEasy Maxi (QIAGEN، هیلدن، آلمان، شماره کات. 76064) طبق پروتکل سازنده انجام شد.
2.3. میکروسکوپ الکترونی انتقالی (TEM)
سوسپانسیونهای اگزوزوم استخراجشده روی مش مسی با پوشش کربنی فرموار لکهدار شدند و اگزوزومها با PBS شسته شدند و به مدت 3 دقیقه در دمای اتاق تحت رنگآمیزی استاندارد اورانیل استات قرار گرفتند. پس از خشک شدن برای چند دقیقه در دمای اتاق، شبکه در 100 کیلوولت با میکروسکوپ الکترونی عبوری تصویربرداری شد (HT{3}}، Hitachi-High Tech، توکیو، ژاپن).
2.4. تجزیه و تحلیل ردیابی نانوذرات (NTA)
اگزوزوم های استخراج شده با تغییر حجم از 10 به 30 میکرولیتر با 1 × PBS رقیق شدند. پس از آزمایش نمونه، غلظت و اندازه اگزوزوم های سرم توسط یک نانو آنالایزر جریان N30E مطابق دستورالعمل سازنده (NanoFCM، Xiamen، چین) آنالیز شد.
2.5. وسترن بلات
نمونههای اگزوزوم استخراجشده به لیزات RIPA مخلوط با بازدارنده پروتئاز (Invitrogen, Waltham, MA, USA) و فنیل متیل سولفونیل فلوراید (PMSF) اضافه شدند تا پروتئین اگزوزوم استخراج شود که به مدت 30 دقیقه روی یخ لیز شد. سپس، طبق دستورالعمل کیت برادفورد، غلظت پروتئین اگزوزوم سرم را اندازهگیری کردیم. پروتئین های اگزوزوم تحت دناتوراسیون حرارتی قرار گرفتند. همان مقدار پروتئین روی ژل SDS-PAGE 12 درصد جدا شد و سپس به غشای پلی وینیلیدین فلوراید (PVDF) (Milipour, Burlington, MA, USA) منتقل شد. آن را در TBST حاوی 5٪ پودر شیر بدون چربی خیسانده و به مدت 1 ساعت در دمای اتاق بسته شد. ما غشاء را در آنتی بادی اولیه رقیق شده (آنتی بادی ضد CD9، Abcam، بوستون، MA، ایالات متحده، #ab92726، آنتی بادی ضد CD81، Abcam، بوستون، MA، ایالات متحده، #ab109201) یک شبه در دمای 4 درجه سانتیگراد خیس کردیم و بهبود یافتیم. آنتی بادی اولیه ما غشا را در آنتی بادی ثانویه رقیق خیس کردیم، آن را در دمای اتاق به مدت 1 ساعت انکوبه کردیم و آنتی بادی ثانویه را بازیابی کردیم. ما فیلم شسته شده PBST را روی فیلم تازه نگه داری قرار دادیم، محلول کروموژنیک مخلوط ECL a/b را با حجم مساوی اضافه کردیم و آن را در تصویرگر نورتابی شیمیایی قرار دادیم.

فواید سیستانچ برای مردان - تقویت سیستم ایمنی بدن
برای مشاهده محصولات Cistanche Enhance Immunity اینجا را کلیک کنید
【بیشتر بخواهید】 ایمیل:cindy.xue@wecistanche.com / Whats App: 0086 18599088692 / Wechat: 18599088692
2.6. توالی یابی RNA کوچک اگزوزومی و تجزیه و تحلیل داده ها
RNA کل از اگزوزوم ها با تریزول طبق دستورالعمل سازنده استخراج شد. سپس غلظت RNA و مقدار چگالی نوری (OD) را شناسایی کردیم و تخریب و خلوص RNA را با الکتروفورز ژل آگارز 1٪ تشخیص دادیم. در همین حال، Agilent Bioanalyzer 2100 برای تشخیص یکپارچگی RNA استفاده شد. ما از RNA کل اگزوزوم ها پس از بررسی کیفیت استفاده کردیم. طبق دستورالعمل سازنده، ما از مجموعه آماده سازی کتابخانه RNA کوچک چندگانه NEB NEXT برای Illumina® (Illumina، San Diego، CA، USA) استفاده کردیم. این کیت یک کتابخانه کوچک cDNA RNA تهیه کرد و آن را برای تولید 5{14}} nt خواندن یکانتها توسط پلتفرم Illumina Novaseq 6000 توالیبندی کرد. تمام مراحل آماده سازی کتابخانه RNA کوچک توسط Novogene (پکن، چین) انجام شد. دادهها پس از کنترل کیفیت با استفاده از پاپیون با ژنوم مرجع خوک (Sus scrofa 11.1) تراز شدند. miRNA های شناخته شده توسط پایگاه داده miRbase (v22.0) [38] (https://www.mirbase.org، مشاهده شده در 14 ژانویه 2022)، miRdeep2 (v0.0.5) [39] و miRevo (نسخه 1.1) شناسایی شدند. ) [40] و برای پیش بینی miRNA های جدید استفاده شدند. در همان زمان، تجزیه و تحلیل بیان دیفرانسیل برای miRNA ها توسط DESeq (v1.24.0) [41] انجام شد، که نیاز به |تغییر برابر| > 1.6 و p <0.05. هم ترازی با استفاده از MEGA (V11) [42] و سپس امتیازدهی تک پایه با استفاده از PHAST (v1.6.9) [43] و ارزیابی حفاظتشدهترین مناطق از 10 ژن ویروس، از جمله WUH3 (GenBank شماره دسترسی HM853973)، VR2332 ( GenBank no. 22-1812 (GenBank Accession No. MN648450)، SC/DJY (GenBank Accession No. MT075480) و Lelystad (GenBank no. M96262.2). RNAhybrid (V2.0) [44] برای پیش بینی اتصال توالی miRNA شناسایی شده به 3 0 UTR ژنوم ویروس CHsx1401 استفاده شد. Miranda (v3.3a) و RNAhybrid برای پیشبینی ژن مورد استفاده قرار گرفت. پروفایل خوشه ای [45] بسته R برای تجزیه و تحلیل غنی سازی عملکردی GO (هستی شناسی ژن) ژن های هدف و KEGG (دانشنامه کیوتو ژن ها و ژنوم ها) تجزیه و تحلیل غنی سازی مسیر استفاده شد.
2.7. اعتبار سنجی بیان miRNA توسط RT-qPCR
RNA کل از اگزوزوم های سرم با استفاده از Trizol (Invitrogen، شانگهای، چین) طبق پروتکل سازنده جدا شد. RNA جدا شده توسط RT-qPCR در نمونه ها (n=6 در هر گروه) تأیید شد. cDNA مطابق دستورالعمل کیت سنتز cDNA رشته 1 miRNA (توسط stem-loop) (Vazyme، نانجینگ، چین) سنتز شد و کمی سازی فلورسانس با استفاده از ABI 7500 مطابق با دستورالعمل های ترکیب اصلی miRNA جهانی SYBR qPCR (Vazyme، نانجینگ، چین). پارامترهای چرخه حرارتی مورد استفاده به شرح زیر بود: مرحله اول: 95 ◦C برای 30 ثانیه; مرحله 2: 95 ◦C برای 5 ثانیه، 60 ◦C برای 34 ثانیه و 40 سیکل. مرحله 3: 95 ◦C به مدت 15 ثانیه، 60 ◦C برای 1 دقیقه و 95 ◦C برای 15 ثانیه. توالی های پرایمر miRNA ها، ژن U6، به عنوان مرجع [46] استفاده شد و در جدول تکمیلی S1 فهرست شده است. تمام تایید QRT-PCR با استفاده از سه تکرار بیولوژیکی و با سه تکرار برای هر نمونه انجام شد. فراوانی نسبی رونوشت ها با روش 2-Ct محاسبه شد و برای تجزیه و تحلیل داده ها و نقشه برداری از SPSS (v22.0) و GraphPad Prism (v8.0) استفاده شد. p <0.05 به این معنی است که این تفاوت از نظر آماری معنی دار است.
3. نتایج
3.1. ارزش نسبی آنتی ژن و آنتی بادی پس از تلقیح ویروس
نتایج آزمایش آنتی ژن و آنتی بادی PRRSV قبل از (روز 0) و بعد از چالش (روز 7) در جدول 1 نشان داده شده است. تشخیص سرولوژیکی آنتی ژن و آنتی بادی PRRSV قبل از چالش منفی بود و آنتی ژن مثبت پس از چالش، نشان می دهد که خوک ها با موفقیت با CHsx1401 آلوده شدند.
3.2. جداسازی و شناسایی اگزوزوم های سرم
وزیکول های جدا شده از سرم توسط TEM کشف شد. اکثر وزیکول ها می توانند اگزوزوم های مقعر بشقاب یا دیسکی شکل را در وسط ببینند. لبه غشایی اگزوزوم ها قابل مشاهده است و مورفولوژی نسبتاً کامل است (شکل 1A, B). تجزیه و تحلیل ردیابی نانوذرات نشان داد که 95.73٪ از اگزوزوم ها دارای قطر 30-150 نانومتر، عمدتاً حدود 72.25 نانومتر، با قطر متوسط 76.22 نانومتر بودند که با مشخصات اندازه اگزوزوم ها مطابقت داشت (شکل 1C). این محدوده اندازه شبیه به آنچه که توسط TEM شناسایی شد بود و هویت این وزیکول ها را به عنوان اگزوزوم تایید کرد. تجزیه و تحلیل وسترن بلات نشان داد که وزیکول های جدا شده از نمونه های سرم برای پروتئین های CD9 و CD81 مثبت بودند (شکل 1D). ویژگی های فوق مطابق با استانداردهای شناسایی اگزوزوم است که توسط انجمن بین المللی وزیکول های خارج شده (ISEV) در MISEV2018 [47] فرموله شده است.
جدول 1. آنتی ژن و آنتی بادی (روز 0) و (روز 7) با ویروس چالش.

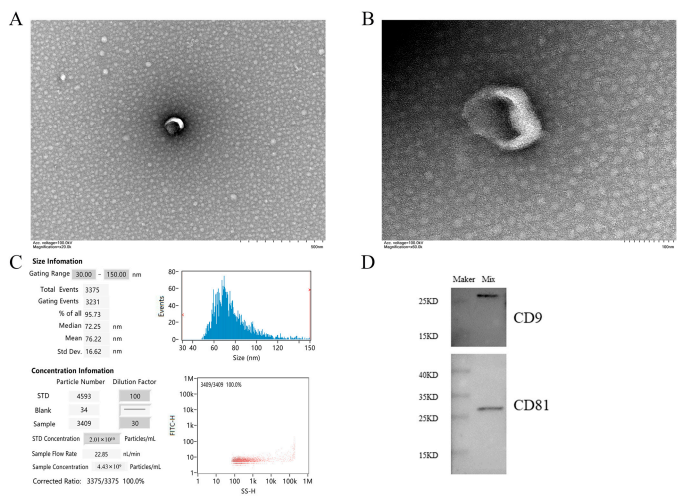
شکل 1. ویژگی های اصلی اگزوزوم های سرم. (A, B) ویژگی های مورفولوژیکی وزیکول ها را توسط TEM نشان می دهد. میله های مقیاس به ترتیب 500 نانومتر و 100 نانومتر هستند. (C) NTA قطر و غلظت اکثر وزیکول ها را نشان می دهد. (D) وسترن بلات وجود نشانگرهای اگزوزوم CD81 و CD9 را در اگزوزوم های سرم نشان داد. توجه: نتایج Mix in WB نمونه ای از تعلیق مخلوط است که توسط کیت exoEasy Maxi جدا شده است.
3.3. توالی RNA کوچک اگزوزوم های سرم
برای هر نمونه، داده های تمیز به 0.5 گیگابیت رسید و درصد پایه Q30 بالای 96.20٪ بود. قرائت تمیز هر نمونه با ژنوم مرجع خوک تراز شد. از بین 12 نمونه، گروه کنترل به ترتیب 10،920،887، 10،248،696، 10،109،117، 10،655،494، 9،217،285، و 9،782،523 قرائت شد. گروه درمان به ترتیب 11889518، 10593504، 10593504، 12846080، 10105325، 11729451 و 9789542 قرائت شد. به طور متوسط، 77.96٪ از کل قرائت های تمیز شامل 19-22 نوکلئوتید (nt) در طول بود (شکل 2A). قرائت پس از کنترل کیفیت بیش از 92.59 درصد از کل خوانده ها را به خود اختصاص داده است. خوانش های تمیز پردازش شده با ژنوم مرجع خوک تراز شد و نرخ نقشه برداری 12 کتابخانه روی ژنوم بیش از 92.30 درصد و نرخ نقشه برداری 94.98 درصد بود (شکل 2B). این نشان داد که کتابخانه miRNA اگزوزومی سرم ساخته شده با کیفیت بالا و مناسب برای تجزیه و تحلیل بیشتر است. جزئیات در جدول تکمیلی S2 فهرست شده است.

شکل 2. نمای کلی داده های رونویسی RNA کوچک. (الف) توزیع طول تعداد خوانده شده نمونه های اگزوزوم سرم (nt=نوکلئوتید). (ب) نرخ 12 نمونه نقشه برداری شده به ژنوم مرجع
3.4. تجزیه و تحلیل بیان متفاوت miRNA ها
پس از تجزیه و تحلیل کمی بیان miRNA شناسایی شده، miRNA ها با آستانه هایی که قبلا در بخش 2.6 توضیح داده شد، غربالگری شدند. در مجموع 305 miRNA قبل و بعد از تلقیح سویه CHsx1401 به دست آمد (کنترل، n=6؛ درمان، n=6). در مجموع 33 miRNA با بیان متفاوت (DE) بین دو گروه شناسایی شد، 13 miRNA DE تنظیم مثبت شد و 20 miRNA DE در گروه درمان کاهش یافت (شکل 3 و جدول تکمیلی S3).
3.5. تجزیه و تحلیل غنیسازی عملکردی ژنهای هدف miRNA
در مجموع 7283 ژن هدف توسط 33 miRNA DE پیشبینی شد و عملکرد ژنهای هدف عمدتاً در تنظیم مثبت آبشار MAPK، فرآیند متابولیسم لیپید، تنظیم انتقال سیگنال درون سلولی، آبشار ERK1 و ERK2 و غیره متمرکز بود (شکل 4A) ). از نظر عملکردهای مولکولی، ژنهای هدف miRNA بیان شده متفاوت عمدتاً بر فعالیت تنظیمی آنزیم GTP، فعالیت کیناز، فعالیت تنظیمی نوکلئوزید تری فسفاتاز و سایر عملکردهای مربوط به انتقال سیگنال و متابولیسم انرژی تمرکز دارند (شکل 4B). علاوه بر این، در بین اجزای سلول، ژنهای هدف عمدتاً در عملکردهای بیولوژیکی پلیمرهای فوق مولکولی، گلژی، اتوفاگوزومها، سطح سلول، اندوزومهای اولیه و غیره شرکت میکنند (شکل 4C). عملکرد این اجزا ارتباط نزدیکی با تشکیل اگزوزوم ها دارد که دقت توالی یابی را نیز توضیح می دهد. تجزیه و تحلیل غنیسازی مسیر KEGG نشان داد که ژنهای هدف در اندوسیتوز، مسیر سیگنالدهی MAPK، مسیر سیگنالدهی Rap1، مسیر سیگنالدهی اسفنگولیپید و مسیر سیگنالدهی PI3K Akt به طور قابلتوجهی غنی شدهاند (p < 0.05) (شکل 5A) ). در همان زمان، مسیرهای غنی شده طبقه بندی و تجزیه و تحلیل شدند. نتایج نشان داد که مسیر KEGG ژن هدف عمدتاً در پردازش اطلاعات محیطی، بیماری های انسانی و سیستم های بیولوژیکی غنی شده است (شکل 5B).

شکل 3. بیان متفاوت miRNA ها در اگزوزوم ها. (الف) نمودار آتشفشانی miRNA ها بین گروه های کنترل و تیمار. (ب) نقشه حرارتی خوشهبندی سلسله مراتبی miRNAهای DE بین گروههای کنترل و درمان.
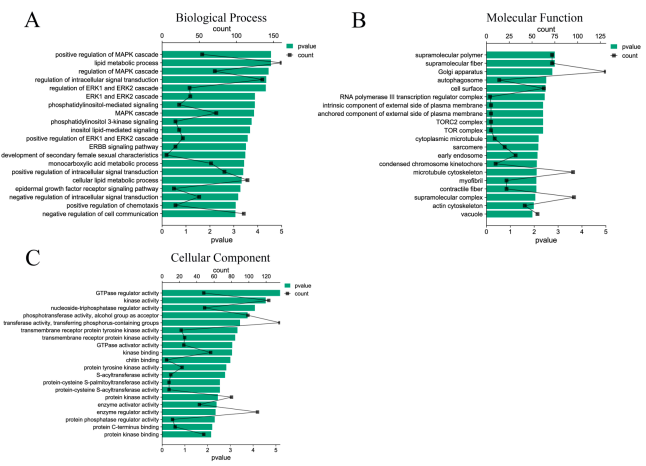
شکل 4. تجزیه و تحلیل غنیسازی تابع GO ژنهای هدف DE miRNA. (الف) فرآیند بیولوژیکی ژنهای هدف miRNA DE. (ب) عملکردهای مولکولی ژنهای هدف miRNAهای DE. (C) اجزای سلولی ژنهای هدف miRNA DE
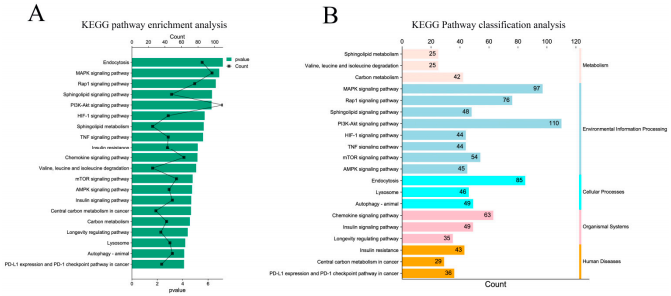
شکل 5. تجزیه و تحلیل غنی سازی مسیر KEGG ژن های هدف. (الف) مسیر KEGG به طور قابل توجهی با ژن های هدف miRNA های DE غنی شده است. (B) طبقه بندی مسیرهای KEGG غنی شده قابل توجهی.
3.6. پیشبینی هدفیابی miRNA اگزوزومی سرم و ژنوم PRRSV CHsx1401
با توجه به امتیاز phastCons از یک پایه منفرد پس از تراز توسط PHAST، در مجموع هشت بخش محافظت شده (نوارهای سیاه بالای نقشه پیک) در بین ژنوم های ویروسی به دست آمد (شکل 6). در مجموع 31 miRNA های DE با پیش بینی miRNA های متصل به بخش حفاظت شده به بخش حفاظت شده متصل شدند. در میان آنها، در ناحیه حفاظت شده (14,644-15,020 nt) نزدیکترین به 30 UTR (14,870-15,020) ژنوم CHsx1401، پیشبینی میشود که 16 miRNA DE به آن متصل شوند، از جمله 5 miRNAs (s{15}miR) c، ssc-miR-375، ssc-miR-378، ssc-miR-486، و ssc-miR-6529) که میتوانند به 30 UTR CHsx1401 متصل شوند. در بین این miRNA ها، تنها ssc-miR{27}} پس از عفونت تنظیم مثبت شد و سایر miRNA ها پس از عفونت تنظیم نشدند. برای جزئیات به جدول تکمیلی S4 مراجعه کنید.
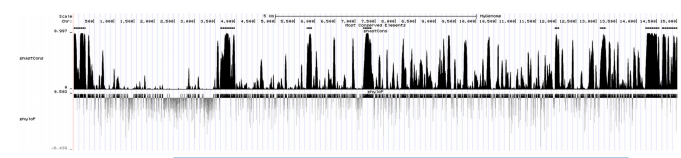
شکل 6. بخش های حفاظت شده در ژنوم سویه CHsx1401 پیش بینی شده توسط PHAST
3.7. غربالگری miRNA های DE مربوط به عملکرد اگزوزوم و PRRSV
انواع miRNA های بیان شده متفاوت مربوط به عملکرد اگزوزوم ها و PRRSV با تجزیه و تحلیل غنی سازی عملکردی ژن های هدف پیدا شد. در میان آنها، 11 miRNA DE مانند ssc-miR-4331-3p، ssc-miR-744 و ssc-miR-320 در جذب اگزوزوم نقش دارند و ژنهای هدف آنها عمدتاً در خانواده ژن Ras، خانواده انکسین و خانواده ژن ریبوسیلاسیون ADP. هجده miRNA DE، از جمله sscmiR-10b، ssc-miR-124a، و ssc-miR{11}} در مسیرهای مرتبط با ایمنی شرکت میکنند و ژنهای هدف آنها عمدتاً در MAPK متمرکز شدهاند. خانواده ژن، خانواده ژن PIK3 و خانواده ژن پروتئین فسفاتاز. در حالی که 11 miRNA DE در تهاجم ویروس نقش دارند، ژنهای هدف مرتبط عمدتاً در خانواده ژن MAPK و خانواده ژن پروتئین فسفاتاز متمرکز هستند. علاوه بر این، miRNA های متعددی که به طور متفاوت بیان می شوند، مانند جدید{15}}. شش DE miRNA، از جمله ssc-miR-320، ssc-miR-423-5p، ssc-miR-4331-3p،ssc-miR-7137-3p، و ssc-miR{{ 25}}، همانطور که در شکل 7 نشان داده شده است، در عملکرد اگزوزوم، تهاجم ویروس PRRSV و مسیرهای مرتبط با ایمنی بیان می شوند. جزئیات در جدول تکمیلی S5 نشان داده شده است.
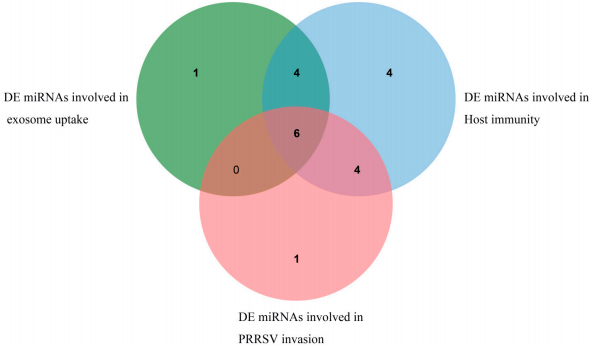
شکل 7. miRNA های DE مربوط به جذب اگزوزوم، تهاجم PRRSV و ایمنی
3.8. سنجش QRT-PCR miRNA های DE بین دو گروه
پنج miRNA DE به طور تصادفی برای تأیید انتخاب شدند. با توجه به نتایج qRT-PCR، بیان ssc-miR-19a و ssc-miR-32 در گروه درمان افزایش یافت، در حالی که ssc-miR-124a، ssc-miR{ {8}} و ssc-miR{10}}c بیان بالاتری را در گروه کنترل نشان دادند که مطابق با دادههای توالییابی بود (شکل 8).

شکل 8. پنج miRNA DE تایید شده توسط qRT-PCR
4. بحث
PRRSV هنوز یک پاتوژن سرسخت در صنعت خوک جهانی است که باعث خسارات اقتصادی بزرگی در جهان می شود. در حال حاضر، واکسیناسیون عمدتاً برای پیشگیری و کنترل PRRSV مورد استفاده قرار می گیرد، که در میان آنها واکسن ویروس زنده اصلاح شده (MLV) بیشترین استفاده را دارد [48]. اگرچه این واکسن در کاهش شیوع و بروز PRRS موثر بود، اما تنوع ژنتیکی و تنوع ویروس را نیز به میزان زیادی افزایش داد و منجر به نوترکیبی ویروسی بین ویروسهای واکسن وحشی و زنده در مزرعه شد [49،50]. در سالهای اخیر، گسترش و شیوع ویروس نوترکیب NADC{3}}مانند سویه PRRSV باعث شیوعهای متعدد سندرم تناسلی و تنفسی خوک در چین شده است. شباهت بین CHsx1401 و NADC30 مورد استفاده در این مطالعه در 92.2-99.1٪ باقی مانده است. از آن زمان، این بیماری در چین به یک گونه اپیدمی تبدیل شده است. اگزوزوم ها به عنوان واسطه های ارتباط سلولی، به طور گسترده در مایعات مختلف بدن یافت می شوند و مزایای منحصر به فردی در تشخیص و درمان بیماری دارند [51،52]. طبق گزارشهای قبلی، اگزوزومها نقش ارتباطی مهمی در ارائه آنتیژن [53]، پاسخ ایمنی [53،54]، تکثیر ویروس [54]، سرطان [55]، بیماریهای نورودژنراتیو [56]، رگزایی [57]، سلول تومور ایفا میکنند. مهاجرت [58] و تهاجم [59] و ارزش تحقیقاتی بالایی دارند.
در این مطالعه، از فناوری توالی یابی با توان بالا برای ساخت پروفایل بیان miRNA اگزوزوم های سرم استفاده شد و 33 miRNA DE شناسایی شد. همانطور که همه ما می دانیم، miRNA رمزگذاری شده توسط میزبان می تواند با ژنوم ویروسی متصل شود و سپس تکثیر، سنتز و انتشار ویروس را تنظیم کند تا عفونت را محدود کند و بر فرآیند پاتولوژیک تأثیر بگذارد [15]. مطالعات miRNA هایی که ژنوم ویروسی را هدف قرار می دهند نیز بارها در حیوانات گزارش شده است. gga-miR-454 و gga-miR-130b در بیماری بورس عفونی جوجه میتواند ژنوم ویروس را برای مهار تکثیر ویروس هدف قرار دهد، در حالی که gga-miR-21 مستقیماً پروتئین ویروسی VP1 را برای مهار کردن هدف قرار میدهد. ترجمه پروتئین ویروسی [60،61]. در مطالعات PRRSV، ssc-miR{14}} به طور خاص به یک منطقه بسیار حفاظت شده در پایین دست ژنوم ویروسی ORF4 متصل می شود و به شدت تکثیر PRRSV را مهار می کند [62]. در این مطالعه، تفاوت بیانی ssc-miR{18}} بین دو گروه به سطح معنیداری نرسید. در مطالعه ما، ژنوم نه ویروس مختلف PRRSV با ژنوم سویه CHsx1401 مقایسه شد و هشت بخش محافظت شده شناسایی شد. پیشبینی شد که 31 miRNA DE میتوانند به 8 بخش حفاظتشده CHsx1401 و 16 miRNA DE میتوانند به توالیهای حفظشده نزدیک به 30 UTR CHsx1401 متصل شوند. در میان آنها، 5 miRNA DE (ssc-miR-34c، ssc-miR-375، ssc-miR-378، ssc-miR-486، و ssc-miR{{ 36}}) می تواند به طور همزمان به CHsx{37}} UTR متصل شود. علاوه بر این، بیان افزایشی ssc-miR{39}} برای اتصال به هدف 30 UTR ژنوم PRRSV پیشبینی شد. نتایج نشان داد که توالیهای حفاظتشده ژنوم ویروس ممکن است نقش کلیدی در بیماریزایی آن داشته باشند و miRNAهایی که میتوانند به توالیهای حفاظتشده بین ژنوم سویههای مختلف PRRSV متصل شوند، ممکن است اهمیت مهمی در کنترل بیماریزایی ویروس داشته باشند. برخی از miRNA های بیان شده متفاوت توسط مطالعات قبلی ثابت شده است که با PRRSV مرتبط هستند و حتی مستقیماً در تنظیم PRRSV نقش دارند، از جمله ssc-miR-10b [63]، ssc-miR{45}} [30] ، ssc-miR-124a [64]، اجازه دهید-7f-5p [65]، ssc-miR-744 [66]، و ssc-miR{{57 }}a [67].
PRRSV می تواند با تداخل در پاسخ ایمنی ذاتی از دفاع میزبان فرار کند. این فرآیند توسط بسیاری از مسیرهای سیگنالینگ، از جمله مسیر سیگنالینگ MAPK، مسیر سیگنالینگ PI3K Akt، اتوفاژی، کموکاین و مسیر سیگنالینگ TNF تنظیم می شود. در حال حاضر مسیر سیگنالینگ MAPK شامل سه مسیر اصلی است: ERK1/2، JNK و مسیر p38. فعالسازی آبشار MAPK میتواند آپوپتوز سلول میزبان را ارتقا دهد، به ویروس در فرار از پاسخ دفاعی ایمنی میزبان کمک کند و تکثیر PRRSV را تقویت کند [68]. علاوه بر این، فعال شدن کینازهای N ترمینال c-Jun (JNKs) و p38 همچنین میتواند باعث آزادسازی فاکتور التهابی IL{8}} [68-70] شود و اثر التهابی را افزایش دهد. علاوه بر القای آپوپتوز، PRRSV می تواند اتوفاژی را نیز القا کند که می تواند تکثیر PRRSV را تقویت کند. فعال شدن PI3K/Akt برای ورود ویروس و ترویج تکثیر ویروس ضروری است و Akt فعال شده با PRRSV با تنظیم منفی مسیر JNK، آپوپتوز سلول میزبان را مهار می کند [71]. TNF می تواند نقش مهمی در القا و تنظیم پاسخ التهابی همراه با سایر عوامل التهابی داشته باشد، اما بیان TNF تحت تأثیر تنظیم منفی تکرار PRRSV قرار می گیرد [72]. در مطالعه حاضر، miRNA ها (ssc-miR-10b، ssc-miR-122-5p، ssc-miR{20}}a، ssc-miR-128، ssc-miR{ {24}}a-5p، و غیره) غنی شده در این مسیرها در آپوپتوز، اتوفاژی و التهاب ناشی از PRRSV نقش دارند و ارتباط نزدیکی با پاسخ ایمنی ویروسی، فرار ایمنی و تکثیر دارند.

cistanche tubulosa - بهبود سیستم ایمنی
غشای پلاسمایی سلولی غنی از انواع قایق های لیپیدی است و اسفنگولیپیدهای غنی از کلسترول و اسفنگولیپید (اسفنگومیلین و گلیکوسفنگولیپیدها) مولکول های کلیدی قایق های لیپیدی هستند. شناسایی لیپیدها توسط برخی از پروتئین های ویروس ممکن است شرط لازم برای ورود ویروس باشد [73]. ویروسهای پاکتی، گلیکوپروتئینهای پوششی ویروسی را در مرحله ورود ویروس به قایقهای لیپیدی وارد میکنند، با گیرندههای واقع در رافتهای لیپیدی تعامل میکنند، یا از حالت طبیعی خود به شکل فعال تغییر میکنند تا درونیسازی/همجوشی ویروسی را آغاز یا ترویج کنند، مانند HSV، SARS کرونا، و ویروس اسهال اپیدمی خوکچه [73،74]. مطالعات قبلی نشان داد که حذف کلسترول از سطح سلولهای MARC به طور قابل توجهی عفونت PRRSV را کاهش میدهد و نشان میدهد که مهار عفونت PRRSV به طور خاص با حذف کلسترول سلولی انجام میشود. کاهش کلسترول غشای سلولی به طور قابل توجهی از ورود ویروس، به ویژه چسبندگی و انتشار ویروس جلوگیری می کند [75]. متابولیسم اسفنگولیپید می تواند ساختار غشاء و چسبندگی را تنظیم کند، که در تهاجم ویروس PRRSV اهمیت زیادی دارد. اندوسیتوز مهم ترین غنی سازی در این مطالعه بود. اندوسیتوز یک مکانیسم مهم جذب اگزوزوم توسط سلول های هدف است. مطالعات قبلی نشان داده اند که جذب اگزوزوم یک فرآیند نیازمند انرژی و وابسته به اسکلت سلولی است که نقش بالقوه اندوسیتوز را در این فرآیند برجسته می کند [76]. ثابت شده است که چندین مسیر می توانند این فرآیند را واسطه کنند، از جمله فاگوسیتوز، ماکروپینوسیتوز، کلاترین و غیره [77،78] که منجر به طبقه بندی و نقش های متفاوتی از مواد اندوسیتوز شده شد. غنیسازی miRNAهای اگزوزومی با بیان متفاوت در این مسیر نشان میدهد که اگزوزومها نقش مهمی در عفونت PRRSV بازی میکنند و تنظیم انتقال محتوا و جذب در اگزوزومها ممکن است منجر به تغییرات پاتوفیزیولوژیکی در سلولها و اندامهای هدف شود.

cistanche tubulosa - بهبود سیستم ایمنی
5. نتیجه گیری ها
از طریق شناسایی و تجزیه و تحلیل بیوانفورماتیکی miRNA های اگزوزومی سرم از خوک های آلوده به PRRSV، انواع مسیرهای مرتبط با PRRSV و miRNA های متفاوت بیان شده در این مطالعه به دست آمد، مانند ssc-miR-4331-3p، ssc-miR{{{ 5}}، sscmiR-320، ssc-miR-10b، ssc-miR-124a، ssc-miR-128، و غیره، که نقشهای عملکردی بالقوه در PRRSV دارند پاسخ ایمنی القایی، تهاجم و جذب اگزوزوم. علاوه بر این، از آنجا که یک miRNA منفرد می تواند چندین ژن را هدف قرار دهد و یک ژن نیز توسط miRNA های متعدد تنظیم می شود، چندین miRNA عملکردهای متعددی را در مسیرهای فوق انجام می دهند. برخی از miRNA ها برای تنظیم عفونت PRRSV با تأثیر بر گیرنده های کلیدی یا هدف قرار دادن مستقیم ژنوم ویروس تأیید شده اند، مانند ssc-miR{15}}b، ssc-miR-378، miR{18}} اجازه دهید-7f-5p، ssc-miR-744، ssc-miR-19a، و غیره. در همین حال، مطالعه حاضر همچنین انواع miRNA ها را پیش بینی کرد که می توانند به حفظ ترین قطعه از 30 UTR ژنوم ویروس CHX1401، شامل ssc-miR-34c, ssc-miR-375, ssc-miR-378, ssc-miR{34} } و ssc-miR{36}}، که ممکن است برای تنظیم بیماری زایی ویروسی مهم باشند.
منابع
1. اسنایدر، ای جی; کیکرت، ام. نیش، Y. بیولوژی مولکولی و پاتوژنز آرتری ویروس. جی ژنرال ویرول. 2013، 94 Pt 10، 2141–2163. [CrossRef] [PubMed]
2. لو، ی. ژانگ، ی. Xiang، X. شارما، م. لیو، ک. وی، جی. شائو، دی. لی، بی. تانگ، جی. اولشفسکی، MA; و همکاران سیگنالینگ Notch به بیان سایتوکاین های التهابی ناشی از عفونت با ویروس سندرم تنفسی و تولید مثلی خوک بسیار بیماری زا در ماکروفاژهای آلوئولی خوک کمک می کند. توسعه دهنده Comp. ایمونول. 2020, 108, 103690. [CrossRef] [PubMed]
3. دی، س. ساویر، ن. آلن، آر. Athanassious، R. ویژگیهای فراساختاری و مورفوژنز ویروس سندرم تنفسی و تولیدمثلی خوک تکثیر شده در کلون سلولی MARC{1}} بسیار مجاز. Adv. انقضا پزشکی Biol. 1995، 380، 95-98. [PubMed]
4. Dokland، T. زیست شناسی ساختاری PRRSV. ویروس Res. 2010، 154، 86-97. [CrossRef] [PubMed]
5. جانسون، CR; گریگز، TF; گناناندراجه، ج. مورتا، MP پروتئین ساختاری جدید در ویروس سندرم تنفسی و تولید مثل خوک کدگذاری شده توسط یک ORF5 جایگزین موجود در همه آرتری ویروس ها. جی ژنرال ویرول. 2011، 92 Pt 5، 1107–1116. [CrossRef] [PubMed]
6. لی، SC; لی، اس. یو، جی وات؛ چوی، HW; نه، YH; پارک، CE; Shin، JH; یون، آی جی. کانگ، سی. لی، سی. تجزیه و تحلیل فنوتیپی و ژنوتیپی یک سویه ویروس سندرم تنفسی و تولید مثلی خوک ضعیف شده پس از پاساژهای سریالی در ماکروفاژهای آلوئولی خوک کشت شده. J. Vet. علمی 2018، 19، 358-367. [CrossRef] [PubMed]
7. زبروسکا، ا. اسکورونک، آ. ووژاکوفسکا، ا. ویدلاک، پ. Pietrowska، M. متابولوم اگزوزوم ها: تمرکز بر وزیکول های آزاد شده توسط سلول های سرطانی و موجود در مایعات بدن انسان. بین المللی جی. مول. علمی 2019, 20, 3461. [CrossRef]
8. ببلمن، نماینده مجلس; اسمیت، ام جی; Pegtel، DM; Baglio، SR بیوژنز و عملکرد وزیکول های خارج سلولی در سرطان. فارماکول. آنجا 2018، 188، 1-11. [CrossRef]
9. Zaborowski، نماینده پارلمان; بالاج، ل. بریکفیلد، XO; Lai، CP وزیکول های خارج سلولی: ترکیب، ارتباط بیولوژیکی، و روش های مطالعه. Bioscience 2015، 65، 783-797. [CrossRef]
10. المغلیق، ف.ب. Koh، YQ; پیریس، HN; واسوانی، ک. هلند، او. مایر، اس. Roche, JR; بورک، CR; Crookenden، MA; Arachchige، BJ; و همکاران اگزوزوم های در گردش ممکن است نشانگرهای زیستی را برای گاوهایی که در معرض خطر اختلال متابولیک هستند شناسایی کنند. علمی نسخه 2019، 9، 13879. [CrossRef]
11. ژانگ، آرسی; Du، WQ; ژانگ، جی. یو، اس ایکس; Lu، FZ; دینگ، اچ ام. چنگ، YB; رن، سی. درمان سلول های بنیادی مزانشیمی Geng، DQ برای آسیب عصب محیطی: مروری روایی. نورال ریجن. Res. 2021، 16، 2170–2176. [PubMed]
12. Bryzgunova، OE; زریپوف، م.م. اسکورتسوا، تی. لکچنوف، EA؛ گریگورووا، AE; Zaporozhchenko، IA; موروزکین، ES; ریابچیکووا، EI; یورچنکو، YB؛ Voitsitskiy، VE; و همکاران بررسی مقایسه ای وزیکول های خارج سلولی از ادرار افراد سالم و بیماران مبتلا به سرطان پروستات. PLoS ONE 2016, 11, e0157566. [CrossRef] [PubMed]
13. کاموسی، جی. Deregibus، MC; برونو، اس. گرانج، سی. فونساتو، وی. تتا، سی. برنامه ریزی مجدد اپی ژنتیکی سلول ها با واسطه اگزوزوم/میکرووزیکول. صبح. J. Cancer Res. 2011، 1، 98-110. [PubMed]
14. Tamkovich، SN; توتانوف، سیستم عامل؛ Laktionov، PP Exosomes: تولید، ساختار، انتقال، فعالیت بیولوژیکی و کاربرد تشخیصی. بیوشیمی. Mosc تامین سر. عضو. سلول بیول. 2016، 10، 163-173. [CrossRef]
15. Bartel، DP MicroRNAs: ژنومیک، بیوژنز، مکانیسم و عملکرد. سلول 2004، 116، 281-297. [CrossRef]
16. گوردینو، جی. کاستا پریرا، اس. کوردیرا، پی. آلوز، پی. کاستا، ال. Gomes، AQ; سیلوا سانتوس، بی. Ribot، JC MicroRNA{3}}a تمایز سلول T T انسان را با هدف قرار دادن Map3k2 و Notch2 محدود می کند. EMBO Rep. 2022, 23, e52234. [CrossRef]
17. لیو، بی. یان، ال. چی، ی. سان، ی. Yang, X. RNA غیر کدکننده طولانی AFAP1-AS1 با تنظیم محور miR-107/PDK4 پیشرفت سرطان تخمدان را تسهیل میکند. J. Ovarian Res. 2021، 14، 60. [CrossRef]
18. کیم، ی. لی، دی اچ. پارک، SH; جئون، تی. یونگ، CH تأثیر متقابل microRNAها و فاکتورهای رونویسی در تنظیم اتوفاژی در بیماری کبد چرب غیر الکلی. انقضا مول. پزشکی 2021، 53، 548-559. [CrossRef]
19. Kazmierczak، D. جوپک، ک. استرزینسکا، ک. نوویکی، ام. روچینسکی، ام. Januchowski، R. مشخصات بیان microRNA و نقش بالقوه در تنظیم ژن های مقاوم به دارو در رده های سلولی سرطان تخمدان مقاوم به سیس پلاتین و پاکلیتاکسل. بین المللی جی. مول. علمی 2022، 23، 526. [CrossRef]
20. گونگ، ی. وی، ایکس. سان، دبلیو. رن، ایکس. چن، جی. آویا، جی جی؛ ما، اچ. چان، KG; ژانگ، ی. Li، S. miR اگزوزومی-224 در هموستاز میکروبیوتای همولنف در طول عفونت باکتریایی در سخت پوستان نقش دارد. PLoS Pathog. 2021, 17, e1009837. [CrossRef]
21. چنگ، ی. کو، دبلیو. زو، دی. یو، ایکس. Zhu، Y. جهت های آینده در تشخیص، پیش آگهی و نظارت بر بیماری کارسینوم قشر آدرنال: نشانگرهای زیستی غیر تهاجمی جدید. جلو. اندوکرینول. 2022, 12, 811293. [CrossRef] [PubMed]
22. گالو، ا. تاندون، ام. Alevizos، I. Illei، GG اکثر میکروRNA های قابل تشخیص در سرم و بزاق در اگزوزوم ها متمرکز شده اند. PLoS ONE 2012, 7, e30679. [CrossRef] [PubMed]
23. فن، بی. چوپ، ام. ژانگ، ZG; Liu, XS نقشهای نوظهور microRNAها به عنوان نشانگرهای زیستی و اهداف درمانی برای نوروپاتی دیابتی. جلو. نورول. 2020, 11, 558758. [CrossRef] [PubMed]
24. وی، اچ. چن، کیو. لین، ال. شا، سی. لی، تی. لیو، ی. یین، ایکس. خو، ی. چن، ال. گائو، دبلیو. و همکاران تنظیم تولید اگزوزوم و مرتب سازی محموله. بین المللی جی. بیول. علمی 2021، 17، 163-177. [CrossRef]
25. جیا، X. بی، ی. لی، جی. Xie، Q. یانگ، اچ. Liu, W. MiR RNA سلولی{1}a با فعال کردن ایمنی ضد ویروسی ذاتی، تکثیر ویروس سندرم تنفسی و تولیدمثلی خوک را سرکوب میکند. علمی Rep. 2015, 5, 10651. [CrossRef]
26. لی، ال. وی، ز. ژو، ی. جیانگ، ی. یو، ال. ژنگ، اچ. تانگ، دبلیو. یانگ، اس. ژنگ، اچ. شان، تی. و همکاران میزبان miR-26a تکثیر ویروس سندرم تناسلی و تنفسی خوک را با تنظیم دخیل اینترفرون های نوع I سرکوب می کند. ویروس Res. 2015، 195، 86–94. [CrossRef]
27. لیو، اف. وانگ، اچ. دو، ال. وی، ز. ژانگ، کیو. Feng، WH MicroRNA{1}}c زنجیره بتا گیرنده اینترفرون-آلفا/بتا را برای ترویج عفونت PRRSV نوع 2 هدف قرار میدهد. جی ژنرال ویرول. 2018، 99، 1671-1680. [CrossRef]
28. ژانگ، ق. هوانگ، سی. یانگ، کیو. گائو، ال. لیو، HC; تانگ، جی. Feng، WH MicroRNA{1}}c پاسخهای IFN نوع I را تعدیل میکند تا با هدف قرار دادن JAK1، عفونت ویروسی سندرم تنفسی و تولیدمثلی خوک را تسهیل کند. J. Immunol. 2016، 196، 2272-2282. [CrossRef]
29. وانگ، دی. کائو، ال. خو، ز. نیش، ال. ژونگ، ی. چن، کیو. لو، آر. چن، اچ. لی، ک. Xiao, S. MiR-125b با تنظیم منفی مسیر NF-kB، تکثیر ویروس های سندرم تنفسی و تولید مثل خوک را کاهش می دهد. PLoS ONE 2013, 8, e55838. [CrossRef]
30. ژانگ، کیو. Guo، XK; گائو، ال. هوانگ، سی. لی، ن. جیا، ایکس. لیو، دبلیو. Feng، WH MicroRNA{1}} با هدف قرار دادن مستقیم PRRSV RNA و احتمالاً با تنظیم مجدد اینترفرون های نوع I، تکثیر PRRSV را مهار می کند. ویروس شناسی 2014، 450-451، 182-195. [CrossRef]
31. وو، ج. پنگ، ایکس. ژو، ا. کیائو، م. وو، اچ. شیائو، اچ. لیو، جی. ژنگ، ایکس. ژانگ، اس. Mei، S. MiR{1}} از طریق CD151 از تکثیر PRRSV در سلولهای MARC-145 جلوگیری میکند. مول. سلول. بیوشیمی. 2014، 394، 275-281. [CrossRef]
32. گائو، ال. Guo، XK; وانگ، ال. ژانگ، کیو. لی، ن. چن، XX; وانگ، ی. Feng، WH MicroRNA 181 با هدف قرار دادن گیرنده PRRSV CD163، عفونت ویروس باروری و تنفسی خوک (PRRSV) را سرکوب می کند. جی. ویرول. 2013، 87، 8808-8812. [CrossRef]
33. شیائو، اس. دو، تی. وانگ، ایکس. نی، اچ. یان، ی. لی، ن. ژانگ، سی. ژانگ، ا. گائو، جی. لیو، اچ. و همکاران MiR{1}} با هدف قرار دادن عامل میزبان HO{2}} تکثیر ویروس سندرم تنفسی و تولیدمثلی خوک را ترویج میکند. دامپزشک میکروبیول. 2016، 192، 226-230. [CrossRef]
34. شیائو، اس. وانگ، ایکس. نی، اچ. لی، ن. ژانگ، ا. لیو، اچ. Pu، F. خو، ال. گائو، جی. ژائو، کیو. و همکاران MicroRNA miR{1}}p تکثیر ویروس های سندرم تنفسی و تولید مثل خوک را از طریق سرکوب بیان هم اکسیژناز-1 ترویج می کند. جی. ویرول. 2015، 89، 4494-4503. [CrossRef]
35. باتلر، جی. سینکورا، م. وانگ، جی. استپانووا، ک. لی، ی. Cai، X. اختلال در رشد تیموسیت زمینه همه گیری PRRS: یک فرضیه قابل آزمایش است. جلو. ایمونول. 2019، 10، 1077. [CrossRef]
36. ژو، ال. وانگ، ز. دینگ، ی. استپانووا، ک. لی، ی. Cai، X. NADC{1}}شبیه ویروس سندرم تنفسی و تولید مثل خوک، چین. ظهور. آلوده کردن دیس 2015، 21، 2256-2257. [CrossRef]
37. ژو، ال. یانگ، بی. خو، ال. جین، اچ. Ge، X. گوا، ایکس. هان، جی. یانگ، اچ. ارزیابی اثربخشی سه واکسن ویروس زنده اصلاحشده علیه سویهای از ویروسهای تولید مثلی و تنفسی خوک مانند NADC30-. دامپزشک میکروبیول. 2017، 207، 108-116. [CrossRef]
38. وانگ، ن. وانگ، X. miRDB: یک منبع آنلاین برای پیشبینی هدف microRNA و حاشیهنویسیهای عملکردی. Nucleic Acids Res. 2015، 43، D146–D152. [CrossRef]
39. Friedländer, MR; Mackowiak، SD; لی، ن. چن، دبلیو. Rajewsky، N. miRDeep2 به دقت صدها ژن microRNA جدید را در هفت کلاد حیوانی شناسایی می کند. Nucleic Acids Res. 2012، 40، 37-52. [CrossRef]
40. ون، م. شن، ی. شی، س. Tang, T. miREvo: یک پلت فرم تجزیه و تحلیل تکاملی microRNA یکپارچه برای آزمایش های توالی یابی نسل بعدی. BMC Bioinform. 2012، 13، 140. [CrossRef]
41. اندرس، اس. Huber, W. تجزیه و تحلیل بیان دیفرانسیل برای داده های تعداد توالی. ژنوم بیول. 2010، 11، R106. [CrossRef] [PubMed]
42. تامورا، ک. استچر، جی. Kumar, S. MEGA11: Molecular evolutionary Genetic Analysis نسخه 11. Mol. Biol. تکامل. 2021، 38، 3022-3027. [CrossRef] [PubMed]
43. Hubisz، MJ; پولارد، KS; Siepel، A. PHAST و RPHAST: تجزیه و تحلیل فیلوژنتیک با مدلهای فضا/زمان. مختصر. بیوانفورم. 2011، 12، 41-51. [CrossRef] [PubMed]
44. کروگر، ج. Rehmsmeier، M. RNAhybrid: پیشبینی هدف microRNA آسان، سریع و انعطافپذیر است. Nucleic Acids Res. 2006، 34، W451–W454. [CrossRef]
45. یو، جی. وانگ، ال جی؛ هان، ی. او، QY clusterProfiler: یک بسته R برای مقایسه مضامین بیولوژیکی در میان خوشههای ژنی. OMICS 2012، 16، 284-287. [CrossRef]
46. کوئه، ر. دینگ، جی. چن، جی. Cao، L. تجزیه و تحلیل microRNA های اگزوزومی سرم و ویژگی های بالینی پاتولوژیک بیماران مبتلا به آدنوکارسینوم پانکراس. جهانی جی. سرگ. اونکول. 2013، 11، 219. [CrossRef]
47. Théry, C.; Witwer، KW; آیکاوا، ای. الکاراز، ام جی; اندرسون، جی دی. اندریانتسیتوهاینا، آر. آنتونیو، ا. عرب، ت. آرچر، اف. اتکین اسمیت، جی.کی. و همکاران حداقل اطلاعات برای مطالعات وزیکول های خارج سلولی 2018 (MISEV2018): بیانیه موضع انجمن بین المللی برای وزیکول های خارج سلولی و به روز رسانی دستورالعمل های MISEV2014. J. Extracell. Vesicles 2018, 7, 1535750. [CrossRef]
48. لیو، ک.- س. چوی، جی. هان، TW; پارک، KT; Kim, HK اثر واکسیناسیون با واکسن اصلاح شده تولید مثلی و ویروسی سندرم تنفسی خوک زنده بر عملکرد رشد در خوک های پروار در شرایط مزرعه. J. Vet. پزشکی علمی 2016، 78، 1533-1536. [CrossRef]
49. بیان، تی. سان، ی. هائو، ام. ژو، ال. Ge، X. گوا، ایکس. هان، جی. یانگ، H. یک ویروس سندرم تنفسی و تولیدمثلی خوک نوترکیب نوع 2 بین NADC30-شبیه و شبه MLV: خصوصیات ژنتیکی و بیماری زایی برای خوکها. آلوده کردن ژنت تکامل. 2017، 54، 279-286. [CrossRef]
50. لی، ی. جی، جی. وانگ، جی. تان، اف. ژوانگ، جی. لی، ایکس. Tian، K. توالی ژنوم کامل یک NADC30-مثل ویروسهای سندرم تنفسی و تولید مثل خوک که با ترکیب مجدد با سویههای دیگر مشخص میشود. ژنوم اعلام کرد. 2016، 4، e{4}}. [CrossRef]
51. کلوری، ر. Lebleu، VS بیولوژی، عملکرد و کاربردهای زیست پزشکی اگزوزوم ها. Science 2020, 367, eaau6977. [CrossRef] [PubMed]
52. Miao، XY پیشرفت های اخیر در درک نقش miRNA ها در اگزوزوم ها و پتانسیل درمانی آنها. جی. اینتگر. کشاورزی 2017، 16، 753-761. [CrossRef]
53. Shenoda، BB; Ajit، SK تعدیل پاسخ های ایمنی توسط اگزوزوم های مشتق شده از سلول های ارائه دهنده آنتی ژن. کلین. پزشکی راهنما بینش. 2016, 9 (Suppl. S1), CPath-S39925. [CrossRef] [PubMed]
54. لی، س. لی، اس. وو، اس. Chen, L. Exosomes تکثیر ویروس و پاسخ های ایمنی میزبان را در عفونت HBV تعدیل می کنند. BioMed Res. بین المللی 2019، 2019، 2103943. [CrossRef]
55. گرینینگ، DW; گوپال، SK; خو، آر. سیمپسون، RJ; Chen, W. Exosomes و نقش آنها در تنظیم ایمنی و سرطان. در سمینارهای زیست شناسی سلولی و تکاملی؛ مطبوعات دانشگاهی: کمبریج، MA، ایالات متحده آمریکا، 2015; جلد 40، ص 72–81.
56. هویت، جی. هیل، اگزوزوم های AF در آسیب شناسی بیماری های عصبی. جی. بیول. شیمی. 2016، 291، 26589–26597. [CrossRef]
57. ریبیرو، MF; زو، اچ. Millard, RW; فن، G. اگزوزوم ها در پرو و ضد رگ زایی عمل می کنند. Curr. آنژیوژنز 2013، 2، 54-59. [CrossRef]
58. لان، ج. سان، ال. خو، اف. لیو، ال. هو، اف. آهنگ، دی. هو، ز. وو، دبلیو. لو، ایکس. وانگ، جی. و همکاران اگزوزوم های مشتق شده از ماکروفاژ M2 باعث مهاجرت و تهاجم سلولی در سرطان روده بزرگ می شود. سرطان Res. 2019، 79، 146-158. [CrossRef]
59. آقا، م. بنتز، جی ال. رافا، س. توریسی، MR; کوندو، اس. واکیساکا، ن. یوشیزاکی، تی. پاگانو، JS؛ Shackelford، J. Exosomal HIF1 از پتانسیل تهاجمی از اگزوزوم های مثبت LMP مرتبط با کارسینوم نازوفارنکس پشتیبانی می کند. Oncogene 2014، 33، 4613-4622. [CrossRef]
60. فو، م. وانگ، بی. چن، ایکس. او، ز. وانگ، ی. لی، ایکس. کائو، اچ. Zheng، SJ gga-miR{2}} تکثیر ویروس بیماری بورس عفونی (IBDV) را از طریق هدف قرار دادن مستقیم بخش ژنومی IBDV B و سرکوبگرهای سلولی سیگنالینگ سیتوکین 6 (SOCS6) سرکوب میکند. ویروس Res. 2018، 252، 29-40. [CrossRef]
61. فو، م. وانگ، بی. چن، ایکس. او، ز. وانگ، ی. لی، ایکس. کائو، اچ. Zheng, SJ MicroRNA gga-miR-130b تکثیر ویروس بیماری بورس عفونی را از طریق هدف قرار دادن ژنوم ویروسی و سرکوبگرهای سلولی سیگنال دهی سیتوکین سرکوب می کند. 5. J. Virol. 2018، 92، e01646-17. [CrossRef]
62. Guo، XK; ژانگ، کیو. گائو، ال. لی، ن. چن، XX; فنگ، WH افزایش بیان microRNA 181 از تکثیر ویروس سندرم تنفسی و تولید مثل خوک جلوگیری می کند و پیامدهایی برای کنترل عفونت ویروسی دارد. جی. ویرول. 2013، 87، 1159-1171. [CrossRef] [PubMed]
63. Cong، P. شیائو، اس. چن، ی. وانگ، ال. گائو، جی. لی، ام. او، ز. گوا، ی. ژائو، جی. ژانگ، ایکس. و همکاران رونوشتهای miRNA و mRNA یکپارچه ماکروفاژهای آلوئولی خوک (سلولهای PAM) امضاهای مولکولی miRNA سویه خاص مرتبط با عفونت H-PRRSV و N-PRRSV را شناسایی میکنند. مول. Biol. 2014، 41، 5863-5875. [CrossRef] [PubMed]
64. لی، ن. هوانگ، ک. چن، ی. هوانگ، ز. ژانگ، ی. لنگ، سی. لیو، ی. شی، ج. شیائو، اس. یائو، ال. دامپزشک میکروبیول. 2021, 261, 109216. [CrossRef] [PubMed]
65. لی، ن. دو، تی. یان، ی. ژانگ، ا. گائو، جی. هو، جی. شیائو، اس. Zhou، EM MicroRNA اجازه میدهد-7f-5p با هدف قرار دادن MYH9، ویروس سندرم تولیدمثلی و تنفسی خوک را مهار کند. علمی Rep. 2016, 6, 34332. [CrossRef]
66. ژن، ی. وانگ، اف. لیانگ، دبلیو. لیو، جی. گائو، جی. وانگ، ی. خو، X. سو، کیو. ژانگ، کیو. لیو، B. شناسایی RNA غیر کد کننده متفاوت بیان شده در ماکروفاژهای آلوئولی خوک از Tongcheng و خوک های سفید بزرگ به PRRSV پاسخ دادند. علمی Rep. 2018, 8, 15621. [CrossRef]
67. ژو، ایکس. مایکل، جی جی; جیانگ، ز. لیو، B. پروفایل بیان MicroRNA در ماکروفاژهای آلوئولی خوکهای بومی چینی Tongcheng آلوده به PRRSV در داخل بدن. J. Appl. ژنت 2017، 58، 539-544. [CrossRef]
68. لی، YJ; لی، سی. تکثیر ویروس سندرم تنفسی و تولید مثلی خوک با مهار مسیر سیگنالینگ کیناز تنظیم شده با سیگنال خارج سلولی (ERK) سرکوب می شود. ویروس Res. 2010، 152، 50-58. [CrossRef]
69. آهنگ، س. بی، جی. وانگ، دی. نیش، ال. ژانگ، ال. لی، اف. چن، اچ. عفونت ویروسی سندرم تنفسی و تولید مثلی Xiao، S. خوک، تولید IL-10 را از طریق مسیرهای NF-κB و p38 MAPK در ماکروفاژهای آلوئولی خوک فعال میکند. توسعه دهنده Comp. ایمونول. 2013، 39، 265-272. [CrossRef]
70. یین، اس. هوو، ی. دونگ، ی. فن، ال. یانگ، اچ. وانگ، ال. نینگ، ی. هو، H. فعال سازی c-Jun NH (2) - ترمینال کیناز برای آپوپتوز ناشی از ویروس سندرم تنفسی و تولید مثل خوک مورد نیاز است اما برای تکثیر ویروس نه. ویروس Res. 2012، 166، 103-108. [CrossRef]
71. Fan, L. مسیرهای سیگنال دهی درگیر در تنظیم القای آپوپتوز در سلول های میزبان بر اثر عفونت PRRSV. ژن های ویروس 2019، 55، 433-439. [CrossRef]
72. لوپز-فورتس، ال. کامپوس، ای. دومنک، ن. ازکورا، ا. کاسترو، جی.ام. دومینگز، جی. آلونسو، F. ویروس سندرم تناسلی و تنفسی خوک (PRRS) تولید TNF- را در ماکروفاژهای آلوده تعدیل می کند. ویروس Res. 2000، 69، 41-46. [CrossRef]
73. Teissier، É. Pécheur، EI لیپیدها به عنوان تعدیل کننده های همجوشی غشایی با واسطه پروتئین های همجوشی ویروسی. یورو بیوفیز. J. 2007, 36, 887-899. [CrossRef]
74. جئون، ج. لی، سی. کلسترول سلولی برای عفونت نیدوویروس خوک مورد نیاز است. قوس. ویرول. 2017، 162، 3753-3767. [CrossRef]
75. سان، ی. شیائو، اس. وانگ، دی. لو، آر. لی، بی. چن، اچ. Fang, L. کلسترول غشای سلولی برای ورود و انتشار ویروس سندرم تنفسی و تولید مثل خوک در سلولهای MARC{1}} مورد نیاز است. علمی China Life Sci. 2011، 54، 1011-1018. [CrossRef]
76. تیان، تی. زو، ی.ال. ژو، YY; لیانگ، جی اف. وانگ، YY; هو، FH; جذب اگزوزوم Xiao، ZD از طریق اندوسیتوز و ماکروپینوسیتوز با واسطه کلاترین و انتقال miR{2}}. جی. بیول. شیمی. 2014، 289، 22258–22267. [CrossRef]
77. Mulcahy، LA; صورتی، RC; Carter، DRF مسیرها و مکانیسم های جذب وزیکول خارج سلولی. J. Extracell. Vesicles 2014, 3, 24641. [CrossRef]
78. ژانگ، م. زنگ، ایکس. وانگ، ام. لی، ز. کیائو، م. متعجب.؛ چن، دی. نانوحامل های مبتنی بر اگزوزوم به عنوان وسایل نقلیه الهام گرفته از زیستی و همه کاره برای تحویل دارو: پیشرفت ها و چالش های اخیر. جی. ماتر. شیمی. B 2019, 7, 2421–2433. [CrossRef]






