استفاده از نشانگرهای زیستی غیر متعارف در تشخیص اولیه آسیب حاد کلیه در نوزادان نارس مبتلا به سپسیس
Jul 11, 2022
خلاصه
آسیب حاد کلیه (AKI) یک یافته رایج در واحدهای مراقبت ویژه نوزادان (NICU) است. سپسیس یکی از علل اصلی AKI در نوزادان نارس است. AKI با نرخ مرگ و میر قابل توجهی همراه است. تشخیص زودهنگام این بیماری اولین قدم برای بهبود پیشگیری، درمان و نتایج است، در حالی که طول مدت بستری، هزینه های مراقبت و مرگ و میر را کاهش می دهد. AKI ممکن است به بیماری مزمن کلیه (CKD) پیشرفت کند، وضعیتی که با دیالیز و خطر بیشتر بیماری قلبی عروقی مرتبط است. این مقاله مروری با هدف بحث در مورد موارد AKI در نوزادان نارس مبتلا به سپسیس، استفاده از نشانگرهای زیستی در کار آزمایشگاهی، و استفاده از نشانگرهای زیستی غیر متعارف برای شناسایی اولیه AKI است. كليد واژه ها: آسيب حاد كليه; سپسیس نوزاد، نارس؛ نشانگرهای زیستی

برای خرید سیستانچ برای آسیب کلیه کلیک کنید
مقدمه
آسیب حاد کلیه (AKI) به عنوان اختلال ناگهانی در عملکرد کلیه و به دنبال آن افزایش حاد قابل برگشت در کراتینین سرم (SCr) مرتبط یا بدون کاهش برون ده ادرار، که منجر به ناتوانی در حفظ هموستاز مناسب مایعات، الکترولیت ها و باقیمانده ها می شود، تعریف می شود. این یک اختلال چند عاملی پیچیده است که از آسیب خفیف تا نارسایی کلیه را در بر می گیرد که ممکن است برای آن درمان جایگزین کلیوی مورد نیاز باشد. AKI را می توان به صورت زیر طبقه بندی کرد: (i) AKI پیش کلیه، وضعیتی ناشی از هیپوولمی، انقباض شریان کلیوی، یا اتساع عروق که ممکن است باعث اختلال پرفیوژن گلومرولی ثانویه به کاهش حجم گردش خون بدون تغییرات کلیوی شود. (ii) AKI کلیه، وضعیتی که توسط سایر انواع بیماری کلیوی، از جمله بیماری مویرگی و گلومرولی، بیماری کلیه عروقی، نفریت بینابینی حاد، و نکروز حاد لولهای ایجاد میشود. و (iii) AKI پس کلیوی، وضعیتی که در موارد انسداد حاد ادرار مشاهده می شود. علل AKI در نوزادان شامل وزن بسیار کم هنگام تولد (وزن بدن کمتر از 1500 گرم)، سندرم دیسترس تنفسی، نمره آپگار کم 5- دقیقه، لوله گذاری در بدو تولد، ایست قلبی و استفاده از دارو می باشد.
نویسندگان
جویسیلن داسیلوا باربوسا 1
جرالدو بزرا داسیلوا جونیور2
Gdayllon Cavalcante Meneses3
آلیس ماریا کاستا مارتینز3
الیزابت دی فرانچسکو داهر3
روزانجلا پینیرو گونسالوز
ماچادو4
روملیا پینیرو گونسالوز
Lemes3
1Universidade Federal do Ceará،Programa de Pós-Graduação emPatologia، Fortaleza، CE، برزیل.
2Universidade de Fortaleza، Centrode Ciências da Saúde، Faculdadede Medicina، Programa de PósGraduação em Saúde Pública،فورتالزا، CE، برزیل.
3Universidade Federal doCeará، Faculdade de Farmácia،Departamento de AnalisesClínicas e Toxicológicas، Fortaleza،CE، برزیل
4Universidade de Fortaleza، Centrode Ciências da Saúde، Faculdadede Medicina، Fortaleza، CE، برزیل.
از نظر زیر گروه های خطر، نوزادان نارس (با سن حاملگی [GA] کمتر از 37 هفته) را می توان به صورت زیر دسته بندی کرد: بسیار نارس - نوزادان متولد شده قبل از هفته 28 بارداری. بسیار نارس - نوزادانی که بین 28 هفته تا 31 هفته و 6 روز بارداری متولد می شوند. نارس متوسط - نوزادانی که بین 32 هفته تا 33 هفته و 6 روز بارداری متولد می شوند. یا دیررس نارس - نوزادانی که بین 34 هفته تا 36 هفته و 6 روز بارداری متولد می شوند. AKI یک بیماری شایع در بخش مراقبت های ویژه نوزادان است که با افزایش مرگ و میر همراه است. یوسف و همکاران (2015) فراوانی 10.8 درصد را برای AKI در بخش مراقبت های ویژه نوزادان (NICU) گزارش کرد و استفاده از تهویه مکانیکی و سپسیس را به عنوان علل اصلی AKI9 توصیف کرد. سپسیس نوزادی عفونتی است که در 28 روز اول زندگی یک نوزاد نارس یا در عرض چهار هفته از تاریخ پیشبینیشده تولد نوزادان نارس رخ میدهد. سپسیس نوزادی یک عارضه شدید به ویژه برای نوزادان نارس است که توسط عوامل بیماری زا پس از تولد ایجاد می شود. این وضعیت به عنوان سپسیس زودرس برای مواردی که در 72 ساعت پس از تولد شروع می شود یا سپسیس دیررس برای مواردی که بعد از 72 ساعت از تولد ایجاد می شود، توصیف می شود.
علائم بالینی سپسیس نوزادان عبارتند از تب، هیپوترمی، هیپوتونی و تشنج، تحریک پذیری و بی حالی، مشکل در تنفس، رنگ پریدگی، علائم گوارشی، زردی ایدیوپاتیک، علائم خونریزی و تاکی کاردی 10،12. زایمان زودرس ممکن است بر سازگاری با زندگی خارج رحمی تأثیر منفی بگذارد و عوارض متعددی را به همراه داشته باشد. عواملی مانند کاهش نرخ فیلتراسیون گلومرولی (GFR)، انقباض عروق کلیوی، و کاهش جریان خون موضعی ممکن است در شروع AKI در افراد مبتلا به سپسیس نقش داشته باشند، وضعیتی که به دلیل پاتوفیزیولوژی چندعاملی آن شامل مکانیسمهای همودینامیک و میکروسیرکولاسیون است که در نهایت منجر به اکسیژنرسانی ضعیف بافت میشود. . وازوپلژی اولین پدیده پاتوفیزیولوژیک در افراد مبتلا به شوک سپتیک است که باعث افت فشار خون می شود{3}}. افراد مبتلا به AKI سپتیک نیز با کاهش GFR ثانویه به افت فشار خون و هیپوولمی همراه با کاهش برون ده قلبی، که باعث الیگوری و افزایش سطح SCr می شود، مراجعه می کنند. شمارش کامل خون یکی از آزمایشاتی است که در بررسی سپسیس استفاده می شود. واکنشدهندههای فاز حاد مانند پروتئین واکنشگر C (CRP) و پروکلسیتونین (PCT) ممکن است در تشخیص مورد استفاده قرار گیرند، اگرچه کشت خون به عنوان توصیهشدهترین آزمایش است. در تلاشی برای استانداردسازی تعاریف و مقولههای مرتبط با تشخیص AKI، معیارهای ریسک، آسیب، شکست، از دست دادن، مرحله پایانی (RIFLE) و شبکه آسیب حاد کلیه (AKIN) بر اساس پارامترهای SCr و برون ده ادرار17 توسعه یافتند. با این حال، معیارهای مورد استفاده برای تعریف AKI از آن زمان تعدیل شده اند و جدیدترین نسخه بیماری کلیوی: بهبود نتیجه جهانی (KDIGO) است که در سال 201218 منتشر شد.

در سال 2013 تغییراتی برای محاسبه جمعیت نوزادان در معیارها انجام شد. مطالعه ای که شامل مؤسسه ملی بهداشت، متخصصان نوزادان، نفرولوژیست ها، متخصصان اطفال و نمایندگان مؤسسه ملی دیابت و بیماری های گوارشی و کلیوی بود، منجر به انتشار طبقه بندی KDIGO شد. برای نوزادان 19. معیارهای KDIGO برای توصیف بهتر AKI در نوزادان 20 به روز شد (جدول 1). هدف این بررسی بررسی AKI در نوزادان نارس مبتلا به سپسیس و بیومارکرهای کارآپ مورد استفاده در تشخیص، پیش آگهی و پیگیری افراد مبتلا به AKI است. به منظور افزایش درک و آگاهی از این شرایط، توجه ویژه به نشانگرهای زیستی غیر متعارف توصیف شده در مقالات اخیر داده شد.
نشانگرهای معمولی
اگرچه معیارهای جدید برای AKI تایید شده است، تشخیص هنوز دشوار است، به ویژه در نوزادان. تشخیص برای نوزادان بر اساس دو ناهنجاری عملکردی است: تغییر در SCr (نشانگر GFR) و اولیگوری، هر دو نشانگر دیررس درگیری کلیه. SCR در مورد عوامل کلیوی و غیرکلیوی محدودیت هایی دارد. در میان عوامل کلیوی، نوزادان اغلب GFR پایینی دارند و فیزیولوژی کلیه ها تا سن دو سالگی ایجاد می شود. پس از تولد و بسته به سن حاملگی، SCr نوزاد تازه متولد شده منعکس کننده مادرش است. تغییرات (یا عدم وجود تغییر) در SCr ممکن است در تشخیص AKI اختلال ایجاد کند. علاوه بر این، SCr آسیب را تخمین نمی زند، بلکه عملکرد گلومرولی را تخمین می زند و ممکن است روزها طول بکشد تا پس از وقوع آسیب افزایش یابد. جالب توجه است، سطح SCr در جمعیت عمومی ممکن است تا زمانی که 25-50 درصد از عملکرد کلیه از بین نرود، تغییر نکند. عوامل غیرکلیوی محدود کننده استفاده از SCr شامل سن، جنس، تغذیه، توده عضلانی و دارو می باشد. علاوه بر این، روشهای مختلف برای تعیین سطح کراتینین سرم - واکنش Jaffe یا روش آنزیمی - نتایج SCr متفاوتی را به همراه دارد.

محدودیتهایی در اندازهگیری برونده ادرار هنوز وجود دارد، زیرا دقت به کارکرد کاتتر ادراری و طیف وسیعی از داروها، بهویژه دیورتیکها و آمینهای وازواکتیو بستگی دارد. بیومارکر سیستاتین C (CysC) یک مهار کننده سیستئین پروتئاز است که در هر سلول هسته دار بدن انسان سنتز می شود. این به عنوان یک نشانگر درون زا برای GFR و اختلال توبولار کلیوی عمل می کند. CysC آزادانه در گلومرول ها فیلتر می شود و کاملاً بازجذب می شود و ترشح نمی شود. دفع CysC در ادرار (uCysC) با آسیب شدید حاد توبولی همراه است24،25. یک مطالعه در چین نشان داد که سطح سرمی و CysC ادرار در بیماران مبتلا به سپسیس و AKI بالاتر از سطوح مشاهده شده در بیماران مبتلا به سپسیس و بدون AKI26 بود. در بیماران مبتلا به AKI، سطح uCysC پس از افزایش سطح سرمی CysC افزایش می یابد. فانگ و همکاران (2018) دریافتند که uCysC یک نشانگر حساس AKI در نوزادان و یک پیشبینی کننده مرگ است.
نشانگرهای زیستی غیر سنتی
توجه به یافتن بهترین نشانگرهای زیستی تشخیص اولیه برای AKI داده شده است تا مداخلات توسعه یافته و نتایج بهبود یابد. بیومارکرها فرآیندهای طبیعی یا بیماری زا و سطوح پاسخ به درمان را بدون دخالت در روند بیماری شناسایی می کنند، که آنها را به ابزاری ارزشمند در ارزیابی وضعیت بیمار تبدیل می کند. آنها ممکن است برای ارزیابی تمایل به یک بیماری یا تشخیص ناهنجاریهای بیولوژیکی استفاده شوند، اگرچه اغلب در تشخیص، اندازهگیری شرایط پاتولوژیک یا پیشبینی توسعه بیماری استفاده میشوند. نشانگرهای زیستی غیر سنتی ممکن است حتی در ارزیابی پاسخ به درمان مفیدتر باشند. در حالت ایدهآل، آنها باید از طریق روشهای غیرتهاجمی (مانند جمعآوری ادرار) یا با حداقل تأثیر بر روی بیماران (مانند نمونهگیری معمولی خون) تهیه شوند. تلاشهایی برای شناسایی بیومارکرهای قابل اعتماد آسیب کلیه در سرم، پلاسما و ادرار انجام شده است. بسیاری از ویژگی های یک نشانگر ایده آل عملکرد کلیه هستند که می توان به موارد زیر اشاره کرد: آزادانه فیلتر شدن در حالی که به ماکرومولکول ها متصل نمی شود. در کلیه ها بازجذب نمی شود یا توسط لوله های کلیوی ترشح نمی شود. تولید تخمین GFR قابل اعتماد با تولید ثابت و انتشار سریع به سایت های خارج سلولی. تجزیه نمی شود یا توسط سیستم هایی غیر از کلیه ها دفع نمی شود. شناسایی و اندازهگیری با تکنیکهای آزمایشگاهی دقیق و قابل تکرار بدون دخالت عناصر دیگر؛ و مقرون به صرفه بودن30. نشانگرهای زیستی را میتوان به صورت زیر دستهبندی کرد: نشانگرهای التهابی، مانند لیپوکالین مرتبط با ژلاتیناز نوتروفیل (NGAL)، اینترلوکین-6 (IL-6)، و اینترلوکین-18 (IL{9}} ) نشانگرهای آسیب سلولی، مانند مولکول آسیب کلیه-1 (KIM-1) و پروتئین اتصال دهنده به اسید چرب نوع کبد (L-FABP). و نشانگرهای توقف چرخه سلولی، مانند بازدارنده بافتی متالوپروتئینازها 2 (TIMP2) و پروتئین متصل شونده به فاکتور رشد شبه انسولین 7 (IGFBP7)31،32 (شکل 1)

NGAL
NGAL در فرم ادراری خود (uNGAL) منحصراً از سلولهای اپیتلیال نفرون دیستال آسیب دیده منشأ میگیرد، در حالی که شکل سرمی آن (sNGAL) ممکن است از آسیب کلیه (در اثر نشت لولهای) یا اندامهای خارج کلیوی در تعامل با کلیهها ناشی شود. NGAL یک نشانگر حساس برای تشخیص زودهنگام، پیشبینی دقیق و طبقهبندی ریسک است. سطوح آن با افزایش شدت AKI افزایش می یابد. محققان چینی یک مرور سیستماتیک و متاآنالیز شامل مقالاتی در مورد استفاده از uNGAL و sNGAL در پیشبینی AKI در بیماران مبتلا به سپسیس منتشر کردند. نتایج آنها دقت تشخیصی خوبی را برای AKI در افراد مبتلا به سپسیس برای هر دو نوع نشانگر نشان داد.
IL-6
IL{0}} گسترده ترین سیتوکین مورد مطالعه در جمعیت نوزادان است. این روی پاسخ اولیه میزبان به عفونت اثر میگذارد، قبل از افزایش CRP انجام میشود و پس از انتشار فاکتور نکروز تومور آلفا (TNF) مشاهده میشود. IL{2}} در سلولهای اندوتلیال، فاگوسیتهای تک هستهای، فیبروبلاستها، آمونیاک، تروفوبلاستها و سایر سلولها بر اثر تحریک با محصولات میکروبی تولید میشود. IL{4}} یک سیتوکین چند عملکردی است که در تنظیم پاسخ ایمنی و التهاب نقش دارد. همچنین به دلیل فعالیت پیش التهابی آن شناخته شده است. IL{5}} یکی از عناصر مسئول شروع و انتشار پاسخ التهابی است و در سنتز برخی از پروتئینهای فاز حاد (APP) نقش دارد. سطح آن حدود سه ساعت پس از آسیب به اوج خود می رسد.
IL-18
IL{0}} یک سایتوکین پیش التهابی است که در سلول های اپیتلیال لوله پروگزیمال در پاسخ به آسیب تولید می شود تا سنتز اینترفرون گاما (IFN ) را تسهیل کند. پس از آسیب کلیه، IL{2}} (uIL-18) ادرار قبل از کاهش قابل توجهی در عملکرد کلیه ترشح می شود. این یک نشانگر اولیه بالقوه AKI39،40 است. مطالعه ای که روی بیماران مبتلا به چندین نوع بیماری کلیوی ثبت نام کرد، نشان داد که سطوح IL{6}} به طور قابل ملاحظه ای در این افراد افزایش یافته است و IL{7}} یک نشانگر حساس و اختصاصی برای نکروز حاد توبولار (ATN) است که نشان می دهد ممکن است نشانگر آسیب لوله پروگزیمال در افراد مبتلا به ATN باشد. نویسندگان همچنین ارتباط بین IL-18 و AKI را توصیف کردند، زیرا سطح IL{9}} قبل از افزایش SCr در بیماران مبتلا به نارسایی حاد تنفسی/سندرم زجر تنفسی حاد که AKI و آن IL را ایجاد کرده بودند به طور قابل توجهی افزایش یافته بود. }} پیش بینی کننده خوبی برای مرگ مرتبط با تهویه مکانیکی بود24.
کیم-1
مولکول آسیب کلیه ادراری{{0}} (uKIM-1) یک گلیکوپروتئین گذرنده است که در کلیهها یا ادرار سالم شناسایی نمیشود. این نشانگر آسیب اپیتلیال توبول کلیه است. سطوح ادراری آن پیش بینی کننده حساس درگیری کلیه در بیماران مبتلا به AKI است و ممکن است به عنوان شاخصی از نتایج ضعیف در غربالگری اولیه بیماران مبتلا به بیماری کلیوی استفاده شود. یک مطالعه آیندهنگر که در چین انجام شد، شامل 150 بیمار مبتلا به سپسیس بود و در میان سایر پارامترها، سطوح uKIM-1 بازماندگان و غیربازماندگان مبتلا به AKI سپتیک را مقایسه کرد. بیماران مبتلا به AKI افزایش قابلتوجهی uKIM-1 را در مدت شش ساعت تجربه کردند که سطح آن در ۲۴ ساعت به اوج خود رسید و تا ۴۸ ساعت پس از بستری شدن در ICU42 ادامه داشت. با این حال، در افراد بدون AKI، KIM{11}} در سطوح پایه در زمانهای مختلف باقی ماند، مشابه افراد سالم (0.85 ± 0.37). افراد غیربازمانده در 24 و 48 ساعت به طور قابلتوجهی سطوح بالاتری داشتند، که نشان میدهد KIM{19}} یک نشانگر زیستی اولیه مفید برای AKI سپتیک است و افزایش مداوم سطوح uKIM{20}} ممکن است با پیامدهای ضعیفتر همراه باشد.
L-FABP
L-FABP ادراری (uL-FABP) یک نشانگر زیستی امیدوارکننده آسیب توبولو بینابینی است. این تنها در سلول های اپیتلیال لوله های پروگزیمال در کلیه ها بیان می شود. آسیب لوله ای ناشی از هیپوکسی باعث افزایش سنتز L-FABP43 می شود. یک مطالعه مورد-شاهدی شامل 27 بیمار کودکی که تحت عمل جراحی بای پس قلبی ریوی (CPB) قرار گرفتند، چند یافته قابل توجه را شرح داد: در گروه مبتلا به AKI، سطح SCr در 48 ساعت به اوج خود رسید، در حالی که uL-FABP 6 ساعت پس از CPB به طور قابل توجهی افزایش یافت. و سطوح L-FABP 6 ساعت پس از CPB به طور قابل توجهی با شروع AKI مرتبط بود. این یافتهها نشان میدهد که L-FABP یک نشانگر زیستی مفید در تشخیص زودهنگام AKI است، زیرا قبل از افزایش SCr تا ساعتهای زیادی است.
TIMP-2
TIMP{0}} باعث توقف چرخه سلولی در فاز G1 میشود، مکانیزمی حیاتی در AKI32. این نشانگر زیستی توسعه AKI را پیشبینی میکند و در بیش از 1 بیمار بدحال برای طبقهبندی خطر آسیب تأیید شده است. عملکرد آن بهتر از سایر نشانگرها بوده و برای بیماران مبتلا به AKI ناشی از سپسیس بهتر در نظر گرفته شده است، اگرچه استفاده از آن برای افراد کمتر از 21 سال تایید نشده است 32،45.
IGFBP7
IGFBP7 باعث توقف چرخه سلولی در فاز G1 در سلول های لوله ای در پاسخ به آسیب می شود. با AKI32,45 همراه بوده است. IGFBP7 یک نشانگر زیستی جدید برای AKI در نظر گرفته می شود. در پیشبینی AKI متوسط تا شدید در طی حداکثر 12 ساعت پس از جمعآوری نمونه، از سایر نشانگرهای زیستی بهتر عمل کرده است. همچنین به نظر می رسد که IGFBP7 در بیماران جراحی بهتر از TIMP-2 عمل کند. با این حال، استفاده از آن برای افراد کمتر از 21 سال تایید نشده است32،45.
Syndecan-1
Syndecan-1 عضوی از خانواده پروتئوگلیکان های گذرنده است که به طور مداوم زنجیره های سولفات هپاران را در ساختار خود بدون بقایای سیستئین ارائه می دهد. در بافت های بالغ، بیشتر در سلول های اپیتلیال ساده، سلول های طبقه بندی شده و سلول های پلاسما بیان می شود. مفهوم آسیب اندوتلیال به عنوان یک پیشبینیکننده اولیه AKI در موارد لپتوسپیروز، که در آن سطوح سندیکان{3}} با آسیب گلیکوکالیکس اندوتلیال کلیه مرتبط بود، توصیف شد، یافتهای که به دلیل ارتباط آن با AKI48 شناخته شده است. مطالعه ای که در آن بیومارکرهای مختلف اندوتلیال مورد تجزیه و تحلیل قرار گرفت، نشان داد که syndecan{5}}، یک نشانگر زیستی اختلال عملکرد گلیکوکالیکس اندوتلیال، به شدت با AKI شدید در بیماران ICU در حال بیماری مرتبط است.
نفرین
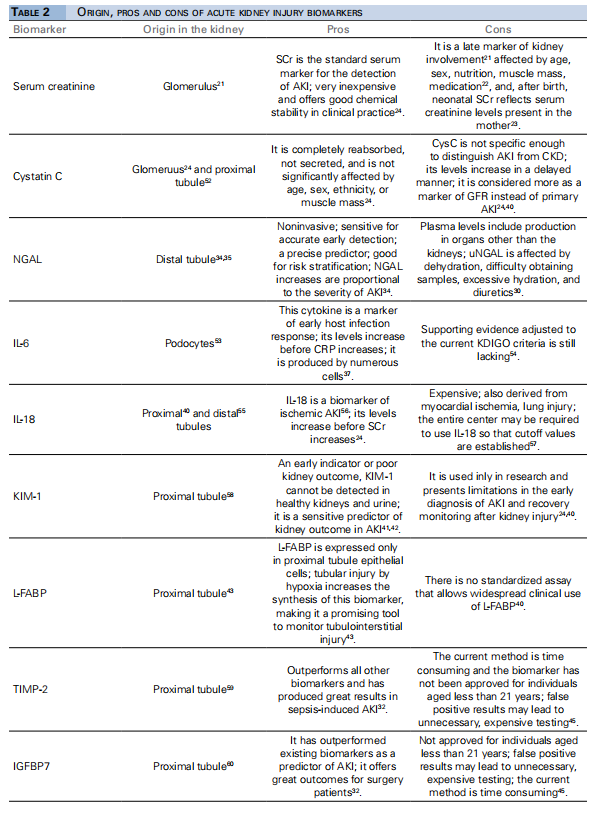
نفرین یک پروتئین غشایی است که در پودوسیت های گلومرولی بیان می شود. تغییرات اولیه ساختار پودوسیت با جدا شدن پودوسیت ها از غشای پایه گلومرولی مشخص می شود. در صورت تداوم شرایط ممکن است این تغییرات باعث آسیب شدید و مداوم گلومرولی شود. بنابراین، تشخیص زودهنگام آسیب پودوسیت اهمیت زیادی دارد. نفرین ادرار ممکن است به یک بیومارکر مهم آسیب اولیه گلومرولی تبدیل شود. مشخص نیست که آیا آسیب گلومرولی در مراحل اولیه AKI نوزاد ایجاد شده است یا خیر. یک مطالعه بر روی نوزادان نفرین ادراری را بهعنوان نشانگر زیستی بلوغ و آسیب گلومرولی توصیف کرد که به طور قابلتوجهی با ایجاد AKI و مرگ در NICU مرتبط است. جدول 2 خلاصه ای از داده های نشانگر زیستی ارائه شده در این بررسی را نشان می دهد.

بحث
The number of reports describing the uses of NGAL in diagnosing AKI has grown steadily. Nga et al. (2015) looked into the development of AKI secondary to sepsis and found that uNGAL was a great predictor of injury within the next 48 hours, with high sensitivity (> 75%) and specificity (>65 درصد)65. مطالعه ای روی 50 نوزاد مبتلا به AKI که در NICU بیمارستان کودکان دانشگاه اسکوپیه، مقدونیه، ثبت نام کردند، بروز، عوامل خطر و اثربخشی NGAL را در تشخیص زودهنگام AKI نوزادان تجزیه و تحلیل کردند. این مطالعه اعتبار بیومارکر را در تشخیص زودرس AKI در نوزادان به شدت بیمار تایید کرد.
NGAL - در اشکال سرمی و ادراری - یک نشانگر امیدوارکننده با نتایج مطلوب توصیف شده در تشخیص و ارزیابی خطر AKI است که می تواند در موارد سپسیس و AKI نوزادان نیز مورد استفاده قرار گیرد. از نظر سیتوکین ها، ادبیات نشان می دهد که سطوح سرمی IL{2}} ممکن است با عفونت - پنومونی، پریتونیت باکتریایی، و عفونت دستگاه ادراری (UTI) - و مرگ و AKI در بیماران مبتلا به سیروز کبدی مرتبط باشد. در موارد سپسیس نوزادی، فن و یو (2012) استفاده جداگانه از نشانگرهای التهابی CRP، PCT، اینترلوکین{7}} (IL{8}})، TNF- و اینترلوکین را توصیه نکردند. بتا (IL{11}} ); اگرچه IL{12}} در رابطه با اکثر نشانگرها برتر ارزیابی شد، اما نباید به صورت مجزا از آن استفاده کرد. گرینبرگ و همکاران (2015) یک مطالعه چند مرکزی را با 106 کودک یک ماهه تا 18 ساله انجام داد که در CBP قرار گرفتند. نویسندگان گزارش کردند که IL{17}} ممکن است مراحل AKI را 2/3 قبل از جراحی پیشبینی کند و این یک نشانگر زیستی مفید در زمانبندی جراحی است. از آنجایی که IL{21}} از زمان شروع التهاب وجود دارد، سطح آن زودتر از سایر نشانگرهای زیستی افزایش مییابد. IL{22}} با عفونت، AKI (همچنین در نوزادان) و احتمالاً سپسیس نوزادی مرتبط است. در مطالعه دیگری در مورد اینترلوکین ها، محققان چینی 62 بیمار NICU شدیداً بیمار را بدون سپسیس تجزیه و تحلیل کردند و نشان دادند که IL{24}} پیش بینی کننده AKI در این جمعیت حتی پس از تعدیل سن حاملگی بدون توجه به جنس، وزن هنگام تولد و نمره آپگار است. با این مزیت اضافه که با بالغ شدن کلیه کاهش نمی یابد69. بنابراین، به دلیل وجود آن در التهاب، ارتباط با ATN و نقش در پاسخ به آسیب، IL{26}} به سرعت افزایش مییابد و ممکن است به عنوان یک نشانگر زیستی بالقوه AKI، از جمله در نوزادان، دیده شود.
تعداد فزاینده ای از مطالعات کاربردهای KIM{0}} را در تشخیص AKI نوزادان بررسی کرده اند. Genc و همکاران (2013) کاربردهای uKIM{2}} را در تشخیص زودهنگام AKI در 48 نوزاد نارس در مراقبتهای ویژه مورد مطالعه قرار دادند. نویسندگان حساسیت 73.3 درصد و ویژگی 76.9 درصد را یافتند و گزارش کردند که افزایش سطح uKIM-1 در روز 7 با افزایش 7.{12}} برابری خطر مرگ مرتبط است. نویسندگان به این نتیجه رسیدند که uKIM{13}} پیشبینیکننده AKI در جمعیتهای نوزادی است. واضح است که KIM{15}} کاربردهای زیادی دارد، از تشخیص زودهنگام AKI تا پیش آگهی بیمار، و میتوان آن را در جمعیتهای نوزادی و افراد مبتلا به AKI سپتیک استفاده کرد. از نظر L-FABP، النادی و همکاران. (2014) یک مطالعه مورد-شاهدی شامل 42 نوزاد مبتلا به سپسیس و AKI در مراقبت های ویژه انجام داد. سطوح uL-FABP آنها به طور قابل توجهی بالاتر از سطوح مشاهده شده در نوزادان بدون AKI71 بود. پیشرفت قابل توجهی در تحقیقات در مورد L-FABP رخ داده است، به ویژه به این دلیل که نشانگر زیستی را می توان در تشخیص اولیه AKI استفاده کرد زیرا سطوح آن قبل از افزایش سطح SCr افزایش می یابد. استفاده از آن در جمعیت نوزادان شرح داده شده است. در زمینه نشانگرهای زیستی توقف چرخه سلولی، چن و همکاران. (2020) سطوح TIMP-2 و IGFBP-7 را برای ارزیابی توسعه AKI در 237 نوزاد در مراقبتهای ویژه اندازهگیری کرد. ترکیب این دو نشانگر به طور مستقل با AKI شدید با حساسیت 88.9 درصد و ویژگی 50.9 درصد همراه بود.
اگرچه TIMP-2 برای افراد کمتر از 21 سال تأیید نشده است، مطالعات در مورد استفاده از آن در جمعیت نوزادان نتایج امیدوارکنندهای را در تشخیص AKI نشان دادهاند. IGFBP7 نیز در وضعیت مشابهی قرار دارد. اگرچه برای استفاده نوزادان تایید نشده است، اما مطالعات استفاده از آن را در نوزادان با نتایج امیدوارکننده توصیف کردهاند. اگرچه مکانیسم های مرتبط با سپسیس به طور کامل مشخص نشده است، این احتمال وجود دارد که ارتباطی بین حذف گلیکوکالیکس و سپسیس وجود داشته باشد. افزایش سطح سیندکان{3}} پلاسما با بقا همبستگی منفی دارد. این ارتباط معنی دار نشان می دهد که افزایش سطوح اجزای گلیکوکالیکس ممکن است به عنوان نشانگرهای زیستی تشخیصی و پیش آگهی در افراد مبتلا به سپسیس مورد استفاده قرار گیرد62،63.

یک مطالعه کوهورت آیندهنگر که روی 289 بیمار کمتر از 18 سال و نوزادانی که تحت عمل جراحی قلب در بیمارستان ارجاعی در ایالت سئارا، برزیل قرار گرفتند، ثبتنام کرد، نشان داد که سطوح اولیه سندکان پلاسمایی بعد از عمل به طور مستقل با AKI شدید و طولانیتر مرتبط است. بستری در آی سی یو و بیمارستان73. ایده AKI ناشی از آسیب اندوتلیال، عمدتاً مربوط به آسیب گلیکوکالیکس اندوتلیال، مورد توجه قرار گرفته و مطالعات جدید مربوط به syndecan{4}}، به ویژه مرتبط با AKI، از جمله جمعیت نوزادان و سپسیس را مورد توجه قرار داده است. گزارش ها نفرین را به عنوان یک نشانگر زیستی AKI در تنظیمات NICU توصیف کرده اند. مطالعه ای که روی نوزادان ثبت نام کرد نتیجه گرفت که سطح نفرین اولیه ادرار در نوزادان مبتلا به AKI بیشتر از نوزادان بدون AKI است، که نشان می دهد افزایش سطح نفرین ممکن است در نتیجه نابالغی گلومرولی، به ویژه در نوزادان نارس رخ دهد. با توجه به توسعه AKI در سطح گلومرولی، نفرین نشانه های جدیدی را در تحقیقات بهداشتی جمع آوری کرده است که منجر به یافته های مرتبط در نوزادان و سایر جمعیت های مبتلا به AKI شده است. نشانگرهای زیستی مرسوم و غیر متعارف مورد استفاده در ارزیابی AKI سطوح مختلفی از ویژگی و حساسیت را نشان میدهند. مشخصات آنها مطابق با روش های آزمایش و اندازه گیری، مقادیر قطع و پروتکل های ذخیره سازی نمونه متفاوت است. پرز و همکاران (2013) 24 پانلی از نشانگرهای زیستی غیر متعارف را برای تشخیص AKI توصیه کرد زیرا هر نشانگر زیستی ویژگی های خود را دارد42. مطالعات بیشتری در مورد نشانگرهای زیستی AKI برای نوزادان نارس مبتلا به سپسیس مورد نیاز است زیرا ادبیات در مورد این موضوع هنوز کمیاب است. همانطور که مطالعات نشان داده است، AKI با مرگ و میر قابل توجهی همراه است. تشخیص زودهنگام امکان معرفی درمان مناسب و دستیابی به نتایج بهتر، علاوه بر کاهش طول مدت بستری، هزینه های غیرپزشکی و مرگ و میر را فراهم می کند. در این زمینه، نشانگرهای زیستی غیر سنتی (مانند NGAL، IL{16}}، IL{17}}، KIM{18}}، L-FABP، TIMP{20}}، IGFBP7، syndecan{{ 22}} و نفرین) نقش مرتبطی در تشخیص زودرس AKI در نوزادان نارس مبتلا به سپسیس و در پیشگیری از بیماری مزمن کلیه و مرگ، علاوه بر کاهش اثرات بر سیستم مراقبتهای بهداشتی دارند.

نتیجه
AKI یک بیماری شایع در بخش مراقبت های ویژه نوزادان است. این یک بیماری چند عاملی است که یکی از علل اصلی آن سپسیس به ویژه در نوزادان است. AKI با افزایش مرگ و میر همراه است. با توجه به محدودیتهای موجود در نشانگرهای معمولی، نشانگرهای زیستی غیرسنتی (مانند NGAL، IL{0}}، IL-18، KIM-1، L-FABP، TIMP-2، IGFBP7، syndecan-1 و nephrin) در تشخیص زودهنگام AKI در نوزادان مبتلا به سپسیس به یک ضرورت تبدیل شده اند، به طوری که میزان مرگ و میر، طول مدت بستری در بیمارستان و بروز عوارض بعدی کاهش می یابد.
سپاسگزاریها
مایلیم از متخصصانی که پشتیبانی فنی مورد نیاز در طول توسعه این بررسی را ارائه کردند تشکر کنیم. Lemes، RPG، Junior، GBS، Daher، EF، و Martins، AMC دارندگان بورسیه های تحصیلی اعطا شده توسط شورای ملی توسعه علمی و فناوری (CNPq) و هماهنگی برای بهبود پرسنل آموزش عالی (CAPES) هستند.
مشارکت نویسندگان
JSB، GBSJ، GCM، AMCM، EDFD، RPGM، و RPGL به طور قابل توجهی به طراحی این مطالعه کمک کردند. جمع آوری، تجزیه و تحلیل و تفسیر داده ها؛ نگارش و بررسی نسخه خطی و تایید نسخه نهایی نسخه ارسالی برای چاپ.
برای اطلاعات بیشتر:Ali.ma@wecistanche.com
