بیماران جراحی عروقی با نسبت نوتروفیل به لنفوسیت بالا، بیان RNA مکمل نوتروفیل را کاهش داده اند.
Nov 24, 2023
افزایش نسبت نوتروفیل به لنفوسیت (NLR) در بیمارانی که تحت عمل جراحی انتخابی عروقی (EVS) قرار میگیرند، مستقل از نتایج جراحی بعد از عمل، مرگ و میر را افزایش داده است. برای درک اینکه چرا NLR بالا با مرگ و میر بالاتر همراه است، بیان نوتروفیل و رونوشت لنفوسیتی را در بیماران تحت EVS بررسی کردیم. نمونه های خون از بیماران تحت EVS و اهداکنندگان سالم برای محاسبه NLR جمع آوری شد. نمونههای RNA از نوتروفیلها و لنفوسیتهای بیماران جدا و به NLR_Low (<3) and NLR_High (≥3) groups (n = 6 each). Paired samples with the highest RNA integrity number (mean = 9.8 ± 0.4) were sequenced and analyzed for differential expression. Normalized data were inputted for downstream analysis using iPathwayGuide (AdvaitaBio) and gene set enrichment analysis using GenePattern and MSigDB (Broad Institute). There was no clinical difference between the patient groups about clinical diagnosis, age, sex, history of hypertension, lipid abnormalities, diabetes mellitus, smoking, or statin use. The mean NLR was 4.37 ± 0.27 SEM in the NLR_High and 1.88 ± 0.16 for the NLR_Low groups. Significantly differentially expressed gene sets identified in the RNA sequence data were enriched highly (P = 1E-24) in the humoral immunity and complement systems. Neutrophils from NLR_High patients downregulated complement genes (C1QA, C1QB, C1QC, C1S, C2, CR2, C3AR1, C3, C8G, and C9 and complement regulatory genes CD59, SERPING1, C4BPA, CFH, and CFI). Downregulation of gene expressions of humoral immunity and complement within the neutrophils are associated with elevated NLR. It remains to be determined whether and how these changes contribute to increased late mortality previously observed in patients undergoing EVS.

فواید سیستانچ برای مردان - تقویت سیستم ایمنی بدن
معرفی
بیماری قلبی عروقی (CVD) یکی از علل اصلی مرگ و میر در سراسر جهان است. تا حد زیادی به دلیل آتروژنز و آترواسکلروز است که علاوه بر ژنتیک و رژیم غذایی فردی، با مکانیسمهای التهابی و ایمنی ایجاد میشود.{0}} اخیراً، شمارش افتراقی لکوسیتها (نوتروفیلها و لنفوسیتها) مورد توجه قرار گرفته است. برای پیش بینی پیامدهای قلبی عروقی (CV). نسبت تعداد مطلق نوتروفیل به لنفوسیت (NLR) به عنوان یک پیشبینیکننده مرگ و میر کلی در چندین مطالعه کوچک در مورد مداخلات حاد کرونری، فشار خون بالا، 7،8، و نارسایی قلبی شناخته شده است.
جدول 1. مشخصات بالینی بیماران جراحی عروقی انتخابی که توسط RNA-seq مورد بررسی قرار گرفتند
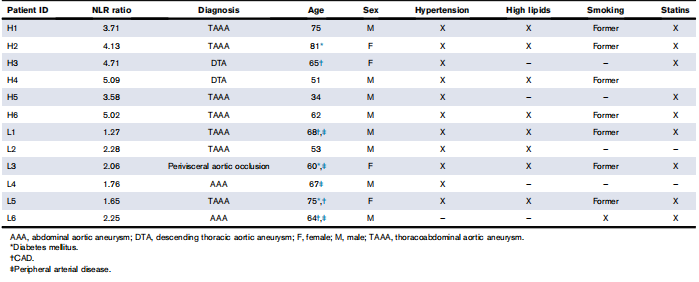
تحقیقات قبلی همچنین نشان داده است که NLR یک پیش بینی کننده پیامدهای طولانی مدت در بیماران مبتلا به بیماری عروق محیطی است.{1}} مطالعات گذشته نگر ما در مورد جمعیت بیماران جراحی عروقی این نتیجه را تأیید می کند. در 1 مطالعه بر روی 108 بیمار با ترمیم آنوریسم آئورت شکمی آندوواسکولار انتخابی، هیچ تفاوتی در 30-روز مرگ و میر پس از عمل بین NLR وجود نداشت.<4 and an NLR of >4 (P = .507). However, the 1-year, 3-year, and 5-year mortality between the groups were 4.2% vs 28.1%, 15.1% vs 64.9%, and 24% vs 90%, respectively.14 In a second study of 290 asymptomatic patients undergoing prophylactic carotid endarterectomy, the risk for stroke was noted to be significantly higher (P < .0001) in patients with an NLR of >3 (n=116 بیمار، 42.6% خطر سکته مغزی) نسبت به بیماران دارای NLR<3 (n = 174 patients, 9.3% stroke risk).15 In a third study with 488 patients who underwent percutaneous interventions of femoropopliteal arteries, the 30-day mortality rates increased significantly (P = .005) with increasing NLR (1.4%, 4.3%, and 7.0% for low [<3], mid [3-4], and high [>4] گروههای NLR. 16 بیماران با NLR پایینتر قبل از عمل، بقای قابلتوجهی بدون قطع عضو در پیگیری سالانه (NLR پایین 65.5٪، NLR متوسط، 37.5٪، و NLR بالا، 17.6) به دست آوردند. ٪ [P <.0001]).16
در این مطالعه، ما توالییابی RNA (RNA-seq) نوتروفیلها و لنفوسیتها را از بیمارانی که واجد شرایط ترمیم جراحی انتخابی عروق (EVS) بودند، انجام دادیم تا مکانیسمهای بالقوه برای NLR بالا را تعیین کنیم. مطالعات بررسی کردند که آیا مبنای مولکولی برای NLR بالا وجود دارد یا خیر. بررسیهای ما نشان میدهد که بیماران مبتلا به NLR بالا که ترمیم EVS داشتند، با کاهش قابل توجه ژنهای ایمونوگلوبولین و مکمل در نوتروفیلها متمایز میشوند.

فواید سیستانچ - تقویت سیستم ایمنی
مواد و روش ها
بیماران
Blood samples were collected from candidate patients for EVS procedures and healthy volunteers for NLR calculation and RNA sequence studies of neutrophils and lymphocytes. In screening patients for participation, any individual with an active local or systemic infection or obvious inflammatory disease was excluded from participation. Peripheral blood collection was approved by the institutional review board of University Hospitals Cleveland Medical Center (#01-06-02). Informed consent was obtained from each patient and healthy volunteer. All patients for EVS seen in the outpatient department were eligible. Patients in the study were characterized for the type of vascular surgery, age, sex, hypertension (blood pressure >130/80 mm Hg), diabetes mellitus (fasting blood glucose >100 میلی گرم در دسی لیتر)، وضعیت سیگار کشیدن، درمان با استاتین، سابقه پزشکی بیماری مزمن انسدادی ریه، سرطان، بیماری مزمن کلیوی، بیماری عروق کرونر (CAD)، بیماری شریانی محیطی، بیماری عروق مغزی، و نارسایی مزمن قلبی. همه بیماران شمارش کامل خون با شمارش گلبول های سفید افتراقی داشتند. بیماران به NLR پایین (NLR_پایین [<3]) and high NLR (NLR_High [≥3]) groups (n = 6 each) and healthy volunteers aged 18 to 71 years (n = 6). Eleven of 12 patients' blood was drawn before surgery. One patient had blood drawn 4 months after surgery.
جداسازی خون
خون کامل (20 میلیلیتر برای هر بیمار) در لولههای واکوتاینر 10 میلیلیتری ضد انعقاد با EDTA جمعآوری شد و خون ظرف یک ساعت پس از جمعآوری جدا شد. جمعیت سلول های نوتروفیل و لنفوسیت هر کدام از 8 میلی لیتر خون با استفاده از کیت های جداسازی مستقیم سلول های انسانی EasySep (STEMCELL Technologies، ونکوور، کانادا) و آهنربای Big EasySep (STEMCELL Technologies، ونکوور، کانادا) طبق پروتکل های سازنده جدا شد. آهنربا قبلاً روی یخ سرد شده بود و سلولهای خون و معرفها به آرامی با معکوس کردن لوله بر خلاف لولهگذاری مخلوط شدند. نسبتهای معرف نیز به روش زیر برای بهینهسازی بازیابی تنظیم شدند: 400 میلیلیتر مخلوط آنتیبادی، 400 میلیلیتر دانههای مغناطیسی و 4 میلیلیتر سالین بافر فسفات قبل از اولین جداسازی به خون اضافه شد و سپس 200 میلیلیتر آنتیبادی به خون اضافه شد. مخلوط و 400 میلی لیتر دانه قبل از جداسازی دوم و 200 میلی لیتر دانه قبل از جداسازی سوم و نهایی. مقدار کمی 200 میلی لیتر از حجم های بازیابی نهایی برای شمارش سلولی و آماده سازی اسلاید گرفته شد. باقیمانده حجم بازیابی با سرعت 1000 دور در دقیقه به مدت 7 دقیقه سانتریفیوژ شد تا سلول ها پلت شوند.

شکل 1. رونوشت کامل RNA از نوتروفیل ها و لنفوسیت های جمع آوری شده از بیماران مبتلا به NLR، بالا (NLR_بالا)، پایین (NLR_کم) یا کنترل (NLR_کنترل) . کد حرف "N" یا "L" در نام نمونه به این معنی است که نوتروفیل ها یا لنفوسیت ها منبع RNA بودند. در هر دسته 6 بیمار وجود داشت. آبی=سطح بیان را کاهش داد. قرمز=سطح بیان بالا.
شمارش سلولی و تهیه اسلاید
سلولهای معلقشده در سالین بافر فسفات بیشتر تقسیمبندی شدند، با تریپان بلو مخلوط شدند و با استفاده از هموسیتومتر به صورت دستی شمارش شدند. به طور معمول، 9×106 تا 15×106 نوتروفیل و 3×106 تا 10×106 لنفوسیت در هر نمونه جدا شد. اسلایدهای سلول های جدا شده با استفاده از سیتوسانتریفیوژ تهیه شد و با سرعت 600 دور در دقیقه به مدت 3 دقیقه چرخانده شد و سپس با رنگ آمیزی رایت-گیمسا رنگ آمیزی شد. خلوص هر جمعیت سلولی با شمارش دستی تعیین شد که در آن حداقل 1000 سلول در هر اسلاید مشخص شد. میانگین خلوص جداسازی نوتروفیل ها و لنفوسیت ها با شمارش سلولی به ترتیب 98.3 و 96.2 درصد بود. فلوسیتومتری بر روی 1 جفت نمونه نوتروفیل و لنفوسیت انجام شد و به ترتیب 90.6% و 92.2% خلوص را نشان داد. سلول های دیگر در آماده سازی نوتروفیل به لنفوسیت (4٪)، مونوسیت (2٪)، ائوزینوفیل (2.3٪)، و بازوفیل (0.3٪) شکسته شدند. در آماده سازی لنفوسیت، سلول های دیگر نوتروفیل (1.2٪)، مونوسیت (1.4٪)، ائوزینوفیل (1.2٪)، و بازوفیل (1.8٪) بودند. دادههای انبوه RNA-seq از همه نمونههای منفرد نیز برای تعیین میزان آلودگی مونوسیتی در آمادهسازی سلولی با تعیین اینکه آیا نوتروفیلها یا لنفوسیتهای NLR{37}}بالا یا NLR{38}}نمونههای پایین به طور قابلتوجهی CD14 را افزایش دادهاند مورد استفاده قرار گرفت. ، CD68، CD83، یا CD163. به طور مستقل، دادههای RNA-seq برای تخمین نسبت سلولهای ایمنی و سرطانی (EPIC) وارد شدند، برنامهای که برای تخمین نسبت سلولهای ایمنی و سرطانی در دادههای بیان ژن انبوه طراحی شده است.17 نمایه مرجع مورد استفاده توسط EPIC برای سلول های ایمنی در گردش خون و حاوی مشخصات سلول های B، سلول های CD4 و CD8 T، مونوسیت ها، نوتروفیل ها و سلول های کشنده طبیعی است. خروجی گزارش شده به صورت کسر سلولی در هر نمونه داده می شود.

شکل 2. ژن هایی که به طور قابل توجهی از نوتروفیل ها و لنفوسیت ها بیان می شوند. (الف) تعداد ژنهایی که بهطور معنیداری در نوتروفیلها (آبی) و لنفوسیتها (نارنجی) بیان میشوند. (ب) نمودار تجزیه و تحلیل مؤلفه اصلی ژنهایی که به طور قابلتوجهی متفاوت بیان شدهاند در نوتروفیلها (سبز و بنفش) و لنفوسیتها (قرمز و آبی) در NLR_بالا (دایرهها) و NLR_کم (مربع). (C) یک نقشه حرارتی از ژنهایی که به طور قابلتوجهی بیان شدهاند از NLR_بالا در مقابل NLR{4}}RNA نوتروفیل کم. (د) یک نقشه حرارتی از ژنهای بیانشده با تفاوت قابلتوجهی از NLR_بالا در مقابل NLR{6}}RNA لنفوسیت کم.
RNA-seq و تجزیه و تحلیل آماری
روش های دقیق برای استخراج و تعیین توالی RNA در روش های تکمیلی ارائه شده است. خواندن توالی از نظر کیفیت مورد ارزیابی قرار گرفت و آداپتور با استفاده از TrimGalore کوتاه شد! (موسسه بابراهام)، یک اسکریپت بسته بندی برای FastQC و CutAdapt. با استفاده از نرم افزار STAR aligner، کنترل کیفیت خوانده شده با ژنوم مرجع انسانی GRCh38 تراز شد. قرائت های تراز شده با استفاده از Cufflinks نسخه 2.2.1 برای تجزیه و تحلیل بیان افتراقی با استفاده از حاشیه نویسی ژن GENCODE برای GRCh38 پردازش شد و داده های بیان سطح ژن در قطعات به ازای رونوشت کیلوباز در هر میلیون خواندن نقشه برداری شده گزارش شد. برش نرخ کشف مقدار P از<.05, after the Benjamini-Hochberg correction for multiple testing. Normalized fold-change and P values for all expressed genes were then used as input for downstream analysis using iPathwayGuide (AdvaitaBio) and gene set enrichment analysis (GSEA) using GenePattern and MSigDB (Broad Institute). Additional figures including heat maps and scatterplots were generated in R and ClustVis.
نتایج
ویژگی های بیمار
شش جفت نمونه از بیماران از بین 7 NLR_بالا و 9 NLR_پایین بر اساس بالاترین کیفیت RNA در جفت انتخاب شدند که توسط عدد یکپارچگی RNA (RIN) ارزیابی شد (جدول 1) ). شش کنترل از 8 اهداکننده سالم نیز مورد بررسی قرار گرفتند. در بیمارانی که در مطالعه شرکت کردند، میانگین ± انحراف استاندارد NLR برای NLR_بالا 4.37 ± 0.66 در مقابل برای NLR_کم، 1.87 ± 0 بود. 39 (P < .{18}}{20}}01). میانگین ± انحراف معیار سن بیماران 0/17 ± 61 سال برای NLR{21}بالا و 5/7 ± 5/64 سال برای NLR{26}}کم بود (P{27}} 0.68). همه به جز 1 بیمار بیماری آنوریسم آئورت داشتند، 9 نفر قفسه سینه/قفسه شکمی و 2 نفر شکمی بودند. هر دو بیمار مبتلا به آنوریسم آئورت شکمی در گروه کم NLR{32}} قرار داشتند. 11 نفر از 12 بیمار سابقه فشار خون داشتند. چهار نفر از 6 بیمار در هر دو گروه NLR{35}بالا یا NLR{36}}پایین، سابقه پزشکی ناهنجاریهای چربی داشتند. چهار بیمار در NLR{37}}بالا و 3 بیمار در NLR{39}}گروه کم سیگاری سابق بودند. یکی از بیماران در گروه پایین{40}NLR سیگاری فعال بود. پنج بیمار در گروه NLR{41}بالا و 4 نفر در گروه NLR{43}پایین، استاتین مصرف میکردند. تنها 3 بیمار در هر دو گروه دیابتی بودند. یک بیمار در هر گروه سابقه CAD و 2 بیمار در گروه NLR{46}}پایین بیماری شریان محیطی داشتند.
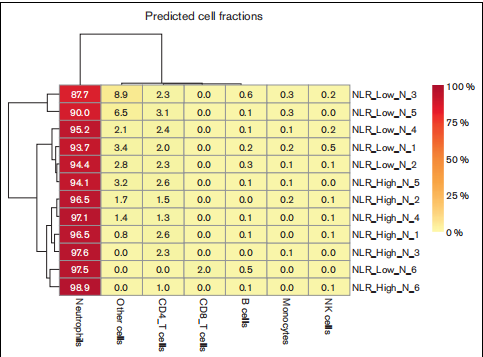
شکل 3. داده های RNA-seq در این تحقیق به عنوان یک ابزار مستقل برای تعیین سایر آلودگی های سلولی در آماده سازی نوتروفیل و لنفوسیت استفاده شد. فقط داده های نوتروفیل ها نشان داده شده است. تجزیه و تحلیل EPIC برای تخمین نسبت سلول های ایمنی و سرطان در داده های بیان ژن توده انجام شد. این تجزیه و تحلیل درصد نوتروفیل ها، مونوسیت ها، سلول های B، سلول های CD4 T، سلول های CD8 T، سلول های کشنده طبیعی (NK) و سایر سلول ها را در آماده سازی نوتروفیل به دست آورد.
رونوشت کامل
ما تفاوت های کلی را در کل رونوشت هنگام مقایسه نمایه های بیان ژن بین نوتروفیل ها و لنفوسیت ها مشاهده کردیم (شکل 1). این یافته تعجب آور نبود زیرا بیان ژن نوع خاص سلول قبلاً متفاوت توصیف شده بود.19 در بخش نوتروفیل، در بین بیماران در NLR_بالا، NLR{3}}کم و NLR{{ 4}}گروههای کنترل، ژنهای زیادی وجود داشتند که به وضوح در بخش لنفوسیت تنظیم نشده بودند و بالعکس. در سطح کل رونوشت، تفاوتهای اختصاصی سلولی بین نوتروفیلها و لنفوسیتها بدون در نظر گرفتن NLR یا اینکه بیمار یا کنترل باشد، متمایز و غالب بود. با این حال، در بررسی دقیق تر، تفاوت ها ظاهر شد. نمودار تجزیه و تحلیل مؤلفه اصلی نشان داد که NLR{6}}کنترل برای نوتروفیل ها یا لنفوسیت ها با NLR_بالا و NLR_ در هر دو سلول همپوشانی دارد (شکل تکمیلی 1). تحقیقات بعدی به دنبال یافتن تفاوتهای اضافی بین گروههای NLR{10}}بالا و NLR{11}}پایین در ژنهای با بیان متفاوت متفاوت بود. مشاهده شد که 900 (74.5%) ژن با بیان متفاوت در نوتروفیلها در گروههای NLR{15}}بالا در مقابل NLR{16}}کم مشاهده شد (شکل 2A). در مقایسه، لنفوسیت ها تنها 190 (7/15%) ژن با بیان متفاوتی داشتند. نمودار تجزیه و تحلیل مؤلفه اصلی NLR_ژن های بالا در مقابل NLR_ژن های کم در نوتروفیل ها و لنفوسیت ها نشان داد که گروه NLR_بالا در مقابل NLR_ژن های کم در نوتروفیل ها به 2 ناحیه مجزا جدا شدند، در حالی که ژن های NLR_High و NLR{27}}لنفوسیت های پایین همپوشانی داشتند (شکل 2B). مجدداً، مانند کل دادههای رونوشت، NLR{29}}کنترل با NRL{30}}High و NLR{31}}تفاوت معنیدار ژنهای کم در نوتروفیلها و لنفوسیتها همپوشانی داشت (شکل تکمیلی 2). بسیاری از ژنهایی که به طور قابلتوجهی بیان شدهاند در NLR_زیاد نوتروفیلها از NLR{34}}کم تنظیم میشوند (شکل 2C). تعداد ژنهای مشابه اما بسیار کمتری در NLR{36}}بالا بودن تعداد لنفوسیتها نسبت به نوتروفیلها کاهش یافت (شکل 2D). این دادهها نشان میدهد که سطوح NLR بیشتر با تغییر بیان ژن در نوتروفیلها مرتبط است. علاوه بر این، باید با بیمارانی از گروه بیماری خود NLR مقایسه شود، نه NLR-کنترل، زیرا گروه قبلی به وضوح از NLR{40}}بالا اما نه NLR{41}}کنترل جدا شد. شکل 2B؛ شکل تکمیلی 2).

cistanche tubulosa - بهبود سیستم ایمنی
قبل از بررسی بیان افتراقی ژن ها و غنی سازی مجموعه ژن، مطالعات اضافی درجه آلودگی مونوسیتی را در آماده سازی نوتروفیل مشخص کردند. با استفاده از دادههای RNA-seq، مشاهده کردیم که بیان نشانگرهای مونوسیتی CD14، CD68، CD83، و CD163 در NLR{5}}بالا در مقابل NLR{6}}نوتروفیلهای کم یا آمادهسازی لنفوسیت تفاوت معنیداری نداشتند. تجزیه و تحلیل EPIC دادههای RNA-seq نوتروفیل نشان داد که سلولهای غیر ایمنی ("سلولهای دیگر") و سلولهای CD4 T آلایندههای اصلی در آمادهسازیهای نوتروفیل هستند (شکل 3). بهجز سلولهای NLR{{1{14}}}}سلولهای T کم CD4 و سلولهای B، هیچ یک از سلولهای آلودهکننده دیگر تفاوت معنیداری در NLR نداشتند_نوتروفیلهای کم در مقابل NLR{13}}نوتروفیلهای زیاد . در آماده سازی نوتروفیل، آلودگی مونوسیتی با تجزیه و تحلیل EPIC تنها 0.17% ± 0 بود. NLR{23}}آمادگی بالا (P=0.12). این مقدار نشان میدهد که آلودگی مونوسیتی زمانی که با تجزیه و تحلیل دادههای RNA-seq در مقابل فلوسیتومتری تعیین میشود، یک مرتبه کمتر بوده است.

شکل 4. نمودار حباب پراکنده دسته های مجموعه ژن GO به طور قابل توجهی برای فرآیندهای بیولوژیکی بین NLR_بالا و NLR_پایین. نسبت k: K بر روی آبسیسا تعداد ژن هایی است که به طور قابل توجهی متفاوت (k) در مقایسه با تعداد کل ژن های دسته (K) بیان می شوند. منظور، اهمیت غنیسازی است که به صورت log (مقدار P) بیان میشود. (الف) مجموعههای ژن GO مشتق شده از RNA-seq نوتروفیل با مقایسه NLR_بالا و NLR_پایین. (ب) مجموعه ژن GO مشتق شده از RNA-seq لنفوسیت. مجموعه های ژن در گوشه سمت چپ پایین هر دو نمودار کمترین معنی را دارند. مجموعه های ژنی در گوشه سمت راست بالای هر دو نمودار مهم ترین هستند.

شکل 4 (ادامه)
برای بررسی ماهیت ژنهای بیانشده متفاوت، ما یک دستهبندی GSEA با هستیشناسی ژن (GO) را برای فرآیندهای بیولوژیکی با استفاده از مجموعههای ژنی با تفاوت معنیدار بین NLR_بالا و NLR{1}}پایین انجام دادیم. نتایج در نمودارهای حباب پراکنده نشان داده شده است (شکل 4). تفکیک مجموعههای ژنی در سمت راست بالای هر یک از نمودارها نشان میدهد (1) درصد بالایی از ژنها در مجموعههای ژنی که به طور قابلتوجهی تغییر کردهاند و (2) درجه بالایی از اهمیت برای غنیسازی مجموعه ژنی. در نمونه ما، نمودارهای حباب پراکنده غنی سازی هر دو دسته مکمل و پاسخ هومورال GO را به طور مستقل برای نوتروفیل ها و لنفوسیت ها نشان داد. در نوتروفیلها، مجموعههای ژنی برای مسیر کلاسیک فعالسازی کمپلمان، تنظیم آبشار فعالسازی پروتئین، و پاسخ ایمنی هومورال با واسطهی ایمونوگلوبولین در گردش، با بیشترین درصد اعضای مجموعه ژن به طور قابلتوجهی تغییر کردهاند، مهمترین هستند (شکل 4A). بهطور مستقل، مجموعههای ژنی یکسان در لنفوسیتها نیز مشاهده شد که دارای نسبت بالایی از ژنهای تغییر یافته قابلتوجه و درجهای از اهمیت مانند مطالعات نوتروفیل هستند (شکل 4B).
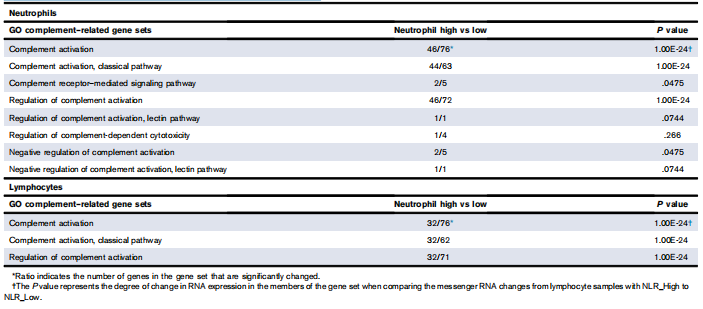
جدول 2. مجموعه ژن های ایمونولوژی در نوتروفیل ها و لنفوسیت ها

جدول 2 تغییرات قابل توجهی در مجموعه ژن های ایمونولوژی در نوتروفیل ها (جدول 2، پانل A) و لنفوسیت ها (جدول 2، پانل B) را فهرست می کند. این مطالعه بیان ژن را در نوتروفیلها یا لنفوسیتها بین نمونههای NLR_بالا و NLR{4}}نمونههای کم مقایسه کرد. NLR سالم_نمونههای کنترل مقایسه نشدند زیرا سطوح بیان آنها با نمونههای NLR_بالا و NLR_در هر دو کل رونوشت و مجموعههای ژنی با بیان متفاوت همپوشانی داشت. علاوه بر این، نمونههای NLR سالم{8}}از نظر سن، بیماری و شرایط جراحی مطابقت نداشتند (شکلهای تکمیلی 1 و 2). در نوتروفیلها (جدول 2) و لنفوسیتها (جدول 2)، دادهها نشان داد که بیان مجموعههای ژنی مرتبط با سیستم ایمنی بسیار متفاوت بود زمانی که NLR{13}}بالا با NLR{14}}کم مقایسه شد. . در RNA seq، هر نوع سلولی یافتههای مشابهی با نوع سلولی دیگر دارد. در هر دو پانل، سطح معنیداری مجموعههای ژن اصلی در P <1E{16}} به حداکثر رسید. این داده ها صرف نظر از اینکه نوتروفیل یا لنفوسیت مورد بررسی قرار گرفت بسیار مهم بود. برای تمرکز بر حوزه محتوای بسیار مهم این تحقیق RNA-seq، بیان ژن ایمونوگلوبولین به طور قابل توجهی متفاوت بیان شده مورد بررسی قرار گرفت. ابتدا، نمودار تجزیه و تحلیل مؤلفه اصلی ژنهای نوتروفیل نشان داد که برای NLR{18}}بالا در مقابل NLR{19}}کم، ژنهای ایمونوگلوبولین به طور قابلتوجهی به 2 گروه تفکیک شدند (شکل 3A تکمیلی). متناوبا، ژنهای لنفوسیتهای NLR_بالا در مقابل NLR{23}}کم بیشتر (شکل 3 الف تکمیلی). سپس، یک نقشه حرارتی ترکیبی از بیان ژن مرتبط با ایمنی بین NLR{26}}بالا با NLR{27}}کم در نوتروفیلها و لنفوسیتها مقایسه شد (شکل 5). به طور کلی، وقتی کل نقشه حرارتی مورد بررسی قرار میگیرد، کاهش آشکار کل خانواده ژنی ژنهای ایمونوگلوبولین در گروه نوتروفیل NLR{29}}بالا در مقایسه با گروه NLR{30}}کم وجود دارد. اکثر ژن ها (69/156، 44%) مربوط به ایمونوگلوبولین بودند. تنها 12 ژن از 156 ژن (7.7%) مرتبط با مکمل بودند: C1QA، C1QB، Serping1، C2، C2R، C4BPA، C3AR1، CR1، CR1L، CFH، CFD، و CD59. در گروه لنفوسیتها، ژنهای عمدتاً ایمونوگلوبولین در دسته NLR{50}}بالا نیز کاهش یافت.
مجموعه ژن های مکمل در نوتروفیل ها و لنفوسیت ها در جدول 3 به تفصیل آمده است. هم در نوتروفیل ها (جدول 3) و هم در لنفوسیت ها (جدول 3)، بیان ژن ها در 3 مجموعه ژنی مربوط به سیستم کمپلمان بسیار متفاوت بود (P <1E{{{{ 5}}) هنگامی که NLR_نمونه های بالا با NLR_نمونه های پایین مقایسه شد. چه مقایسه بین RNA نوتروفیل ها یا لنفوسیت ها، این مشاهدات یکسان بود. 3 مجموعه ژن شامل فعال سازی کمپلمان، مسیر کلاسیک فعال سازی کمپلمان و تنظیم فعال سازی کمپلمان است. نمودار تجزیه و تحلیل مؤلفه اصلی ژنهای نوتروفیل دوباره نشان داد که برای NLR{9}}بالا در مقابل NLR{10}}کم، ژنهای مکمل به طور قابلتوجهی به 2 گروه تفکیک شدند (شکل 3B تکمیلی). همچنین، ژنهای لنفوسیتی NLR_بالا در مقابل NLR{14}}همپوشانی کم دارند (شکل 3B تکمیلی).

شکل 5. نقشه حرارتی ژنهایی که به طور قابلتوجهی متفاوت بیان میشوند در ژن ایمونوگلوبولین مجموعه در نوتروفیلها (سمت چپ) و لنفوسیتها (راست). ژن هایی که در سمت راست هر نقشه حرارتی فهرست شده اند، اعضای ایمونوگلوبولین هستند
یک نقشه حرارتی از نوتروفیل ها و بیان لنفوسیتی یک مجموعه ژن مرتبط با مکمل که NLR_بالا با NLR_پایین را مقایسه میکند در شکل 6 نشان داده شده است. در نوتروفیلها، تعداد زیادی از ژنها کاهش یافت NLR{4}}جمعیت بالا. در این مجموعه ژنی، مشابه مجموعه های ژن ایمونوگلوبولین، اکثر ژن ها (69/ 86، 80%) مرتبط با ایمونوگلوبولین بودند. تنها 12 مورد از 86 (14%) ژن های جزء مکمل و تنظیم کننده بودند (C1QA، C1QB، SERPING1، C2، CR2، C4BPA، C3AR1، CR1، CR1L، CD59، CFH، و CFD). به طور کلی در گروه لنفوسیت، بیان ژنهای کمپلمان کمتر بود، و ژنهای ایمونوگلوبولین در گروه NLR{23}High کمی کاهشتر بودند. از آنجایی که درک بیشتری از ژنهای سیستم کمپلمان در مقایسه با ژنهای سیستمهای ایمونوگلوبولین وجود دارد، توجه به سیستم مکمل به عنوان یک نامزد بالقوه برای ژنهای هدف مرتبط با NLR بالا و پایین متمرکز شد. یک نقشه حرارتی مرکب با مقایسه NLR{24}High با NLR_Low تهیه شد که بیان سیستم مکمل و ژنهای مرتبط را در نمونههای نوتروفیل و لنفوسیت نشان میدهد (شکل 7). در بیشتر موارد، لنفوسیت یک سیستم سلولی مخزنی برای سیستم کمپلمان نیست. بیشتر ژن های مکمل در لنفوسیت ها تنظیم نشده اند. فقط C1S، CR2، C5، C8G، C5، و CFB با تفاوت در بیان بین لنفوسیتهای NLR{32}بالا و NLR{33}}کم وجود داشتند (شکل 7). CD81 در لنفوسیت ها یک تتراسپانین سلول B است. به نظر میرسد که بیانهای C1S و C8G در NLR لنفوسیتی_زیاد نسبت به NLR لنفوسیتی_Low، مشابه ژن KLKB1، ژن پرکالیکرئین پلاسما، بهطور قابلتوجهی بالاتر باشد.
در مقابل، در نوتروفیلها، NLR{0}High نشان داد که ژنهای جزء مکمل C1QA، C1QB، C1QC، SERPING1، C1R، C4BPA، C3، و C3AR1 و ژنهای تنظیمکننده مکمل (بازدارنده) CD59، CFB، و CFI کاهش مییابد. . فقط ژنهای C2 و CFD در بیماران NLR{12}}High_N تنظیم مثبت شد. CD59 و C9 در نوتروفیل NLR_پایین_N در مقایسه با NLR{18}}بالا_N نسبتاً افزایش یافته اند. FGFR4 یک گیرنده فاکتور رشد است. CFH وجود داشت اما به نظر میرسید که تحت تأثیر NLR{21}}بالا یا NLR{22}} نوتروفیل قرار نگرفت. در لنفوسیت ها بیشتر بیان می شود.

فواید سیستانچ برای مردان - تقویت سیستم ایمنی بدن
برای مشاهده محصولات Cistanche Enhance Immunity اینجا را کلیک کنید
【بیشتر بخواهید】 ایمیل:cindy.xue@wecistanche.com / Whats App: 0086 18599088692 / Wechat: 18599088692
بحث
NLR در شمارش افتراقی لکوسیت ها به یک نشانگر ساده و پرکاربرد برای تشخیص پیامدهای مضر بالقوه در طیف وسیعی از اختلالات، از جمله CVD، تومورهای جامد، و اختلالات التهابی مانند لوپوس اریتماتوز سیستمیک و اسکلروز سیستمیک تبدیل شده است. در تحقیقات گذشته نگر خودمان بر روی بیماران مبتلا به CVD آترواسکلروتیک، مشاهده کردیم که بیماران مبتلا به NLR بالا، میزان مرگ و میر دیرهنگام بالاتری پس از ترمیم آنوریسم انتخابی آئورت، نرخ سکته دیرهنگام/مرگ دیررس بعد از اندارترکتومی پیشگیرانه کاروتید، و کاهش بقای بدون قطع عضو پس از آن دارند. در صورتی که NLR آنها بالا باشد، عروق ران-پوپلیتئال انتخابی.{1}} تحقیقات حاضر برای یافتن یک مبنای مکانیکی برای NLR بالا آغاز شد. لنفوم، تومورهای جامد متعدد و اختلالات التهابی مانند لوپوس اریتماتوز سیستمیک و اسکلروز سیستمیک. در تحقیقات گذشته نگر خودمان بر روی بیماران مبتلا به CVD آترواسکلروتیک، مشاهده کردیم که بیماران مبتلا به NLR بالا، میزان مرگ و میر دیرهنگام بالاتری پس از ترمیم آنوریسم انتخابی آئورت، نرخ سکته دیرهنگام/مرگ دیررس بعد از اندارترکتومی پیشگیرانه کاروتید، و کاهش بقای بدون قطع عضو پس از آن دارند. در صورتی که NLR آنها افزایش یابد، عروق ران-پوپلیتئال انتخابی.{3}} تحقیقات حاضر برای یافتن یک مبنای مکانیکی برای NLR بالا آغاز شد.
جدول 3. مجموعه ژن های مکمل در نوتروفیل ها و لنفوسیت ها
برای ایجاد یک رویکرد بی طرفانه در مورد مکانیسم(های) اثرات افتراقی NLR بر نتایج CV، ما RNA-seq را بر روی نوتروفیلها و لنفوسیتهای همان بیماران انجام دادیم. برای این مطالعه، تمام بیماران مبتلا به بیماری آئورت به صورت آیندهنگر جمعآوری و با نتایج آنها در دستههای NLR دستهبندی شدند. 6 نمونه نهایی در هر یک از 2 نوع سلول با بالاترین سطح RIN آنها در RNA تهیه شده از نمونه های زوج نوتروفیل و لنفوسیت بدون توجه به جنس، سن یا شرایط پزشکی قبلی انتخاب شدند. همانطور که در جدول 1 مشاهده می شود، بیماران در گروه های NLR_High و NLR_Low کاملاً مشابه بودند و فقط با NLR خود متمایز می شدند.
کیفیت RNA مورد استفاده در این مطالعه با RIN و جداسازی کامل الگوی بیان ژن بین نوتروفیل ها و لنفوسیت ها در همه گروه های بیمار جمع آوری شده (NLR بالا، NLR پایین و گروه شاهد) نشان داده شده است (شکل 1). نمودار تجزیه و تحلیل مؤلفه اصلی نشان میدهد که دادههای NLR_در این تحقیق نامربوط بود زیرا NLR بیماران با NLR_بالا و NLR{3}}در جمعیت نوتروفیل و لنفوسیت بیماران همپوشانی داشت. . تجزیه و تحلیل GSEA بینش بسیار خوبی در مورد اینکه کدام مجموعه ژن در مجموعه های ژن GO فرآیندهای بیولوژیکی غنی شده است، ارائه کرد، و نمودار حباب پراکنده به وضوح این را با ترسیم معنی لگاریتم در برابر نسبت تعداد ژن های تغییر یافته بر تعداد کل ژن ها نشان داد. در مجموعه های ژنی هنگامی که بررسی شد، مجموعههای ژنی که خود را از کل فهرست جدا میکنند، آنهایی بودند که در سیستم ایمنی هومورال (ایمونوگلوبولین) و سیستم مکمل (جدول 2 و 3) بر اساس نسبت و اهمیت آماری در یک رویکرد کشف بیطرفانه بودند.
کار با تعداد زیادی از ژن های ایمونوگلوبولین ایمنی هومورال درگیر دشوار است زیرا تفاوت های مهم بین این ژن ها به خوبی شناخته نشده است. روش دیگر، اطلاعات بسیار بیشتری در مورد سیستم کمپلمان وجود دارد، و تمرکز بر سیستم مکمل کلاسیک که توسط ایمونوگلوبولین فعال می شود، یک هدف قابل تشخیص برای التهاب و بیماری مربوط به ایمونوگلوبولین ها است. دادههای ما نشان میدهد که ژنهای جزء مکمل کلاسیک C1QA، C1QB، C1R، CR1، C1S، SERPING1، C2، C4BPA، C3 C3AR1، C8G، C9، و چندین ژن تنظیمکننده (CD59، CFB CFI، و CFH) در نوتروفیلهای بیماران کاهش مییابند. با NLR بالا (شکل 7). این یافته ها به 3 دلیل قابل توجه است. اول، ژن های درگیر آنهایی هستند که عمدتاً از مسیر مکمل کلاسیک هستند. دوم، در بیماران NLR بالا، این ژن های مکمل، در اکثر موارد، در مقایسه با بیماران NLR پایین، تنظیم شده اند. در نهایت، F12 بیشتری در نوتروفیلهای NLR{17}}بالا نسبت به نمونههای NLR{18}}کم بیان میشود. اشکال آنزیمی محصول پروتئینی F12 (فاکتور XII [FXII]) مسیر کلاسیک کمپلمان و نوتروفیل ها را فعال می کند. {21}}بالا، نشان میدهد که فعالسازی FXII خود ممکن است تنظیمکننده فعالسازی مکمل باشد.
علاوه بر این، نشان داده شده است که سیستم مکمل کلاسیک در CVD تسریع شده دخیل است. جزء مکمل 1q (C1q) عامل اولیه مسیر کمپلمان است که نقش مهمی در سیستم ایمنی ذاتی و اکتسابی دارد. مسیر کمپلمان، C1q با تنظیم سیگنال مولکولی ماکروفاژ از طریق یک مسیر مستقل از مکمل، تعدیل جذب لیپوپروتئین آتروژنیک، واسطه سلول های آپوپتوز و حذف بقایای سلولی، نقش محافظتی در آترواسکلروز در مراحل اولیه دارد. مطالعه اخیر توسط Jia. و همکاران 23 نشان می دهد که کاهش C1q سرم با CAD مرتبط است. مطالعه دیگری توسط Guo و همکاران 24 نشان می دهد که افزایش فعالیت C1q با CAD مرتبط است. در نهایت، مطالعات اخیر نشان میدهد که بیماران مبتلا به دیابت با کاهش C1q، بقای خود را کوتاهتر کردهاند. این دادهها نشان میدهند که بررسی سیستم کمپلمان ممکن است در درک پاتوژنز ناشی از التهاب CVD مهم باشد.

شکل 6. نقشه حرارتی ژنهایی که به طور قابلتوجهی متفاوت بیان شدهاند در مجموعه ژن مکمل در نوتروفیلها (سمت چپ) و لنفوسیتها (راست). ژن های ذکر شده در سمت راست هر نقشه حرارتی اعضای مجموعه ژن مکمل هستند. RNA از نوتروفیل ها یا لنفوسیت های جمع آوری شده از بیماران با NLR بالا (NLR_ زیاد) یا پایین (NLR_ پایین) است. شش نمونه جداگانه از NLR_High با 6 نمونه جداگانه از NLR_Low از نوتروفیل ها و لنفوسیت ها مقایسه می شود.

شکل 7. نقشه حرارتی ترکیبی از مکمل و ژن های مرتبط از نوتروفیل یا لنفوسیت NLR_بالا یا NLR_کم. در هر دسته، نقشه حرارتی مرکب از 6 نمونه RNA-seq منفرد از هر نوع سلول تهیه شد.
Recently, a retrospective investigation of the data from the CANTOS, JUPITER, SPIRE-1, SPIRE-2, and CIRT trials on 60 087 patients was conducted to determine whether NLR predicts major adverse CV events and is modified by anti-inflammatory therapy.26 NLR modestly correlated (ie, r 2 ≤ 0.26) with interleukin 6, C-reactive protein, and fibrinogen levels but minimally with lipids.25 In all 5 trials, NLR predicted incident CV events and death in patients with NLR >3.08.26 اگرچه کاهش چربی تاثیری بر NLR نداشت، درمان ضد التهابی با کاناکینوماب، یک مهارکننده اینترلوکین 1، NLR را کاهش داد (0001/0 P <). تاثیر استاتین ها این تجزیه و تحلیل موقت از کارآزماییهای تصادفیشده آیندهنگر متعدد نشان میدهد که NLR ممکن است یک عامل خطر مستقل برای مرگ و میر در CVD باشد.
محدودیت هایی در این مطالعه وجود دارد. آماده سازی نوتروفیل ما دارای 4٪ آلودگی لنفوسیت و 2٪ مونوسیت توسط فلوسیتومتری بود. از آنجایی که نوتروفیل ها برای سنتز ایمونوگلوبولین شناخته شده نیستند، تغییرات ژن ایمونوگلوبین نوتروفیل می تواند ناشی از آلوده کردن سلول های B باشد. در تجزیه و تحلیل EPIC، افزایش قابل توجهی در آلودگی سلول های B نمونه های NLR-Low وجود داشت. این مشاهدات نشان میدهد که افزایش سطح ژنهای ایمونوگلوبولین در نمونههای NLR{4}}کم نوتروفیل ممکن است ناشی از آلودگی سلولهای B باشد. بنابراین، کاهش ژنهای ایمونوگلوبولین در نمونههای NLR{6} بالا ممکن است به دلیل افزایش سلولهای B در NLR باشد_نمونههای کم و نه لزوماً کاهش سطح ژن ایمونوگلوبولین در نمونههای NLR_بالا. به همین ترتیب، نوتروفیل ها به عنوان سلول های سازنده مکمل شناخته نمی شوند. آلودگی دو درصدی به مونوسیت ها می تواند منبع ژن های مکمل باشد. با این حال، با استفاده از دادههای seq RNA، مشاهده کردیم که تفاوت معنیداری در آلودگی مونوسیتی آمادهسازیهای نوتروفیلی بین NLR{10}}کم و NLR{11}}بالا وجود ندارد. علاوه بر این، انجام یک تجزیه و تحلیل EPIC از دادههای RNA-seq نشان میدهد که آلودگی مونوسیتی<0.1% (<1:1000) of the neutrophil preparations, indicating that the RNA-seq was unlikely influenced by contaminating monocytes (Figure 3). The contaminating B cells in the NLR_Low samples do not influence the complement data observed. Finally, even now, it is not known that the changes we observed in complement and immunoglobulin genes are specific to vascular surgery patients with high NLR or older patients in general. NLR and genetic studies need to be performed on healthy age- and sex-matched patients without CVD.

فواید سیستانچ برای مردان - تقویت سیستم ایمنی بدن
در مجموع، یافته اصلی در این تحقیق این است که، در حالتهای NLR بالا، بسیاری از ژنهای مکمل و برخی از تنظیمکنندههای آنها در نوتروفیلها کاهش مییابند. مشخص نیست که معنی کلی و وضعیت فعال سازی ژن های مکمل با تنظیم پایین شناسایی شده است. از آنجایی که مجموعه ژن های مکمل به طور قابل توجهی کاهش یافته است، ما حدس می زنیم که افراد مبتلا به NLR{1}}بالا و کوتاه شدن بقای پس از عمل، مکانیسم های حفاظتی اصلی CV ارائه شده توسط سیستم های مکمل را از دست می دهند. این ارزیابی نیاز به بررسی آینده نگر در تحقیقات بالینی برای مکانیسم(های) اساسی این پیامد دارد.
منابع
1. راس آر. آترواسکلروز - یک بیماری التهابی. N Engl J Med. 1999؛ 340 (2): 115-126.
2. Getz GS. سری بررسی موضوعی: سیستم ایمنی و آتروژنز. عملکرد سیستم ایمنی در آتروژنز J Lipid Res. 2005؛ 46 (1): 1-10.
3. Hansson GK، Hermansson A. سیستم ایمنی در آترواسکلروز. نات ایمونول. 2011؛ 12 (3): 204-212.
4. دافی بی کی، گورم اچ اس، راجاگوپال وی، گوپتا آر، الیس اس جی، بات دی ال. سودمندی افزایش نسبت نوتروفیل به لنفوسیت در پیش بینی مرگ و میر طولانی مدت پس از مداخله عروق کرونر از راه پوست. جی کاردیول هستم. 2006؛ 97 (7): 993-996.
5. Tamhane UU، Aneja S، Montgomery D، Rogers EK، Eagle KA، Gurm HS. ارتباط بین نسبت نوتروفیل به لنفوسیت پذیرش و پیامدها در بیماران مبتلا به سندرم حاد کرونری جی کاردیول هستم. 2008؛ 102 (6): 653-657.
6. Gibson PH، Croal BL، Cuthbertson BH، و همکاران. نسبت نوتروفیل به لنفوسیت قبل از عمل و نتیجه پیوند عروق کرونر Am Heart J. 2007;154(5):995-1002.
7. Fici F، Celik T، Balta S، و همکاران. اثرات مقایسه ای نبیولول و متوپرولول بر عرض توزیع گلبول های قرمز و نسبت نوتروفیل به لنفوسیت در بیماران مبتلا به فشار خون اساسی تازه تشخیص داده شده J Cardiovasc Pharmacol. 2013؛ 62 (4): 388-393.
8. Karaman M, Balta S, Ay SA, et al. اثرات مقایسه ای والزارتان و آملودیپین بر سطوح vWf و نسبت N/L در بیماران مبتلا به فشار خون تازه تشخیص داده شده Clin Exp Hypertens. 2013؛ 35 (7): 516-522.
9. Uthamalingam S، Patvardhan EA، Subramanian S، و همکاران. کاربرد نسبت نوتروفیل به لنفوسیت در پیشبینی پیامدهای بلندمدت در نارسایی حاد قلبی جبراننشده. جی کاردیول هستم. 2011؛ 107 (3): 433-438.
10. Bhat TM، Afari ME، Garcia LA. نسبت لنفوسیت نوتروفیل در بیماری عروق محیطی: مروری Expert Rev Cardiovasc Ther. 2016؛ 14 (7): 871-875.
11. بوتا اچ، آغا آر، وونگ جی، تانگ تی، ویلسون وای جی، والش اس آر. نسبت نوتروفیل به لنفوسیت بقای میان مدت را پس از جراحی بزرگ عروقی انتخابی پیش بینی می کند: یک مطالعه مقطعی. Vasc Endovasc Surg. 2011؛ 45 (3): 227-231.
12. Appleton ND، Bailey DM، Morris-Stiff G، Lewis MH. نسبت نوتروفیل به لنفوسیت مرگ و میر حین عمل را به دنبال ترمیم انتخابی باز آنوریسم های آئورت شکمی پیش بینی می کند. Vasc Endovasc Surg. 2014؛ 48 (4): 311-316.
13. Bath J, Smith JB, Kruse RL, Vogel TR. نسبت نوتروفیل به لنفوسیت شدت و نتیجه بیماری را پس از عمل اندام تحتانی پیش بینی می کند. J Vasc Surg. 2020; 72 (2): 622-631.
14. King AH, Schmaier AH, Harth KC, et al. افزایش نسبت نوتروفیل-لنفوسیت مرگ و میر را به دنبال ترمیم انتخابی آنوریسم اندوواسکولار پیش بینی می کند. J Vasc Surg. 2020؛ 72 (1): 129-137.
15. پادشاه ق، کیم ه، کوان اس، و همکاران. افزایش نسبت نوتروفیل به لنفوسیت با پیامدهای بدتری پس از اندارترکتومی کاروتید در بیماران بدون علامت همراه است. J Stroke Cerebrovasc Dis. 2021؛ 30 (12): 106120.
16. King AH, Kwan S, Schmaier AH, et al. افزایش نسبت نوتروفیل به لنفوسیت با کاهش بقای بدون قطع عضو پس از عروق از راه پوست فموروپوپلیتئال همراه است. اینت آنژیول. 2021؛ 40 (5): 442-449.
17. Racle J، de Jonge K، Baumgaertner P، Speiser DE، Gfeller D. شمارش همزمان انواع سرطان و سلول های ایمنی از داده های بیان ژن تومور حجیم. الیف 2017؛ 6: e26476.
18. Trapnell C, Roberts A, Goff L, et al. تجزیه و تحلیل بیان ژن دیفرانسیل و رونوشت آزمایشهای RNA-seq با TopHat و Cufflinks. پروتوک Nat. 2012؛ 7 (3): 562-578.
19. Palmer C, Diehn M, Alizadeh AA, Brown PO. پروفایل های بیان ژن خاص نوع سلولی لکوسیت ها در خون محیطی انسان BMC Genomics. 2006؛ 7:115.
20. Stavrou EX, Fang C, Bane KL, et al. فاکتور XII و uPAR عملکرد نوتروفیل ها را تنظیم می کند تا بر بهبود زخم تأثیر بگذارد. جی کلین سرمایه گذاری. 2018؛ 128 (3): 944-959.
21. Dunkelberger JR، Song WC. مکمل و نقش آن در پاسخ های ایمنی ذاتی و سازگار Cell Res. 2010؛ 20 (1): 34-50.
22. Speidl WS، Kastl SP، Huber K، Wojta J. مکمل در آترواسکلروز: دوست یا دشمن؟ جی ترومب هموست. 2011؛ 9 (3): 428-440.
23. Jia Y، Wen W، Yang Y، و همکاران. نقش بالینی ترکیبی C1q و hsCRP سرم در پیش بینی بیماری عروق کرونر کلین بیوشیم. 2021؛ 93: 50-58.
24. Guo S، Mao X، Li X، Ouyang H، Gao Y، Ming L. فعالیت مکمل سرمی C1q با بیماری انسدادی عروق کرونر مرتبط است. قلب و عروق جلو. 2021؛ 8:618173.
25. Cavusoglu E, Kassotis JT, Anwar A, et al. سودمندی مکمل C1q برای پیش بینی مرگ و میر 10- ساله در مردان مبتلا به دیابت قندی مراجعه کننده برای آنژیوگرافی عروق کرونر. جی کاردیول هستم. 2018؛ 122 (1): 33-38.
26. Adamstein NH، MacFadyen JG، Rose LM، و همکاران. نسبت نوتروفیل به لنفوسیت و رویدادهای آترواسکلروتیک رخ داده: تجزیه و تحلیل از پنج کارآزمایی تصادفی معاصر. Eur Heart J. 2021;42(9):896-903.
